西地那非类似物的合成
2016-06-12帅放文黄祖云王向峰龙泽昕
帅放文, 黄祖云, 王向峰, 龙泽昕, 肖 江*
(1. 湖南省药用辅料工程技术研究中心有限公司,湖南 长沙 410331;2. 湖南尔康制药股份有限公司,湖南 长沙 410331)
·制药技术·
西地那非类似物的合成
帅放文1,2, 黄祖云1, 王向峰1,2, 龙泽昕1, 肖江1*
(1. 湖南省药用辅料工程技术研究中心有限公司,湖南 长沙410331;2. 湖南尔康制药股份有限公司,湖南 长沙410331)
摘要:报道了一种合成西地那非类似物的新方法。以邻丙氧基苯甲酸为原料,经5步反应制得西地那非类似物的关键中间体——硫代西地那非氯{1-甲基-3-丙基-5-(2-丙氧基-5-氯磺酰苯基)-1,6-二氢-7H-吡唑并[4,3-d]嘧啶-7-硫酮}(7); 7与哌嗪衍生物反应合成了4个新型的西地那非类似物,收率72.3%~80.9%,纯度99.0%,其结构经1H NMR和ESI-MS表征。
关键词:邻丙氧基苯甲酸; 哌嗪; 西地那非类似物; 中间体合成; 药物合成
西地那非(SDF)是首种临床用于治疗男性勃起功能障碍的口服药[1-6]。国内外对SDF的合成工艺已有较多报道[7-12]。随着SDF的广泛使用和临床研究深入,合成新型的SDF类似物对样品对照和提高药效均有重要意义。
本文报道了一种合成SDF类似物的新方法。以邻丙氧基苯甲酸(1)为原料,经5步反应制得SDF类似物的关键中间体——硫代西地那非氯{1-甲基-3-丙基-5-(2-丙氧基-5-氯磺酰苯基)-1,6-二氢-7H-吡唑并[4,3-d]嘧啶-7-硫酮}(7, Chart 1); 7与哌嗪衍生物(8a~8d)反应合成了4个新型的SDF类似物(9a~9d, Scheme 1),收率72.3%~80.9%,纯度99.0%,其结构经1H NMR和ESI-MS表征。

Scheme 1
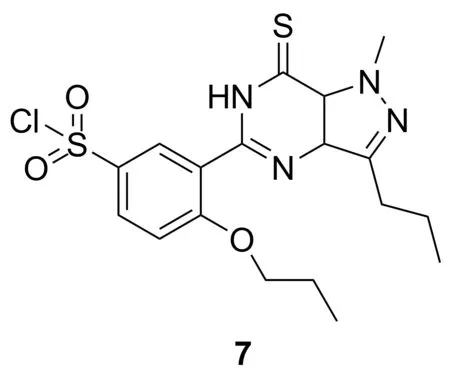
Chart 1
1实验部分
1.1仪器与试剂
Brucker-400型核磁共振仪(CDCl3为溶剂,TMS为内标);AB Sciex 3200 QTRAP型高效液相色谱质谱联用仪;LC-15C型高效液相色谱仪。
所用试剂均为分析纯。
1.2合成
(1) 邻丙氧基苯甲酰氯(2)的合成
在三颈瓶中加入1 100.0 g(555 mmol),氮气保护,搅拌下缓慢滴加氯化亚砜300 mL,滴毕,回流(80 ℃)反应6 h。反应液减压浓缩得淡黄色黏稠液体2。
(2) 1-甲基-3-丙基-4-(2-丙氧基苯甲酰胺基)吡唑-5-甲酰胺(4)的合成[13]
在三颈瓶中加入二氯甲烷500 mL和三乙胺100 mL,搅拌下加入4-氨基-1-甲基-3-丙基吡唑-5-甲酰胺盐酸盐(3)80.5 g(368 mmol),冰浴冷却,缓慢滴加2 110.0 g(554 mmol),滴毕,于室温反应12 h。过滤,滤液用1 mol·L-1NaOH溶液(3×300 mL)洗涤,无水硫酸钠干燥,减压浓缩后用乙酸乙酯重结晶得白色晶体4 95.0 g,收率75%。
(3) 1-甲基-3-丙基-5-(2-丙氧基苯基)-1,6-二氢-7H-吡唑并[4,3-d]嘧啶-7-酮(5)的合成[14]
在三颈瓶中加入4 57.0 g(165 mmol),乙醇200 mL, 1 mol·L-1NaOH溶液350 mL和30%双氧水50.6 mL,搅拌下回流(80 ℃)反应12 h。冰浴冷却下用1 mol·L-1盐酸调至pH呈中性,析出大量白色固体,过滤,滤饼用乙醇重结晶得白色固体5 43.5 g,收率80.5%。
(4) 1-甲基-3-丙基-5-(2-丙氧基苯基)-1,6-二氢-7H-吡唑并[4,3-d]嘧啶-7-硫酮(6)的合成
在三颈瓶中加入5 34.0 g(104 mmol),五硫化二磷5.8 g(26 mmol)和甲苯200 mL,搅拌下回流(110 ℃)反应5 h。反应液减压浓缩,残余物加入6 mol·L-1NaOH溶液500 mL,用二氯甲烷(3×200 mL)萃取,合并有机相,用无水硫酸钠干燥,减压浓缩得黄色固体6 33.8 g,收率94.7%。
(5) 7的合成
在反应瓶中加入氯磺酸50 mL,于-10 ℃搅拌20 min;分批加入6 15 g(440 mmol),加毕,加入二氯亚砜5 mL,于室温反应8 h。反应液缓慢倒入冰水中,析出大量灰色固体,过滤,滤饼真空干燥得灰色固体7 16.5 g,收率85.5%。
(6) 9a~9d的合成(以9a为例)
在反应瓶中加入7 4.0 g(9.0 mmol)和二氯甲烷50.0 mL,搅拌使其溶解;依次加入N-甲基哌嗪(8a)1.0 g(10.8 mmol)和三乙胺1.8 g(18.0 mmol),于室温反应6 h。反应液用水(3×100 mL)洗涤,用无水硫酸钠干燥,减压浓缩,残余物用无水乙醇重结晶得黄色固体9a 3.5 g。
以2,6-二甲基哌嗪(8b),N-乙基哌嗪(8c)和N-羟乙基哌嗪(8d)替代8a,用类似的方法合成黄色固体9b~9d。
1-甲基-3-丙基-5-[2-丙氧基-5-(4-甲基哌嗪-1-磺酰基苯基)]-1,6-二氢-7H-吡唑并[4,3-d]嘧啶-7-硫酮(9a): 收率76.4%,纯度99.0%;1H NMRδ: 12.34(br s, 1H), 8.85~8.84(d,J=2.4 Hz, 1H), 7.86~7.83(dd,J=2.4 Hz, 8.8 Hz, 1H), 7.19~7.17(d,J=8.8 Hz, 1H), 4.52(s, 3H), 4.29~4.26(t,J=6.4 Hz, 2H), 3.10(br s, 4H), 2.96~2.92(t,J=7.2 Hz, 2H), 2.50~2.48(t,J=4.8 Hz, 4H), 2.26(s, 3H), 2.14~2.07(q,J=6.8 Hz, 2H), 1.88~1.82(q,J=7.6 Hz, 2H), 1.22~1.18(t,J=7.2 Hz, 3H), 1.03~0.99(t,J=7.2 Hz, 3H); ESI-MSm/z: 504.9{[M+H]+}。
1-甲基-3-丙基-5-[2-丙氧基-5-(2,6-二甲基哌嗪-1-磺酰基苯基)]-1,6-二氢-7H-吡唑并[4,3-d]嘧啶-7-硫酮(9b): 收率72.3%,纯度99.0%;1H NMRδ: 8.83~8.82(d,J=2.4 Hz, 1H), 7.87~7.84(dd,J=2.4 Hz, 8.8 Hz, 1H), 7.19~7.17(d,J=8.8 Hz, 1H), 4.52(s, 3H), 4.30~4.26(t,J=6.4 Hz, 2H), 3.69(d,J=2.0 Hz, 1H), 3.66(d,J=1.60 Hz, 1H), 3.03~2.92(m, 4H), 2.16~2.07(m ,2H), 1.94~1.82(m, 4H), 1.23~1.19(t,J=7.6 Hz, 3H), 1.04~0.98(m, 9H); ESI-MSm/z: 519.2{[M+H]+}。
1-甲基-3-丙基-5-[2-丙氧基-5-(4-乙基哌嗪-1-磺酰基苯基)]-1,6-二氢-7H-吡唑并[4,3-d]嘧啶-7-硫酮(9c): 收率80.9%,纯度99.0%;1H NMRδ: 12.34(br s, 1H), 8.86~8.85(d,J=2.4 Hz, 1H), 7.87~7.84(dd,J=2.4 Hz, 8.8 Hz, 1H), 7.19~7.17(d,J=8.8 Hz, 1H), 4.53(s, 3H), 4.29~4.26(t,J=6.4 Hz, 2H), 3.11(br s, 4H), 2.97~2.93(t,J=7.2 Hz, 2H), 2.55~2.52(t,J=4.8 Hz, 4H), 2.43~2.38(q,J=7.2 Hz, 2H), 2.14~2.09(q,J=6.8 Hz, 2H), 1.90~1.81(m, 2H), 1.23~1.19(t,J=7.2 Hz, 3H), 1.04~1.00(m, 6H); ESI-MSm/z: 519.2{[M+H]+}。
1-甲基-3-丙基-5-[2-丙氧基-5-(4-羟乙基哌嗪-1-磺酰基苯基)]-1,6-二氢-7H-吡唑并[4,3-d]嘧啶-7-硫酮(9d): 收率74%,纯度99.0%;1H NMRδ: 12.33(br s, 1H), 8.85~8.84(d,J=2.4 Hz, 1H), 7.87~7.84(dd,J=2.4 Hz, 8.8 Hz, 1H), 7.21~7.19(d,J=5.2 Hz, 1H), 4.52(s, 3H), 4.30~4.27(t,J=6.4 Hz, 2H), 3.58~3.55(t,J=5.2 Hz, 2H), 3.10(br s, 4H), 2.96~2.93(t,J=7.2 Hz, 2H), 2.62~2.60(t,J=4.8 Hz, 4H), 2.56~2.53(t,J=5.2 Hz, 2H), 2.16~2.07(m, 2H), 1.90~1.81(m, 2H), 1.23~1.19(t,J=7.2 Hz, 3H), 1.03~1.00(t,J=7.2 Hz, 3H); ESI-MSm/z: 535.0{[M+H]+}。
2结果与讨论
以.1为原料,依次经酰氯化,氨偶合和过氧化氢环化反应合成了5,条件温和,操作简单,收率(60.4%)和纯度(98%)均较高。关键中间体7由6经氯化反应制得。
我们曾尝试了5先与氯磺酸反应,再与哌嗪衍生物反应,最后经硫代反应合成SDF类似物的路线。该路线存在反应时间较长,原料很难反应完全,产品纯化困难等缺点。
参考文献
[1]Bell A, Brown D, Terrett N K. Pyracolopyrinidinone agents:EP 463 756[P].1991.
[2]Boolell M, Allen M J, Ballard S A,etal. Sildenafil:An orally active type 5 cyclic GMP-specific phosphodiesterase inhibitor for the treatment of penile erectile dysfunction[J].Int J Impot Res,1996,8(2):47-52.
[3]Corbin J D, Francis S H. Cyclic GMP phosphodiesterase-5:Target of sildenafil [J].J Biol Chem,1999,274(20):13729-13732.
[4]唐芳,夏志辉,陈笑志. 治疗勃起功能障碍药物的研究现状与进展[J].医药导报,2002,9(9):556-557.
[5]何鹏飞,张培福,丁以绚. 西地那非研究进展[J].中国医学科学院学报,1999,12(6):493-495.
[6]王进欣,储刚,孙飘扬,等. 伐地那非衍生物的合成和体内活性评价[J].化学学报,2007,65(24):2917-2922.
[7]戴慧芳,王红华,熊方均,等. 西地那非合成路线图解[J].中国医药工业杂志,2010,41(2):948-950.
[8]徐宝峰,赵爱华,吴秋业. 西地那非的合成[J].化学研究与应用,2002,14(5):605-607.
[9]宫平,王立新,周华明,等. 柠檬酸西地那非的合成[J].沈阳药科大学学报,2002,19(3):173-174.
[10]邢杰,宫平,钟大放,等. 西地那非哌啶衍生物的负离子电喷雾多级质谱研究[J].质谱学报,2002,23(3):146-150.
[11]仇镇武,叶汝汉,柳亚玲,等. 一种新西地那非类似物的结构确证[J].分析测试学报,2013,32(4):488-493.
[12]笪远锋,黄绎纶,莫文娟,等. 一种西地那非类似物的合成工艺研究[J].中国当代医药,2014,21(5):15-17.
[13]彭安顺,徐宝峰,张爱阳. 邻乙氧基苯甲酸合成方法的改进[J].化学试剂,2002,24(4):238-239.
[14]Venhuis B J, Zomer G, de Kaste D. Structure elucidation of a novel synthetic thiono analogue of sildenafil detected in an alleged herbal aphrodisiac[J].J Pharm Biomed Anal,2008.46(4):814-817.
Synthesis of Sildenafil Analogues
SHUAI Fang-wen1,2,HUANG Zu-yun1,WANG Xiang-feng1,2,LONG Ze-xin1,XIAO Jiang1*
(1. Hunan Engineering Research Center for Pharmaceutical Excipients Co. Ltd., Changsha 410331, China;2. Hunan ER-KANG Pharmaceutical Co.Ltd, Changsha 410331, China)
Abstract:A novel route for synthesizing sildenafil analogue was reported. The key intermediate, sulfur-substituted sildenafil chloride(7), was obtained by a five-step reaction from 2-propoxybenzoic acid. Four novel sildenafil analogues(9a~9d) were synthesized by the reaction of 7 with piperazine derivatives. The yield and purity of 9a~9d were 72.3%~80.9% and 99.0%, respectively. The structures were characterized by1H NMR and ESI-MS.
Keywords:2-propoxybenzoic acid; piperazine; sildenafil analogue; intermediate synthesis; drug synthesis
收稿日期:2015-05-13;
修订日期:2016-03-18
作者简介:帅放文(1966-),男,汉族,湖南长沙人,博士,主要从事药物合成的研究。 E-mail: 461848994@qq.com通信联系人: 肖江,硕士,工程师, E-mail: xiao341@126.com
中图分类号:O621.3; R914.5
文献标志码:A
DOI:10.15952/j.cnki.cjsc.1005-1511.2016.05.15171
