格尔伯特醇制备中镍铝合金与氢氧化钾的协同效应
2016-06-02罗学清周玉鹏孙培永张胜红姚志龙
张 芳,罗学清,周玉鹏,孙培永,张胜红,姚志龙
1.北京石油化工学院,北京1026172.恩泽生物质精细化工北京市重点实验室,北京102617
格尔伯特醇制备中镍铝合金与氢氧化钾的协同效应
张 芳1,2,罗学清1,2,周玉鹏1,2,孙培永1,2,张胜红1,2,姚志龙1,2
1.北京石油化工学院,北京102617
2.恩泽生物质精细化工北京市重点实验室,北京102617
摘要:分别以氢氧化钾为提供碱活性中心的催化剂,镍铝合金为提供金属脱氢活性中心的催化剂,催化癸醇合成二十碳格尔伯特醇反应,考察碱催化活性中心、金属催化脱氢活性中心、以及金属催化脱氢与碱催化活性中心同时存在对格尔伯特反应的影响。结果表明:只有碱催化活性中心存在,与金属催化脱氢与碱催化活性中心同时存在,格尔伯特反应机制不同;金属催化脱氢与碱催化中心之间存在协同效应,碱性活性中心存在的条件下,有利于金属催化醇脱氢生成相应的醛;而仅有金属活性中心时,在常压和液相条件下,醇脱氢生成醛的反应难以实现。
关键词:格尔伯特反应 镍铝合金 氢氧化钾 协同效应
格尔伯特醇(Guerbet alcohols)是一种在β位上带有较长支链的脂肪伯醇。与碳数相同的直链醇相比,格尔伯特醇无色无味,对人体几乎无不良影响,具有凝固点低、挥发性低、刺激性低以及润湿性和渗透性优良等优点,在化妆品、工业润滑剂、表面活性剂、印染印刷化学品、纤维树脂和石油化工等方面有着广泛的应用。格尔伯特醇可以直接用作非离子表面活性剂、溶剂、助剂或润滑材料,也可以作为原料制备阴离子表面活性剂、异构羧酸或增塑剂,还可以用于制备合成酯和多烷基环戊烷等特种合成润滑油[1-4]。
目前制备高碳醇有两种常用方法:一种是羰基合成(OXO)制醇,即烯烃与合成气甲酰化得到醛,然后由醛缩合生成碳数增加一倍的不饱和醛,最后加氢得到碳数较大的醇[3];另一种方法是直接由醇的缩合制备碳数增加的醇[4],醇-醇缩合生成高碳醇的反应称为格尔伯特反应,生成的醇为格尔伯特醇。关于格尔伯特醇的合成机理,一般机理认为反应底物醇在催化剂的作用下失氢生成醛,然后进行羟醛缩合,脱去一分子水得到不饱和烯酮,最后在催化剂作用下选择性加氢得到产物,且认为醇脱氢生成相应的醛是在金属催化剂催化作用下发生的[5,6];而杨春等[7,8]提出,在固体碱催化剂的作用下格尔伯特反应遵循碱活化醇羟基和β-H,然后醇分子间脱水的反应历程。本工作以癸醇为原料通过实验设计,在常压和液相条件下,分别以氢氧化钾为提供碱活性中心的催化剂,镍铝合金为提供金属脱氢活性中心的催化剂,考察碱催化活性中心、金属催化脱氢活性中心,以及同时存在金属催化脱氢活性中心和碱催化活性中心的反应体系中格尔伯特反应的规律,探寻在格尔伯特反应中金属脱氢和碱催化协同效应,为新型格尔伯特反应催化剂的开发提供理论指导。
1 实验部分
1.1 实验方法
称取一定量的原料癸醇(化学纯)和催化剂加入到250 mL三口烧瓶中,油浴加热,控制反应体系温度为230 ℃,三口烧瓶分别连接水循环冷却器和分水器,将反应生成水移出。通过气体质量流量计控制通入反应体系中气体流速,反应在常压下进行,反应结束后,待反应温度降到室温,分离出固体催化剂并称量反应产物,进行色谱或质谱分析。
1.2 分析方法
反应原料及产物分析采用Agilent 公司7890A型气相色谱仪。色谱柱固定相为交联键合聚乙二醇(PEG)的极性RTX-WAX毛细管柱(30 m×0.32 mm×0.5 μm);进样口温度250 ℃;FID检测器,检测器温度设定为250 ℃。
实验产物定性分析采用Shimadzu岛津公司的GC-MS-QP2010型气相色谱-质谱联用分析仪对部分反应产物进行定性分析。色谱条件:色谱柱为HW-5毛细柱(30 m×0.32 mm×0.25 μm),高纯氦气为载气,进样口温度250 ℃,检测器温度为250 ℃,分流比为50:1。质谱条件:EI离子源,电压-0.15 kV,温度200 ℃,接口温度230 ℃,Scan扫描;升温程序:初温35 ℃,保留5 min,以5 ℃/min升至200 ℃,保留5 min。
2 结果与讨论
2.1 碱催化剂的作用及反应机制探讨
以氢氧化钾为催化剂,在230 ℃和常压条件下,考察不同催化剂用量(为反应原料癸醇质量的百分含量)对癸醇缩合制备格尔伯特醇反应的影响。为消除反应过程中空气对反应过程的影响,在反应体系温度升到230 ℃前,反应体系通入氮气来置换体系中的空气,当反应温度升到230 ℃后,停止通入氮气,并控制反应时间2 h,反应结果见表1。

表1 碱催化剂含量的影响Table 1 Effect of content of KOH on Guerbet reaction
由表1数据可以看出,在癸醇缩合合成格尔伯特醇的反应中,碱是有效催化剂,且随着用量的增加,反应转化率与目标产品收率均增加,当用量超过2.0%以后,反应转化率降低,反应选择性却升高。根据一般格尔伯特醇反应机理(如图1所示),反应体系中若没有金属脱氢活性中心,则基本没有中间产物癸醛的生成,反应就不能进行,显然本实验结果与这一机理不符。为验证该格尔伯特醇反应机理,在碱催化条件下,通入空气或氮气,提高原料癸醇脱氢反应速率,则可能会由于醇脱氢产生的氢气被空气和氮气携带,将降低氢转移反应速率,在反应产物中检测到酮或烯醇等中间产物。表2是在不同氮气和空气流速下,碱催化剂含量为2.0%时,原料癸醇转化率与目标产物选择性的结果。

图1 格尔伯特醇缩合反应机理Fig.1 Mechanism of Guerbet reaction by aldol condensation

表2 空气和氮气对反应结果的影响Table 2 Effects of N2and air on Guerbet reaction
由表2可看出,在催化剂氢氧化钾含量为2.0%条件下,无论是在反应体系中通入空气或氮气,原料癸醇的转化率和生成目标产物的格尔伯特醇的选择性均升高,尤其是选择性升高更显著,而且在反应产物中未发现醛、酮等预计的中间产物。反应结果进一步证实了,在只有碱性催化活性中心时,醇-醇缩合并不经过醇脱氢生成醛的中间态,而应遵守碱性催化活性中心活化反应原料癸醇的羟基和与羟基相连的β-H,反应原料癸醇分子间脱水生成目标产物格尔伯特醇,如图2所示。
对于在反应体系中通入空气或氮气提高目标反应的转化率和产物选择性,主要是由于在反应体系中通入空气或氮气,降低了反应体系中水的分压,从而在碱性催化剂作用下,打破活化后的癸醇分子间脱水反应平衡,推动反应向正方向进行。而对比反应体系中通入相同流速的空气和氮气数据,可以看出,通入氮气反应转化率低于通入空气,但选择性显著提高,这主要是由于在反应体系中通入空气,提高了体系中氧含量,使部分原料癸醇发生氧化脱氢反应,原料癸醇生成了癸酸,并进一步与氢氧化钾反应,生成了皂。但提高空气流量后,反应的转化率和目标产物选择性得到提高,这说明在碱催化作用下,原料醇分子间脱水反应速率要高于原料醇的氧化脱氢反应速率。

图2 分子间脱水反应历程Fig.2 Mechanism of Guerbet reaction by dehydration
2.2 金属催化剂的作用
在相同反应条件下,考察了不同金属催化剂含量(为反应原料癸醇质量的百分含量)对癸醇缩合制备格尔伯特醇的反应结果,反应分析结果列于表3。

表3 不同金属催化剂含量的影响Table 3 Effect of content of metal catalyst on Guerbet reaction
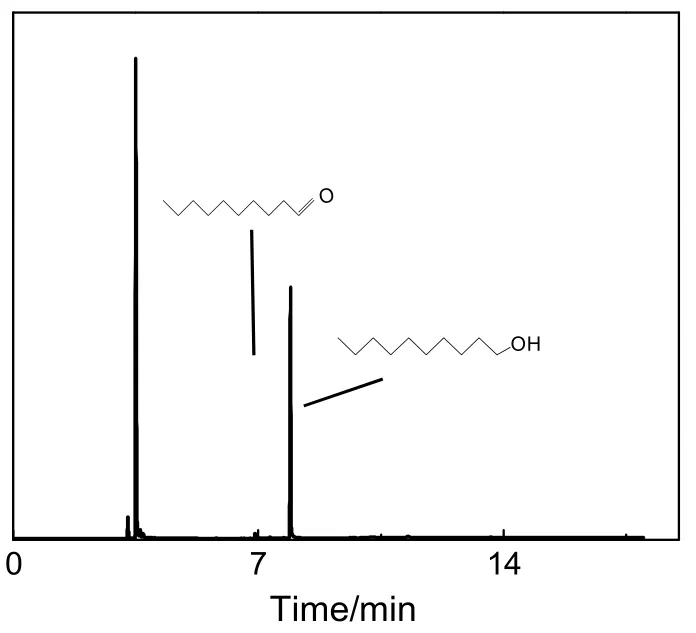
图3 反应产物GC-MS图谱Fig.3 GC-MS spectra of products
图3是反应体系中只引入金属催化剂的反应产物GC-MS分析结果。由表3和图3可看出,在反应体系中只引入金属催化剂,在反应条件下没有目标产物生成,只有微量癸醛生成。说明在液相条件下,癸醇脱氢是很难进行的,而且,癸醛分子间的缩合脱水反应需要碱性催化活性中心,因此,在反应产物中没有目标产物格尔伯特醇,这与文献报道结果一致[5]。
2.3 金属催化剂与碱性催化剂的协同作用
为研究金属催化剂与碱性催化剂的协同作用,分别考察了在碱性催化剂含量为2.0%的条件下,金属催化剂含量对反应结果的影响,以及在金属催化剂含量为1.5%的条件下,碱催化剂含量对反应结果的影响,结果分别列于表4和5。
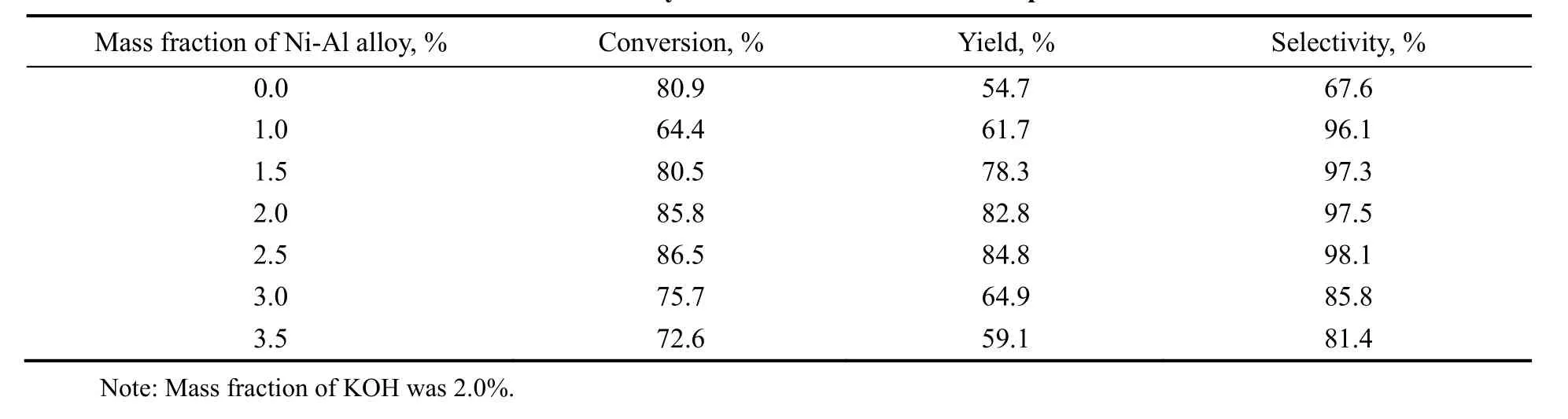
表4 碱性催化剂存在下不同含量金属催化剂对反应的影响Table 4 Effect of metal catalyst on the Guerbet reaction at presence of KOH

表5 金属催化剂存在下不同含量碱催化剂对反应的影响Table 5 Effect of KOH on Guerbet reaction at the presence of Ni-Al alloy
由表4可看出,在反应体系中碱性催化剂含量为2.0%不变的条件下,当在反应体系中引入1.0%的金属催化剂后,反应转化率大幅度下降,但目标产物选择性急剧上升,这说明金属催化剂的引入,格尔伯特醇合成反应途径可能发生了改变。另外,随着金属催化剂加入量的增大,反应转化率和目标产物选择性均先升高后降低,目标产物选择性先维持在一个相当高的水平,当金属催化剂加入量达到3.0%后,转化率与选择性又明显降低,同时反应产物中出现明显的皂化物。这可能是由于金属催化剂与碱性催化剂同时存在于反应体系中,二者之间有协同效应。当金属催化剂量增加,反应体系中有利于醇脱氢的活性中心数增多,从而反应转化率升高,而随着金属脱氢活性中心数进一步增加,但体系中碱性活性中心数不变,由于反应体系并未与空气完全隔绝,随着金属脱氢活性中心数的增加,醇脱氢生成醛的中间化合物量增加,导致中间产物醛被空气进一步氧化为酸,并与体系中作为缩合催化活性中心的碱反应生成皂,降低了反应体系中碱性活性中心数,从而导致反应转化率和目标产物选择性同时降低,这进一步说明在金属催化剂与碱性催化剂同时存在于反应体系中,二者应存在较强的协同效应。
由表5可知,当反应体系中金属催化剂含量不变的条件下,随着碱性催化剂的加入,反应转化率和选择性均升高。这进一步说明在反应体系中同时存在金属和碱催化活性中心,反应的历程与碱催化不同。而表3中数据表明,在反应条件下,当金属催化剂含量为1.5%时,金属催化剂本身基本不能催化醇发生脱氢生成醛反应的发生,或者说金属催化剂催化醇脱氢反应速率很低,但当反应体系中同时存在碱性活性中心时,使醇脱氢反应能很好的进行,这进一步说明金属与碱活性中心存在相互协同效应,且反应可能是由于金属催化剂的存在,反应底物伯醇分子上与羟基相连的α-H在碱性活性中心的作用下得到活化,与金属催化剂相作用而形成了活泼H。为验证上述设想,在金属和碱催化剂同时存在的反应体系中通入空气或氮气,考察其反应结果。金属催化剂含量为1.5%,碱催化剂加入量为1.5%的配比组成中,氮气或空气流速均控制在10 mL/min,在上述相同条件下进行反应。通入空气的反应产物基本上不含目标产物格尔伯特醇,几乎完全是皂;而通入氮气后的反应产物色谱图也与以前不同,如图4a所示,与不通氮气的产物色谱图(如图4b)相比,在原料癸醇与产品格尔伯特醇之间出现了两个新物种峰,且含量较高。对通入氮气反应产物进行了GC-MS分析,结果表明,在原料癸醇与产物格尔伯特醇之间的新物种峰归属于醛和烯醇,且醛的含量显著高于烯醇。这进一步证实了,金属催化活性中心与碱催化活性中心同时存在的条件下,醇能实现脱氢转化为相应的醛,这可能是由于碱基团对伯醇羟基间存在相互作用,使与伯醇上与羟基相连的α碳上的H与α碳,以及与羟基上与氧相连的H之间的σ键弱化,易于被金属催化中心吸附,从而使醇转化为相应的醛。这与反应体系中只有碱基团存在的条件下,醇发生β-H活化的机制也不同。

图4 反应产物GC-MS图谱Fig.4 GC-MS spectra of products
可见,在格尔伯特反应中,同时存在碱性催化活性中心和金属催化活性中心,两者之间存在相互协同效应,且醇脱氢转化为醛是反应的控制步骤;格尔伯特反应遵循醇脱氢生成醛、羟醛缩合、烯醛加氢的反应机理,反应历程如图5所示。

图5 金属与碱活性中心同时存在格尔伯特反应历程Fig.5 Mechanism of Guerbet reaction over metal and KOH catalysts
3 结 论
醇缩合实现碳链增长的格尔伯特反应,在不同催化剂体系作用下,遵循不同的反应机制。在常压,液相条件下,只有金属脱氢催化活性中心时,醇难以发生脱氢生成相应醛的反应;只有碱催化活性中心的反应体系中,格尔伯特反应遵循醇分子间脱水的反应机制;反应体系中同时存在碱催化和金属脱氢催化活性中心时,金属脱氢催化活性中心与碱催化活性中心存在协同效应,碱性催化活性与醇羟基发生强相互作用,使醇上与羟基相连的α碳上的H与α碳,以及与羟基上与氧相连的H之间的σ键弱化,在金属脱氢催化活性中心的作用下,实现醇脱氢生成相应的醛反应发生。
参考文献:
[1] 田烈光. 格尔伯特醇及其衍生物[J]. 合成润滑材料, 1998, 15(1): 19-22. Tian Lieguang. Guerbet alcohol and its deviations[J]. Synthetic Lubricants, 1998, 15(1): 19-22
[2] 靳志强, 王涵慧, 俞稼镛. Guerbet十四醇的合成与表征[J]. 精细化工, 2002, 19(1): 9-11. Jin Zhiqiang, Wang Hanhui, Yu Jiayong. Synthesis and characterization of Guerbet tetradecyl alcohol[J]. Fine Chemicals, 2002, 19(1): 9-11.
[3] 刘 春, 梅建庭, 金子林. 铑催化高碳烯烃氢甲酰化合成高碳醇进展[J]. 化工进展, 2000, 19(1): 28-31. Liu Chun, Mei Jianting, Jin Zilin. A review on hydroformylation of higher olefins to higher alcohol over rhodium catalysts[J]. Chemical Industry and Engineering Progress, 2000, 19(1): 28-31.
[4] Ndou A S, Plint N, Coville N J. Dimerisation of ethanol to butanol over solid-base catalysts[J]. Appl Catal A: Gen, 2003, 251(2): 337-345.
[5] Weizmann C, Bergmann E, Sulzbacher M. Further observations on the Guerbet reaction[J]. J Org Chem, 1950, 15(1): 54-57.
[6] Dvornikoff M N, Farrar M N. Condensation of alcohols[J]. J Org Chem, 1957, 22(5): 54-57.
[7] Yang C, Meng Z Y. Bimolecular condensation of ethanol to 1-butanol catalyzed by alalicationzelites[J]. J Catal, 1993,142(1): 37-44.
[8] 杨 春, 孟中岳. 沸石的碱性催化乙醇双分子缩合反应[J]. 化学学报, 1993, (51): 79-84. Yang Chun, Meng Zhongyue. Basic catalysis of zeolites-bimolecular condensation of ethano[J]. Acta Chimica Sinica, 1993, (51): 79-84.
Catalytic Synergistic Effects of Ni-Al Alloy and KOH in Guerbet Reaction
Zhang Fang1,2, Luo Xueqing1,2, Zhou Yupeng1,2, Sun Peiyong1,2, Zhang Shenghong1,2, Yao Zhilong1,2
1.Beijing Institute of Petrochemical Technology, Beijing 102617, China;
2.Beijing Key Laboratory of Enze Biomass Fine Chemical, Beijing 102617, China
Abstract:C20Guerbet alcohol was synthesized from n-decanol over Ni-Al alloy catalyst, KOH catalyst, and Ni-Al alloy catalyst with KOH, respectively. The results indicated that the mechanism of Guerbet reaction over KOH was different from that over Ni-Al alloy catalyst with KOH. The dehydrogenate activity of metal catalyst was promoted by the synergistic effect of Ni-Al alloy and KOH. It was difficult to dehydrogenate n-decanol to form decanal catalyzed by metal catalyst only under normal pressure in liquid phase.
Key words:Guerbet reaction; Ni-Al alloy; potassium hydroxide; synergistic effect
基金项目:北京市长城学者计划(CIT&TCD20150316)。
作者简介:张 芳(1990—),女,硕士研究生;姚志龙(1971—),男,研究员,通讯联系人。E-mail: yaozl@bipt.edu.cn。
收稿日期:2015-11-27;
修订日期:2016-02-01。
文章编号:1001—7631 ( 2016 ) 02—0152—06
中图分类号:TQ032.4
文献标识码:A
