一测多评法测定咽立爽口含滴丸中的4种成分
2016-06-01游正琴吴琳琳茅向军
游正琴, 罗 奕, 吴琳琳, 茅向军, 苏 菊
(1.贵州医科大学,贵州贵阳550004;2.贵州省食品药品检验所,贵州贵阳550004)
一测多评法测定咽立爽口含滴丸中的4种成分
游正琴1,2, 罗奕1, 吴琳琳1, 茅向军2*, 苏菊1
(1.贵州医科大学,贵州贵阳550004;2.贵州省食品药品检验所,贵州贵阳550004)
摘要:目的 建立一测多评法(QAMS)同时测定咽立爽口含滴丸中薄荷酮、樟脑、薄荷脑和龙脑的含有量。方法分析采用DB-WAX毛细管柱(30 m×0.32 mm×0.25 μm);载气为氮气;FID检测器;升温程序为初始柱温55℃,以1℃/min速率升至75℃,再以5℃/min速率升至105℃,维持10 min。以龙脑为内参物,建立其与薄荷酮、樟脑、龙脑的相对校正因子,并将其应用于计算,同时内标法对4种成分进行含有量测定。然后,比较两种方法的结果。结果薄荷酮在0.056 8~0.511 1 mg/mL、樟脑在0.058 7~0.528 0 mg/mL、薄荷脑在0.399 2~1.995 8 mg/mL、龙脑在0.724 8~3.624 1 mg/mL范围内线性关系良好,平均回收率(n =3)分别为97.07%(RSD=1.23%)、96.68% (RSD=1.38%)、98.57%(RSD=1.82%)、99.50%(RSD=1.20%)。龙脑与薄荷酮、樟脑、薄荷脑的相对校正因子分别为1.024 1、1.018 5、1.013 0,而且一测多评法的计算结果与内标法无明显差异。结论 该方法准确可靠,可控制咽立爽口含滴丸的质量。
关键词:咽立爽口含滴丸;薄荷酮;樟脑;薄荷脑;龙脑;一测多评法(QAMS);内标法
咽立爽口含滴丸是由艾片、艾纳香油、薄荷素油、薄荷脑和甘草酸单铵盐组成的苗药复方制剂,用于急性咽炎、慢性咽炎急性发作、咽痛、咽黏膜红肿、咽干、口臭等症,其现行局颁标准在挥发性成分中仅测定了薄荷脑和龙脑的含有量[1],不能全面控制该复方制剂的质量。本实验同时测定咽立爽口含滴丸中薄荷酮、樟脑、薄荷脑和龙脑的含有量,并且引入一测多评法[2-5],以含有量相对较高、便宜易得的龙脑为内参物。然后,将该方法和常规内标法进行比较,以期更全面有效地控制该制剂的质量。
1 仪器与材料
1.1 仪器 Agilent 7890N气相色谱仪、Ailgent 7693自动进样装置、氢火焰化检测器(SPH-500氢气发生器,A-10全自动空气源);DB-WAX毛细管柱(30 m×0.32 mm× 0.25 μm);XS 205电子天平;KQ-300 DE超声波数控清洗器。
1.2 材料 薄荷酮(批号11706-201205)、樟脑(批号110747-201008)、薄荷脑(批号110728-200506)和龙脑(批号110881-201107)对照品均购自中国食品药品检定研究院。水杨酸甲酯和乙醇均为分析纯。咽立爽口含滴丸样品(批号20140630、20140701、20141203、20141204、20141205、20141208、20141209、20141221、20150310、20150311、20150413)和阴性样品由贵州黄果树立爽药业有限公司提供。
2 方法与结果
2.1 色谱条件 DB-WAX毛细管柱(30 m×0.32 mm× 0.25 μm);载气为氮气(14 mL/min)、氢气(40 mL/min)、空气(400 mL/min);体积流量1.0 mL/min;进样口温度220℃;检测器(FID)温度250℃;分流比10∶1;进样量1 μL;程序升温(初始55℃,以1℃/min速率升至75℃,再以5℃/min速率升至105℃,保持10 min)。
2.2 溶液制备
2.2.1 对照品贮备液 精密称取薄荷酮、樟脑、薄荷脑、龙脑对照品适量,置于10 mL量瓶中,乙醇稀释至刻度,制成质量浓度分别为薄荷酮2.840 mg/mL、樟脑2.934 mg/mL、薄荷脑9.979 mg/mL、龙脑18.120 mg/mL的对照品贮备液。
2.2.2 内标溶液 精密称取水杨酸甲酯适量,置于100 mL量瓶中,乙醇稀释至刻度,制成质量浓度为11.738 2 mg/mL的内标溶液。
2.2.3 混合对照品溶液 精密量取“2.2.2”项下内标溶液和“2.2.1“项下对照品贮备液适量,置于5 mL量瓶中,乙醇稀释至刻度,制成质量浓度分别为薄荷酮0.284 0 mg/mL、樟脑0.293 4 mg/mL、薄荷脑0.798 3 mg/mL、龙脑1.449 6 mg/mL、水杨酸甲酯1.173 8 mg/mL的混合对照品溶液。
2.2.4 供试品溶液 取样品研细,精密称取0.2 g,置于具塞锥形瓶中,精密加入“2.2.2”项下内标溶液1 mL,再精密加入乙醇9 mL,密塞称重,超声处理(300 W、40 kHz)5 min,放冷,乙醇补足减失的质量,摇匀,即得。
2.2.5 阴性供试品溶液 按处方量制备缺艾片、艾纳香油、薄荷脑和薄荷素油的阴性供试品,再按“2.2.4”项下方法制备阴性供试品溶液。
2.3 系统适用性 在“2.1”项色谱条件下,精密吸取“2.2”项下混合对照品、供试品、阴性供试品溶液各1 μL注入气相色谱仪中分析,结果见图1。由图可知,各色谱峰均达到基线分离,而且各待测成分色谱峰的理论塔板数均大于15 000,而且阴性供试品溶液对待测成分无干扰。
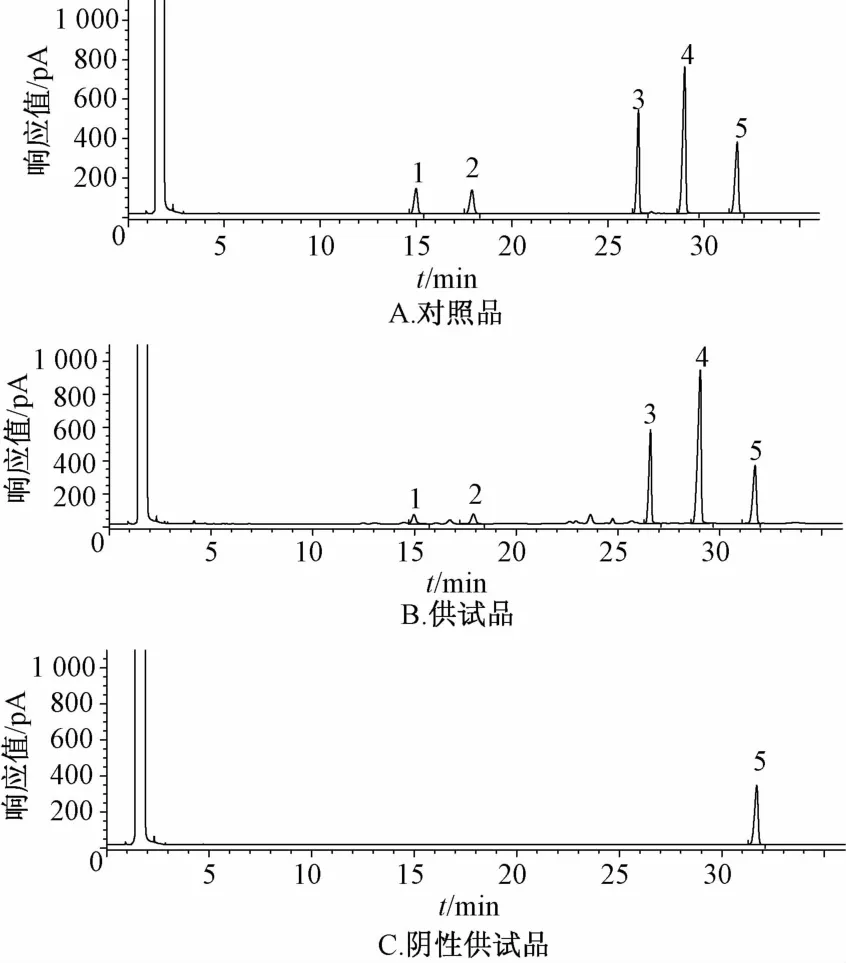
1.薄荷酮 2.樟脑 3.薄荷脑 4.龙脑 5.水杨酸甲酯图1 各成分色谱图
2.4 方法学验证
2.4.1 线性关系考察 分别精密量取“2.2.1”项下薄荷酮、樟脑对照品贮备液0.1、0.3、0.5、0.7、0.9 m L,薄荷脑、龙脑对照品溶液0.2、0.4、0.6、0.8、1.0 mL,置于5 mL量瓶中,精密加入“2.2.2”项下水杨酸甲酯溶液0.5 mL,加乙醇溶液至刻度,摇匀,制得标准系列溶液,在“2.1”项色谱条件下进样,测定峰面积。以对照品溶液与内标溶液质量浓度的比值为横坐标(X),两者峰面积的比值为纵坐标(Y)进行回归,结果见表1,表明4种成分在各自范围内均呈现出良好的线性关系。
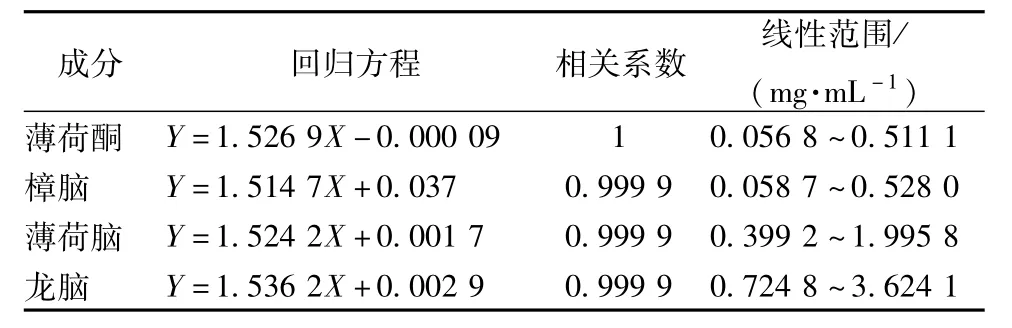
表1 4种成分的回归方程及线性范围
2.4.2 精密度试验 取“2.2.3”项下混合对照品溶液适量,在“2.1”项色谱条件下连续进样6次,测得薄荷酮、樟脑、薄荷脑和龙脑的峰面积RSD值分别为0.09%、0.06%、0.19%、0.30%,表明仪器精密度良好。
2.4.3 稳定性试验 取同一供试品溶液(批号20140701)适量,在“2.1”项色谱条件下分别于0、2、4、8、12、18、24 h测定,测得薄荷酮、樟脑、薄荷脑和龙脑与内标物峰面积比值的RSD分别为0.84%、0.59%、0.60%、0.62%,表明供试品溶液在24 h内稳定性良好。
2.4.4 重复性试验 精密称取同一批样品(批号20140701)0.2 g,平行6份,按“2.2.4”项下方法制备供试品溶液,测得薄荷酮、樟脑、薄荷脑和龙脑含有量分别为7.74、8.68、45.41、98.34 mg/g,RSD分别为0.97%、1.13%、0.78%、0.87%,表明该方法重复性良好。
2.4.5 加样回收率试验 取含有量已知的样品(批号20140701)研细,精密称定9份,每份0.1 g,置于10 mL量瓶中,分别按各成分质量浓度的80%、100%、120%精密加入薄荷酮、樟脑、薄荷脑、龙脑的对照品贮备液,再加入内标溶液1 mL,乙醇定容,按“2.2.4”项下方法制备供试品溶液,在“2.1”项色谱条件下测定,结果见表2。

表2 加样回收率试验结果(n=3)
2.5 相对校正因子的计算及耐用性验证
2.5.1 相对校正因子的计算 取“2.2.3”项下混合对照品溶液,在“2.1”项色谱条件下分别进样0.5、0.8、1.0、1.5、2.0 μL,记录各组分峰面积。按公式RCF =计算龙脑与薄荷酮、樟脑与薄荷脑之间的相对校正因子。其中,As为龙脑对照品的峰面积,Cs为龙脑对照品的质量浓度,Ai为某待测成分(薄荷酮、樟脑和薄荷脑)的峰面积,Ci为某待测成分(薄荷酮、樟脑和薄荷脑)的质量浓度。结果见表3。
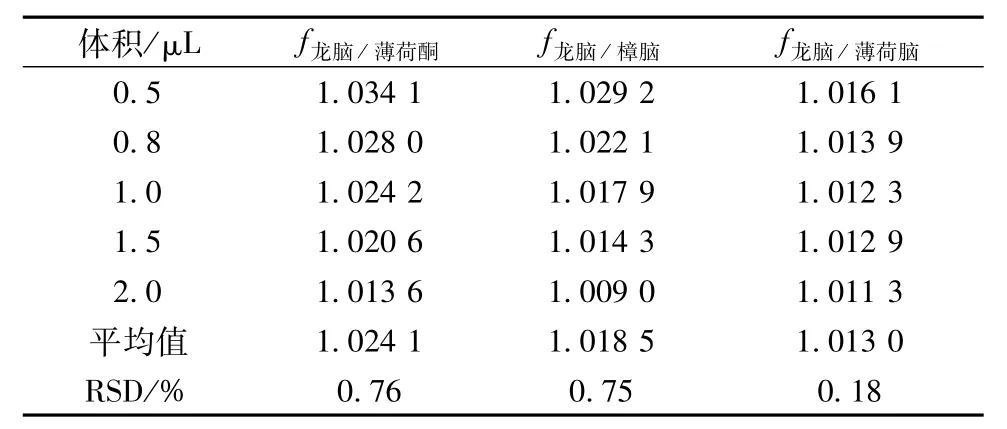
表3 4种成分的相对校正因子(n=2)
2.5.2 耐用性验证 按“2.5.1”项下方法考察了2种气相色谱系统(Agilent 7980和岛津GC-2014)和3种不同品牌色谱柱[DB-WAX、Rtx®-WAX、Elite-WAX毛细管柱(30 m×0.32 mm×0.25 μm)],以龙脑为内标物,计算薄荷酮、樟脑和薄荷脑的RCF值及RSD值,结果见表4,表明不同气相色谱系统和色谱柱对4种成分相对校正因子的影响均较小。
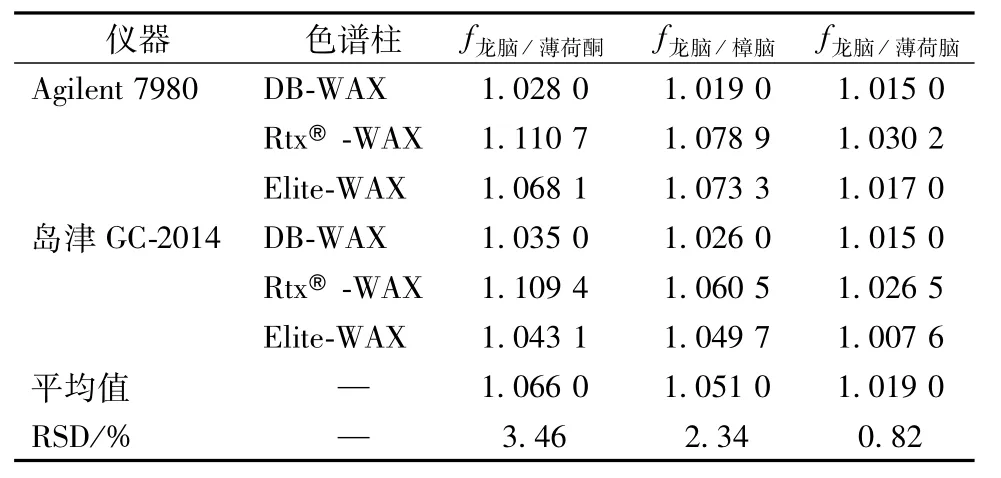
表4 不同气相色谱系统和色谱柱测得的相对校正因子(f)
2.6 待测色谱峰的定位 通过计算在上述不同气相色谱系统和色谱柱中各待测成分色谱峰与龙脑色谱峰的相对保留时间,对各成分进行定位,结果见表5,表明相对保留时间随不同气相色谱系统和色谱柱的变化较小,即可采用相对保留时间进行定位。
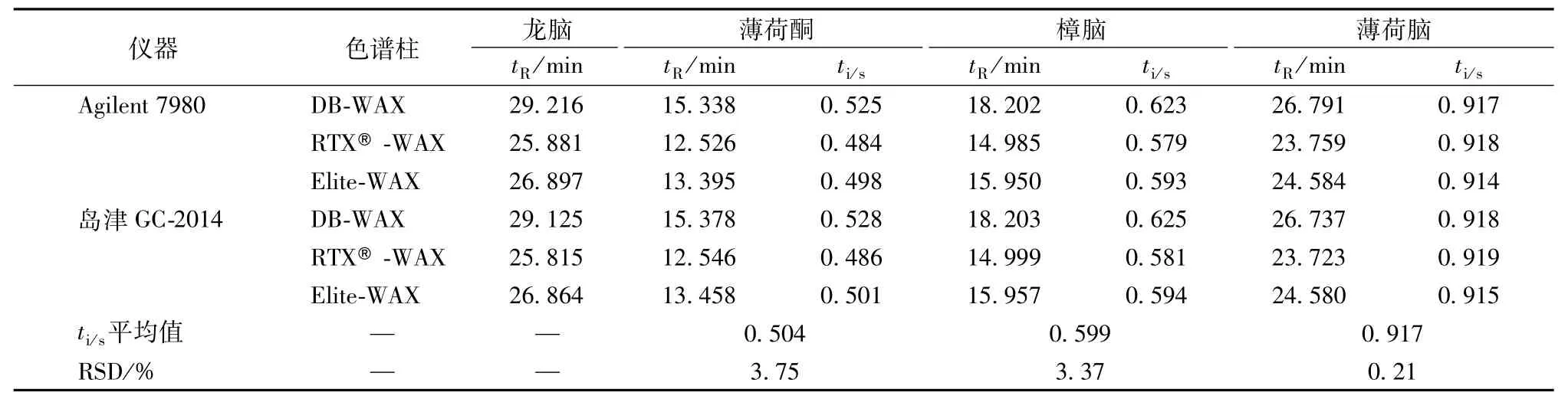
表5 不同仪器和色谱柱测得的相对保留时间(t i/s)
2.7 一测多评法和内标法测定结果的比较 取咽立爽口含滴丸11批,按“2.2.4”项下方法制备供试品溶液,在“2.1”项色谱条件下进行测定,分别以内标法和一测多评法计算供试品溶液中各待测成分的含有量,并采用准确度[6]来评价两者的接近程度,结果见表6。由表可知,两种方法无显著性差异,即一测多评法可用于咽立爽口含滴丸的质量控制。

表6 内标法和一测多评法测定结果的比较(mg/g,n=2)
3 讨论
原标准采用水饱和乙酸乙酯作为供试品溶液的溶剂,但在低温(低于15℃)下溶剂中的水会和乙酸乙酯产生一定程度的分离,从而影响待测成分的溶解度[7]。本实验在同一温度下分别考察了甲醇、乙醇、无水乙醇和水饱和乙酸乙酯的提取率,发现四者无明显差异。然而,无水乙醇和水饱和乙酸乙酯溶液在低温储存过程中会析出白色沉淀,而甲醇和乙醇稳定性良好,故最终选择毒性小、无污染的乙醇作为溶剂。
原标准在恒温(140℃)下分离薄荷脑和龙脑,但无法将薄荷酮和樟脑完全分离。本实验采用程序升温(初始55℃,以1℃/min速率升至75℃,再以5℃/min速率升至105℃,保持10 min),发现在该条件下4种成分可完全分离,分离度均大于5.0。
薄荷酮来源于薄荷素油,而樟脑来源于艾片和艾纳香油。现代药理研究表明[8-9],薄荷酮和樟脑具有重要的药理活性,故增加两者作为该制剂质量控制的指标成分。另外,龙脑作为处方中艾片和艾纳香油的主要成分,含有量较高,价格便宜,容易获取,故选择其作为一测多评法的内参物。
除采用准确度对两种方进行相关性分析外,还以相关系数和夹角余弦来进行分析。结果,11批样品中薄荷酮相关系数为0.998 995,夹角余弦为0.999 993;樟脑相关系数为0.999 777,夹角余弦为0.999 993;薄荷脑相关系数为0.999 802,夹角余弦为1.000 00,表明这两种方法无显著性差异。
本实验根据《一测多评法建立的技术指南》[10],建立了龙脑相对于薄荷酮、樟脑和龙脑的相对校正因子,并对其适应性进行考察。然后,通过比较一测多评法和内标法的测定结果来验证其准确性。结果表明,该方法能通过测定咽立爽口含滴丸中4种指标性成分的含有量,从而更有效地控制该制剂的质量。
参考文献:
[1] WS-10237(ZD-0237)-2002-2011Z,咽立爽口含滴丸[S].
[2] 沈小钟,刘 瑶,杨燕军,等.一测多评法研究进展[J].中国药业,2013,22(13):1-5.
[3] 董 宇,陈 新.一测多评法在舒肝健脾丸质量控制中的应用[J].中国实验方剂学杂志,2014,20(4):70-73.
[4] 高慧敏,宋宗华,王智民,等.适合中药特点的质量评价模式—QAMS研究概述[J].中国中药杂志,2012,37 (4):405-416.
[5] 付滢舟,冯有龙,曹 玲,等.一测多评法测定速效救心丸中冰片的含量[J].药物分析杂志,2012,32(5):775-778.
[6] 赵一懿,郭洪祝,陈有根,等.中药多组分含量测定中相对校正因子计算方法的比较与建议[J].中国药品标准,2014,15(4):245-251.
[7] 熊慧林,叶阳明,林开中.气相色谱法测定咽立爽滴丸中艾片、薄荷脑的含量[J].药物分析杂志,1998(S1):104-106.
[8] 汤 奇,杨发龙,曾 南,等.荆芥挥发油及其主要成分抗流感病毒作用研究[J].中药药理与临床,2012,28 (2):29-32.
[9] 丁元刚,马红梅,张伯礼.樟脑药理毒理研究回顾及安全性研究展望[J].中国药物警戒,2012,9(1):38-42.
[10] 王智民,钱忠直,张启伟,等.一测多评法建立的技术指南[J].中国中药杂志,2011,36(6):657-658.
*通信作者:茅向军(1964—),男,博士,主任药师,研究方向为药品质量标准。Tel:(0851)86808857,E-mail:1074459931@ qq.com
作者简介:游正琴(1987—),女,硕士生,初级药师,研究方向为药品质量标准。Tel:18275629973,E-mail:2640437537@qq.com
基金项目:贵州省中药现代化科技产业研究开发专项项目(黔科合中药字20125030);贵阳市科技计划项目(筑科合同2012204-1)
收稿日期:2015-11-10
doi:10.3969/j.issn.1001-1528.2016.05.049
中图分类号:R284.1
文献标志码:B
文章编号:1001-1528(2016)05-1180-04
