硅烷的生产工艺研究进展
2016-05-27罗建志李丹丹孙秋丽
柳 彤,罗建志,李丹丹,孙秋丽
(中国船舶重工集团公司 第七一八研究所,河北 邯郸 056027)
硅烷的生产工艺研究进展
柳彤,罗建志,李丹丹,孙秋丽
(中国船舶重工集团公司 第七一八研究所,河北 邯郸 056027)
摘要:硅烷在现代电子工业中应用非常广泛。简介了硅烷的性质及应用;介绍了硅烷的几种合成工艺,催化歧化法是工业化生产最为可行的方法;概述了硅烷的纯化方法;对硅烷产业的发展前景进行了展望。
关键词:硅烷;合成;纯化
硅烷(silane)在现代高科技中被广泛应用并且越来越重要,首先是与它的特性有关,同时也与现代高技术的特殊需求有关。通过热分解或与其它气体的化学反应,可由硅烷制得单晶硅、多晶硅、非晶硅、金属硅化物、氮化硅、碳化硅、氧化硅等一系列含硅物质。利用硅烷可以实现最高的纯度、最精细(可达原子尺寸)的控制和最灵活多变的化学反应。从而将各种含硅材料按各种需要制成复杂精细的结构,这正是现代具有各种特异功能的材料和器件所要求的基本条件。
硅烷已成为半导体微电子工艺中使用的最主要的特种气体,用于各种微电子薄膜制备,包括单晶膜、微晶、多晶、氧化硅、氮化硅、金属硅化物等。硅烷的微电子应用还在向纵深发展:低温外延、选择外延、异质外延。不仅用于硅器件和硅集成电路,也用于化合物半导体器件(砷化镓、碳化硅等)。在超晶格量子阱材料制备中也有应用。可以说现代几乎所有先进的集成电路的生产线都需用到硅烷。硅烷的纯度对器件性能和成品率关系极大,更高级的器件需要更高纯度的硅烷。
1硅烷的物化性质[1]
硅烷的分子式为SiH4,分子量为32。1个大气压下熔点为-184.7 ℃,沸点为-112 ℃,0 ℃和1个大气压下的气体密度为1.44 g/m3,-185℃下的液体密度为711 kg/m3。
硅烷为极活泼压缩气体,与空气接触可能自燃,与空气混合形成爆炸性混合物。加热或燃烧时,该物质分解生成硅和氢气。该物质是一种强还原剂,与氧化剂反应,与水缓慢反应,与氢氧化钾溶液和卤素反应。于600℃即以晶态硅分解出来。
2硅烷的制备方法
2.1非均化法制备SiH4[2-3]
2.1.1反应原理
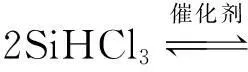
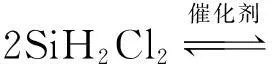
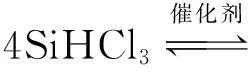
即在催化剂的催化下,在一定的压力1~8 atm(注:1 atm=101.325 kPa)和温度-80~120 ℃下,SiHCl3本身发生不均匀的歧化反应。歧化反应可通过三步来完成:首先由SiHCl3制备SiH2Cl2;再由SiH2Cl2制备SiH3Cl;最后由SiH3Cl生成SiH4和SiCl4。
2.1.2歧化反应具备的条件
高度氯化的硅烷通过具有催化床反应器逐步发生歧化反应,最后得到SiH4和SiCl4。其反应条件是:
压力:0.1~30 atm,优选1~8 atm;温度:-120~180 ℃,优选-80~120 ℃。催化剂:1. 具有叔氨基的大孔离子交换树脂;2. 烷基氨基三烷氧基硅烷改性;3. 氨基官能化的聚苯乙烯;4. 有机聚硅氧烷;5. 氨基官能化的无机载体。
2.1.3反应装置[2]

图1 催化歧化装置图
2.1.4歧化制备简述
歧化制备SiH4关键的设备为具有催化床的反应器。由于相对慢的歧化反应,为了确保反应物在催化剂上的充分停留时间,即为了要达到近似化学平衡而确保在催化剂上的低空速,就必须使得反应器反应空间大,来实现最大可能的转化。催化剂床的安装必须有利于反应物的通过,即阻力要小。为了保证催化剂床的反应温度,反应器上必设有夹套通过冷却或加热而方便的调节或控制。
由于歧化反应转化率受化学平衡限制的制约,这种情况需要从未反应的原料中将反应物及时分离出来,以达到使整个过程转化完全的目的。这就要求配套反应器的装置须有分离反应原料和产物的功能即具有蒸馏、冷却分离系统,将产品分离出来,而未反应的原料和中间反应物随新补充的高氯硅烷再送回反应器。
2.1.5歧化制备SiH4需引起重视的问题
1. 由于歧化反应速率慢,需要反应器的催化床有尽可能大的空间,使反应物与其有大的接触界面,来弥补反应速率低的不足,因此反应器的尺寸相对要大,且催化床中的催化剂易更换和活化再生。为了确保连续反应和反应速率,须并联多个反应器。
2. 由于歧化反应速率受化学平衡的制约,因此必须设计蒸(精)馏、冷却系统,将反应产物从未反应的原料中及时分离出来。将未反应的原料和中间产物再送回反应器,使其转化完全。
3. 该歧化法生产所用的原料和产物,均属化学活性物质。除SiCl4外与空气接触有燃烧和爆炸的危险,氯硅烷与水或蒸汽接触生成SiO2和HCl,其SiO2沉积物可堵塞系统的管道。另一方面系统的反应压力又偏高。因此其生产装置的各个系统要求加工精确、严密,绝对不能漏气。尤其是所使用的阀门等部件要求的质量要高,在30 atm下不漏气。
4. 从第2.1.1节歧化反应原理可得知,由4 mol的SiHCl3催化歧化生成1 mol的SiH4和3 mol的SiCl4。其产物SiH4和SiCl4的体积比为1:3,质量比为0.063。也就是说1000 kg的SiHCl3只能产出59.3 kg的SiH4,其余产品为SiCl4,这是歧化方法的严重缺陷。原料这么低的利用率,必须考虑将SiCl4再转化成SiHCl3,以达到提高原料利用率的目的。这样就不可避免的增加SiCl4转化成SiHCl3的新问题。
根据沈祖祥等人[4]所提供的转化方法即首先将触媒镍粉与硅粉按一定比例混合均匀后,在H2气氛和一定温度范围下活化处理。然后将SiCl4与H2按一定比例混合通到活化过的镍硅触媒剂层而实现氢化反应。其反应温度为400~500 ℃,压力为1.2~1.5 MPa,接触反应时间为10~100 s。同样本转化方法要求的压力相对较高,要求反应设备加工必须精确严密,对使用的阀门等部件要求的质量也相当高。
2.2硅化镁(Mg2Si)法[5]
2.2.1原理
Mg2Si+NH4Cl→SiH4+2MgCl2+4NH3
2.2.2制备方案描述
该方法制备SiH4所用原料是在H2气的环境中将硅粉和活性镁粉加热到500~600℃制取的,进行反应的镁粉应过量10%~20%,才能反应的更充分。
硅化镁法制备SiH4需在液氨中进行,先将液氨和硅化镁加入到反应器中,然后逐步向反应器中少量加入氯化铵或滴加盐酸,随着白色烟雾的散发,硅烷混合气体就产生了。
由于NH3对各种金属离子有络合作用,因此生成的SiH4所含金属杂质相对较少。粗制的SiH4采用精馏、吸附、络合、吸收等净化工艺,可制造高纯SiH4。此方法在SiH4生产史上持续了近1/4世纪,至今仍有一些制造商采用此工艺。
2.2.3硅化镁法制备SiH4存在的问题
用氯化铵或盐酸逐渐加入到存有Mg2Si和液氨的反应器中生成的是包含SiH4、Si2H6、Si3H8等物质的混合物,其中硅烷中所用的硅仅占全部反应硅含量的14%左右,其产率较低。
2.3金属氢化物与氯(氢)硅烷反应法[6]
2.3.1原理
SiCl4+LiAlH4→SiH4+LiCl+AlCl3
2.3.2制备方案描述
该合成硅烷方法是采用强还原剂LiAlH4在二甲醚四氢呋喃的溶剂中,通过还原反应产生硅烷,而粗制硅烷再经蒸馏提纯等得到高纯度的硅烷。由于SiCl4和LiAlH4化学活性较强,反应剧烈,需谨慎处理,因此不易大规模生产。
该反应分二级来完成,反应的温度范围为350~410 ℃,在一级反应器里将供有的氯代硅烷和氢化锂形成熔盐混合物和没反应的氢化锂。二级反应器里有氯代硅烷、熔盐混合物和一级反应器中转来的没有反应的氢化锂,将反应生成的硅烷通过蒸馏柱分离,分离出的氯代硅烷再返回至一级反应器或二级反应器。
2.4几种方法比较
硅化镁(Mg2Si)法源于1935年,生产历史长。我国在20世纪70年代为满足超纯硅生产的需要,也开始研制生产硅烷。当时曾建起数家生产厂,生产净化工艺基本上引用了硅化镁生产法,由于受当时条件的限制,大多数工厂只是做了大量的先期工作,而最终停产。另一方面硅化镁法也存在硅烷产率低的问题,在生产出的产品中硅烷仅占反应硅的14%左右,其余产品是多元硅烷。因此该生产方法目前尽管国际上有些公司在应用,但已走势枯萎。
金属氢化物与氯硅烷反应生产硅烷法,只适合小规模生产方式,对小规模生产也较适用方便。但由于SiCl4和LiAlH4等属化学活性很强的物质,反应剧烈,需倍加谨慎处理,不太适合大规模生产。
非均匀化法制备硅烷,是目前国际上通用的工业生产方法,也是一种可以生产几种硅源气体(SiH4、SiH2Cl2、SiHCl3)的理想方法。本方法可首先合成生成SiHCl3或由SiCl4转化成SiHCl3,再由SiHCl3于催化床中,在一定的温度和压力条件下,逐步进行歧化反应最终可得到硅烷产品。由于该方法歧化速率受化学平衡的制约,要求需将歧化反应产物及时的从反应混合物中分离出来,须有严格的蒸(精)馏冷却系统工作,这样严格分离出的产品,其纯度也相对较高。
本方法生产硅烷,如原料由购进的SiHCl3开始歧化,最终产出硅烷和SiCl4。其SiH4产品重量仅占产品SiCl4的6.3%,占产物总质量的5.93%。因此,必须将SiCl4转化成SiHCl3才有实际生产的意义。
3硅烷的纯化方法
硅烷主要应用于半导体行业,产业的精密程度对于原料气硅烷的要求很高,工业化合成的硅烷中根据生产工艺的不同存在很多种类不同的杂质,这就需要对粗品硅烷依据杂质的物化性质选择相应的纯化方法进行处理,主要的方法有吸附、冷凝分离法、精馏等方法。
3.1吸附法
3.1.1吸附剂为金属或合金
Succi M[7]用氢化的吸气金属作为吸附剂去除硅烷中水分和二硅氧烷杂质的方法。最适合的吸气金属为Zr-V-Fe合金,该合金可以粉末或粒子形式作为吸附剂,配比以ω(Zr)=75%、ω(V)=20%、ω(Fe)=5%为最佳。该合金使用前需在350℃下在氩气中加热活化4 h,然后用氢气、氩气混合气使其降至室温。该吸附剂的吸附温度为100℃,通过吸附剂后能将硅烷中水分和二硅氧烷的体积分数降至0.1×10-6。
3.1.2吸附剂为活性炭
田中秀二等人[8]介绍了使用活性炭作为吸附剂去除硅烷中甲氧基硅烷杂质的方法。该方法使用粉末状的活性炭在常温常压下进行吸附,可将硅烷中甲氧基硅烷的含量降至分析仪器检测限以下。
3.1.3吸附剂为网状聚合物
Tom G M[9]介绍了一种用金属化的网状聚合物作吸附剂从SiH4中去除AsH3和PH3的方法。网状聚合物优选孔径为5~10 nm的(苯乙烯一二乙烯基苯)聚合物,使其与过量的正丁基锂的烃溶液在常温下进行金属化反应,未反应的金属被强烈吸附于聚合物的孔隙中。吸附剂在使用前于140~250 ℃下加热活化6 h,以除去游离的烃溶剂。吸附在惰性气体保护下进行,温度优选0~30℃,压力优选34.5~165.5 kPa。该法可使产物中PH3和AsH3体积分数降至0.3×10-6。
3.2冷凝分离法
日合淳彦等人[10]介绍了一种通过冷冻法提纯硅烷的方法,该方法是将硅烷通过两个串联的冷凝器,第一个冷凝器的温度为-80~-10℃,硅烷通过时烃类杂质和大部分氯硅烷等高沸点杂质被冷凝下来,硅烷及低沸点杂质通过第一个冷凝器后进入到第二冷凝器,第二冷凝器的温度低于-112℃,硅烷在其中冷凝,氮气、氢气等低沸点气体可以通过排轻等方式分离。接下来使冷凝液部分蒸发,再用活性炭、分子筛去除沸点和硅烷接近杂质,最后使高纯硅烷气体冷凝为液体,填充在压力容器中,纯度(体积分数)大于99.9998%。
3.3精馏纯化法
Robert H A等人[11]使用精馏去除硅烷中杂质的方法。其工艺流程为:首先使粗品硅烷引入精馏塔(I),在2.1~2.2 MPa下操作,塔顶除去轻组分(如H2、CH4等);其塔底馏分进入精馏塔Ⅱ,在1.96~2.07 MPa下操作,从塔底除去重组分,如CO2、CO、O2等,含乙烯和硅烷的塔顶馏分被送入填充有4A分子筛的固定床Ⅲ,在1.10~1.96 MPa下吸附去除大部分的乙烯,同时剩余的乙烯被转化为乙基硅烷。从分子筛固定床出来的气体经过滤器V除去夹带的固体粒子,然后被送入精馏塔Ⅳ,在1.86~1.96 MPa下操作,从塔顶得到高纯硅烷,乙基硅烷杂质质量分数降至0.0l×10-6以下。
4总结
硅烷是一种高附加值的精细化学品,在电子和半导体行业中有着广泛的应用。目前高纯硅烷的生产技术为日本、美国等国家所垄断。随着微电子行业的快速发展以及技术方面的不断进步,对于硅烷纯度的要求也越来越高,我们应密切关注这方面的工艺和技术进展,早日实现高纯度电子级硅烷的国产化,为提高我国电子和半导体工业水平做出应有的贡献。
参考文献:
[1] 电子特种气体,NK0018.电子级硅烷[M]//中国化工产品大全:下卷. 3版. 北京:化学工业出版社, 2002: 1218-1219.
[2] 赵贤和.烷类气体的净化设备和研制:中国,1751774A [P]. 2006-03-29.
[3] BLOCK Hans-Dieter. Method and system for producing silane: US, 6905576 [P]. 2005-06-14.
[4] 沈祖祥. 一种四氯化硅氢化生产三氯氢硅的装置:中国,2547719 [P]. 2003-04-30.
[5] HARADA Junzo. Process for production of silane: US, 4704264 [P]. 1987-11-03.
[6] GROSBOIS Jean. Prepration of silane: US, 4499063 [P]. 1985-02-12.
[7] SUCCI M, BOEFITO C, SOLCIA C. Removal of impurities from a hydride gas: EP, 0470936A1 [P]. 1992-02-12.
[8] 田中秀二,清水孝明.硅烷精制方法:日本,62-070217 [P]. 1987-03-3.
[9] TOM G M.Removal of arsine and phosphine from silane: EP, 0299488A2 [P]. 1989-01-1.
[10] 日合淳彦,腕村和生,田中将夫. 硅烷的精制方法:日本,61-063514 [P]. 1986-04-01.
[11] ROBERT H A,DOUGLAS M R.Removal of ethylene from silane using a distillation step after separation using a zeolite molecular sieve: US, 5211931 [P]. 1993-05-18.
柳彤(1981),山东泰安人,现于中船重工第七一八研究所工作,从事高纯电子气体研发工作。
Advances in Production Study of Silane
LIU Tong, LUO Jianzhi, LI Dandan, SUN Qiuli
(The 718 Research Institute of CSIC, Handan 056027, China)
Abstract:Silane has a far-ranging potential application in electronic industry fields. The property and application of silane has be introduced. Research generalization of synthesis processes of silane reviewed in detail. The catalytic disproportionation is available solutions of industrial production. The purification method of silane is briefly described; predicted the development prospects of silane.
Key words:silane; synthesis; purification
作者简介:
doi:10.3969/j.issn.1007-7804.2016.02.002
中图分类号:TQ117
文献标志码:A
文章编号:1007-7804(2016)02-0007-04
收稿日期:2016-01-04
