八种氟喹诺酮类药物人工抗原的合成及鉴定
2016-11-09李琳万忠海文学忠
李琳+万忠海++文学忠
摘 要:建立诺氟沙星( Enrofloxacin,NOR)、环丙沙星(Ciprofloxacin,CIF)、恩诺沙星(Enrofloxacin,ENR)、沙拉沙星(Sarafloxacin,SAR)、氧氟沙星(Ofloxacin,OFL)、双氟沙星(Difloxacin ,DIF)、培氟沙星(Pefloxacin,pef)和氟罗沙星(Fleroxacin,FLX,)8种氟喹诺酮类药物人工抗原的合成及鉴定方法。采用碳二亚胺(EDC)法将8种氟喹诺酮类药物与载体蛋白进行偶联,用于制备免疫抗原与包被抗原,通过紫外扫描和SDS-PAGE 对人工抗原进行鉴定,免疫原免疫Balb/c 小鼠,获得抗体。试验结果表明,采用间接ELISA方法检测小鼠血清抗体效价均达到1:8000以上。为进一步制备抗氟喹诺酮类药物单克隆抗体提供了良好的免疫原。
关键词:氟喹诺酮;人工抗原;合成;鉴定
中图分类号:R978.1 文献标识码:A DOI:10.11974/nyyjs.20160832005
氟喹诺酮药物(fluoroquinolones,FQs),又名6-氟喹诺酮类,是第3代喹诺酮类抗菌药。相比第1代和第2代喹诺酮类药物(quinolones,QNs)具有抗菌谱更广、抗菌作用更强、副作用低和不易产生耐药性等特点,故在医学和兽医学中很快取得广泛应用。FQs是小分子化合物,属于半抗原,将其与蛋白质载体进行偶联后,再制备成完全抗原,即指小分子物质必须和载体蛋白偶联之后方能刺激机体产生特异性的抗体,并包被于固相载体上用于ELISA检测。
1 材料与方法
1.1 试验材料
1.1.1 试剂
诺氟沙星(99.6%)、环丙沙星(99.7%)、恩诺沙星(100%)、沙拉沙星(99.6%)、氧氟沙星(99.0%)、双氟沙星(100%)、培氟沙星(98%)和氟罗沙星(99.1%)购买于中国兽医药品监察所;弗氏完全佐剂、弗氏不完全佐剂、碳二亚胺(EDC)、卵清蛋白(OVA)、牛血清白蛋白(BSA)、N-羟基琥珀酰亚胺(NHS)均购买于Sigma-Aldrich公司,其余试剂均为国产分析纯购于鼎国生物技术有限公司。
1.1.2 主要仪器
BECKMAN DU-640核酸蛋白分析仪(USA);自动凝胶成像仪(美国伯腾); SZ-93自动双重纯水蒸馏器(上海垒固);超纯水仪(ELGA); CO2细胞培养箱(力康HF90型气套式); -80℃冰柜(日本三洋);TECAN酶联免疫检测仪(AUSTRIA)。
1.1.3 试验动物和细胞
雌性,8周龄,体重14~16g BALB/c 小鼠购于长春市生物制品所;SP2/0骨髓瘤细胞,由本室保存。
1.2 方法
1.2.1 完全抗原的制备采用碳二亚胺法
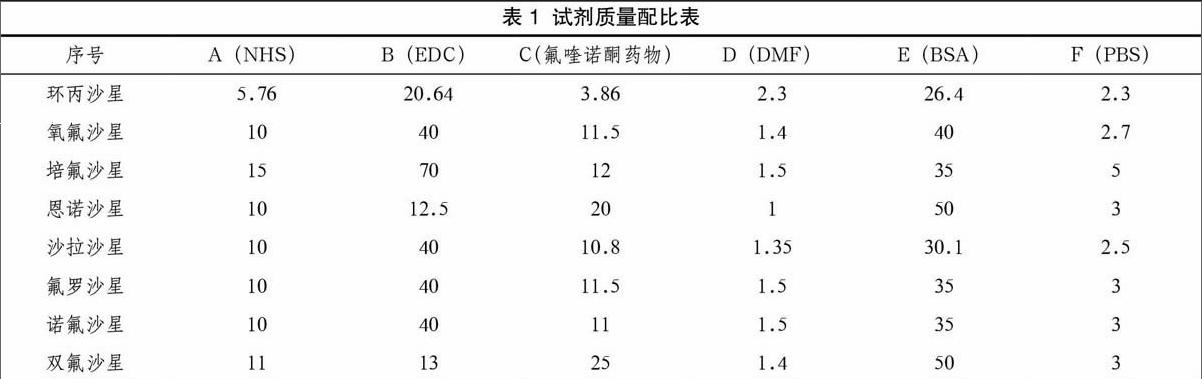
8种氟喹诺酮药物完全抗原制备方法步骤基本相同,但秤取的量不尽相同,详见试剂质量配比表。实验步骤如下:准确称取N-羟基琥珀酰亚胺(NHS)A mg,碳二亚胺(EDC)B mg,氟喹诺酮药物 C mg,加入 D μL 的N,N-二甲基甲酰胺(DMF)此溶液命名为Ⅰ,并放置在室温下遮光搅拌孵育24h;准确称取牛血清白蛋白(BSA)E mg, 加入0.01 mol/L(pH 值7.4)磷酸盐缓冲液(PBS)F mL,此溶液命名为Ⅱ。将孵育好的溶液Ⅰ逐滴加入到Ⅱ,同时搅拌,室温下搅拌3h。 反应结束,用0.01 mol/L(pH 值7.4)PBS 透析,透析后溶液定容至3 mL,零下20℃分装保存。合成包被抗原方法同上。
1.2.2 试剂质量配比表
1.2.3 偶联产物分析及分子结合比测定
采用聚丙烯酰胺非变性凝胶电泳分析和紫外分光光度法测定半抗原与载体蛋白的分子结合比方法测定。
1.2.4 完全抗原的鉴定
采用SDS-PAGE 凝胶电泳鉴定和紫外扫描鉴定。
1.2.5 雌性56日龄BALB/c小鼠(体重14~16g),分成3批次进行免疫(4只/批)
混合完全抗原与等量福氏完全佐剂乳化完全后作为首次免疫用,以剂量为200?g/只注射腹腔。第2次免疫在28d后进行,加强免疫时间间隔为14d1次,换用福氏不完全佐剂,其余同前。小鼠断尾采血在第3次免疫后进行,检测血清效价采用间接ELISA方法,待血清效价达到1:8000以上。融合前3d,不加佐剂,进行强化免疫。
1.2.6 小鼠血清效价测定及检测方法
小鼠尾部采血0.1mL,5000r/min离心5min,收集血清,采用间接ELISA方法检测血清效价,并设阴性和空白对照。
2 结果与分析
2.1 8种氟喹诺酮类药物
与BSA的偶联产物BSA-X(8种氟喹诺酮类药物)聚丙烯酰胺非变性凝胶电泳分析及其与OVA的偶联产物OVA-X聚丙烯酰胺非变性凝胶电泳分析结果可以看出:偶联物的电泳条带与载体蛋白均不相同,证实已经成功偶联。
2.2 紫外分光光度法测定半抗原与载体蛋白的分子结合比
将每种溶液稀释至200?g/mL(偶联产物按蛋白计),经过紫外扫描获得每种溶液的紫外吸收光谱,并发现BSA、X、BSA- X3者的紫外吸收光谱差异明显(OVA及其处理对照类同),可以说明偶联成功。而经测定各溶液的吸光值,代入公式计算X与BSA和OVA的分子结合比分别为2:1和3:1不等。
2.3 免疫小鼠血清抗体效价
8周龄BALB/c雌鼠进行首免,三免10d后应用间接ELISA法检测小鼠血清效价通过实验获得小鼠均已经产生了特异性抗体。
2.4 筛选方法的可行性分析
分别把BSA、OVA、BSA-X(8种氟喹诺酮类药物)和OVA-X 5μg/ml包被过夜,每孔100μl。阴性血清1:400倍稀释,阳性血清1:4000倍稀释,并设置空白对照。显示结果为OVA与阳性血清反应的OD值在0.1左右,表明与OVA发生特异性反应。而阳性血清与BSA-X反应的OD值比与BSA反应的OD值要高,这样阳性血清中不仅产生了针对BSA的抗体还产生了针对8种氟喹诺酮类药物的抗体。因此采用OVA-X作为包被抗原是必须且可行的。
3 小结
3.1 氟喹诺酮类药物
是兽医临床常用的一种兽药,近年来使用量较大。由于其具有潜在致癌的危害性,故而一旦在畜禽产品中残留量过高,人类长期使用便会危及健康。同时对畜牧业发展也会产生重要的影响,带来巨大的经济损失。
3.2 本试验
将8种氟喹诺酮类药物与蛋白质载体偶联制备人工抗原,该试验结果奠定了8种氟喹诺酮类药物ELISA检测试剂盒组装的理论和实践基础。
参考文献
[1]贾国超,职爱民,李梦琴,等.氟罗沙星残留检测间接竞争ELISA试剂盒的研制[J].中国农业科学,2014,47(11):2251-2261.
[2]刘儒彪,胡骁飞,孙亚宁,等.沙拉沙星完全抗原的合成及多克隆血清制备[J].河南农业科学,2014,43(5):167-171.
[3]范国英,刘俊伟,钟华,等.培氟沙星人工抗原的合成与鉴定[J].湖北农业科学,2011,50(11):2278-2279.
[4]杨先乐,黄宜运,胡鲲,等.环丙沙星单克隆抗体的制备及鉴定[J].食品科学,2010,31(12):16-20.
[5]刘庆棠,职爱民,李青梅,等.诺氟沙星单克隆抗体的制备及其特性鉴定[J].中国预防兽医学报,2010,32(9):716-720.
[6]于海峰,张森,万忠海,等.氧氟沙星完全抗原的合成鉴定及其单克隆抗体的制备纯化[J].食品科学,2006,27(10):223-228.
