宽温度范围纳米多孔硅/高氯酸钠热分解特性
2016-05-08刘玉存张志军于国强李尚杰
付 琼, 刘玉存, 张志军, 武 晔, 于国强, 李尚杰, 刘 媛
(1. 中北大学化工与环境学院, 山西 太原030051; 2. 中国五洲工程设计集团有限公司, 北京 100053; 3. 陕西应用物理化学研究所, 陕西 西安 710061; 4. 西安物化巨能爆破器材有限责任公司, 陕西 西安 710061)
1 引 言
纳米多孔硅( Nano Porous Silicon, nPS)是一种在硅表面形成微纳米多孔结构的硅基底材料[1],自发明以来被广泛应用于电子及发光元件中,其存在形式包括纳米多孔硅片以及纳米多孔硅粉。1992年,McCord P[2]首次报道了纳米多孔硅片的爆炸性能,在随后的20年,纳米多孔硅与固体氧化剂之间的爆炸反应被陆续发现[3-4],此后其作为新型燃烧剂引起了广泛关注。nPS的制备方法包括电化学腐蚀法[5]、化学腐蚀法[6]、固体火焰放热法[7]、Si2H6化学气相沉积技术[8-11]、钠热还原法[12]、Bottom-up 合成法[13],其中电化学腐蚀法和化学腐蚀法被普遍采用。利用化学腐蚀法制备纳米多孔硅粉,操作简便且成本较低,实现了nPS的工业化生产[14-15],为其大规模应用于含能材料领域迈出了重要一步。纳米多孔硅基复合含能材料燃烧及爆炸性能良好,国外学者对其进行了系统研究[16-17],美国已经成功将其应用于无起爆药雷管[18]。而关于纳米多孔硅基复合含能材料热分解特性及燃烧机理报道较少,已有研究也主要针对片状纳米多孔硅复合含能材料[19-20],且其温度测试范围相对较窄,如Becker C R等[21]报道了25~550 ℃温度范围内nPS/NaClO4复合含能材料的热分解性能,无法反映此类材料的热分解全过程。
基于此,本研究以化学腐蚀法制备的纳米多孔硅粉为燃烧剂,高氯酸钠(NaClO4)为氧化剂,制备nPS/NaClO4复合含能材料,采用差示扫描量热-热重(DSC-TG)法,在25~1200 ℃宽温度范围对其热性能进行分析。为了更好地反映该复合含能材料的热分解特性,分别测试了nPS和NaClO4的热分解特性,同时制备了Si/NaClO4复合含能材料进行对比实验,并分析了nPS在氧气(O2)氛围下的反应特性以及nPS/NaCl复合材料热分解特性。探讨宽温度范围内nPS/NaClO4复合含能材料的热分解机理,研究结果对更好地认知nPS/NaClO4的燃烧机理具有指导意义。
2 实验部分
2.1 实验
2.1.1 实验原料
纳米多孔硅粉 (中北大学采用化学腐蚀法[22]自制,Brurauer-Emmerr-Teller(BET)比表面积72.4327 m2/g,Barrett-Joyner-Halenda(BJH)平均孔径7.67 nm); NaClO4,分析纯,天津福晨化学试剂厂; 无水乙醇,分析纯,国药集团; 实验用水均为蒸馏水。
2.1.2 样品制备
nPS/NaClO4(质量比为1∶1[22])复合含能材料的制备方法如下: 将10 mL含有1g NaClO4的乙醇溶液分三次加入装有1 g nPS粉末的表面皿中,制备过程中保持超声波震荡,使得NaClO4乙醇溶液与nPS混合均匀充分,待溶剂挥发后NaClO4在纳米孔洞内发生重结晶,从而形成nPS/NaClO4复合含能材料。以同样方法制备Si/NaClO4复合含能材料。样品在60 ℃烘干24 h。
nPS/NaCl复合材料制备方法如下: 将1 g nPS投入到8.2 mL的浓度为1 mol·L-1的NaCl水溶液中(1 g NaClO4受热分解,理论上产生0.48 g NaCl),由于nPS 具有较强的疏水性,充分搅拌后,进行超声波震荡至溶剂挥发,nPS/NaCl复合材料制备完成,60 ℃烘干24 h。
2.2 实验仪器及方法
Elementar元素分析仪(STA_449F3,GER); DX-2700型X射线衍射仪(丹东方圆仪器有限公司)。
热分析实验: Netzsch同步热分析仪(STA_449F3,GER),加盖三氧化二铝(Al2O3)坩埚盛放样品,样品用量约为3 mg,气氛为氩气(Ar),吹扫气体流量为30 mL·min-1,测试温度范围为25~1200 ℃,升温速率为15 ℃·min-1,以初始质量为基准计算分解放热量ΔHd。
3 结果与讨论
3.1 nPS元素分析测试
表1为分三次取样以燃烧法[23]测定的nPS中氢元素的含量。由表1可知,nPS中H含量约为0.5%,有少量的C以及N元素,这可能是由于在测试过程有少量空气进入仪器中造成。其中nPS中氢元素是以最简单的硅氢基团(Si—H和SiH2)形式存在[22]。
表1nPS的元素分析(燃烧法)
Table1The elemental analysis of nPS by combustion method

mass/mgcontent/%CNH5.2900.0360.0800.5004.8200.0270.1000.4884.5400.0310.1000.516
3.2 nPS/NaClO4的热分解特性
3.2.1 nPS的DSC-TG分析
nPS样品的DSC-TG曲线如图1所示。由图1 中的TG曲线可知,nPS在820.0 ℃开始增重。随着温度的逐渐升高,硅颗粒受热膨胀,硅氢键发生断裂,nPS被坩埚中残留的少量空气所氧化,直至升温结束,nPS样品增重量为10.5%。DSC曲线表明,nPS在25~1200 ℃没有出现明显的放热或吸热峰。

图1nPS在氩气氛围下的DSC-TG曲线
Fig.1DSC-TG curves for nPS in argon flow
3.2.2 NaClO4的DSC-TG分析
NaClO4为无色晶体,有吸潮性,其分解机理至今仍没有确切的定论。NaClO4的DSC-TG曲线如图2所示。
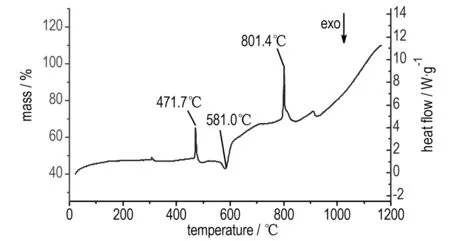
图2NaClO4在氩气气氛下DSC-TG曲线
Fig.2DSC-TG curves of NaClO4in argon flow
DSC-TG结果显示,在氩气保护下,NaClO4在471.7 ℃发生相变并观察到吸热峰。565.2~602.9 ℃出现最强的分解放热峰,峰温为581.0 ℃,ΔHd=130.2 J·g-1。798.5~831.5 ℃出现一个尖锐的熔融吸热峰,峰温为801.4 ℃,这可能是因为NaCl发生相变,呈熔融状态。TG曲线显示,NaClO4样品共有两
个失重阶段,其中469.0~602.9 ℃为第一失重阶段,失重量为36.26%,667.5~985.1℃为第二失重阶段,失重量为32.05%,总失重量达到68.31%,其中52.4%是NaClO4分解放出O2的理论失重量,其余可能是NaCl达到熔点后部分挥发造成的。
3.2.3 nPS/NaClO4形貌
光学显微镜放大40倍后nPS/NaClO4复合含能材料表面形貌如图3所示。

图3nPS/NaClO4复合含能材料形貌(×40)
Fig.3The morphology of nPS/NaClO4(×40)
图3中透明晶体为NaClO4,黑褐色物质为nPS,可以看出,部分NaClO4晶体颗粒并没有进入到nPS孔洞之内。这意味着对于nPS/NaClO4来说,部分NaClO4与Si发生反应。而进入纳米孔内的NaClO4,则与nPS发生反应。
3.2.4 复合含能材料的DSC-TG分析
nPS/NaClO4和Si/NaClO4两种复合含能材料在氩气气氛下的DSC-TG曲线如图4所示。

图4nPS/ NaClO4与Si/NaClO4在氩气氛围下DSC-TG曲线
Fig.4DSC-TG curves of nPS/ NaClO4and Si/NaClO4in argon flow
由图4可知,nPS/NaClO4复合含能材料在468.1 ℃附近熔化吸热,随后在587.5 ℃出现最强放热峰,这是由于NaClO4与燃烧剂nPS 之间发生反应,混合物着火燃烧并放出大量的热。相比Si/NaClO4复合含能材料在该阶段的放热量ΔHd=344.2 J·g-1,nPS/NaClO4放热量较大,ΔHd=359.5 J·g-1,这是由于硅氢键参与放热反应造成了放热量的增大,这与Becker C.R等[21]的研究结果相吻合。值得注意的是,800.0 ℃ NaCl熔化后,与Si/NaClO4复合含能材料的热反应特性相比,nPS/NaClO4复合含能材料基本处于吸放热平衡状态。温度上升到1031.8 ℃后,nPS/NaClO4复合含能材料开始快速放热,但因仪器测试温度范围的限制,没有检测出完整的放热峰。由此推测当温度达到800 ℃以后,未发生断裂的硅氢键与NaClO4的分解产物之间发生了某种放热反应,放出的热量被吸收,使得nPS/NaClO4复合含能材料在该温度范围内出现了吸放热平衡现象。基于此,分析了nPS与NaClO4的分解产物O2和NaCl的热反应过程。
图5是nPS样品在O2吹扫条件下的DSC-TG曲线; 图6为nPS/NaCl复合材料在氩气保护下的DSC-TG曲线。
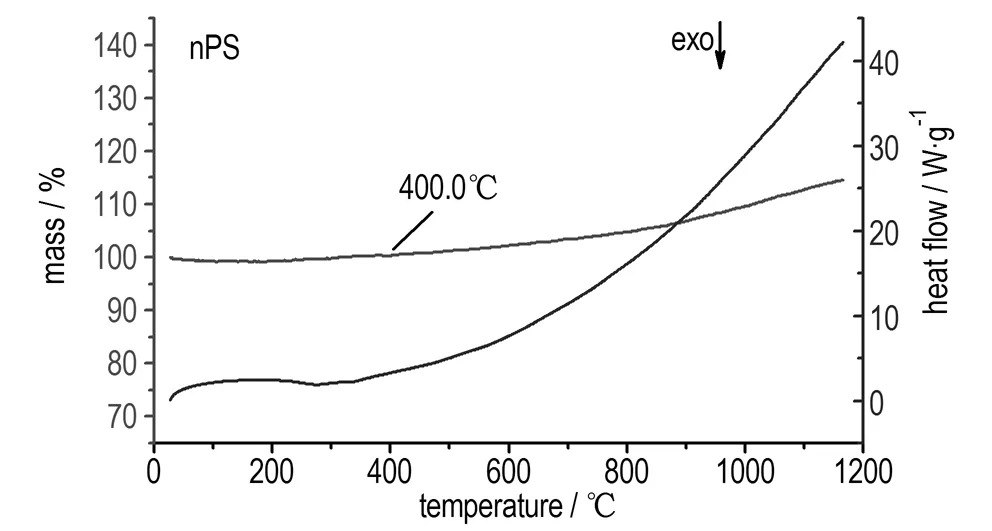
图5nPS在氧气气氛围下DSC-TG曲线
Fig.5DSC-TG curves of nPS in O2flow
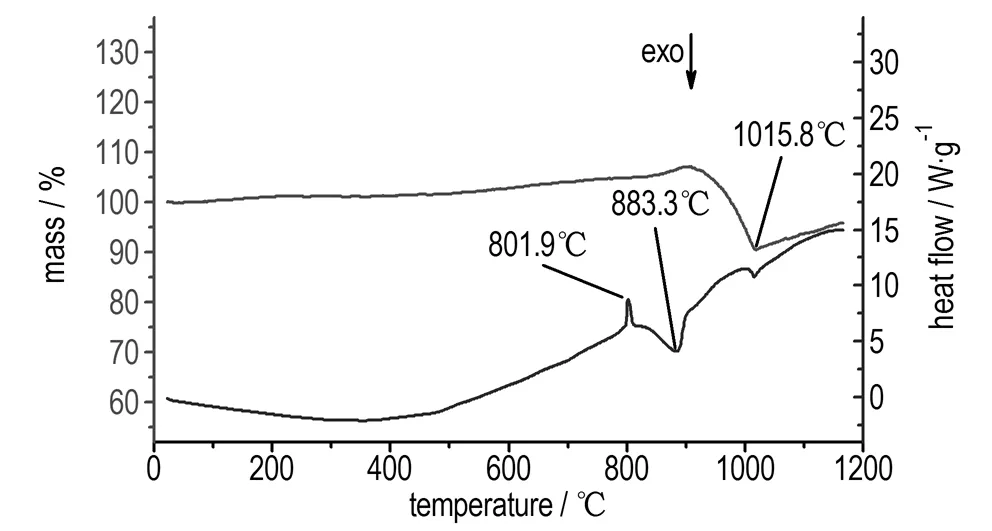
图6nPS/NaCl在氩气氛围下DSC-TG曲线
Fig.6DSC-TG curves of nPS/NaCl in argon flow
由图5可知,nPS 在O2吹扫条件下,DSC曲线没有出现明显的峰,TG曲线显示nPS在400.0 ℃开始增重,这表明在O2充足的条件下,硅氢键发生断裂的温度与氩气氛围下相比提前了420.2 ℃。O2因扩散作用进入nPS颗粒内部,氧化反应开始,直至反应结束,nPS增重14.5%。图6表明,799.2~808.2 ℃,NaCl熔化发生相变。840.4~934.9 ℃出现一个明显的、意料之外的放热峰,峰温为883.3℃,ΔHd=567.0 J·g-1。这一放热峰的出现表明在该温度范围内两种物质之间发生某种放热反应,由于相关反应特性未见报道,因此参照硅氢化合物反应特性,推测在800~1200 ℃发生如下反应,其反应流程如图7所示:
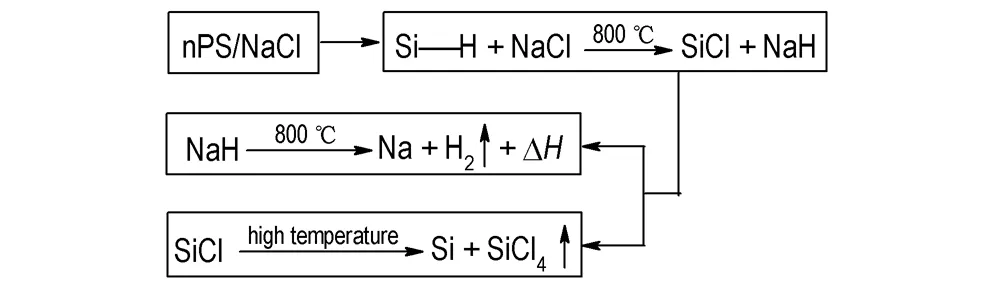
图7nPS/NaCl在800~1200 ℃反应流程
Fig.7The reaction scheme of nPS/NaCl at 800~1200℃
推测nPS/NaClO4复合含能材料的热分解机理如下: nPS/NaClO4复合含能材料在587.5 ℃着火燃烧,NaClO4受热分解放出O2并生成NaCl,O2使硅氢键提前发生断裂,参与反应使放热量增大。当温度上升到800 ℃后,NaCl融化离子键被破坏,离子呈现游离态并开始自由移动。未断裂的硅氢键与熔融态NaCl发生卤代反应,这一推测与文献[24]中所描述的硅氢键与无机卤化物发生卤代反应的机理相吻合。NaH(氢化钠)的熔点为800 ℃,同时在该温度下开始分解,产生氢气(H2)并放出热量[25],840.4~898.9 ℃区间出现明显放热峰。nPS颗粒受热膨胀吸收了NaH分解所放出的热量,因此nPS/NaClO4在该温度范围内呈现热平衡状态。另外一氯化硅(SiCl)寿命极短,温度过高发生歧化反应生成Si以及挥发性液体SiCl4,SiCl4沸点57.6℃,高温条件下迅速挥发[26],图6中TG曲线在1015.8 ℃有小幅度上升,这可能是SiCl4气体快速挥发对天平造成冲击而产生的波动。
3.2.5 固体燃烧产物的XRD衍射
为了验证以上推论的合理性,利用X射线衍射仪分析nPS/NaClO4复合含能材料的固体燃烧产物组分,测试结果与JCPDS粉末衍射卡271402进行对比,如图8所示。
由图8可知,固体燃烧产物的衍射峰与271402的Si(syn)完全一致,除此之外,并没有发现其他物质。测试结果与推测可能产生的分解产物相一致,从而验证了关于nPS/NaClO4复合含能材料热分解机理推论的合理性。
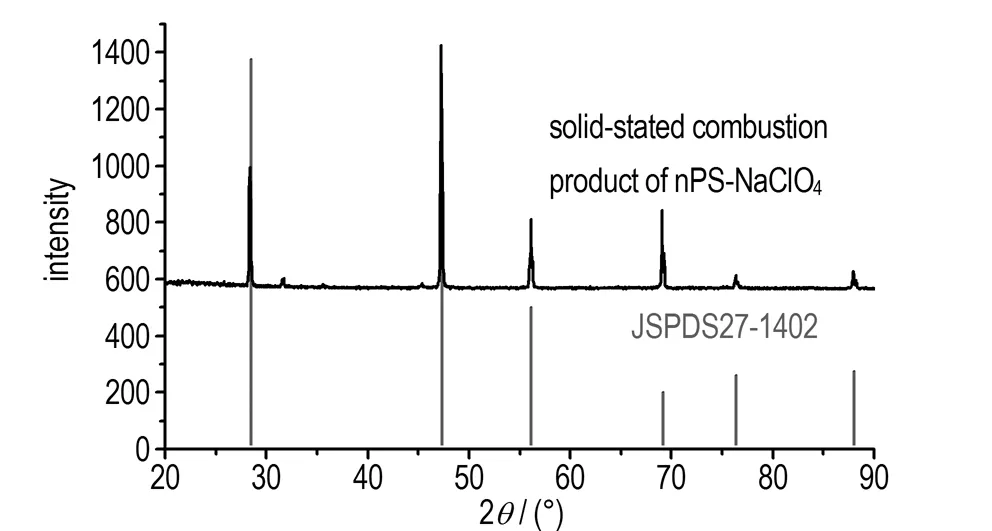
图8nPS/ NaClO4固体燃烧产物的XRD分析
Fig.8XRD analysis of solid-stated Combustion product of nPS/NaClO4
4 结 论
(1) O2对硅氢键发生断裂的温度具有显著影响。nPS在氩气氛围下的硅氢键断裂的温度为820.0 ℃,但在O2吹扫条件下,硅氢键断裂温度提前至400.0 ℃,其断裂温度降低了420.0 ℃。
(2) NaClO4在581.0 ℃出现最强分解放热峰,该温度范围内共有两个失重阶段,总失重量68.31%大于理论失重量52.4%,推测是由于达到熔点后NaCl部分挥发造成的。
(3) 硅氢键可以增大复合含能材料的分解放热量。nPS/NaClO4在587.5 ℃出现最强放热峰分解,硅氢键参与放热反应,放热量增加至359.5 J·g-1,大于Si/NaClO4所释放的热量344.2 J·g-1。
(4) 综合热分析测试结果,得出nPS/NaClO4复合含能材料的热分解机理如下: 复合含能材料在587.5 ℃着火燃烧,NaClO4分解释放O2并生成NaCl,O2使硅氢键提前断裂并参与放热反应,放热量增大。温度上升到800 ℃以后,NaCl熔化,未断裂的硅氢键与其发生卤代反应,生成NaH和SiCl。NaH达到熔点分解并放出热量,SiCl高温下发生歧化反应,生成Si以及SiCl4。
参考文献:
[1] 单燕,徐伯庆,陈麟. 电化学制备多孔硅的工艺对其形貌的影响[J]. 光学仪器, 2015, 37(1): 9-13.
SHAN Yan, XU Bo-qing, CHEN Lin. Preparation andmorphology influence of porous silicon by electrochemical etching condition[J].OpticalInstruments, 2015, 37(1): 9-13.
[2] McCord P, Yau S L, Bard A J.Chemiluminescence of anodized and etched silicon: evidence for a luminescent siloxene-like layer on porous silicon[J].Science, 1992, 257: 68-69.
[3] Kovalev D, Timoshenko V Y, Kunzner N, et al. Strong explosive interaction of hydrogenated porous silicon with oxygen at cryogenic temperatures[J].PhysicalReviewLetters, 2001, 87(6): 683011.
[4] Mikulec F V, Kirtland J D, Sailor M J. Explosive nanocrystalline porous silicon and its use in atomic emission spectroscopy[J].AdvancedMaterials,2002, 14(1): 38-41.
[5] 薛艳,卢斌,解瑞珍,等. 纳米多孔硅含能芯片性能研究[J]. 火工品, 2008, 3(6): 9-11.
XUE Yan, LU Bin, XIE Rui-zhen, et al. Study on the property of nano-proous silicon/oxidant systems[J].Initiators&Pyrotechnics, 2008, 3(6): 9-11.
[6] Farrell D, Limaye S Y, Subramanian S .Vesta Research,Ltd,US7560085B2[P]. 2009.
[7] Wona C W, Nersisyan H H , Shin C Y, et al. Porous silicon microparticles synthesis solid flame technique[J].MicroporousandMesoporousMaterials, 2009, 126(1): 166-170.
[8] Fenollosa R, Manzano F R, Tymczenkoab M, et al. Porous silicon microspheres: synthesis characterization and application to photonic microcavities[J].JournalofMaterialsChemistry, 2010, 20(25): 5210-5214.
[9] Magasinski A, Dixon P, Hertzberg B, et al. High-performance lithium-ion anodes using a hierarchical bottom-up approach[J].NatureMaterials, 2010, 9(4): 353-358.
[10] Evanoff K, Magasinski A, YANG Jun-bing, et al. Nanosilicon-coated grapheme granules as anodes for Li-ion batteries[J].AdvancedEnergyMaterials, 2011, 1(4): 495-498.
[11] Fenollosa R, Manzano F R, Tymczenkoab M, et al. Porous silicon microspheres: synthesis, characterization and application to photonic microcavities[J].JournalofMaterialsChemistry, 2010, 20(25): 5210-5214.
[12] WANG Jing-feng, WANG Kai-xue, DU Fei-hu, et al. Amorphous silicon with high specific surface area prepared by a sodiothermic reduction method for supercapacitors[J].ChemicalCommunications, 2013, 49(44): 5007-5009.
[13] FANG Dai, ZAI Jian-tao, RAN Yi, et al. Bottom-up synthesis of high surface area mesoporous crystalline silicon and evaluation of its hydrogen evolution performance[J].Naturecommunications, 2014, 5(4): 3908-3915.
[14] Farrell D, Limaye S, Subramanian S . Vesta Research, Ltd, US 7569202[P], 2009.
[15] CJément D, Diener J, KovaJev D. Explosive Porous silicon-from laboratory accident to industrial application[C]∥35th Int. Annual Conference of ICT. Karlsruhe, Germany, June 29-July 2, 2004: 5-1-5-11.
[16] Shanthi S, Terry T, Santosh L, et al. Nanoporous silicon based energetic materials[R]. US Vesta Sciences. 2008: 1-7.
[17] Plummer A, Cao H, Dawson R, et al. The influence of pore size and oxidizing agent on the energetic properties of porous silicon [J].ProceedingofSPIE, 2008, 7627(1): 263-270.
[18] Oyler K D, Cheng G, Mehta G, et al. Green explosive: potential replacements for lead azide and other toxic detonator and primer constituents[EB/OL]. Scribd Com, [2012-3-10].
[19] 薛艳,卢斌,任小明,等. 纳米多孔硅含能材料性能研究[J]. 含能材料2010, 18(5): 523-526.
XUE Yan, LU Bin, REN Xiao-ming, et al. Properties ofenergetic materials based on nano-porous silicon[J].ChineseJorunalofEnergeticMaterials(HannengCailiao), 2010, 18(5): 523-527.
[20] 王守旭,沈瑞琪, 叶迎华. 多孔硅含能芯片的制备工艺和性能研究[J], 含能材料,2010,18(5): 527-531.
WANG Shou-xu, SHEN Rui-qi, YE Ying-hua. Preparation andproperties of porous silicon energetic chips[J].ChineseJorunalofEnergeticMaterials(HannengCailiao), 2010, 18 (5): 527-531.
[21] Becker C R, Currano L J, Churaman W A. Thermal analysis of the exothermic reaction between galvanic porous silicon and sodium perchlorate[J].AppliedMaterials&Interfaces, 2010, 2(11): 2988-3003.
[22] 付琼,刘玉存,柴涛,等. 纳米多孔硅粉的化学腐蚀及其理化性质表征[J]. 含能材料, 2015,23(2): 146-150.
FU Qiong, LIU Yun-cun, CHAI Tao, et al. Preparation ofnanoporous silicon powder by chemical etching and its physicochemical properties characterization[J].ChineseJorunalofEnergeticMaterials(HannengCailiao), 2015, 23(2): 146-150.
[23] 李晓银,丛日新,范国宁,等. 燃烧法测定丁腈橡胶中结合丙烯晴含量[J]. 合成橡胶工业, 2013,36(3): 186-188.
LI Xiao-yin, CONG Ri-xin, FAN Guo-ning, et al. Determination of bound acrylonitrile content in nitrile rubber by combustion method[J].ChinaSyntheticRubberIndustry, 2013, 36(3): 186-188.
[24] 杜作栋, 陈剑华, 贝小来, 等. 有机硅化学[M]. 北京: 高等教育出版社,1990: 124.
DU Zuo-dong, CHEN Jian-hua, BEI Xiao-lai, et al. Organosilicon chemistry[M]. Beijing: Higher Education Press,1990: 124.
[25] 大角泰章. 金属氢化物的性质与应用[M]. 吴永宽,苗艳秋,译. 北京: 化学工业出版社, 1990: 19-32.
OSumi Y. Theproperties and applications of metal hydrides[M]. Beijing: Chemical Industry Press, 1990: 19-32.
[26] 天津化工研究院. 无机盐工业手册[M]. 北京: 化学工业出版社, 1999: 591-594.
Tianjin Chemical Research & Design Institute, Inorganicsalt industry handbook[M]. Beijing: Chemical Industry Press, 1999: 591-594.
