以问题为中心的化学教学设计分析
2016-04-28刘双红
以问题为中心的化学教学设计分析
◇湖北刘双红
“以问题为中心的教学”是要求教师在教学过程中,有意识地去营造问题环境,使学生主动发现问题、提出问题以及思考问题,在此过程中提升学生的学习积极性、激发学生的学习兴趣、提高学生的创造力等.
1以问题为中心的教学设计中的重点分析
1.1营造问题教学环境
在教学过程中可以有意识地设计几个学生容易忽视或混淆的“陷阱”,让学生利用自身所学的知识去寻找,一方面可以提升学生的上课积极性,另一方面可以巩固和加深学生对这些知识细节的掌握.
1.2确定中心问题
在教学设计中要先确定好中心问题,然后围绕这个中心问题设置一些对学生有吸引力的讨论问题,通过对这些问题的积极讨论,最终指向中心问题,使学生更好地掌握重点进而提升学习的效果.
1.3分小组进行问题讨论
让每个小组的同学对教师提出的问题进行讨论,然后每个小组分别派代表阐述自己小组内成员讨论的意见,并进行总结,最后由教师点评,进一步加深对知识点的掌握.
1.4对于疑难问题进行引导
由于学生本身的知识储备问题,在进行以问题为中心的教学设计中有时会遇见疑难问题,此时不应该直接给出正确答案,可给予一点提示与引导,让学生顺着引导进一步思考,以期将问题一步步解决.
2以问题为中心的“离子键”教学设计
2.1离子键概念
【说明】 展示氯化钠晶体样品以及结构模型.说明无数个Na+与Cl-连接,并向空间无限延伸排列而形成氯化钠晶体.
【设置问题】 Na+与Cl-是通过什么方式形成的NaCl?请写出钠与氯原子的结构示意图.钠与氯原子结构稳定吗?怎样使二者形成稳定结构?写出Na+与Cl-结构示意图,并表示出NaCl的形成过程.
【多媒体动画】
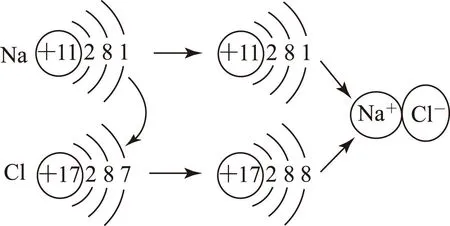
【知识讲述】 通过原子结构示意图将原子核所带电荷与核外不同层电子数进行表示,钠原子失去最外层1个电子变为Na+的8电子稳定结构,而氯原子则因得到1个电子变为Cl-的8电子稳定结构,Na+与Cl-结合即形成NaCl.
【设置问题】 Na+与Cl-之间是通过什么作用使之相互结合的?二者之间能否无限制地靠近?
【知识讲述】 结合投影分析,引出稳定的“离子键”.
2.2离子键的本质、形成条件与原因
【设置问题】 离子键形成的粒子是什么?粒子间形成化合物的作用方式是什么?哪些粒子可形成离子键?通过“新物质的生成必须有新化学键的生成”引出化学反应本质.
【思考讨论】 离子化合物化学式与电子式表达的区别?采用电子式表示离子化合物NaCl、Na2O与CaCl2的形成过程.
3以问题为中心的“盐类水解”教学设计
【问题引入】 溶液酸碱性测定最简单的方法是什么?
【实验操作】 回顾旧知识,让学生使用pH试纸对桌上的盐溶液进行pH测定,判定酸碱性并记录.
【设疑激思】 盐溶液呈现酸碱性原因?NH4Cl、CH4COONa与水发生了什么反应?NaCl为何没有呈现酸碱性?
【问题讨论】 以NH4Cl为例,溶于水发生的电离过程中离子间有无相互作用?水的电离平衡是否受到影响?是怎样影响的?
【思考讨论】 给予学生肯定,设置相应的练习,并分析NaCl呈中性的原因.引入盐类水解的概念.
【知识讲解】 1)盐类水解的概念、水解实质与形式; 2)盐类水解规律.
以问题为中心的高中化学教学设计的确是适合高中生使用的,因为通过问题教学环境的营造、中心问题的确定、分小组进行的问题讨论、对于疑难问题的引导等方式进行学习,能够使得学生有更高的学习积极性,进而提高课堂的效率,达到预期目标.
