N-亚硝基化合物的危害及其在体内外合成和抑制的研究进展
2016-04-15蔡鲁峰王远亮湖南农业大学食品科学技术学院食品科学与生物技术湖南省重点实验室湖南长沙4028湖南省商业技师学院烹饪系湖南株洲42000
蔡鲁峰,李 娜,杜 莎,谭 雅,李 珂,王远亮,*(.湖南农业大学食品科学技术学院,食品科学与生物技术湖南省重点实验室,湖南 长沙 4028;2.湖南省商业技师学院烹饪系,湖南 株洲 42000)
N-亚硝基化合物的危害及其在体内外合成和抑制的研究进展
蔡鲁峰1,2,李 娜1,2,杜 莎1,谭 雅1,李 珂1,王远亮1,*
(1.湖南农业大学食品科学技术学院,食品科学与生物技术湖南省重点实验室,湖南 长沙 410128;2.湖南省商业技师学院烹饪系,湖南 株洲 412000)
摘 要:本文首先对N-亚硝基化合物(N-nitroso compounds,NOCs)分类进行了简单的介绍,比较了其两大类物质N-亚硝胺和N-亚硝酰胺的性质;接着从致癌性、致畸性和毒性三方面概述了NOCs对动物及人体的危害;之后从体内和体外两个方面探讨了NOCs的合成途径,并对其合成机理和影响其体内外合成的因素进行了归纳;最后从消除和阻断两个方面探讨了体内外抑制NOCs的方法及机理。以期为其他研究人员寻找抑制和降解NOCs的方法以及其作用机理研究提供理论参考。
关键词:N-亚硝基化合物;危害;合成;抑制
湖南农业产业技术体系加工岗位专家经费资助项目;公益性行业(农业)科研专项(201303082);
湖南省科技计划项目(2015WK3015)
引文格式:
蔡鲁峰,李娜,杜莎,等.N-亚硝基化合物的危害及其在体内外合成和抑制的研究进展[J].食品科学,2016,37(5):271-277.
CAI Lufeng,LI Na,DU Sha,et al.Progress in hazards,synthesis and inhibition of N-nitroso compounds in vitro and in vivo[J].Food Science,2016,37(5):271-277.(in Chinese with English abstract)DOI:10.7506/spkx1002-6630-201605047.http://www.spkx.net.cn
在许多国家,癌症已经成为了一个主要的公共卫生问题。已有资料报道在美国每4 人死亡就有1人是由于癌症导致的[1]。在中国,因肿瘤引起的死亡率也在急剧上升,2012年统计表明在所有病因中肿瘤引发的致死率居第二位,仅次于心脑血管疾病[2]。引起机体患癌的物质广泛存在于自然界中,N-亚硝基化合物(N-nitroso compounds,NOCs)就是其中的一种,该物质广泛存在于环境以及动植物体内,如Flower等[3]的研究结果表明烟草烟雾中存在大量NOCs,为了提高瓜果蔬菜的产量,经常使用氮肥,这造成了瓜果蔬菜中高的硝酸根离子残留,这些残留的硝酸根离子通过食物链进入人体中后被转化为亚硝酸盐,成为人体内源NOCs合成的前体物质。在已知的NOCs家族中有超过300 种物质具有致癌活性,并且其中90%以上已经证实具有致癌性[4],其强烈的致癌性引起了人们的广泛关注。
1 NOCs及其对动物和人体的危害
1.1NOCs的分类及其性质
NOCs的分子结构通式为R1(R2)=N—N=O,根据R1和R2基团的不同又可分成N-亚硝胺和N-亚硝酰胺两大类。N-亚硝酰胺的R1为烷基或芳基,R2为酰胺基,包括氨基甲酰基、乙氧酰基及硝咪基等。N-亚硝胺的R1和R2为烷基或芳基。对于N-亚硝胺来讲R1和R2基团可以相同,也可以不同,相同时称为对称性N-亚硝胺,否则为非对称性N-亚硝胺。低分子质量的N-亚硝胺在常温下为黄色液体;高分子质量的亚硝胺多为固体。其各自的属性和差异见表1所示。
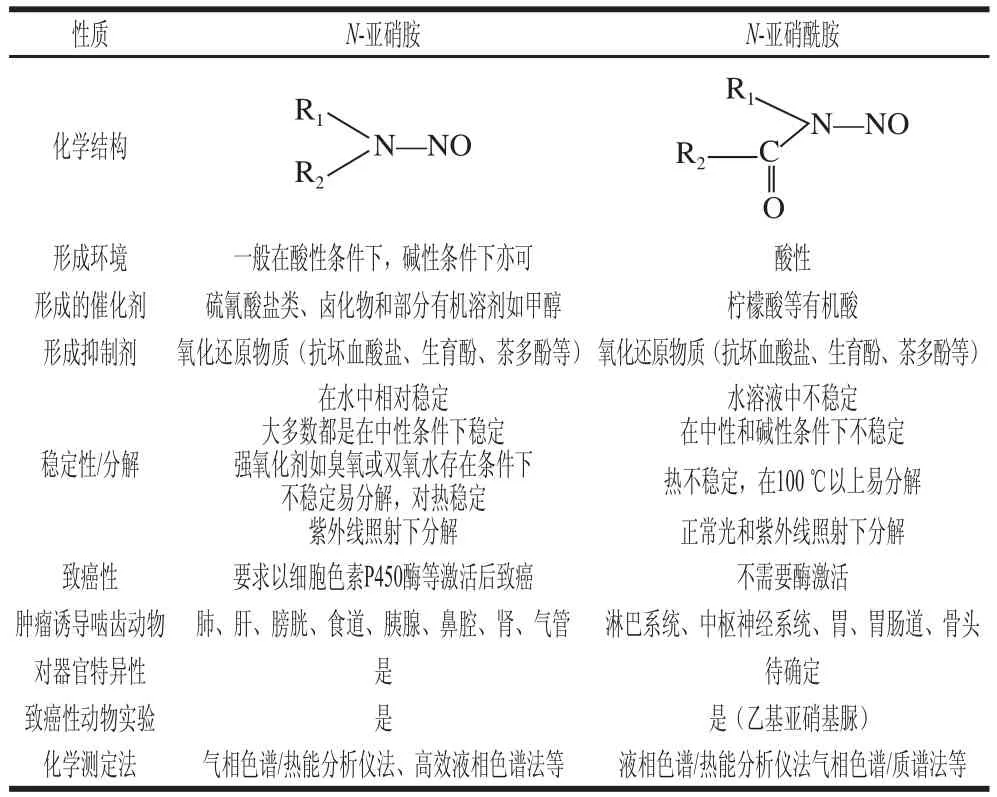
表11 N--亚 硝胺与N-亚硝酰胺的属性和差异[[55--88]]Table 1 Properties and differences between -nitrosamines and -nitrosamides[5-8]
1.2NOCs对动物及人体的危害
1.2.1致癌性
NOCs已被广泛证实具有致癌作用,而具有短脂肪链的NOCs通常导致癌症的风险更大[9]。诸多研究已证明NOCs具有间接或直接致癌作用,如Kok等[10]对已有病例资料研究显示,发现肠炎患者体内NOCs合成速率增大,导致患者患结肠癌的风险增大。戴乾圜等[11]利用DNA碱稀释过滤法证明了NOCs等致癌剂能使DNA互补碱对之间发生交联而导致细胞的癌变。Zhou Hongning等[12]报道,用100、400 mg/mL的烟草特有亚硝胺处理人类支气管上皮细胞7 d后,均可见此类细胞发生恶性转化,这充分说明了NOCs能诱导支气管上皮细胞的恶性转化。
NOCs对哺乳动物的器官致癌具有特异性。肿瘤诱导的主要器官是大脑、口腔、食道、胃、肠道、气管、肺、肝、肾、膀胱、胰腺、心脏和皮肤。如N-亚硝基哌啶(1-nitrosopiperidine,NPIP),能诱导哺乳动物的食管、鼻腔、肝和胃形成肿瘤[13];N-亚硝基二丁胺(N-nitrosodibutylamine,NDBA)能诱导哺乳动物的肺、食管、前胃和尿膀胱形成肿瘤[14]。与其他致癌物具有协同致癌也是NOCs致癌的特点,潘世宬[15]指出向田鼠器官内注入低于致癌剂量的苯并芘和氧化铁,田鼠并没有出现癌变现象,若同时在皮下注射小量的二乙基亚硝胺即可诱发田鼠的气管、支气管癌。NOCs亦可通过胎盘引起下一代动物的某些器官产生肿瘤,胡荣梅等[16]指出以不同给药途径使受孕的母鼠受到NOCs的冲击可使新生动物致畸,或存活一段时间后使不同的器官产生肿瘤。
已知在NOCs的两大类中,N-亚硝酰胺是直接致癌物,可以直接烷化DNA,形成DNA 加合物;而N-亚硝胺是间接致癌物,但是在亚硝胺如何引起癌变的机理有多种解释,代表性的论点包括以下几种:
1.2.1.1氧化脱氨作用
在N-亚硝胺的亚硝基作用下DNA碱基中的氨基可氧化脱氧,以致妨碍DNA的代谢[17]。
1.2.1.2重氮烷作用
N-亚硝胺进入机体,经过羟化酶的作用转变为重氮烷,再通过烷基化或者氨甲酰化反应形成DNA加合物。图1所示为生理条件下诱导N-亚硝基脲转化及致癌的一般机制。
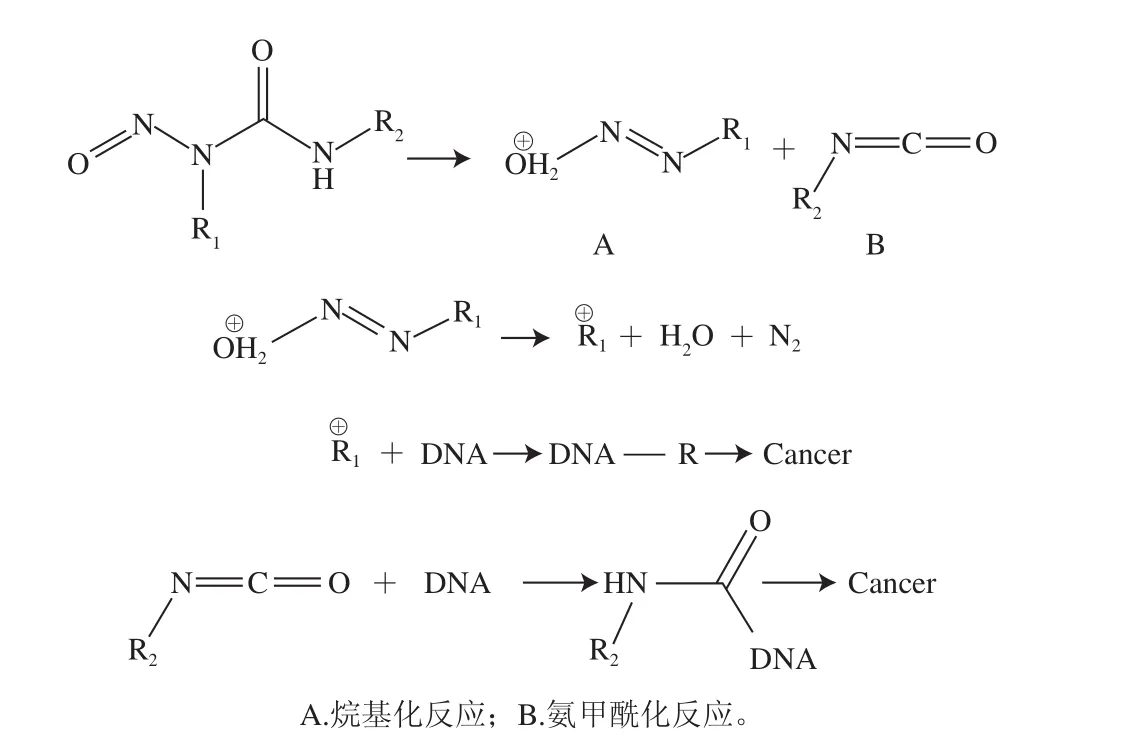
图1 生理条件下诱导N-亚硝基脲转化及致癌的一般机制(pH 77..44)[[1188]]Fig.1 General mechanism for the biotransformation of N-nitrosureas responsible for the induction of cancer under physiological conditions(pH 7.4)[18]
1.2.1.3细胞色素P450酶的激活作用
N-烷基亚硝胺具有共同的诱变机制,都是通过细胞色素P450酶家族的代谢激活作用,不稳定代谢分解的产物变成了高度亲电物质,这种亲电物质与DNA反应形成烷基化的DNA碱基,烷基化DNA碱基导致DNA碱基对在复制过程中不匹配(图2)。
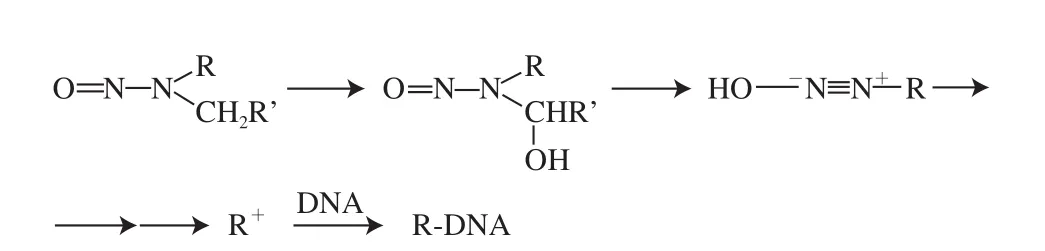
图22 N-烷基亚硝胺在细胞色素P450酶作用下典型的激活和转化途径[199--2200]]Fig.2 Typical activation and transformation pathways of N-alkylation nitrosamines under the action of cytochrome P450 enzyme[19-20]
1.2.2致畸性
除了致癌作用外,动物实验结果表明母体接触NOCs可引起仔鼠出现脑、眼、肋骨和脊柱畸形,通过这一结果可以推测NOCs可能具有致畸作用[21]。除此NOCs还可通过胎盘使子代受损,在妊娠初期使胚胎致死、妊娠中期使胚胎致畸、妊娠后半期诱发子代发生肿瘤,另外NOCs亦可通过乳汁诱发子代产生肿瘤[22]。
1.2.3毒性
NOCs的急性毒性表现为头晕、乏力、肝脏肿大、腹水、黄疸及肝脏病变[23]。如二烷基或者环状的N-亚硝胺主要是造成肝脏损伤,包括肝脏出血及小叶中心性坏死。N-亚硝酰胺所致肝中毒病变较轻,如有肝坏死则多为小叶周缘坏死。N-亚硝酰胺还可引起摄入部位的局部损伤,如经胃、皮肤、皮下时则可分别使胃、皮肤、皮下组织损伤[24]。
2 NOCs的体内外合成
2.1体外合成
NOCs是由亚硝化试剂(亚硝酸盐、氮氧化物等)与胺类物质(主要是二级胺类物)反应生成的[25]。这个二级胺可能由三级胺转化,而这个亚硝酸可能由铵和硝酸转化而来,这种含氮的前体物质(铵和硝酸转)广泛分布于水、土壤、植物中。大量的硝酸盐和亚硝酸盐的添加可在肉制品中防腐和发色;仲胺也存在于尿中和微生物生长的地方,三甲胺存在于鱼肉和海藻中。另外也有研究说明季胺也是NOCs合成的前体物质[26]。在微生物、天然催化剂以及人体内各种催化剂存在的情况下,这些前体物质被转化成相对应的NOCs,其反应速率与亚硝酸盐、胺类或酞胺类物质的浓度以及环境的pH值等有关,另外某些卤化物和有机溶剂如甲醇对其合成也有一定的催化作用[27]。在含有二级胺及NO2的典型的酸性环境中NOCs的合成途径[28-29]如下:
NO2+H+⇄HNO2(亚硝酸)
2 HNO2⇄N2O3+H2O(亚硝酐)
HNO2+H+⇄(H2NO2)+(氮酸离子)
N-亚硝胺的生成反应:
RR’NH+N2O3→RR’NNO+HNO2
N-亚硝酰胺的生产反应:
RNHCOR’+(H2NO2)+→RN(NO)COR’+H2O+H+
许多微生物在含有二甲胺和亚硝酸盐存在且pH值合适的食品中时都能合成NOCs,如米曲霉、大肠杆菌、链球菌和表皮葡萄球菌等。Ayanaba等[30]的研究表明被孢霉属的小孢褶孔菌能将三甲胺转化成二甲胺,而且这种细菌在有亚硝酸盐存在条件下能将二甲胺转化形成二甲基亚硝胺。食品中NOCs含量受许多因素,如肉类类型、亚硝酸盐、生物胺、具有氨基酸脱羧酶的活性微生物、水分、温度、pH值和潜在的氧化还原反应的影响[31]。食品加工过程中影响食品中N-亚硝胺生成量的因素也有很多,除了前体物质(亚硝酸盐、生物胺)的浓度、pH值、亚硝化反应的促进剂和抑制剂(抗坏血酸钠)的存在、预处理程序和条件、烟熏过程外,加热方式、加热温度和时间也有影响[32-33]。
2.2体内合成
硝酸盐以及亚硝酸盐作为NOCs合成的前体物质,来源广泛,其中饮食摄入的含量占总摄入量的87%[34]。除此之外还可通过呼吸作用吸入氮氧化物以及内源性合成,Green等[35]通过膳食研究指出尿液排出硝酸含量是人体摄入量的5 倍,所以硝酸盐以及亚硝酸盐以某种方式在活体组织合成。
在已被发现的NOCs中估计有45%~75%是由内源性合成[36]。而诸多的研究已经表明人和许多哺乳动物的胃是合成N-亚硝基化合物的主要场所。人的正常胃液pH值大致为pH 1.8~2.0,进食后可使pH值升到7.0左右,但经过大概20 min,又恢复到3.0,这种强酸性条件对二级胺和亚硝酸盐的体内合成是十分有利的[37]。而NOCs的合成量与亚硝酸盐成正比,反应最理想的酸度是pH值为1~3。因此若胃内含有足够的二级胺和亚硝酸盐时就可以形成NOCs[38]。在中性或者是微碱性条件下胃内也可以生成N-亚硝基化合物,那是由具有硝酸盐还原能力的细菌代谢活性增高造成的。除了哺乳动物的胃,受感染的膀胱和肠道等病变组织或器官也可形成NOCs,另外还有报告称NOCs在健康人的口腔内亦可形成[24]。
3 NOCs的体内外抑制研究
3.1NOCs的体外降解
从广义上讲抑制包括了阻断和降解,而NOCs的降解主要有吸附降解、高温裂解、紫外照射降解、氧化剂氧化裂解等方式。
3.1.1吸附降解
目前研究较多的是沸石吸附消除。沸石分子筛是具有形状选择性的多孔性材料,是一种高效吸附剂,在石油化工和精细化工中应用比较广泛。NOCs在H+型与Na+型沸石上分别是以酸催化及自由基热裂化进行裂解反应的,沸石上的质子酸中心是沸石催化降解NOCs的活性中心,ZSM-5沸石能够从溶液中强吸附N-亚硝基吡咯烷(N-nitrosopyrrolidine,NPYR),这将有利于沸石在环境保护中消除NPYR所产生的污染[39]。
烟气中N P Y R、N -亚硝基二甲胺(N-nitrosodimethylamine,NDMA)、六亚甲基亚硝胺(N-hexamethyleneimine,NHMI)等有害成分在HZSM-5、NaZSM-5、NaY等沸石上的脱附及分解效果,说明分子筛的孔径、亚硝胺分子的直径及其空间构型是影响吸附量的3 个重要因素;沸石上的质子酸中心是催化裂解N-亚硝胺的活性位,而质子酸中心与亚硝胺的相互作用过强,虽然不利于亚硝胺的分解却有利于对亚硝胺的吸附[40]。
除了沸石外,活性炭也可吸附一定量的NOCs,如Bombick等[41]研究了一种含有活性炭的滤嘴对卷烟气相成分的吸附作用,结果表明该滤嘴对卷烟气相成分中的特有的N-亚硝胺物质具有较高吸附率。
3.1.2高温裂解
NOCs中N—N=O基团在有水性有机酸存在的情况下,通过加热或者紫外照射,能生成相应的二级胺和亚硝酸[42]。加热使NOCs降解的原因是亚硝胺官能团N—N=O 中N—N键通常比C—H、C—C、C—N键弱,能在300 ℃左右热解过程中被断开。鉴于此人们尝试用高温催化法去除烟气中的N-亚硝胺,当卷烟燃烧时,高温活化催化剂,使N-亚硝胺瞬时催化降解,从而达到降低毒性的效果[43]。
3.1.3紫外照射降解
紫外照射降解NOCs的原理是利用羟基自由基(一种非选择性和强大的氧化剂)去撞击亚硝胺。在253.7 nm紫外照射,双氧水存在的情况下影响NOCs降解的主要因素包括过氧化氢量、紫外线照射强度、pH值、溶液中的无机阴离子。在有双氧水存在和紫外线照射条件下所有的NOCs退化表现出符合一级动力学模式,在60 min内,0.1 mg/L的任何亚硝胺都能被降解,除了N-亚硝基二苯胺(N-nitrosodiphenylamine,NDPhA)需要在25 μmol/L H2O2,pH 7.0,120 min条件下才能降解[44]。NOCs在N—N=O基团存在和水性有机酸,在加热或者紫外照射条件下,生产相应的二级胺和亚硝酸[45]。
3.1.4氧化剂氧化裂解
氧化剂氧化裂解NOCs,是一个极其复杂的氧化还原反应过程,并伴随着一系列的副产物的生成。羟自由基撞击是臭氧氧化降解NOCs的机理,羟自由基撞击胺氮和甲基生成甲胺;羟自由基撞击亚硝酰氮生成二甲胺。而在臭氧的氧化过程中还伴有铵的生成,那可能是由于甲胺在羟基存在下降解产生的,而氧化分解后甲胺、二甲胺和铵的量的比例是随着臭氧量的变化而变化的[46]。
在废水处理技术中有一种以Fe2+为催化剂,用H2O2进行化学氧化的方法,这种Fe2+与过氧化氢组成的体系,也称芬顿试剂。Hiramoto等[47]研究了生理条件下模拟芬顿试剂降解NDMA,结果表明不仅降解效果良好,反应过程中还能释放NO。芬顿试剂之所以能降解亚硝胺是因为在自由基反应中能生成强氧化性的羟自由基,在水溶液中与难降解的有机物生成有机自由基使之结构遭到破坏,最终氧化分解。降解机理如图3所示(以NDMA为例)[48]。
Fe2++H2O2=Fe3++OH-+·OH
Fe3++H2O2+OH-=Fe2++H2O+·OH
Fe3++H2O2=Fe2++H++HO2
HO2+H2O2=H2O+O2↑+OH
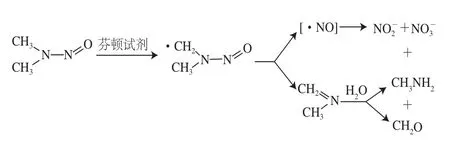
图3 酸性条件下芬顿试剂降解NDMA的机理[[4488]]Fig.3 Proposed mechanism of NDMA degradation by Fenton reagent in an acidic solution[48]
虽然对NOCs的降解已有较多的研究,且一些结果较令人满意,但由于高水溶性以及半挥发性、生物富集性、生物降解性以及颗粒的吸附性,完全消除NOCs是不切实际的[49]。
3.2NOCs的体外阻断
在减少NOCs对人体危害最好的办法就是在其形成前去除其前体物质,阻断其合成来达到防癌的目的。阻断是通过阻断NOCs形成途径,降低其浓度,从而达到去除效果,这个过程发生在NOCs形成之前。研究表明一些天然产物在体内外对NOCs的合成都具有阻断作用,如咖啡因、胱氨酸、组氨酸、半胱氨酸、丙氨酸、甘氨酸、三肽、谷胱甘肽及一些食品抗氧化剂[50]。在抗氧化剂中VC已被广泛地证实具有阻断NOCs合成的效果[51-52]。VE也被证实对亚硝胺具有较好的阻断作用[52],而VC在所有可阻断NOCs的物质中是最有效的,当其分子浓度2 倍于亚硝酸盐时,可完全阻断NOCs的生成,无论是在机体内还是在食品中皆能起到阻断效果[24]。
除了上述一些天然产物和抗氧化剂外,诸多的研究者通过在体外模拟人胃液条件下,研究了部分果蔬及其提取物对NOCs的体外合成的抑制实验,证明了这些物质具有阻断NOCs合成作用和抑制变异原作用[53]。这些物质之所以能够抑制NOCs的合成,主要是含有抗坏血酸、黄酮类、多酚类、硫化物等。抗坏血酸对NOCs的阻断机理可能是通过还原亚硝化试剂比如亚硝酸生成无害的产物N2和NO,或者清除亚硝基阳离子(NO+)来实现对NOCs的生成阻断。
大量的研究已经证实大蒜中含有的硫化物和苯二羧酸类是大蒜产生阻断作用的主要活性成分。这些物质能与亚硝酸盐结合生成硫代亚硝酸酯,从而抑制亚硝基化反应的发生[54-55]。黄酮类化合物则可能与其通过提高机体超氧化物歧化酶(superoxide dismutase,SOD)水平,清除自由基的作用来阻断NOCs在体内的合成。有报道指出,酚类化合物在酸性条件下易被NO2氧化成醒类化合物,并将NO2-还原成一氧化氮,从而抑制NOCs的生成[56]。姜慧萍[57]的研究表明:在苯酚、二甲胺、NO2-共存的反应体系中,苯酚的酚轻基竞争性的与NO2-结合,阻断二甲胺与NO2-发生亚硝化反应,从而能够有效抑制N-亚硝基二甲胺的生成。
茶多酚具有多个酚羟基,酚羟基中的氧原子为SP2杂化状态,氧原子上两对未共用电子对之一占据未参与杂化的P轨道,可以与苯环形成P-π共扼体系,电子云密度向苯环转移,氢氧之间的电子云密度比醇中的低,即氢氧之间的结合减弱,使氢离子能以H+的形式解离,H+能与亚硝酸反应,消耗亚硝酸根[58]。以下列举了一些可阻断NOCs合成的果蔬和某些天然产物及其对NOCs的阻断率。
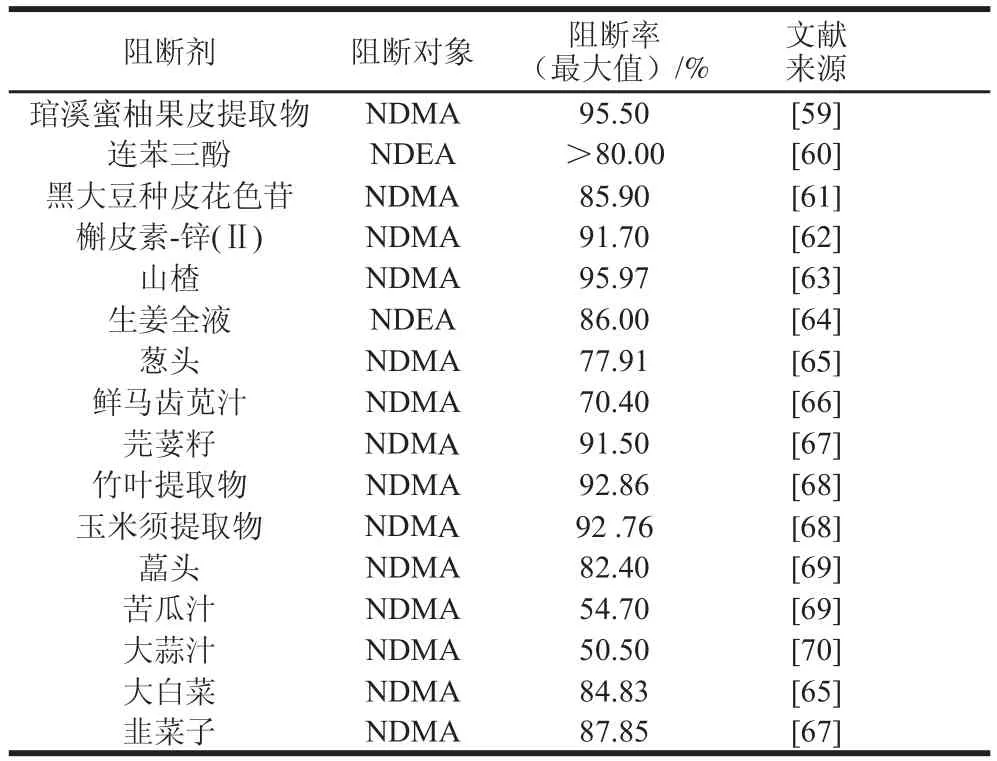
表2 部分果蔬及其提取物对NOCs合成的阻断作用Table 2 Blocking effects of fruits and vegetables and their extracts on the synthesis of NOCs
3.3NOCs的体内抑制研究
在体内如何抑制NOCs合成这个问题上,研究人员主要研究方向集中在食用果蔬、中草药及其提取物对NOCs合成的抑制,这符合现代人追求饮食健康以及食疗的理念。流行病学研究表明山东居民食大蒜的量与胃癌死亡率成显著负相关,同时体外实验也表明大蒜素具有抑制NOCs合成的作用[71],这说明食用大蒜后,进入人体内的大蒜素等物质可以抑制NOCs的合成。而体内抑制NOCs的效果主要是以血清谷丙转氨酶为评价指标。在体内酸性环境中,仲、叔胺类与亚硝胺盐反应形成强致癌物——NOCs,NOCs通过血液循环进入肝细胞中,破坏肝细胞,致使肝组织中的谷丙转氨酶进入血液。吴春等[62]的研究表明给药组血清谷丙转氨酶较对照组明显降低,其中高剂量组血清谷丙转氨酶接近正常组,且槲皮素-锌(Ⅱ)配合物的浓度与血清谷丙转氨酶的量存在剂量效应关系。金长炼等[72]的研究表明洋虫除了清除具有亚硝酸钠及阻断二甲基亚硝胺合成作用外,可能还有很强的保护肝组织,降低血清谷丙转氨酶的作用途径。
4 结 语
本文综述了强致癌物NOCs在体内外合成及抑制的研究进展,总结了NOCs的分类、性质和对人体的危害、体内外合成、以及消除和阻断方法,得到了一些阻断及降低NOCs对人体危害的方法。为了能够有效控制人体摄入NOCs的前体物,控制整个食物链中亚硝酸盐和生物胺等前体物的含量将会是研究人员的一个着手点,这也意味着严密监控从动植物生长、采收、加工再到被消费者消费的整个环节将会显得越来越重要。随着科技和人类文明的进步,NOCs对人体的危害将会降到最低。
参考文献:
[1]SIEGEL R,NAISHADHAM D,JEMAL A.Cancer statistics,2013[J].CA:A Cancer Journal for Clinicians,2013,63(1):11-30.DOI:10.3322/caac.21166.
[2]郭瑞杰.P450催化下几种不同类型亚硝胺羟基化代谢机理的理论研究[D].北京:北京工业大学,2013:1-2.
[3]FLOWER C,CARTER S,EARLS A,et al.A method for the determination of N-nitrosodiethanolamine in personal care productscollaboratively evaluated by the CTPA Nitrosamines Working Group[J].International Journal of Cosmetic Science,2006,28(1):21-33.DOI:10.1111/j.1467-2494.2006.00294.x.
[4]PREUSSMANN R.Carcinogenic N-nitroso compounds and their environmental signifi cance[J].Naturwissenschaften,1984,71(1):25-30.DOI:10.1007/BF00365976.
[5]DIETRICH M,BLOCK G,POGODA J M,et al.A review:dietary and endogenously formed N-nitroso compounds and risk of childhood brain tumors[J].Cancer Causes & Control,2005,16(6):619-635.DOI:10.1007/s10552-005-0168-y.
[6]YAMAMOTO H,MOMIYAMA N.Rich chemistry of nitroso compounds[J].Chemical Communications,2005,36(46):3514-3525.DOI:10.1039/b503212c.
[7]LEE J,CHEN L,WEST A H,et al.Interactions of organic nitroso compounds with metals[J].Chemical Reviews,2002,102(4):1019-1066.DOI:10.1021/cr0000731.
[8]LEE M,LEE Y,SOLTERMANN F,et al.Analysis of N-nitrosamines and other nitro(so)compounds in water by high-performance liquid chromatography with post-column UV photolysis/Griess reaction[J].Water Research,2013,47(14):4893-4903.DOI:10.1016/j.watres.2013.05.031.
[9]ANDRZEJEWSKI P,KASPRZYK-HORDERN B,NAWROCKI J.The hazard of N-nitrosodimethylamine(NDMA)formation during water disinfection with strong oxidants[J].Desalination,2005,176(1):37-45.DOI:10.1016/j.desal.2004.11.009.
[10]KOK T M C M D,ENGELS L G J B,MOONEN E J,et al.Inflammatory bowel disease stimulates formation of carcinogenic N-nitroso compounds[J].Gut,2005,54(5):731-731.DOI:10.1136/gut.2004.057471.
[11]戴乾圜,逯萍,彭少华,等.黄曲霉素和N-亚硝基化合物借诱发DNA互补碱对交联而启动癌变[J].自然科学进展,2003,13(7):693-697.
[12]ZHOU H N,CALAF G M,HEI T K.Malignant transformation of human bronchial epithelial cells with the tobacco-specifi c nitrosamine,4-(methylnitrosamino)-1-(3-pyridyl)-1-butanone[J].International Journal of Cancer,2003,106(6):821-826.DOI:10.1002/ijc.11319.
[13]PREUSSMANN R,STEWART B W.N-Nitroso carcinogens[J].Chemical Carcinogens,1984,2(2):643-828.DOI:10.1016/0015-6264(68)90297-6.
[14]SHIBATA M A,FUKUSHIMA S,TAKAHASHI S,et al.Enhancing effects of sodium phenobarbital and N,N-dibutylnitrosamine on tumor development in a rat wide-spectrum organ carcinogenesis model[J].Carcinogenesis,1990,11(6):1027-1031.DOI:10.1093/carcin/11.6.1027.
[15]潘世宬.亚硝胺类化合物致癌作用的某些问题[J].生理科学进展,1979,10(2):124-133.
[16]胡荣梅,马立珊.化学致癌物质N-亚硝基化合物的研究概述[J].江苏医药,1978(6):12.
[17]方如康.亚硝胺类化合物致癌问题的探讨[J].肿瘤,1985,5(2):13.
[18]GNEWUCH C T,SOSNOVSKY G.A critical appraisal of the evolution of N-nitrosoureas as anticancer drugs[J].Chemical Reviews,1997,97(3):829-1014.DOI:10.1021/cr941192h.
[19]MESTANKOVA H,SCHIRMER K,CANONICA S,et al.Development of mutagenicity during degradation of N-nitrosamines by advanced oxidation processes[J].Water Research,2014,66(12):399-410.DOI:10.1016/j.watres.2014.08.012.
[20]INAMI K,ISHIKAWA S,MOCHIZUKI M.Activation mechanism of N-nitrosodialkylamines as environmental mutagensand its application to antitumor research[J].Genes and Environment,2009,31(4):97-104.DOI:10.3123/jemsge.31.97.
[21]林昆.食物中总亚硝基化合物及其相关危险因素研究[J].卫生研究,2005,34(3):350-352.DOI:10.3969/j.issn.1000-8020.2005.03.031.
[22]魏法山,徐幸莲,周光宏.挥发性N-亚硝基化合物的分析方法[J].食品科学,2008,29(7):479-484.
[23]郑雯,邵英秀.N-亚硝基化合物的危害性,来源及预防措施[J].北京农业,2011(15):8-9.
[24]宋圃菊.N-亚硝基化合物[J].中国酿造,1995,14(3):3-8.
[25]LUNN J C,KUHNLE G,MAI V,et al.The effect of haem in red and processed meat on the endogenous formation of N-nitroso compounds in the upper gastrointestinal tract[J].Carcinogenesis,2006,28(3):685-690.DOI:10.1093/carcin/bgl192.
[26]KEMPER J M,WALSE S S,MITCH W A.Quaternary amines as nitrosamine precursors:a role for consumer products?[J].Environmental Science & Technology,2010,44(4):1224-1231.DOI:10.1021/es902840h.
[27]李腾,李捍东,王平,等.N-亚硝基化合物的检测及去除方法研究进展[C]//中国毒理学会环境与生态毒理学专业委员会第二届学术研讨会暨中国环境科学学会环境标准与基准专业委员会2011年学术研讨会会议论文集.南京:中国环境科学出版社,2011:256-261.
[28]MIRVISH S S.Role of N-nitroso compounds(NOCS)and N-nitrosation in etiology of gastric,esophageal,nasopharyngeal and bladder cancer and contribution to cancer of known exposures to NOCS[J].Cancer Letters,1995,93(1):17-48.DOI:10.1016/0304-3835(95)03786-V.
[29]MIRVISH S S.Formation of N-nitroso compounds:chemistry,kinetics,and in vivo occurrence[J].Toxicology and Applied Pharmacology,1975,31(3):325-351.DOI:10.1016/0041-008X(75)90255-0.
[30]AYANABA A,ALEXANDER M.Microbial formation of nitrosamines in vitro[J].Applied Microbiology,1973,25(6):862-868.
[31]WANG Y,LI F,ZHUANG H,et al.Effects of plant polyphenols and α-tocopherol on lipid oxidation,residual nitrites,biogenic amines,and N-nitrosamines formation during ripening and storage of dry-cured bacon[J].LWT-Food Science and Technology,2015,60(1):199-206.DOI:10.1016/j.lwt.2014.09.022.
[32]YURCHENKO S,MÖLDER U.The occurrence of volatile N-nitrosamines in Estonian meat products[J].Food Chemistry,2007,100(4):1713-1721.DOI:10.1016/j.foodchem.2005.10.017.
[33]BYUN M W,AHN H J,KIM J H,et al.Determination of volatile N-nitrosamines in irradiated fermented sausage by gas chromatography coupled to a thermal energy analyzer[J].Journal of Chromatography A,2004,1054(1):403-407.DOI:10.1016/S0021-9673(04)01302-0.
[34]HUARTE-MENDICOA J C,ASTIASARAN I,BELLO J.Nitrate and nitrite levels in fresh and frozen broccoli.Effect of freezing and cooking[J].Food Chemistry,1997,58(1):39-42.DOI:10.1016/S0308-8146(96)00193-8.
[35]GREEN L C,de LUZURIAGA K R,WAGNER D A,et al.Nitrate biosynthesis in man[J].Proceedings of the National Academy of Sciences,1981,78(12):7764-7768.DOI:10.1073/pnas.78.12.7764.
[36]TRICKER A R.N-Nitroso compounds and man:sources of exposure,endogenous formation and occurrence in body fluids[J].European Journal of Cancer Prevention,1997,6(3):226-268.DOI:10.1097/00008469-199706000-00003.
[37]马泰,徐德祥.食品中N-亚硝基化合物及其致癌作用[EB/OL].(2005-12-22)[2015-02-11].http://d.wanfangdata.com.cn/Conference/7056395.
[38]惠永倩.强化学致癌物:N-亚硝基化合物[J].人民军医,1982,15(1):25-27.
[39]马丽丽,严冬.沸石对于亚硝胺的吸附和裂解[J].宁夏大学学报(自然科学版),2001,22(2):208-210.DOI:10.3969/j.issn.0253-2328.2001.02.048.
[40]缪应菊,刘维涓,王亚明,等.沸石分子筛降低卷烟烟气中亚硝胺的研究进展[J].化工科技市场,2007,30(9):6-9.
[41]BOMBICK D W,BOMBICK B R,AYRES P H,et al.Evaluation of the genotoxic and cytotoxic potential of mainstream whole smoke and smoke condensate from a cigarette containing a novel carbon filter[J].Toxicological Sciences,1997,39(1):11-17.DOI:10.1006/faat.1997.2334.
[42]MITCH W A,SHARP J O,TRUSSELL R R,et al.N-Nitrosodimethylamine(NDMA)as a drinking water contaminant:a review[J].Environmental Engineering Science,2003,20(5):389-404.DOI:10.1089/109287503768335896.
[43]谢兰英,刘琪,朱效群,等.卷烟烟气N-亚硝胺化合物及其吸附催化降解研究进展[J].环境科学与技术,2006,29(增刊1):133-135.
[44]ZHOU C,GAO N,DENG Y,et al.Factors affecting ultraviolet irradiation/hydrogen peroxide(UV/H2O2)degradation of mixed N-nitrosamines in water[J].Journal of Hazardous Materials,2012,231(32):43-48.DOI:10.1016/j.jhazmat.2012.06.032.
[45]KODAMATANI H,YAMAZAKI S,SAITO K,et al.Highly sensitive method for determination of N-nitrosamines using high-performance liquid chromatography with online UV irradiation and luminol chemiluminescence detection[J].Journal of Chromatography A,2009,1216(1):92-98.DOI:10.1016/j.chroma.2008.11.025.
[46]LÜ J,LI Y,SONG Y.Reinvestigation on the ozonation of N-nitrosodimethylamine:influencing factors and degradation mechanism[J].Water Research,2013,47(14):4993-5002.DOI:10.1016/j.watres.2013.05.035.
[47]HIRAMOTO K,RYUNO Y,KIKUGAWA K.Decomposition of N-nitrosamines,and concomitant release of nitric oxide by Fenton reagent under physiological conditions[J].Mutation Research/Genetic Toxicology and Environmental Mutagenesis,2002,520(1):103-111.DOI:10.1016/S1383-5718(02)00168-7.
[48]HEUR Y H,STREETER A J,NIMS R W,et al.The Fenton degradation as a nonenzymic model for microsomal denitrosation of N-nitrosodimethylamine[J].Chemical Research in Toxicology,1989,2(4):247-253.DOI:10.1021/tx00010a006.
[49]DAVIE M G,REINHARD M,SHAPLEY J R.Metal-catalyzed reduction of N-nitrosodimethylamine with hydrogen in water[J].Environmental Science & Technology,2006,40(23):7329-7335.DOI:10.1021/es061097d.
[50]张文敏.N-亚硝基化合物在动物及人体内的合成[J].国外医学(卫生学分册),1981,2(3):78-81.
[51]MIRVISH S S,GOLD B,EAGEN M,et al.Kinetics of the nitrosation of aminopyrine to give dimethylnitrosamine[J].Zeitschrift für Krebsforschung und Klinische Onkologie,1974,82(4):259-268.DOI:10.1007/BF00285560.
[52]RYWOTYCKI R.The effect of baking of various kinds of raw meat from different animal species and meat with functional additives on nitrosamine contamination level[J].Food Chemistry,2007,101(2):540-548.DOI:10.1016/j.foodchem.2006.02.012.
[53]SUZZI G,GARDINI F.Biogenic amines in dry fermented sausages:a review[J].International Journal of Food Microbiology,2003,88(1):41-54.DOI:10.1016/j.foodchem.2006.02.012.
[54]CHOI S Y,CHUNG M J,LEE S J,et al.N-Nitrosamine inhibition by strawberry,garlic,kale,and the effects of nitrite-scavenging and N-nitrosamine formation by functional compounds in strawberry and garlic[J].Food Control,2007,18(5):485-491.DOI:10.1016/j.foodcont.2005.12.006.
[55]CHUNG M J,LEE S H,SUNG N J.Inhibitory effect of whole strawberries,garlic juice or kale juice on endogenous formation of N-nitrosodimethylamine in humans[J].Cancer Letters,2002,182(1):1-10.DOI:10.1016/S0304-3835(02)00076-9.
[56]PIGNATELLI B,BEREZIAT J C,DESCOTES G,et al.Catalysis of nitrosation in vitro and in vivo in rats by catechin and resorcinol and inhibition by chlorogenic acid[J].Carcinogenesis,1982,3(9):1045-1049.DOI:10.1093/carcin/3.9.1045.
[57]姜慧萍.黄酮类化合物体外抑制N-亚硝基二乙胺生成的研究[D].杭州:浙江工商大学,2009:74-79.
[58]邢必亮,徐幸莲.降低腌肉亚硝胺含量的复合抗氧化剂研究[J].食品科学,2011,32(1):104-107.
[59]黄高凌,翁聪泽,倪辉,等.琯溪蜜柚果皮提取物抑制亚硝化反应的研究[J].食品科学,2007,28(12):36-39.DOI:10.3321/j.issn:1002-6630.2007.12.003.
[60]董彦佐,李学理,何秀丽,等.典型酚类化合物清除亚硝酸钠及对二乙基亚硝胺生成的影响[J].食品科学,2014,35(13):132-136.DOI:10.7506/spkx1002-6630-201413025.
[61]吴春,陈林林,李俊生.黑大豆种皮花色苷对亚硝胺体内外合成的阻断作用[J].中国粮油学报,2012,27(1):25-28.DOI:10.3969/j.issn.1003-0174.2012.01.006.
[62]吴春,黄梅桂.槲皮素-锌(Ⅱ)配合物体内外抑制亚硝胺合成的研究[J].食品科学,2007,28(9):35-38.
[63]赵二劳,王晓妮,张海容,等.山楂清除亚硝酸盐及阻断亚硝胺合成的研究[J].食品与发酵工业,2006,32(10):29-31.DOI:10.3321/j.issn:0253-990X.2006.10.008.
[64]陈小国.生姜对亚硝胺合成阻断作用初探[J].食品科学,1989,10(6):35-38.DOI:10.3321/j.issn:1002-6630.1989.06.002.
[65]于世光,刘志诚,于守洋.常见蔬菜阻断N-亚硝基化合物(NC)形成的研究[J].营养学报,1988,10(1):26-34.
[66]李洪军,阚建全,解纯刚,等.野生马齿苋抑制亚硝胺合成的体外试验[J].营养学报,1998,20(3):361-366.DOI:10.3321/j.issn:0512-7955.1998.03.025.
[67]时艳玲,王光慈.某些香辛料精油抑制N-二甲基亚硝胺体外合成的研究[J].西南农业大学学报,1997,19(4):359-362.
[68]许钢.玉米提取物抑制亚硝化反应的研究[J].中国粮油学报,2004,19(4):42-45.DOI:10.3321/j.issn:1003-0174.2004.04.011.
[69]阚健全,王光慈,陈宗道,等.藠头和苦瓜汁抑制亚硝胺合成的体外试验[J].营养学报,1995,17(4):409-413.
[70]CHOI S Y,CHUNG M J,LEE S J,et al.N-Nitrosamine inhibition by strawberry,garlic,kale,and the effects of nitrite-scavenging and N-nitrosamine formation by functional compounds in strawberry and garlic[J].Food Control,2007,18(5):485-491.DOI:10.1016/j.foodcont.2005.12.006.
[71]王美岭,高曼玲,杜晓力,等.大蒜在体内外抑制亚硝胺合成的研究[J].实用肿瘤学杂志,1990,11(4):26-29.
[72]金长炼,张善玉,金龙顺,等.洋虫对清除体内外亚硝酸钠和阻断二甲基亚硝胺合成的影响[J].延边大学医学学报,1997,20(1):10-12.
Progress in Hazards,Synthesis and Inhibition of N-Nitroso Compounds in Vitro and in Vivo
CAI Lufeng1,2,LI Na1,2,DU Sha1,TAN Ya1,LI Ke1,WANG Yuanliang1,*
(1.Hunan Province Key Laboratory of Food Science and Biotechnology,College of Food Science and Technology,Hunan Agricultural University,Changsha 410128,China; 2.Cooking Department of Hunan Commercial Technician Institute,Zhuzhou 412000,China)
Abstract:In this article,the properties of N-nitrosamines and N-nitrosoamides are introduced briefly.The hazards of NOCs to human and animals are summarized with respect to carcinogenicity,teratogenicity and toxicity.Subsequently,the pathways and mechanisms for the synthesis in vivo and in vitro of the N-nitroso compounds(NOCs)and the affecting factors are discussed.Finally,the methods used to inhibit N-nitrosamines and N-nitrosoamides in vivo and in vitro by elimination and blocking and the underlying mechanism are reviewed,aiming to provide theoretical references to fi nd other methods or mechanisms for NOC suppression and elimination.
Key words:N-nitroso compounds; harm; synthesis; inhibition
中图分类号:R151;R155
文献标志码:A
文章编号:1002-6630(2016)05-0271-07
DOI:10.7506/spkx1002-6630-201605047 10.7506/spkx1002-6630-201605047.http://www.spkx.net.cn
*通信作者:王远亮(1977—),男,教授,博士,研究方向为食品生物技术。E-mail:Wang@hunau.net
作者简介:蔡鲁峰(1989—),男,硕士研究生,研究方向为食品生物技术。E-mail:xslhdb@163.com
基金项目:湖南省战略性新兴产业项目(2014GK1034);湖南省自然科学基金资助项目(11JJ4019);
收稿日期:2015-05-25
