腹腔镜超声在腹腔镜左半肝切除术中的应用研究
2016-03-30汪磊李宏宁波市医疗中心李惠利医院肝胆微创外科浙江宁波315000
汪磊,李宏(宁波市医疗中心李惠利医院肝胆微创外科,浙江宁波315000)
腹腔镜超声在腹腔镜左半肝切除术中的应用研究
汪磊,李宏
(宁波市医疗中心李惠利医院肝胆微创外科,浙江宁波315000)
[摘 要]目的 探讨腹腔镜超声(laparoscopic ultrasound,LUS)在腹腔镜左半肝切除术(laparoscopic left hemi-hepatectomy,LLH)中的应用价值。方法 选取2012年3月至2014年3月我院肝胆微创外科收治的66例行腹腔镜左半肝切除术患者的临床资料。根据是否使用LUS分为两组:超声组36例,术中使用LUS;对照组30例,未使用LUS者。比较两组患者的手术时间、术中出血量、肝中静脉损伤率、术后并发症、术后住院时间等。结果 与对照组比,超声组术中出血量、肝中静脉损伤率、中转开腹率减少,差异有统计学意义(P<0.05);但手术时间、术后并发症、术后住院时间差异无统计学意义(P>0.05)。结论 在腹腔镜左半肝切除术中使用LUS可以有效减少术中出血量、肝中静脉损伤从而避免中转开腹,但并不会延长手术时间,不会增加术后并发症发生率,不会缩短住院时间。LUS可以为腹腔镜左半肝切除手术提供“指引”,增加了手术的安全性,值得临床推广。
[关键词]腹腔镜;腹腔镜超声;左半肝切除;肝胆管结石;肝肿瘤
与开腹手术比,腹腔镜左半肝切除术比具有术中出血少、手术创伤小、机体应激反应轻、患者痛苦少、术后住院时间短等优势,已被广大肝脏外科医师所认可[1-2]。但在腹腔镜手术中术者不能对腹腔内重要脏器或者重要结构进行触诊,产生“触觉丧失”;还有腹腔镜显示器提供的“二维平面”视野缺乏手术立体感,视觉信息不如开腹手术充分,使得腹腔镜左半肝切除手术的风险较开腹手术高[3]。而腹腔镜超声的出现解决了这些问题,提高了腹腔镜左半肝切除手术的安全性,增加了手术的精准性。本研究选取2012年3月至2014年3月在我院肝胆微创外科开展的部分腹腔镜左半肝切除术患者共计66例,探讨腹腔镜超声在腹腔镜左半肝切除术中的临床应用价值。
1 资料和方法
1.1一般资料
入选66例,包括肝内胆管结石48例,原发性肝癌18例。根据术中是否使用腹腔镜超声分为超声组(36例)和对照组两组(30例)。两组患者的性别比、年龄、BMI指数、病例分类数、Child分级等各项临床资料具有可比性,差异无统计学意义(P>0.05),见表1。
1.2纳入标准
(1)肝功能Child分级B级及以上,吲哚菁绿排泄试验评估肝脏储备功能在相对正常范围;(2)原发性肝癌:病变局限于左半肝内,直径<8 cm,行半肝切除可根治性切除肿块,肿块内侧缘距离肝中静脉的最短距离≥3 cm;(3)肝内胆管结石:结石范围局限于左半肝;(4)无上腹部手术史。
1.3排除标准
参照文献[4]。(1)不能耐受气腹及全身麻醉;(2)手术部位以外其他器官存在重大疾病;(3)术前怀疑为肝内胆管细胞癌或肝内胆管细胞癌患者;(4)原发性肝癌:病变紧邻第一、第二或第三肝门影响暴露和分离,肝门被侵犯或病变本身需要大范围的肝门淋巴结清扫,病变紧邻或直接侵犯大血管,门静脉内、胆管内癌栓,肿瘤肝内或远处广泛转移而无法手术等情况;(5)腹腔内粘连难以分离暴露病灶者。
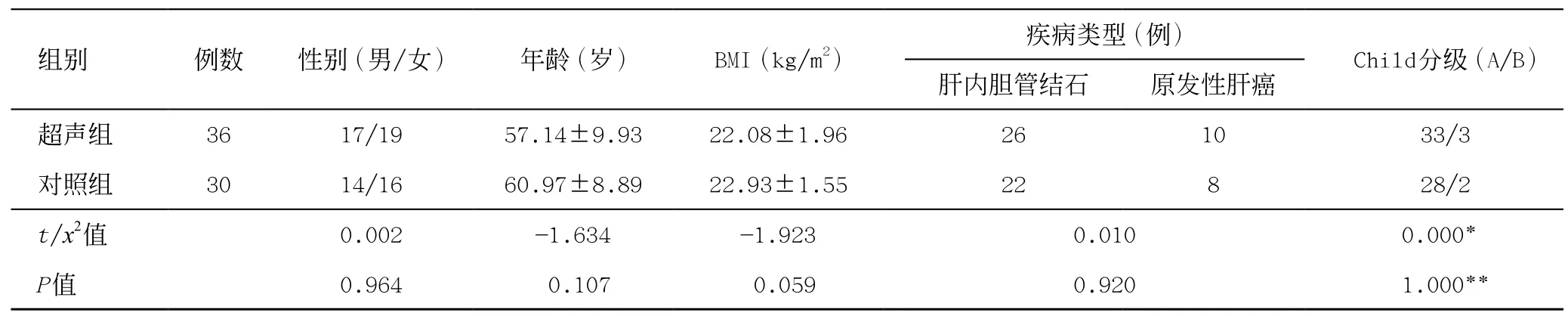
表1 超声组和对照组患者一般基本资料的比较

表2 两组患者术中各项指标的比较
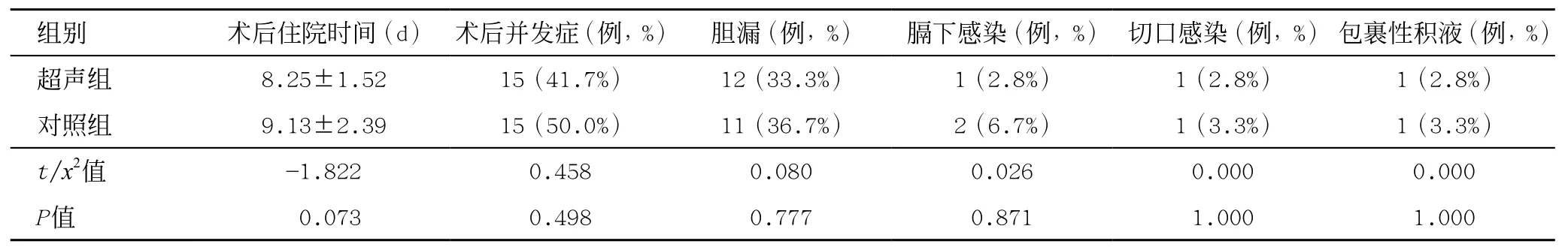
表3 两组患者术后各项指标比较
1.4LUS检查方法
首先需要建立人工气腹,压力设定为13 mmHg,其次根据检查目的选取LUS的穿刺部位,使用12 mm一次性Trocar建立LUS检查通道。如为恶性肿瘤应先行腹腔镜探查整个腹腔,随后LUS检查肝脏。剑突下,左、右上腹肋缘下,脐平面左、右腹直肌外侧缘等通道均可作为LUS检查肝脏的通道。相应通道的选择往往是依据检查目的和术者的操作习惯而确定,可以通过在多个通道内相互转换LUS探头完成对整个肝脏的扫描。LUS扫描顺序为先进行肝脏膈面的扫描,再进行肝脏脏面的扫描;先扫描需要保留的无病灶侧肝叶(段),再扫描病灶所在侧肝叶(段)。对于位置深在的肝段(如第I、VII、VIII段等),可切断肝三角韧带、镰状韧带、肝圆韧带等肝脏周围韧带,使肝脏趋于游离,通过助手使用腹腔镜器械的牵拉,利用LUS探头的末端可屈曲性,将探头伸入“肝裸区”,扫描第VII、VIII肝段以检查第二肝门肝静脉起始部位。借助腹腔镜器械向上牵拉肝脏,可在脏面扫描第I肝段。LUS检查肝脏的整个过程应该保持连续的“逐层”扫描,避免“跳跃式”检查,操作时应细致、全面,应强调从肝脏的脏面和膈面两面进行扫描,避免疏漏肝内微小病灶。对怀疑病灶附近有重要血管或者需要明确肝内重大血管位置情况时,LUS的彩色多普勒(color dropper flow imaging,CDFI)功能可以清晰显示探头下方血管及血管内血流情况,可以通过变换探头角度,取得最满意的超声窗。
1.6统计学分析
2 结果
2.1术中各项指标
与对照组比,超声组手术时间接近,差异无统计学意义(P>0.05)。但术中出血量、肝中静脉损伤率方面,超声组要少于对照组,差异有统计学意义(P<0.05)。对照组中出现肝中静脉损伤造成大出血均发生在开展腹腔镜左半肝切除的早期,因早期腹腔镜下止血技术有限,防止术中因发生二氧化碳气栓造成更严重的并发症,均中转开腹手术。见表2。
2.2术后各项指标
两组在术后并发症、术后住院时间方面比较差异均无统计学意义(P>0.05),见表3。胆漏患者通过术中放置的引流管通畅引流后治愈,膈下感染患者经过术后穿刺引流后治愈,切口感染均经过长期换药处理后愈合,无术后切口疝形成。腹腔内包裹性积液患者6个月后积液自行吸收。
2.3随访情况
所有患者无术中及住院死亡病例,18例肝癌患者标本切缘均阴性。术后所有患者采取门诊复查随访方式,内容包括腹部B超、CT、MRI检查。随访时间6~18个月,平均12个月。超声组:26例肝内胆管结石患者2例术后2周T管造影提示肝内胆管内有结石,于术后2月行胆道镜取石,其余患者未发现残留结石。10例原发性肝癌患者中2例分别于术后第11、13个月后出现肝癌复发,CT证实1例为右肝前叶单个病灶(术中证实为2枚),给予射频消融治疗;1例为肝内多发癌灶,行DSA介入化疗。对照组:22例肝内胆管结石患者2例术后复查CT、T管造影发现肝内胆管残留结石,行胆道镜取石,其余患者未发现残留结石;8例原发性肝癌患者中2例于术后第10、14个月出现肿瘤复发,CT证实2例均为肝内多发癌灶,1例行DSA介入化疗,1例放弃治疗;其余原发性肝癌患者术后定期复查满18个月未发现肿瘤复发、转移。
3 讨论
3.1LUS的学习曲线
在本次研究中,术中使用LUS检查肝脏的时间一般在5~30 min。刚开始使用LUS,往往耗时稍长,为了获得更好的超声窗,需要不断调试。对肝内结构超声图像的判断,也由不熟悉逐渐向熟悉过度。我们认为,一个有经验的外科医生,需要在医院的超声科室正规学习6个月左右,才能掌握对超声图像的基本特点,而术中全程操作LUS超过20例,才能熟练运用LUS的使用技巧,获得满意的超声窗。在一段时间的学习和使用后,逐渐掌握LUS的操作技巧,术中使用LUS的时间明显呈下降趋势,说明LUS的使用存在一定的学习曲线,一旦熟练掌握和运用LUS后,并不会对整体手术时间有明显延长,这与本组研究数据结论符合。
3.2腹腔镜左半肝切除术技术要点
笔者的操作体会是:采取“五孔法”切肝,脐下为腹腔镜观察孔,左中、上腹部,右中、上腹部分别建立四个操作孔。其中,使用12 mm一次性Trocar建立的右中腹操作孔,既可以作为腹腔镜左半肝切除术的主操作孔,也可以作为术中LUS检查的操作孔,见图1。首先处理第一、二肝门部血管,阻断相应左半肝入肝血流,再行肝切除术,以避免术中发生难以控制的出血,减少气栓发生。超声刀解剖第一肝门,分离肝动脉、门静脉和胆管左右支,Hem-o-lok夹闭患侧半肝入肝血管、胆管后离断,解剖第二肝门,仔细分离肝左、肝中、肝右静脉,钛夹夹闭后切断,如术中发现解剖第二肝门困难,可不必强行游离,LUS确定肝中静脉后使用超声刀、LigaSure切肝[5]。肝创面≥3 mm管道使用可吸收夹、Hem-o-lok关闭,<3 mm管道超声刀凝闭即可,超声刀在凝闭3 mm以下的肝内管道的效果是可靠的[6]。肝创面渗血处使用氩气刀喷凝或腔镜下缝扎止血。创面内放置1~2根腹腔引流管以利术后引流。
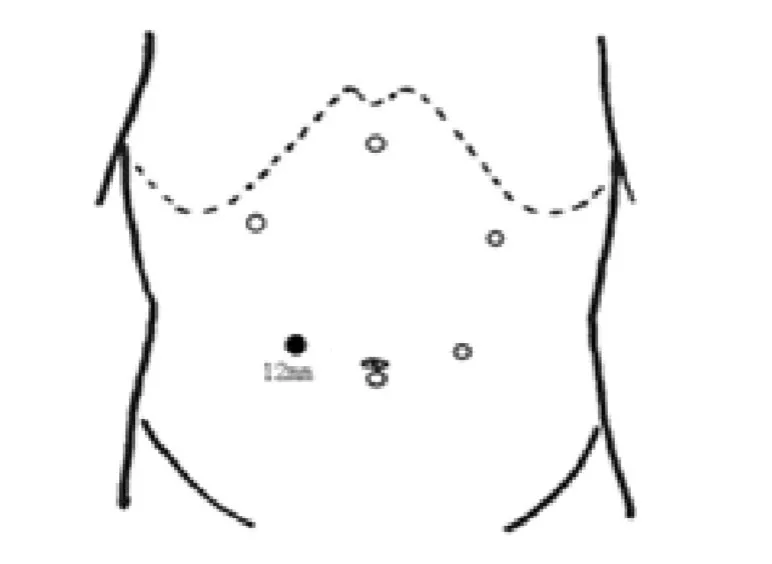
图1 腹腔镜左半肝切除术Trocar位置分布
3.2LUS在“精准”确定半肝切除线中的应用
LUS的CDFI功能准确判定了肝中静脉位置及走行,能够显示“肉眼”无法辨别的肝脏内部结构,增加了手术的“直观感”,为实施“精准”肝切除提供了条件。传统的Cantlie线或半肝阻断后形成的缺血线,可能产生偏差的原因有:(1)受困于腹腔镜镜头和屏幕的二维呈像效果的限制,实际中发现在腹腔镜下观察肝缺血线有时很不明显,镜下定位困难;(2)肝动脉和门静脉常常存在交通支和侧支血管,只阻断入肝血流往往阻断效果欠佳,因此缺血线无法形成或不明显;(3)半肝阻断法只是阻断第一肝门内入肝血供,并没有考虑其到残存肝叶的静脉回流,而肝静脉的变异情况较多;(4)门静脉存在变异情况或由于肝内病灶挤压、肝内炎症因素造成的牵拉导致肝中静脉偏移,导致缺血线和肝中静脉实际位置存在较大偏差;(5)部分患者存在肝中动脉,实施腹腔镜左半肝切除术时需要切断此动脉,但切断后会对剩余肝脏血供产生影响,造成缺血范围增大,缺血线与肝中静脉偏差增大[7-9]。这些均可能造成术中缺血线或者解剖学上的Cantile线均可能与肝内肝中静脉实际走行不符合,有时可能偏差较大,容易造成误伤。LUS术中实时“导航”降低了肝中静脉的损伤率和术中出血量[10],因为LUS在术中可以提供术者更全面、更详细的手术信息,可以清楚确定肿瘤边界及切缘,给术者提供指导,避免盲目操作而导致不必要的损伤。但LUS技术并不能显著提高术者的手术操作水平,且目前腹腔镜左半肝切除技术已经趋于成熟,手术路径基本固定,所以两组患者在术后并发症、平均住院时间方面比较差异无统计学意义。
在腹腔镜左半肝切除术中使用LUS并不明显延长手术时间,虽然不能明显降低术后并发症及缩短住院时间,但LUS可以有效减少术中出血、减少肝中静脉损伤,为“精准”肝切除创造条件。总之,LUS提高了腹腔镜手术的安全性,增加了操作的精准性,是腹腔镜左半肝切除术中的一项重要辅助工具,值得在临床中推广应用。
参考文献:
[1]PARK J, KIM S, SONG I, et al.Experience of laparoscopic liver resection for various liver diseases[J].Korean J hepatobiliary pancreat Surg, 2014,18(4):112-117.
[2]HEUER M, ALESINA P F, HINRICHS J, et al.Laparoscopic liver resection:A retrospective analysis of 94 clinical cases[J].Chirurg, 2015, 86(7):676-681.
[3]陈训如.腹腔镜超声—安全实施腹腔镜手术的重要辅助工具[J].中国微创外科杂志, 2007, 7(2):89 -90.
[4]中华医学会外科学分会肝脏学组, 腹腔镜肝切除术专家共识(2013版)[J].中国肿瘤临床, 2013, 40(6):303 -306.
[5]汪磊, 李宏.腹腔镜超声在腹腔镜解剖性肝切除术中的应用[J].中国微创外科杂志, 2014, 14(5):385 -388
[6]赵大建, 吴伟顶, 张成武, 等.超声刀联合高频电凝断肝法在腹腔镜肝部分切除术中的应用[J].肝胆胰外科杂志, 2011, 23 (1):18-20.
[7]耿小平, 刘付宝.遵循肝中静脉解剖学特点的精准半肝切除术[J].中国实用外科杂志, 2010, 30(8):717 -718.
[8]张慧, 周庭永, 钱学华, 等.肝门静脉的应用解剖[J].中国临床解剖学杂志, 2010, 28(6):62 5-628.
[9]宋庆轮, 陈卫霞, 陈军法.多层螺旋CT增强扫描显示肝静脉正常解剖及变异[J].中国临床解剖学杂志, 2008, 26(1):56 -58.
[10]LANGØ T, VIJAYAN S, RETHY A, et al.Navigated laparoscopic ultrasound in abdominal soft tissue surgery:technological overview and perspectives[J].Int J comput assist radiol surg, 2012, 7(4):585-599.
(本文编辑:张和)
·病例报告·
[通讯作者简介]李宏,主任医师,硕士生导师,E-mail:lancet2010@aliyun.com。
作者简介][第一汪磊(1980-),男,安徽芜湖人,主治医师,硕士。
[收稿日期]2015-09-04
[中图分类号]R445.1; R657.3
[文献标识码]B
DOI:10.11952/j.issn.1007-1954.2016.01.018
