荧光免疫层析法降钙素原检测试剂盒临床性能评估
2016-03-30郭莉娜杨启文谢秀丽徐英春
郭莉娜,杨启文,伊 洁,谢秀丽,王 瑶,王 贺,徐英春
中国医学科学院 北京协和医学院 北京协和医院检验科,北京100730
荧光免疫层析法降钙素原检测试剂盒临床性能评估
郭莉娜,杨启文,伊 洁,谢秀丽,王 瑶,王 贺,徐英春
中国医学科学院 北京协和医学院 北京协和医院检验科,北京100730
目的 评估荧光免疫层析法试剂盒检测降钙素原的性能。方法 参照美国临床实验室标准化协会 (Clinical and Laboratory Standards Institute,CLSI)EP5-A和EP6-A文件方法,对荧光免疫层析法试剂盒 (TEBSUN)检测降钙素原的精密度、线性、方法学比对、相对灵敏度和特异性进行评估。结果 荧光免疫层析法试剂盒检测降钙素原精密度较好,低浓度和高浓度样本精密度的变异系数分别为8.3%和4.7%;线性验证试验结果显示,在试剂盒标示的检测范围内具有良好的线性梯度关系 (r=0.9989);方法学比对结果显示,荧光免疫层析法试剂盒与梅里埃VIDAS酶联免疫荧光法分析系统的降钙素原试剂盒检测结果一致性良好 (r=0.9770);在0.5和2.0 ng/ml两个浓度水平,荧光免疫层析法试剂盒相对于酶联免疫荧光法试剂盒的灵敏度和特异性均大于86%,与其测定结果的总体符合率为93.75%。结论 荧光免疫层析法试剂盒检测降钙素原的精密度、线性、方法学比对、相对灵敏度和相对特异性等性能评价较好,适用于临床标本检测。
降钙素原;荧光免疫层析法;酶联免疫荧光法;性能评估
Med J PUMCH,2016,7(3):208-211
降钙素原 (procalcitonin,PCT)是降钙素的前体,是由116个氨基酸组成、相对分子质量为127 000的糖蛋白。在正常生理情况下,由甲状腺C细胞分泌产生,健康人血液中PCT浓度非常低,小于0.05 ng/ml[1]。在脓毒血症、系统性感染及促炎症反应刺激下,机体多个组织、多种细胞均可产生PCT并释放进入血液循环系统,血清 PCT值将成百上千倍于正常水平[2]。PCT在感染发生后的最初3 h即可测得,6~12 h达到峰值,其半衰期长,血PCT水平与感染及损伤的严重程度呈正相关,已被推荐作为细菌感染脓毒症的诊断、疗效检测及预后评估的有效指标[3]。本研究以梅里埃VIDAS酶联免疫荧光法分析系统检测结果为参照,对荧光免疫层析法试剂盒检测PCT的性能进行评估,以期了解该试剂盒能否满足临床需求。
材料和方法
标本来源
收集2014年5月至8月北京协和医院门诊及住院患者中可疑细菌感染者无溶血、无脂血、无黄疸血清标本共112份,其中男性64例,女性48例,患者平均年龄57.3岁;经检测血清PCT浓度覆盖待评估试剂盒检测线性区间0.01~100 ng/ml;按照VIDAS酶联免疫荧光法分析系统的检测结果,112例血清PCT浓度分布为:PCT≤0.25 ng/ml共21例,>0.25~0.5 ng/ml共16例,>0.5~2 ng/ml共30例,>2~10 ng/ml共30例,>10 ng/ml共 15例;其中重症监护室标本占67.9%(76/112)。样本来自临床常规检测剩余血清。
仪器与试剂
梅里埃VIDAS酶联免疫荧光法分析系统及PCT检测试剂盒(批号1002934040),为梅里埃诊断产品 (上海)有限公司产品;天宝颂原生物荧光免疫分析仪(TEBSUN)及PCT检测试剂盒 (批号01220140426),为北京瑞禾宏业生物技术有限公司产品。
研究方法
检测原理:酶联免疫荧光法分析系统的检测原理是结合一步免疫测定夹心法和最终荧光检测法来检测,固相管作为固相及移液装置,检测所需试剂预先配制好,分装在密封的试剂条中待用。待检样本先与包被在固相上的抗PCT抗体结合,再与孔中碱性磷酸酶标记的抗PCT单克隆抗体结合;以405 nm波长检测底物水解后产生的荧光强度以反映PCT的浓度。检测线性范围为0.05~200 ng/ml。生物荧光免疫分析仪是利用荧光免疫层析技术,采用双抗体夹心法原理进行检测。层析过程中,样本中PCT与荧光标记的PCT单克隆抗体反应形成复合物,在层析作用下沿着硝酸纤维素膜向前移动至检测区域,被硝酸纤维素膜上包被的PCT单克隆抗体捕获并形成复合物沉淀在T区。在激发光源的作用下,荧光物质发射特定波长的荧光信号,荧光免疫分析仪俘获荧光信号,通过信号转化及设定的定标曲线自动转化为定量数据,计算出样本中PCT的浓度。检测线性范围为0.01~100 ng/ml。
精密度评价:参照美国临床实验室标准化协会(Clinicaland Laboratory Standards Institute,CLSI) EP5-A程序[4],以VIDAS试剂盒检测结果为准,选取高值和低值血清作为测试样本,同一批测定中,用TEBSUN试剂盒分别重复测定高值和低值血清20次,评估试剂质控品也要测试一次。试验完成后收集数据应先检查有无离群点,离群点的判定标准:计算20次数据的均值和标准差,任何结果和均值的差值超过3倍标准差可认为是离群点。追查离群点发生的原因,原因不明时,不能去除离群点。
方法学比对:112例血清标本在同一时间分别应用VIDAS试剂盒和TEBSUN试剂盒测定PCT值,按照配对样本设计,使用SPSS 19.0统计分析软件行配对t检验,以判断两种试剂盒检测结果的差异。
线性范围验证:参照CLSI EP6-A程序[5],收集高值标本 (H)和低值标本 (L)。H为试剂盒说明书线性范围上限血清标本,无溶血、脂血及黄疸干扰; L为试剂盒说明书线性范围下限的血清标本,无溶血、脂血及黄疸干扰。将H和L按0∶10、1∶9、2∶8……9∶1、10∶0的比例各自配置混合,形成11个水平浓度的系列测试标本。每个浓度样本测试4次,所有样本应尽量在一次试验中测试完成。记录测定结果并计算均值。以测得的均值为实测值,与所计算的理论值进行比较。用直线回归分析对数据作处理,计算回归方程Y=bX+a,b值 (斜率)应在0.95~1.05之间。
相对灵敏度和特异性:以VIDAS试剂盒为参比试剂盒,分别以0.5和2.0 ng/ml为临界值,计算TEBSUN试剂盒的各项特异性指标。包括相对灵敏度、相对特异性、相对总体符合率。
质量控制:质控品 (批号:01220160316DC)随每批次检测样本平行操作,当质控品结果超出规定范围,不论试验结果是否满意都应将数据弃之不用,重新进行检测。低浓度C1参考范围:1.09~2.58 ng/ml;高浓度C2参考范围:14.60~27.12 ng/ml。
结果
精密度
荧光免疫层析法检测试剂盒批内精密度验证试验结果显示,高值和低值标本测定的变异系数分别为8.3%和4.7% (表1),符合试剂盒性能要求,具有较好的精密性。
线性
荧光免疫层析法检测试剂盒线性验证试验结果见表2。线性回归方程为 Y=0.9989 X-0.207(r= 0.9989),在试剂盒标示的检测范围内具有良好的线性梯度关系 (图1)。

表1 荧光免疫层析法检测试剂盒精密度试验结果 (ng/ml)
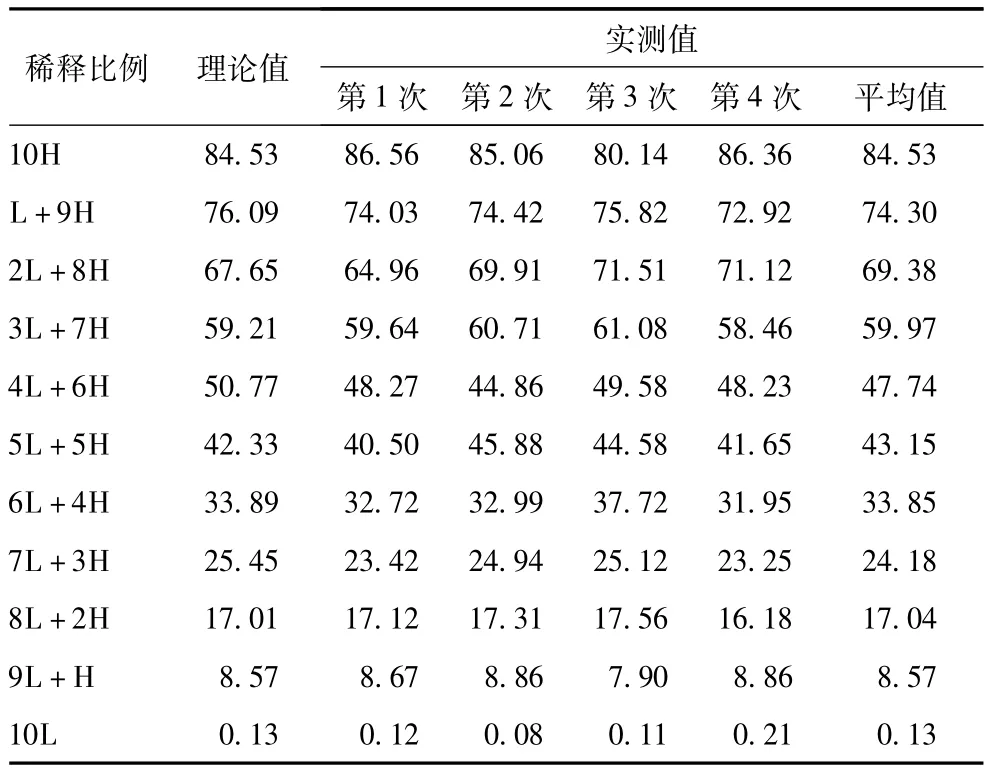
表2 荧光免疫层析法检测试剂盒线性验证结果 (ng/ml)
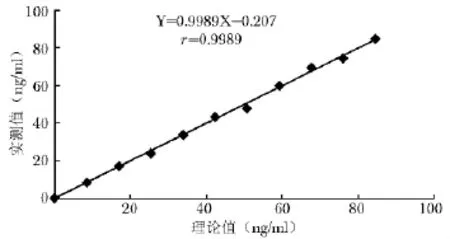
图1 荧光免疫层析法检测试剂盒线性验证分析结果
方法学比对
方法学比对试验共检测血清标本112例,其中VIDAS试剂盒检测结果中有5例<0.05 ng/ml,为便于分析记为0.05 ng/ml;另有1例样本检测结果高于TEBSUN试剂盒检测上限,予以去除。因此,将其中用2种试剂盒检测均获有效数据的111对数据行配对t检验,结果显示两种试剂盒测定结果差异无统计学意义 (t=-0.550,P=0.583)。成对样本相关系数 r=0.9770 (P=0.000),两种试剂盒检测结果呈显著相关。
相对灵敏度和相对特异性
112例样本的测定值以0.5 ng/ml为临界值进行定性统计分析,结果显示TEBSUN试剂盒相对于VIDAS试剂盒的检测灵敏度为 97.30%,相对特异性为86.49%,与VIDAS试剂盒测定结果的相对总体符合率为93.75%(表3);以2.0 ng/ml为临界值进行定性统计分析,结果显示TEBSUN试剂盒测定的相对灵敏度为86.67%,相对特异性为98.50%,与VIDAS试剂盒测定结果的相对总体符合率为93.75%(表4)。

表3 以0.5 ng/ml为临界值对试剂盒检测结果的定性分析结果
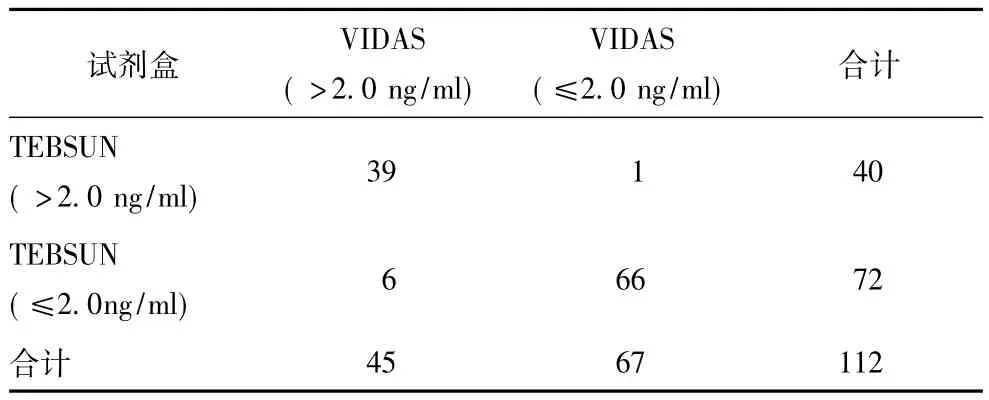
表4 以2.0 ng/ml为临界值对试剂盒检测结果的定性分析结果
讨论
随着社会进步,新型诊疗手段、治疗方法及疫苗不断出现,但感染性疾病仍然是威胁人类健康的重要因素[6]。由于感染性疾病临床缺乏特异性,血常规、胸部影像学或微生物学检查均无法快速鉴别致病菌。因此,如何早期诊断感染、评估感染程度并有效指导抗菌药物的使用成为临床诊疗所面临的重要挑战,特别对于危、急重症感染,早期诊断并给予及时治疗是提高生存率的关键。
PCT作为一个敏感性较高的生物学指标,已成为与细菌性感染炎性反应相关的特异性指标,特别对于快速鉴别细菌性感染所致的全身炎症反应综合征 (systemic inflammatory response syndrome,SIRS)及脓毒症,尤其是重症脓毒症和感染性休克具有重要意义。
本研究表明荧光免疫层析法检测试剂盒在线性范围内具有良好的精密度,在试剂盒标示的检测范围内具有良好的线性梯度关系;可满足临床检测需要;方法学比对试验显示TEBSUN试剂盒与VIDAS试剂盒具有良好的相关性,两种试剂盒测定值间线性偏倚无统计学意义;选择0.5和2.0 ng/ml这两个医学决定水平是因为血PCT含量低于0.5 ng/ml通常认为可排除脓毒血症,介于0.5~2.0 ng/ml之间为可能脓毒血症,高于2.0 ng/ml则为脓毒血症或由细菌感染所致的SIRS[7]。在0.5和2.0 ng/ml这两个水平,荧光免疫层析法检测试剂盒的相对灵敏度和相对特异性均大于86%,与VIDAS试剂盒测定结果的相对总体符合率为93.75%。
研究中选择法国梅里埃VIDAS酶联免疫荧光法分析系统的PCT检测试剂盒为参比试剂,该试剂是目前本院及国内多家医院检验科常规采用的PCT检测试剂盒,检测性能良好。以该试剂盒为“金标准”,对国产荧光免疫层析法分析试剂盒性能评估发现:该产品检测PCT灵敏度和特异性较高,不需要昂贵的大型设备,利于床旁检测,既节约了医疗成本,同时也实现了更快速 (检测时间8 min)报告,为临床感染诊疗提供较为快速准确的检验结果。
本研究在选取标本时排除了溶血、脂血、黄疸血清,故用荧光免疫层析法检测试剂盒检测PCT时,对于上述干扰因素的屏蔽能力还有待进一步研究探讨。
综上,荧光免疫层析法试剂盒检测PCT无需昂贵的设备,操作简单,耗时短,与酶联免疫荧光法试剂盒测定结果总体符合率较高,分析性能基本可满足临床检测要求。
[1]Lee H.Procalcitonin as a biomarker of infectious diseases[J].Korean J Intern Med,2013,28:285-291.
[2]Becker KL,Snider R,Nylon ES.Procalcitonin in sepsis and systemic inflammation:a harmful biomarker and a therapeutic target[J].Br J Pharmacol,2010,159:253-264.
[3]降钙素原急诊临床应用专家共识组.降钙素原 (PCT)急诊临床应用的专家共识[J].中华急诊医学杂志,2012,21:944-951.
[4]CLSI.EP5-A.Evaluation of precision performance of clinical chemistry devices[S].Wayne,PA:CLSI,1999.
[5]CLSI.EP6-A.Evaluation of the linearity of quantitative measurement procedures:a statistical approach[S].Wayne,PA: CLSI,2003.
[6]Morens DM,Fauci AS.Emerging Infectious Diseases:Threats to Human Health and Global Stability[J].PLoS Pathog,2013,9:e1003467.
[7]Schneider HG,Lam QT.Procalcitonin for the clinical laboratory:a review[J].Pathology,2007,39:383-390.
Performance Evaluation of Fluorescence Immunochromatography Kit in Detection of Procalcitonin
GUO Li-na,YANG Qi-wen,YI Jie,XIE Xiu-li,WANG Yao,WANG He,XU Ying-chun
Department of Clinical Laboratory,Peking Union Medical College Hospital,Chinese Academy of Medical Sciences&Peking Union Medical College,Beijing 100730,China
XU Ying-chun Tel:010-69159766,E-mail:xycpumch@139.com
Objective To evaluate the performance of fluorescence immunochromatography kit in detecting procalcitonin.Methods According to the Clinical and Laboratory Standards Institute(CLSI)EP5-A and EP6-A,the performance of fluorescence immunochromatography kit(TEBSUN)in detecting procalcitonin was evaluated in the aspects of precision,linearity,methodology comparison,relative sensitivity,and relative specificity.Results The fluorescence immunochromatography kit showed high precision,the coefficients of variation (CV)of low and high concentration samples were 8.3%and 4.7%,respectively.Result of liner verification test showed good linear correlation within the indicated test range(r=0.9989).In methodology comparison tests,the fluorescence immunochromatography kit had good consistency with VIDAS enzyme-linked immunofluorescence kit(r=0.9770).The relative sensitivity and specificity of the fluorescence immunochromatography kit compared with the enzyme-linked immunofluorescence kit were both higher than 86%at 0.5 ng/ml and 2.0 ng/ml level.The total consistency of the two diagnostic kits was 93.75%.Conclusion The fluorescence immunochromatography kit has good performance in precision,linearity,methodology comparison,relative sensitivity,and relative specificity,suggesting that it meets the requirements of clinical tests.
procalcitonin;fluorescence immunochromatography;enzyme-linked immunofluorescence;performance evaluation
徐英春 电话:010-69159766,E-mail:xycpumch@139.com
R446.11
A
1674-9081(2016)03-0208-04
10.3969/j.issn.1674-9081.2016.03.010
2015-02-02)
