高压镍锰酸锂电池电解液体系探索研究①
2016-03-28秦银平刘杨王德宇
秦银平,刘杨,王德宇
(1.中国科学院宁波材料技术与工程研究所,浙江 宁波 315201;2.上海大学材料基因组工程研究院,上海 200444)
自1990年诞生以来,锂离子电池得到了快速的发展,目前已经占据了手机、笔记本电脑、数码产品等便携式设备市场,并开始应用于电动汽车和和储能电站等领域。在这些大型电池领域的商业应用,尤其是电池汽车领域,将会为目前的锂离子电池市场带来5~10倍的增长,为锂电池行业的发展注入新的动力。
目前,商品化动力电池材料的负极材料以石墨为主,正极材料主要是LiFePO4、LiMn2O4和LiNi1/3Co1/3Mn1/3O2等。近年来,为了进一步提高电动汽车的续航里程,降低电池每瓦时的成本,人们对于高电压、高容量正极材料的关注和研究也越来越多[1-5]。在已报道的诸多材料中,LiNi0.5Mn1.5O4是一类颇具应用前景的正极材料,它的充放电平台在~ 4.75 V vs Li/Li+,可逆容量在130mAhg-1左右,且材料兼具原料成本低、制备容易、倍率容量高、循环性能好等综合优点,成为取代传统正极材料的最佳选择之一[6-8]。
从有关LNMO正极材料的合成和电化学性能测试的文献报道中看到,已经找到了多种合成长循环、高倍率的LNMO材料的方法[9-11]。但是将这些LNMO正极材料替换已有正极材料应用到全电池中却遇到了极大的困难,LNMO/Graphite全电池循环容量衰减较快[12-14]。Kim等[13]针对LNMO/Graphite全电池的容量衰减原因设计了一系列分析实验进行探讨,推测出循环过程中Mn的溶解以及在石墨表面的还原是造成容量衰减的重要因素。Yang等[14]采用XPS和FTIR光谱技术分析了LNMO电极在4.0-5.3V的不同电位下表面成分的变化,推测电解液中有机碳酸酯在高压下的分解是LNMO电池容量衰减的原因。研究者们对于LNMO/Graphite全电池容量衰减较快的原因的探索,主要集中在正极材料和有机溶剂上,却忽略了电池中电解液添加剂的影响。
锂离子电池中电解液添加剂的量很少(一般体积比或质量比不超过电解液含量的5%),但在整个电池体系中起着非常关键的作用。针对于Graphite(plateau ~ 0.1V vs Li/Li+)负极,需要在电解液中加入SEI成膜添加剂来形成保护层,阻止溶剂化锂离子(Li+(solvent)χ)向石墨层间的嵌入(其嵌入电位与有机碳酸酯溶剂的还原电位(LUMO)相近,约为1.0V vs Li/Li+)[15,16]。常用的 SEI成膜添加剂有碳酸亚乙烯酯(VC)[17-19]、亚硫酸乙烯酯(ES)[20-22]、碳酸丙烯乙酯[23]、亚硫酸丁烯酯[24]等,本文主要以VC和ES添加剂对高压LNMO正极材料的电化学性能的影响为例,介绍了LNMO/Graphite全电池容量衰减较快的又一重要因素。
1 实验部分
1.1 实验材料和测试设备
实验所用正极活性材料为四川兴能新材料有限公司提供的LiNi0.5Mn1.5O4粉末,粘结剂为聚偏氟乙烯(PVDF),电池隔膜用Celgard 2300 PP/PE/PP三层复合材料。实验中的电解液均是按照溶剂质量比进行配制,电解液中有机溶剂碳酸乙烯酯(EC)、碳酸二甲酯(DMC)、碳酸二乙酯(DEC)、碳酸甲乙酯(EMC)、碳酸丙烯酯(PC)、添加剂VC、ES由山东海容电源材料有限公司提供;电解液中锂盐为日本森田化学生产的LiPF6。
文中所用X-ray衍射仪为德国BRUKER公司生产的BrukerD8 advance-X,使用Cu靶,Kα射线,入射管电压为40KV,管电流为40mA,2θ扫描范围10°~80°,扫描步长0.02°;所用扫描电子显微镜为日本日立公司生产的FESEM S-4800型场发射SEM。电化学测试设备主要有雷磁DDS-307A型电导率仪、CT2001A型LAND电池测试系统、上海辰华chi1000b和chi660D电化学工作站。
1.2 电池制备和电化学性能测试
LNMO极片的制备:将活性材料LNMO粉末、导电剂Super-P、粘结剂PVDF按照质量比8∶1∶1混合,加入适量的N-甲基吡咯烷酮(NMP)调节浆料粘稠度,并在磁力搅拌器上搅拌2小时,以确保浆料均匀分散。将搅拌好的浆料倒在Al箔集流体上均匀涂布,然后在鼓风干燥箱中干燥,再放置于真空干燥箱中恒温120℃烘12小时。烘干处理后的极片进行冲片再压片,就得到了合适扣式电池大小的正极片,放置于手套箱中备用。Super-P(SP)极片的制备过程与LNMO极片一样,浆料成分按照质量比为Super-P:PVDF=8∶2。
电解液的制备:用移液枪按已计算好的比例称量不同的溶剂放入瓶中,充分混匀后加入LiPF6进行搅拌溶解后即得到所需要的不同种类电解液,文中主要电解液有:①1M LiPF6-EC∶DMC (1∶1), ②1M LiPF6-PC:DMC (1∶1), ③1M LiPF6-EC∶PC∶DMC(2∶3∶5), ④1M LiPF6-EC∶DEC∶EMC(1∶1∶1)。另外,在1M LiPF6-EC∶DEC∶EMC(1∶1∶1)电解液中分别加入1%ES、2%VC添加剂,均匀混合后备用。为了考察ES、VC的氧化电位,文中配制了1M LiPF6-ES、1M LiPF6-VC。这些电解液制备好后用电导率仪测试电导率,并记录数据。
扣式半电池的组装和测试:用制备好的LNMO极片做工作电极,Li片为对电极和参考电极,以Celgard 2300复合膜为隔膜,滴入一定量的电解液,装备CR2032扣式电池。将扣式电池静止4小时,确保电解液与隔膜、极片完全浸润后,装在电化学测试设备上。电化学工作站上线性扫描伏安法的扫描速率为0.1mV/s,范围2.5-7V。电化学阻抗谱中频率测试范围为102~105,施加的交流信号振幅为5mV。充放电循环测试以1C倍率,在3.5-4.9V电压范围内进行;循环之前先化成三周,化成时倍率为0.2C,电压范围为3.5-4.9V。
2 结果与讨论
2.1 不含添加剂的电解液在高压下的电化学性能
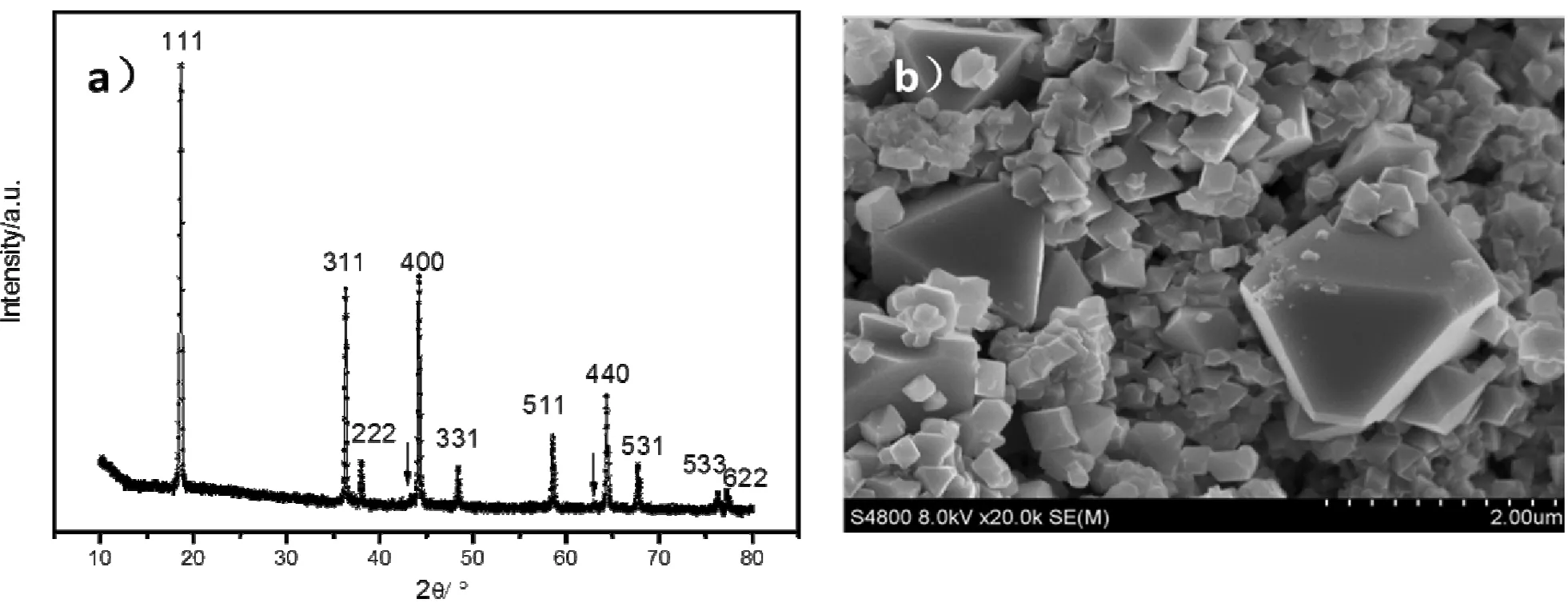
图1 a) LNMO粉末的XRD图谱;b) LNMO粉末的SEM照片Fig.1 a) XRD pattern of LNMO powders;b) SEM images of LNMO powders
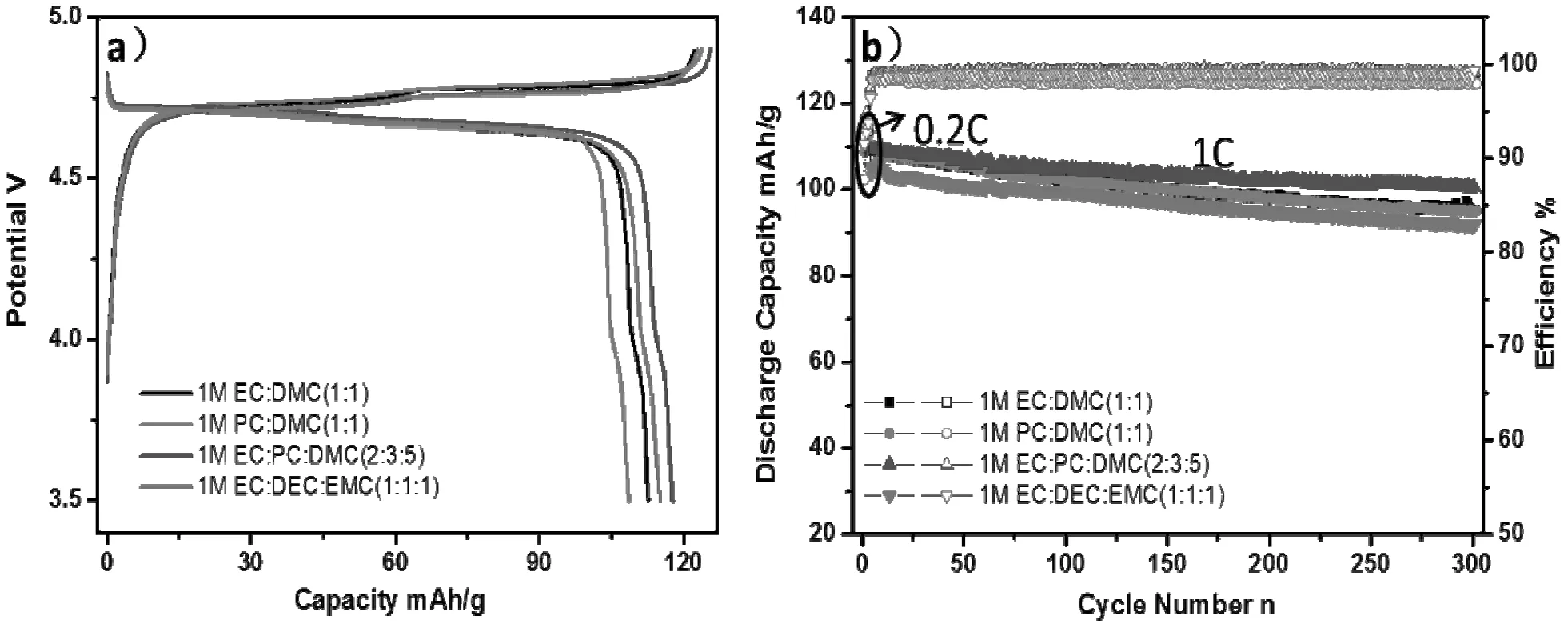
图2 LNMO/Li电池在不同碳酸酯溶剂电解液中a) 以0.2C倍率进行首次充放电时的容量-电压曲线; b) 以1C倍率进行循环时的放电容量曲线Fig .2 a) The first cycle potential-capacity curves ofLNMO/Li cells;b) Cyclic performance of LNMO/Li cells
图1 a)为LNMO粉末的XRD图谱,根据标准图谱标出了所有特征峰。b)为LNMO粉末的SEM照片,结合图1 a)说明所采用的LNMO材料为纯相的尖晶石结构。图2为含有不同溶剂的电解液在LNMO/Li扣式半电池上,3.5-4.9V电压范围内,以1C倍率进行的充放电循环图。图2中,循环开始的前3周为0.2C倍率下进行的化成过程,实心图标所示曲线为放电容量对应的曲线,空心图标所示曲线为放电效率对应的曲线。图2a)中实验数据显示,LNMO/Li半电池在这些电解液中化成时首次放电容量在109-117mAh/g之间,其中,首次放电效率最高的为1M LiPF6-EC:PC:DMC(2∶3∶5)电解液,93.7%;首次放电效率最低的为1M LiPF6- PC:DMC (1∶1),87.7%。当以1C倍率循环时,这四种不同溶剂的电解液①②③④循环300周后的容量剩余率分别为87.6%、92.0%、91.9%、87.3%。
我们的实验结果表明,虽然镍锰酸锂的平台电位在4.75V vs. Li+/Li,但对电解液并没有提出特别的需求,常规碳酸酯溶剂可以基本满足电池循环性的要求。
2.2 含有负极成膜添加剂的电解液在高压下的电化学性能
为了研究VC、ES两种负极成膜添加剂在高压下的电化学行为,实验中使用VC、ES分别做溶剂溶解1mol/L的LiPF6获得了1M LiPF6-VC、1M LiPF6-ES电解液,用电导率仪测试电导率分别为11.0ms/cm、9.58ms/cm。运用Super-P∶PVDF=8∶2的极片作为工作电极,Li片为对电极和参比电极,分别加入这两种电解液组装电池在电化学工作站上进行2.5-7.0V的线性扫描,如图3示。图中VC在4.6V出现第一个电流峰,5.5V出现第二个电流峰,说明VC在4.6V时发生了氧化反应并且可能在SP电极上成膜,从而一定程度上抑制了其在电极上的持续氧化反应。图中ES从3.45V开始有氧化电流出现,在4.05V出现较大的氧化电流峰,并且持续不断的氧化,说明ES在SP电极上没有形成致密的膜,拆电池后有刺激性气体溢出,可能是ES氧化形成SO2气体。
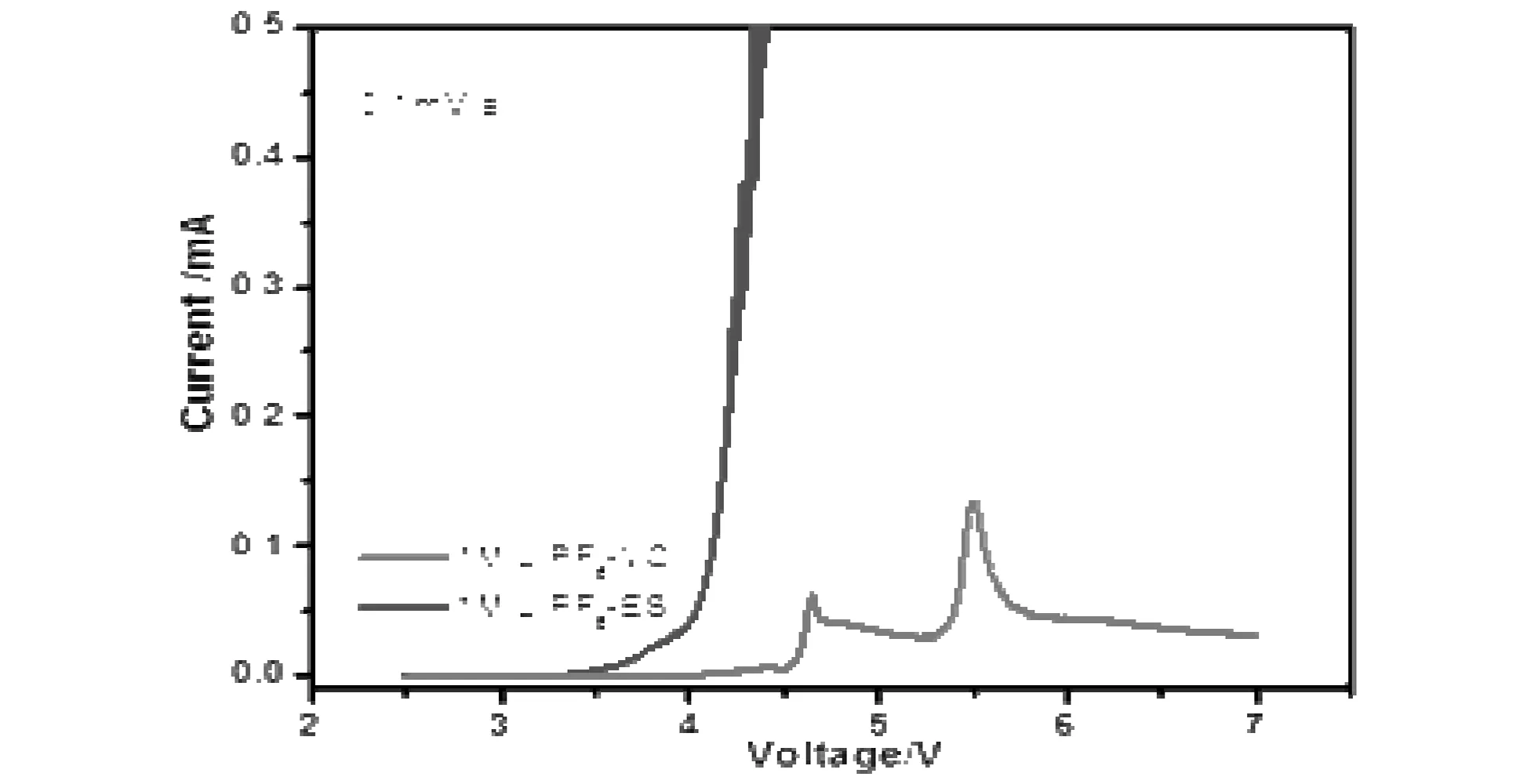
图3 SP/Li电池分别在1M LiPF6-VC和1M LiPF6-ES电解液中,以0.1mV/s的速度进行2.5-7.0V范围下的线性扫描曲线Fig.3 Linear sweep voltammetry of SP/Li cells
图4示1M LiPF6-EC∶DEC∶EMC(1∶1∶1)为基础电解液,在里面分别添加2%VC、1%ES的负极成膜添加剂后获得的三种电解液。这三种电解液在LNMO/Li扣式半电池中以0.2C倍率化成3周后,以1C倍率进行3.5-4.9V电压范围下的循环性能测试。从图4a)中可以看出加入添加剂后电池的放电容量均较低,含有2%VC的电解液首次充电容量为119.6mAh/g,首次放电容量仅有72.1mAh/g;含有1%ES的电解液首次充电容量为368.3mAh/g,放电容量仅有10.3mAh/g,并且充电时电压一直在波动,充电到4.0V左右出现一个非常大的平台。从图4b)中可以看出含有成膜添加剂的电解液在高压LNMO电池中循环容量非常低,分别约是45mAh/g和15mAh/g,并且放电效率也低于纯碳酸酯溶剂。
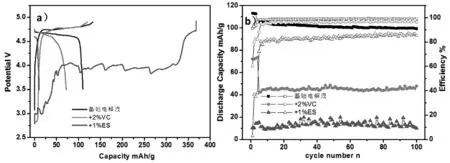
图4 LNMO/Li电池在1M LiPF6-EC:DEC∶EMC(1∶1∶1)基础电解液和在分别含有2%VC、1%ES添加剂的电解液中进行的电化学测试: a) 以0.2C倍率进行首次充放电时的容量-电压曲线; b) 以1C倍率进行循环时的放电容量曲线Fig.4 a) The first cycle potential-capacity curves ofLNMO/Li cells;b) Cyclic performance of LNMO/Li cells
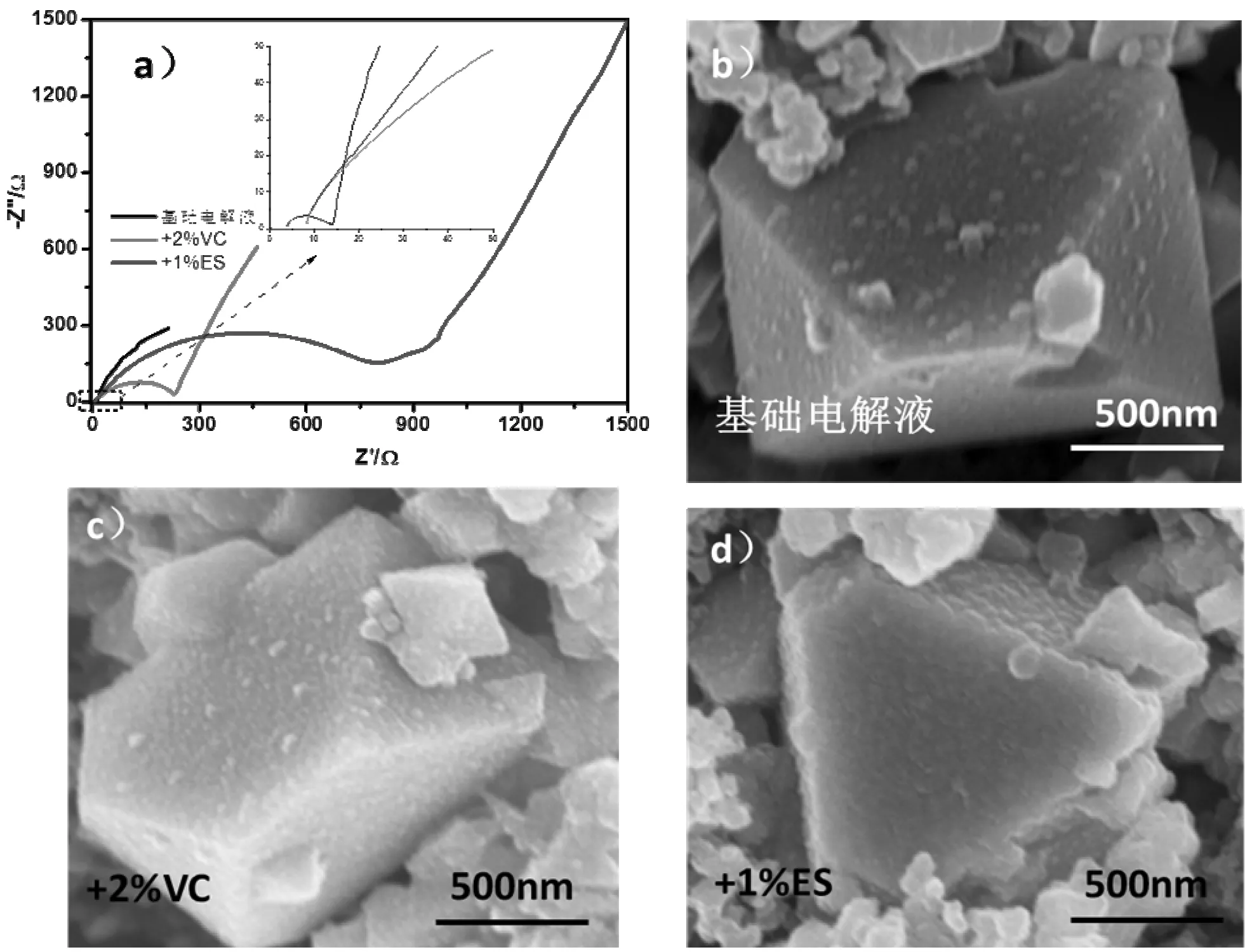
图5 LNMO/Li电池在不同种电解液中循环100周后,a)放电态电化学阻抗图; b)、c)、d)为LNMO电极表面的SEM照片Fig.5 LNMO/Li cells in different electrolyte after 100 cycles,a) Electrochemical impedance spectra;b), c), d) SEM images of LNMO electrode
对电解液中加入少量的VC、ES作添加剂后使得LNMO/Li电池的循环容量非常低的原因进行探索,实验中将循环100周后的放电态电池拆下,静止24h后测试阻抗,如图5 a)所示。测试完阻抗的电池拆解下来,取出正极片用DMC溶剂清洗后在烘箱中进行干燥,对电极表面形貌进行SEM观察,如下图5 b)、c)、d)所示。从SEM照片和电化学阻抗谱结合来看,含有VC和ES添加剂的电解液在LNMO电池上循环时,正极表面会生长出一层阻抗较大的覆盖物,阻止充放电过程中锂离子的脱嵌行为。
我们的实验结果表明,石墨一侧的添加剂可能会优先、或部分在正极表面发生氧化分解,界面阻抗显著增加,造成放电容量过低。如果负极一侧使用钛酸锂,不需要使用成膜添加剂,电池表现出优异的循环性能。Wu等[25]研究了LNMO/LTO体系,使用1.2M LiPF6-EC: EMC(3∶7)电解液,室温下循环1000周仍有98%的剩余容量,从侧面表明了镍锰酸锂的循环稳定性和常规石墨添加剂的非兼容性。
3 结论
虽然高压镍锰酸锂的放电平台在4.75 V vs Li+/Li,但该材料本身表现出稳定的循环性能。当使用不含添加剂的电解液时,在1C倍率循环300周后容量保持率为90%。但是,当电解液内含有VC、ES等电解液添加剂时,电池的可逆容量大幅度降低,其主要是添加剂在电极表面分解、沉积、形成高阻抗覆盖层造成的。这些负极成膜添加剂在正极材料一侧的电化学稳定性是造成其可逆容量极低的主要原因,其它电解液添加剂也存在稳定性方面的隐患,因此,开发镍锰酸锂-石墨全电池体系可能需要重新设计电解液体系。
[1] Wolfenstine J, Allen J. Ni3+/Ni2+redox potential in LiNiPO4[J]. Journal of Power Sources, 2005, 142(1-2):389-390.
[2] Devaraju M K, Truong Q D, Hyodo H, et al. Synthesis, characterization and observation of antisite defects in LiNiPO4nanomaterials[J]. Scientific Reports, 2015, 5:11041.
[3] Okada S, Sawa S, Egashira M, et al. Cathode properties of phospho-olivine LiMPO4for lithium secondary batteries[J]. Journal of Power Sources, 2001, 97-98:430-432.
[4] Amine K, Yasuda K, Yamachi M. Olivine LiCoPO4as 4.8V electrode material for lithium batteries[J]. Electrochemical and Solid-State Letters, 2000, 3(4):178-179.
[5] Wang Y L, Zhao H X, Ji Y F, et al. Long-life and high-rate LiVPO4F/C nanocrystals modified with graphene as cathode material for lithium-ion batteries[J]. Solid State Ionics, 2014, 268(Part A):169-173.
[6] Liu G Q, Wen L, Liu Y M. Spinel LiNi0.5Mn1.5O4and its derivatives as cathodes for high-voltage Li-ion batteries[J]. Journal of Solid State Electrochemistry, 2010, 14(12):2191-2202.
[7] Feng J J, Huang Z P, Guo C, et al. An organic coprecipitation route to synthesize high voltage LiNi0.5Mn1.5O4[J]. ACS Applied Materials & Interfaces, 2013, 5(20):10227-10232.
[8] Zhang X L, Cheng F Y, Zhang K, et al. Facile polymer-assisted synthesis of LiNi0.5Mn1.5O4with a hierarchical micro-nano structure and high rate capability[J]. RSC Advances, 2012, 2(13):5669-5675.
[9] Zhao Q L, Ye N Q, Li L, etal. Oxalate coprecipitation process synthesis of 5V cathode material LiNi0.5Mn1.5O4and its performance[J]. Rare Metal Materials and Engineering, 2010, 39(10):1715-1718.
[10] Kim J H, Hong Y J, Park B K, et al. Nano-sized LiNi0.5Mn1.5O4cathode powders with good electrochemical properties prepared by high temperature flame spray pyrolysis[J]. Journal of Industrial and Engineering Chemistry, 2013, 19(4):1204-1208.
[11] Mo M Y, Ye C C, Lai K, et al. Gelatin-assisted synthesis of LiNi0.5Mn1.5O4cathode material for 5V lithium rechargeable batteries[J]. Applied Surface Science, 2013, 276:635- 640.
[12] Pieczonka N P W,Liu Z Y,Lu P,et al. Understanding transition-Metal dissolution behavior in LiNi0.5Mn1.5O4high-voltage spinel for lithium ion batteries[J]. The Journal of Physical Chemistry C,2013,117(31):15947-15957.
[13] Kim J H, Pieczonka N P W, Li Z C, et al. Understanding the capacity fading mechanism in LiNi0.5Mn1.5O4/graphite Li-ion batteries[J]. Electrochimica Acta, 2013, 90(5):556-562.
[14] Li Y, Ravdel B, Lucht B L. Electrolyte reactions with the surface of high voltage LiNi0.5Mn1.5O4cathodes for lithium-ion batteries[J]. Electrochemical and Solid-State Letters,2010, 13(8):A95-A97.
[15] Goodenough J B, Kim Y S. Challenges for rechargeable Li batteries[J]. Chemistry of Materials, 2010, 22(3):587-603.
[16] Xu K. Nonaqueous Liquid electrolytes for lithium-based rechargeable batteries[J]. Chemical Reviews, 2004, 104(50):4303-4417.
[17] Ota H, Sakata Y, Inoue A, et al. Analysis of vinylene carbonate derived SEI layers on graphite anode[J]. Journal of The Electrochemical Society, 2004, 151(10): A1659-A1669.
[18] Ota H, Sakata Y, Otake Y, et al. Structural and functional analysis of surface film on Li anode in vinylene carbonate-containing electrolyte[J]. Journal of The Electrochemical Society, 2004, 151(11):A1778-A1788.
[19] Aurbach D, Gamolsky K, Markovsky B, et al. On the use of vinylene carbonate (VC) as an additive to electrolyte solutions for Li-ion batteries[J]. Electrochimica Acta, 2002, 47(9):1423-1439.
[20] Wrodnigg G H, Besenhard J O, Winter M. Ethylene sulfite as electrolyte additive for lithium-ion cells with graphitic anodes[J]. Journal of The Electrochemical Society, 1999, 146 (2):470-472.
[21] Wrodnigg G H, Besenhard J O, Winter M. Cyclic and acyclic sulfites: new solvents and electrolyte additives for lithium ion batteries with graphitic anodes[J]. Journal of power sources, 2001, 97-98(3):592-594.
[22] Ota H, Sato T, Suzuki H, et al. TPD-GC/MS analysis of the solid electrolyte interface (SEI) on a graphite anode in the propylene carbonate/ethylene sulfite electrolyte system for lithium batteries[J]. Journal of Power Sources, 2001, 97-98(01):107-113.
[23] Lee J T, Lin Y W, Jan Y S. Allyl ethyl carbonate as an additive for lithium-ion battery electrolytes[J]. Journal of Power Sources, 2004, 132(1):244-248.
[24] Chen R J, Wu F, Li L, et al. Butylene sulfite as a film-forming additive to propylene carbonate-based electrolytes for lithium ion batteries[J]. Journal of Power Sources, 2007, 172(1):395-403.
[25] Wu H M, Belharouak I, Deng H, et al. Development of LiNi0.5Mn1.5O4/Li4Ti5O12system with long cycle life[J]. Journal of The Electrochemical Society, 2009, 156(12): A1047-A1050.
