影响特发性肺纤维化预后的相关因素分析
2016-03-26秦文婧单远莹孟德荣河南大学第一附属医院呼吸内科河南开封475001
秦文婧 梁 宇 单远莹 孟德荣河南大学第一附属医院呼吸内科,河南开封 475001
影响特发性肺纤维化预后的相关因素分析
秦文婧梁宇单远莹孟德荣
河南大学第一附属医院呼吸内科,河南开封475001
[摘要]目的探讨影响特发性肺纤维化(Idiopathic pulmonary fibrosis,IPF)患者预后的相关因素。方法选择IPF患者58例的临床资料进行回顾性分析。检测血气分析、胸部HRCT、肺功能、心脏超声、支气管肺泡灌洗结果等,分析各因素对患者预后的相关性。结果单因素分析结果显示,杵状指、BMI、圣乔治评分、6 min步行试验、FVC%、TLC%、DLCO%、PaO2、血沉、PaO2/FIO2、SaO2、PAP、BALF与患者的预后密切相关(P<0.05或P<0.01)。多因素分析结果显示:TLC%、血沉、杵状指、BMI、PAP是影响患者预后的主要相关因素(P<0.05或P<0.01)。TLC%、BMI指标HR值低于1,说明其与患者预后有正相关的关系,血沉、杵状指、PAP指标的HR值高于1,说明与患者预后有负相关的关系,是患者不良预后的危险因素。结论IPF患者营养状况、肺功能、炎性指标、杵状指、肺动脉压与患者预后具有密切的关系。
[关键词]特发性肺纤维化;预后;影响因素;杵状指
特发性肺纤维化(idiopathic pulmonary fibrosis,IPF)是特发性间质性肺炎的一种,属于弥漫性肺实质疾病,病因不明,主要特征是寻常性间质性肺炎,表现为弥漫性肺泡炎、肺纤维化、肺泡单位结构紊乱等[1]。IPF进展快,预后差,但也有部分患者可长期稳定生存。目前还没有有效逆转IPF的治疗方法,因此了解影响患者预后的相关因素,给予相应的治疗,对改善患者预后具有重要的临床意义。本研究选择IPF患者58例的临床资料进行回顾性分析,探讨影响患者预后的相关因素。现报道如下。
1 资料与方法
1.1一般资料
选择2013年1月~2014年12月在我院治疗的IPF患者58例的临床资料进行回归性分析。纳入标准:所有患者诊断明确,均符合2011年ATS/ERS/JRS/ ALAT制定的最新IPF循证医学诊治指南[2],临床资料完整。排除标准:临床资料不完整,合并其他肺部疾病或者严重心血管疾病患者,排除合并肿瘤患者以及其他系统严重疾病的患者。58例患者中男41例,女17例;年龄58~72岁,平均(63.9±8.6)岁;吸烟30例,杵状指34例,肺动脉高压27例;肺气肿15例;病程3.8~26.0个月;呼吸困难评分4~8分;FEV1%:52.3%~81.8%,FVC%:51.3%~82.5%,TLC%:47.2%~67.2%,RV%:40%~75%,DLCO%:36.7%~75.2%;PaO2:62~80 mmHg,PaCO2:32.5~38.8 mmHg,SaO2:91%~96%,BALF(N%):4%~18%。
1.2研究方法
通过病历资料及电话随访确定患者的生存情况,死亡患者记录死亡时间,确定死因,排除非IPF所致的死亡患者。记录患者BMI,评价患者营养状况。记录患者动脉血气结果,包括氧分压(PaO2)、二氧化碳分压(PaCO2)、血氧饱和度(SaO2),因检测的结果均是在吸氧状况下,因此计算氧合指数进行矫正,氧合指数= PaO2/FiO2。肺功能检测结果,包括一秒钟用力呼气量(FEV1)、肺总量(TLC)、用力肺活量(FVC)、一氧化碳弥散量(DLCO)。肺功能检测仪为捷斯特(chest)肺功能测试仪,型号HI-101。观察患者HRCT结果,记录是否合并肺气肿。采用西门子心脏超声仪检测患者心脏超声,记录三尖瓣返流速度、肺动脉压力(PAP)。所有患者均行支气管肺泡灌洗(BALF)检查,进行肺泡灌洗液细胞分类计数、T细胞亚群分析等,包括巨噬细胞百分比(M%)、中性粒细胞百分比(N%)、淋巴细胞百分比(L%)、嗜酸性粒细胞百分比(E%)、CD4+T淋巴细胞、CD8+T淋巴细胞、CD4+/CD8+。根据患者的结局,分析与预后相关的因素。
1.3统计学方法
采用SPSS15.0统计学软件进行分析。计数资料采用χ2检验,计量资料采用均数±标准差(±s)表示,采用t检验。死亡风险度(HR)采用单因素及多因素Cox比例风险回顾检测。P<0.05为差异有统计学意义。
2 结果
2.1随访结果
至2015年1月随访结束,58例患者死亡23例。平均生存时间(38.9±12.6)个月。
2.2单因素Cox比例回归分析结果
单因素分析结果显示,杵状指、BMI、圣乔治评分、6分钟步行试验、用力肺活量占预计值百分比(FVC%)、肺总量占预计值百分比(TLC%)、一氧化碳弥散量占预计值百分比(DLCO%)、PaO2、血沉、PaO2/FiO2、SaO2、PAP、BALF与患者的预后密切相关(P<0.05或P<0.01)。见表1。
2.3多因素Cox比例回归分析结果
对单因素分析结果有意义的项目纳入多因素Cox比例回归分析,见表2。多因素分析结果显示:TLC%、血沉、杵状指、BMI、PAP是影响患者预后的主要相关因素(P<0.05或P<0.01)。TLC%、BMI指标HR值低于1,说明其与患者预后有正相关的关系,血沉、杵状指、PAP指标的HR值高于1,说明与患者预后有负相关的关系,是患者不良预后的危险因素。

表1 单因素Cox比例回归分析结果
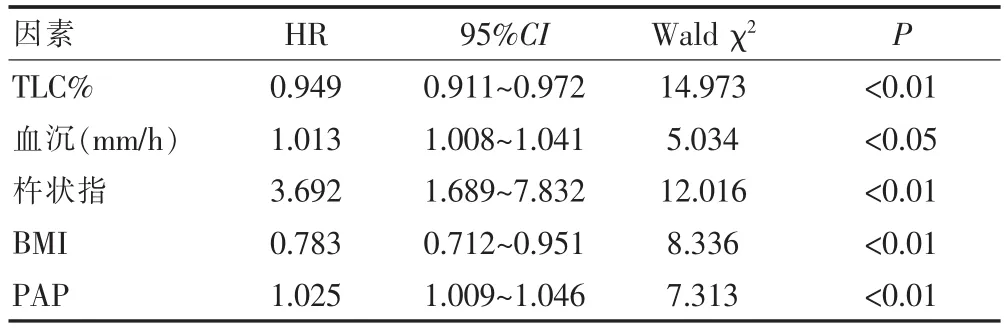
表2 多因素Cox比例回归分析结果
3 讨论
IPF是一种原因不明、以弥漫性肺泡炎和肺泡结构紊乱最终导致肺间质纤维化为特征的疾病[3]。按病程有急性、亚急性和慢性之分,本病多为散发,估计发病率(3~5)/10万,占所有间质性肺病的65%。此病见于各年龄组,而作出诊断常在50~70岁之间,男女比例1.5~2∶1,预后不良,早期病例即使对激素治疗有反应,生存期一般也仅有5年。作为一种慢性间质性肺炎,IPF起病隐匿、病情逐渐加重,也可表现为急性加重。有研究指出,IPF患者1年、3年急性加重发生率为14.2%和20.7%,65~70岁男性IPF患者更易出现急性加重。IPF急性加重临床表现包括呼吸困难、咳嗽迅速恶化、低热、气体交换指标明显下降,影像学提示新的渗出性改变[4,5]。几乎所有IPF急性加重患者的BALF检查均表现为中性粒细胞升高[6,7]。诊断基于IPF患者在30 d内出现不明原因病情加重,结合影像学表现并且除外肺部感染、心功能不全、肺栓塞或药物因素诱发的急性肺损伤等。IPF急性加重病理表现为寻常型间质性肺炎基础上出现弥漫性肺泡损伤,部分患者同时出现机化性肺炎改变,与急性呼吸窘迫综合征和急性间质性肺炎有相似之处,需仔细鉴别。如IPF急性加重患者循环纤维细胞数在急性加重期明显升高,而急性呼吸窘迫综合征与健康对照或稳定期IPF患者无明显差异。一些与肺泡Ⅱ型上皮细胞受损和(或)增殖、血管内皮细胞损伤及胶原沉着相关的生物标志物在IPF急性加重患者明显升高,提示与肺泡上皮损伤和异常修复有关[8,9]。2013年《美国呼吸与危重症医学杂志》发表IIP最新分类:主要的特发性间质性肺炎、少见的特发性间质性肺炎和未分类的特发性间质性肺炎。主要的特发性间质性肺炎分为三类:①慢性纤维化性间质性肺炎,包括IPF和特发性非特异性间质性肺炎;②吸烟相关性间质性肺炎,包括闭塞性细支气管炎并间质性肺炎和脱屑性间质性肺炎;③急性或亚急性间质性肺炎,包括隐源性机化性肺炎和急性间质性肺炎。少见的特发性间质性肺炎包含特发性淋巴细胞性间质性肺炎、特发性胸膜肺实质弹力纤维增生症及一些临床未能命名的病理改变。
杵状指的发生与患者长期慢性缺氧有关,缺氧导致末端肢体毛细血管增生扩张,软组织增生。杵状指是患者预后不良的预测因素之一[10]。我们的研究结果显示,有杵状指的患者生存期明显缩短,死亡风险度显著升高。BMI反映患者的营养状况,BMI水平越高,患者的生存期越长。既往研究显示,体重低的COPD患者,死亡风险要高于体重正常或者肥胖的患者[11,12]。营养不良的患者,容易出现胸腺萎缩,T细胞功能下降,增加感染风险。目前学者普遍认为IPF有慢性炎症参与,但是抗炎治疗的临床疗效并不明显,学者认为与炎症反应在IPF的过程中所发挥的作用不同有关,另外个体炎症反应程度也有一定的相关性。在本次研究中,血沉是影响患者预后的影响因素之一。血沉是炎症相关指标,反映机体处于炎性反应状态。血沉增快是IPF患者不良预后的危险因素。既往有研究显示,炎症指标包括血沉与患者的预后并没有相关性[13]。考虑原因可能与本次研究中纳入的部分患者合并有肺部感染,部分患者为急性加重期,导致结果存在一定的偏差。目前炎症在IPF发病过程中的具体作用还需要进一步研究,目前临床上糖皮质激素及细胞毒类药物仍然是常用的治疗方法之一[14]。血气分析是常规检查之一,反应患者缺氧情况,对肺脏受累情况有一定的认识。动脉血氧分压越低的患者,更容易合并肺动脉高压[15]。在本次研究中,单因素分析结果显示,PaO2、PaO2/FiO2、SaO2与患者的预后具有密切的关系,而多因素分析将血气分析的各指标排除,考虑可能是因为收集的数据均为患者在吸氧状况下测得,因此及时进行FiO2矫正,但是仍然受到一定程度的影响。IPF患者主要表现为限制性通气障碍,肺功能指标参数在一定程度上反映患者的严重程度。在本次研究中,肺功能指标TLC%与患者的预后具有密切的关系,是患者不良预后的高危因素。肺功能指标差,说明患者病情严重,因此预后越差。
综上所述,目前还没有治疗IPF的有效药物以及治疗方法。在本次研究中,IPF患者营养状况、肺功能、炎性指标、杵状指、肺动脉压与患者预后具有密切的关系。
[参考文献]
[1]孙辉,李建生,谢洋.重视特发性肺纤维化的并发症[J].中国全科医学,2015,18(26):3248-3252.
[2] ATS/ERS/JRS/ALAT Committee on Idiopathic Pulmonary Fibrosis.An official ATS/ERS/JRS/ALAT statement:Idiopathic oulmonary fibrosis:Evidence-based guidelines for diagnosis and management[J].Am J Respir Crit Care Med,2011,183:788-824.
[3]李珊,黄慧,徐作军.特发性肺纤维化治疗的新进展[J].中华医学杂志,2015,101(32):2651-2653.
[4]张坚,徐作军,朱元珏.特发性肺纤维化的分子发病机制及靶向药物研究进展[J].中华结核和呼吸杂志,2009,32(12):945-947.
[5]陈豪,江涛,周蜜.特发性肺纤维化治疗进展[J].临床肺科杂志,2015,20(9):1725-1727.
[6]王艳辉.孟鲁司特治疗特发性肺纤维化的临床疗效分析[J].中国继续医学教育,2015,7(10):216-217.
[7]贺琛,俞小卫.特发性肺纤维化的治疗与进展[J].临床肺科杂志,2015,20(10):1890-1892.
[8]刘建,刘燕梅,王玉光.肺泡上皮细胞凋亡与特发性肺纤维化的研究进展[J].医学综述,2015,21(16):2893-2895.
[9]满红霞,肖培云,杨永寿,等.特发性肺纤维化的发病机制及药物治疗研究进展[J].中国现代应用药学,2015,32(8):1024-1028.
[10]邓永红,王宏坤,刘伟.特发性肺纤维化预后危险因素分析[J].陕西医学杂志,2015,(9):1149-1151.
[11]于洋,韩春生,韩桂玲,等.特发性肺纤维化患者相关预后影响因素的临床研究[J].世界中医药,2014,9(8):978-982.
[12]胡旭,彭守春,魏路清.特发性肺纤维化预后相关因素的研究进展[J].实用检验医师杂志,2013,3(1):54-57.
[13]刘寅,蔡礼鸣,赵弘卿,等.特发性肺纤维化急性加重21例临床回顾分析[J].中国呼吸与危重监护杂志,2012,11(4):362-366.
[14]李燕,苗立云,姜涵毅,等.特发性肺纤维化预后相关因素的回顾性研究[J].中国呼吸与危重监护杂志,2012,11(3):257-261.
[15]徐作军.特发性肺纤维化相关性肺动脉高压[J].中华结核和呼吸杂志,2012,35(9):643-644.
Influencing factors of idiopathic pulmonary fibrosis prognosis
QIN Wenjing LIANG Yu SHAN Yuanying MENG Derong
Respiratory Medicine Department, the First Affiliated Hospital of He'nan University, Kaifeng 475001, China
[Abstract]Objective To discuss influencing factors of idiopathic pulmonary fibrosis prognosis. Methods Clinical data of 58 cases with idiopathic pulmonary fibrosis were respectively analyzed. Blood gas analysis, chest HRCT, pulmonary function, cardiac ultrasound, and bronchoalveolar lavage were detected. Influencing factors of idiopathic pulmonary fibrosis prognosis were analyzed. Results Univariate analysis showed that, clubbing, BMI, St. George's score, 6-minute walk test, FVC%, TLC%, DLCO%, PaO2, erythrocyte sedimentation rate, PaO2/FIO2, SaO2, PAP, and BALF were correlation with prognosis of idiopathic pulmonary fibrosis(P<0.05 or P<0.01). Multivariate analysis showed that, TLC%, erythrocyte sedimentation rate, clubbing, BMI, and PAP correlation with prognosis of idiopathic pulmonary fibrosis(P<0.05 or P<0.01). HR values of TLC%and BMI were lower than 1, which explained that they showed a positive relationship with the prognosis; HR values of ESR, clubbing and PAP were higher than 1, which explained that they showed a negative correlation with prognosis, and which were risk factors for poor prognosis. Conclusion Nutritional status, lung function, inflammatory markers, clubbing, and pulmonary artery pressure have close relationship with IPF prognosis.
[Key words]Idiopathic pulmonary fibrosis; Prognosis; Influencing factors; Clubbing
收稿日期:(2015-11-20)
[基金项目]河南省开封市科技社会发展攻关计划项目(1403 125)
[中图分类号]R563.9
[文献标识码]B
[文章编号]1673-9701(2016)02-0033-03
