星座药理学与中药研究*
2016-03-04谢伟东徐晨珂赵玉男杜力军
谢伟东,蒋 鑫,雷 帆,徐晨珂,赵玉男,杜力军
(1.清华大学深圳研究生院生命与健康学部健康科学与技术重点实验室 深圳 518055;2.清华大学药学院 北京 100084;3.南京中医药大学基础医学院病理教研室 南京 210046;4.清华大学生命科学院药物药理实验室 北京 100084)
星座药理学与中药研究*
谢伟东1,蒋 鑫1,雷 帆2,徐晨珂1,赵玉男3,杜力军4**
(1.清华大学深圳研究生院生命与健康学部健康科学与技术重点实验室 深圳 518055;2.清华大学药学院 北京 100084;3.南京中医药大学基础医学院病理教研室 南京 210046;4.清华大学生命科学院药物药理实验室 北京 100084)
星座药理学是一种基于细胞表型的高内涵药物筛选新方法,该方法主要根据关键信号蛋白、特定表型的细胞群,将多种药物在这些细胞上的作用情况整合成具有特定药理调节功能的药物组合和细胞星座,强调这些细胞之间能进行病理、生理功能上的有机组合与整体联系。基于不同分子靶点的药物组合,进行特定的药理调控,形成药理意义上的星座效应。星座药理学的运用可提高整体疗效、减少不良反应及药物的耐受性。星座药理学适合中药等复杂成分群在细胞水平进行活性筛选与功能评价,在中药新药研究方面具有较大的灵活性与创新活力,因而对于创新中药研究与开发具有积极的推动作用。
星座药理学 协同作用 中药 细胞实验
分子生物学技术的运用在分子层面阐释了中药药理效应与药物靶点,在一定程度上促进了中药的现代化发展。然而,这种技术应用没有使“可成药的新靶点分子”发现出现质的飞跃,使药物研发中单一靶点筛选逐渐转变为细胞或器官水平的表型筛选[1]。中药含有成百上千的化合物,药物还原论研究者试图找到这些药物的有效组分,然后鉴定其分子靶点,即所谓的药物靶点(Drug Targets)。早期,有学者预测与小分子化合物结合的靶点大约有3 000个,而目前上市药物对应的靶点仅200多个[2],因而成药性靶点的鉴定仍是相当困难。而对于病因复杂,病机广泛的疾病,“单组分、单靶点、单效应”的策略明显不符合中药药物研发的实际情况。大量研究证明,中药通过“多成分、多靶点、多效应”模式来治疗病因复杂的疾病,这也是网络药理学(Network Pharmacology)的基本内涵之一[3]。然而,如何对这些成分和靶点进行有机组合,提高药物的研发效率,目前我们还缺乏有效的研究思路。
实际上,机体某个生理功能的完成是由一系列功能不同的细胞共同实施的,在细胞内部,某一功能活动也是由许多潜在的靶点因子协同参与完成。对于某些疾病,由一系列不同细胞的集体病变所致,每种细胞的病变都有可能是该疾病发生的重要组成部分。有些中药单体成分或因靶点太单一,或因仅纠正部分病变的细胞而不能全面覆盖病变细胞群,不能发挥较好的整体调理作用,故其单体成分疗效不如中药有效部位或粗提物。将作用于不同细胞、具有特定分子作用机理的化合物进行功能上的有机组合,可较好地调理机体生理功能,形成星座药理学效应,这可能是提高整体药效、实现中药创新的重要策略之一。本文对星座药理学这一新概念及方法进行讨论,以期对中药药物研发有所裨益。
1 星座药理学
星座药理学(Constellation Pharmacology)是一种基于细胞表型的高内涵药物筛选新方法,该方法基于不同关键信号蛋白、表型的细胞群或“星座”(Constellation),调查多种有效化合物组合或“团伙”(Cabal)在这些细胞的特定作用情况,对这些作用进行功能整合[4]。星座药理学具有特定表型的细胞群,这些不同亚型的细胞可以整合具有特定的生理学功能,是药物作用最基本的靶标实体之一,通常可以由一些具有选择性分子靶点的工具药物得到鉴定。有人用星座药理学调查了小鼠小脑神经元和胶质细胞不同亚型情况,主要基于谷氨酰胺、乙酰胆碱、GABA受体和其他离子通道,用工具药分别鉴定了小脑颗粒神经元细胞和Purkinje细胞等[5]。由于这些细胞有不同的起关键作用的信号蛋白分子,从而有不同的细胞功能和表型特点。这些不同表型的细胞,单独并不一定起决定性作用,但联合在一起却成一个整体功能十分强大的“星座”,反映体内特定的生理学功能。单体化合物药效微弱或范围较窄,不能起整体调控作用,而作用于不同表型细胞的药物可以组合成化合物“团伙”,共同作用于不同表型的细胞,发挥相似、互补或协同药理作用,形成可检测的显著“星座”药理效应,对机体起到整体调控作用。
星座药理学的灵感最初来自于芋螺(Cone Snail)用毒液来捕获鱼的研究,这些注射进入鱼体内的毒液组分能组成一个“团伙”,协同作用于神经传递的不同信号蛋白,改变鱼体内正常的神经运动传递,抑制鱼的整体运动[6]。这些毒液“团伙”各自作用的靶点,比如突触前电压门控钙离子通道,突触后烟碱型乙酰胆碱受体受体,突触后电压门控钠离子通道等可组成生理功能上同系列的“星座”。有学者用星座药理学发现,在躯体感觉神经元上Na+通道异构体NaV1.7突变会出现兴奋作用,而交感神经元上NaV1.7异构体同样突变会出现抑制效应,主要原因是NaV1.7Na通道可以偶联NaV1.8通道,躯体感觉神经元上表达NaV1.8通道,但交感神经元上不表达NaV1.8通道有关[5]。这种有相同的靶点改变,但在不同特点的细胞,出现不同表型改变,说明星座药理学中的细胞表型筛选比靶点筛选更符合机体的实际情况。细胞是发挥生理功能的基本单位,星座药理学的概念开始延伸到特定细胞表型,甚至超出细胞表型的星座。基于此,一些药物完全可以形成一个“团伙”以获得更好的治疗效果。当前一些重大疾病的治疗如肿瘤、糖尿病、神经系统疾病、心血管疾病和感染性疾病(如艾滋病)等采用鸡尾酒疗法或不同机理的协同用药实际上均用到星座药理学的概念。
2 星座药理学特征
星座药理学强调整体功能效应,不同药物分子作用于特定表型的细胞,重视特定表型细胞群体与药物分子群的整体机能协调与调控效应,较少关注强大的单体药理效应或者靶点效应。如果把人体生命活动比喻成一个宇宙,某个生理机能比喻成机体内某个星座,不同的生理机能参与因子就是星座的各个星球。星座药理学,强调多个药物形成一个集团对这些星球予以微弱的调控,然后将这些效应整合,以达到显著的星座式整体效应。这种整体效应是基于特定表型的细胞群的药效组合,有别于整体动物实验,但可以反映动物或人类的某些生理功能。具有特定分子机理的细胞表型研究,也有利于药物的作用机制分析和相关活性药物的筛选。
星座药理学可以最大程度地减少不良反应。对于已经上市的药物或即将开发的药物,如果分别有不同的作用机制,我们可以建立一个药物作用“星座”,尽可能减少药物剂量,但整体上的“星座”效应仍然可以取得,因此星座药理学的引入可以减少药物由于剂量过高所引起的不良反应。
星座药理学也可以减少药物应用的耐受性。药物对单一靶点的调控时间过长或剂量过大,往往会使药物的疗效减低,需要加大剂量才能维持原有疗效,从而产生耐受性。建立由不同药物作用组成的星座,可以产生减少药物用量,同时减少用于用量过高所引起耐受性的产生。
3 星座药理学与多向药理学的异同
多向药理学(Polypharmacology)指一个药物有多个靶点,对于病因复杂的疾病如肿瘤、神经系统和炎症性疾病,可以从多个层面进行特异性药理调控[7]。多向药理学试图通过多靶点调节开发出疗效更好和副作用更少的药物。多向药理学可能作用某个疾病某一个信号通路的多个分子靶点,也有可能作用于与某个疾病相关的多个信号通路的相关分子[8]。该学科的发展可促进已上市药物发现更多靶点和新的适应症,它的挑战主要来自目前所提供的靶点远远不能诠释疾病的本质情况,另外对药物结构改造也是一项艰巨的工作。多向药理学强调一个药物有多个分子靶点,而星座药理学强调多个药物在细胞表型筛选与功能整合。
4 星座药理学与网络药理学的异同
网络药理在多向药理学的基础上进一步发展,引入了系统生物学理论,对生物系统进行网络分析,强调各靶点之间的网络调控与相互影响,选取特定信号节点进行多靶点药物分子设计。它强调通过信号通路的网络调节,以求药物效应最大化、不良反应最小化[9]。网络药理学试图通过网络分析鉴定某个疾病的一系列药物靶点和通过化学生物学的方法调查药物对这些靶点的结合效应。通过鉴定生物学网络的连接性,冗余性以及多效性可以加速药物的发现[11],可以促进理解药物作用与复杂疾病的关系,帮助提高药物设计的效率,有助于发现新的活性组分以及揭示中药复方的作用机理,比如清络饮与六味地黄丸的研究[3]。由于网络药理学考虑整个复杂的生物系统,基于网络药理学原理开发新药仍然十分困难。总之,网络药理学强调多个分子靶点筛选和生物系统内分子靶点的网络整合,但星座药理学强调多个特定细胞表型筛选与功能整合。
5 星座药理学与系统药理学的异同
系统药理学(Systems Pharmacology)在网络药理学基础上进一步延伸,研究范围更广,是利用系统生物学研究药物与机体相互作用及其规律和作用机制的一门新兴学科。由于药物、机体和环境之间的复杂相互作用,影响了药物安全性和有效性,从而容易导致药物在Ⅱ和Ⅲ临床实验中失败。系统药理学不仅在系统层面上提供药物的药效评价和靶点鉴定,而且对药物和复杂疾病之间的相互作用机制提供系统水平上的理解[11]。因而,系统药理学可以有效提高药理效应和减少不良反应。有学者运用系统药理学对中药红花复方制剂进行了心血管疾病活性相关研究,先系统性进行ADME药代动力学分析,结合药物靶点分析,得到103个潜在的活性组分和219个相应的靶点,随后建立活性组分,靶点和疾病之间的网络,对于揭示中药在复杂疾病的应用提供了一个较好的研究模式[12]。然而在实际运用过程中,运用系统药理学成功开发出中药新药的案例非常罕见。系统药理学贯穿药物研发整个过程,系统水平理解药物与机体相互作用,包括整合药代动力学、靶点捕获与网络药理学等,而星座药理学主要基于细胞水平的高内涵药物表型筛选与功能整合(表1)。

表1 多向药理学、网络药理学、系统药理学和星座药理学的比较
6 星座药理学在中药研究中的运用
对药物单一靶点的研究是一种必要手段,由于目前对某种病理或生理机能的分子靶点研究尚不透彻,疾病发病机理与药物效应始终是一个黑箱。疾病像一个浩瀚无边的“宇宙”,人类要穷尽所有疾病相关因子的“星系”非常困难,或者说这就是一个伪命题。对复杂疾病的研究如果过于依赖单一靶点,会犯“一叶障目,不见森林”的错误。单一靶点虽然可以使中药组分中疗效确切的有效成分得到发掘,但也会忽略部分不能匹配该靶点但有其他疗效的成分。
网络药理学能够在一定程度上解决上述问题,它所提倡的多靶点相互作用会产生许多药理效应(包括不良反应)。如何保留有贡献的靶点连接,而去掉那些无关或有害的靶点连接还是有些难度,且需要分离鉴定大量化合物,计算机药物靶点模拟,最后进行这些网络靶点之间的相互作用验证,这是一个耗时耗力的过程,需要较大团队或科研群体去研究,这可能使许多医药科研工长时间停留于复杂的化合物、蛋白分子网络研究,而未取得较好的实际应用效果。
特定疾病的模式动物可以用于中药药效的整体评价与筛选,但对于含量较少的中药测试物却仍不是很合适。细胞是组成生命体的基本单位,发挥基本的生理功能;不同表型的细胞可以形成一个功能集团,行使生命体特有的生理机能。分子生物学的进展如Crisp/Cas9的研究技术使细胞基因编辑变得简单可行[13],从而使特定表型的细胞获得和靶点鉴定变得简便易行。由于细胞实验需要药物剂量非常少,发展一种基于细胞表型活性检测的中药活性筛选方法值得深入研究。目前,高内涵药物筛选是基于细胞活性检测的筛选平台,可以获得大量关于细胞形态、生长、代谢和信号通路方面的信息。但是,该方法需要解决一些功能特异性问题,并且缺乏有机组合的整体观。
星座药理学强调表型研究和功能整合,可以解决以上靶点研究困难、耗时、耗力、高成本低效等不足,用于复杂组分的创新中药研究。星座药理学能增强中药疗效,减少不良反应。星座药理学强调整体细胞表型功能,能确保每一种功能星座中的药物在一个较小的剂量,发挥特定的合力或协同效应,同时能减少不良反应。中药是多成分,具有多个靶点,这恰恰或是中药的优势。中药运用星座药理学的观点将会有较大的发展前景。不同中药,或中药中的有效成分形成一个组分“团伙”,发挥特定的协同作用,将会使所使用的剂量大大减少,但可以看到理想的表型(星座药理效应),最大程度减少不适表型(不良反应)。
星座药理学还可以对“无效”中药组分进行二次开发。星座药理学可以解释中药有效部位或粗提物显示功能强大,有效成分单独应用药效微弱的原理,有利于发现一些具有药理活性但现有方法无法检测的有效化合物,我们可以通过星座药理学的平台,对这些看似无效的中药成分进行活性研究,会对这些成分的功效发掘研究有新的理解。
另外,星座药理学可以减少中药复杂组分的分离成本。我们暂时无法对每一个成分进行完全分离,但可以获得不同的有效部位,应有不同表型的细胞星座对不用部位进行筛选,获得不同有效部位的功能,组成新的有效部位作用群,产生新的具有知识产权的创新药物。因此,星座药理学是可以指导中药有效成分的分离纯化。例如,一个降糖中药组分含A、B、C和D4种有效组分,我们可以选取胰岛β细胞来进行实验(图1)。
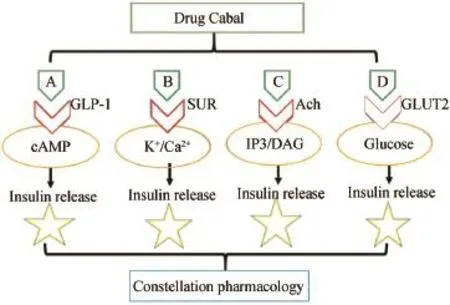
图1 星座药理学中降糖中药的研究举例
由图1可知,如果A药激活胰岛细胞上的胰高血糖素样肽受体1(GLP-1),促使细胞内cAMP含量增加,进而激活蛋白激酶A,可以促使胰岛素释放;如果B药激活磺酰脲受体(SUR),抑制ATP敏感性的钾离子通道,导致去极化,打开电压依赖的钙离子通道,导致钙内流,从而可以促进胰岛素释放;如果C药激活乙酰胆碱受体(Ach),促使生成磷酸肌醇3(IP3)和二酰甘油(DAG),激活蛋白激酶C,也可以促使胰岛素释放;如果D药促使胰岛细胞上葡萄糖转运体(GLUT2)的表达或从胞浆转位到胞膜,促进葡萄糖转运入胞,升高ATP,抑制ATP敏感性的钾离子通道,同样可促使胰岛素释放。这些药物组合(Drug Cabal),作用于具有特定信号蛋白分子的细胞,将形成具有调节胰岛素释放的“星座”,发挥相加或协同调节胰岛素释放的作用,如果这些药物运用到整体动物和临床试验,各自剂量将会大大减少,相应不良反应也会大大降低。
尽管星座药理学具有较大的灵活性与创新活力,但其对技术要求仍较高,其模型的建立以及在中药新药研究的应用,需要确定一系列具有代表性的不同表型的细胞。而且,这些细胞群的建立,需要较高水平的分子与细胞生物学技术鉴定其分子机理,还需要生理学和病理学知识进行功能整合,同时还要有相关中医药理论指导,因而需要很长时间的积累与完善。另外,该方法目前主要基于细胞模型,如何排除体外实验中药复合物中非特异性成分的刺激所带来的假阳性结果,如何进行有效成分与相关表型效应间的一一对应,这是目前面临的技术方面的挑战。
7 小结
星座药理学促进了学科交叉与知识融合,基于细胞表型的中药药效筛选与功能整合研究,有利于发现以往被忽略的中药组分集体效应,对过于重视单体的靶点效应却并无收获的陈旧思路有较大的启示作用。因此,星座药理学在复杂疾病中药新药研发及相关药物研究方面具有较大的理论指导意义。
1 Kell D B. Finding novel pharmaceuticals in the systems biology era usingmultiple effective drug targets, phenotypic screening and knowledge oftransporters: where drug discovery went wrong and how to fix it. FEBS J, 2013, 280(23): 5957-5980.
2 Imming P, Sinning C, Meyer A. Drugs, their targets and the nature and number of drug targets. Nat Rev Drug Discov, 2006, 5(10): 821-834. Review. Erratum in: Nat Rev Drug Discov, 2007, 6(2): 126.
3 Li S, Zhang B. Traditional Chinese medicine network pharmacology: theory,methodology and application. Chin J Nat Med, 2013, 11(2), 110-120.
4 Teichert R W, Schmidt E W, Olivera B M. Constellation pharmacology: a newparadigm for drug discovery. Annu Rev Pharmacol Toxicol, 2015, 55: 573-589.
5 Curtice K J, Leavitt L S, Chase K, et al. Classifying neuronal subclasses of the cerebellum through constellation pharmacology. J Neurophysiol, 2016, 115(2), 1031-1042.
6 Terlau H, Shon K, Grilley M, et al. Strategy for rapid immobilization of prey by a fish-hunting cone snail. Nature, 1996, 381: 148-151.
7 Anighoro A, Bajorath J, Rastelli G. Polypharmacology: challenges and opportunities in drug discovery. J Med Chem, 2014, 57(19): 7874-7887.
8 Reddy A S, Zhang S. Polypharmacology: drug discovery for the future. Expert Rev ClinPharmacol, 2013, 6(1): 41-47.
9 Hao da C, Xiao P G. Network pharmacology: a Rosetta Stone for traditional Chinese medicine. Drug Dev Res, 2014, 75(5): 299-312.
10 Westerhoff H V. Network-based pharmacology through systems biology. Drug Discov Today Technol, 2015, 15: 15-16.
11 Zhou W, Wang Y, Lu A, et al. Systems Pharmacology in Small Molecular DrugDiscovery. Int J Mol Sci, 2016, 17(2), pii: E246.
12 Liu J, Mu J, Zheng C, et al. Systems-Pharmacology Dissection of Traditional Chinese Medicine Compound Saffron Formula Reveals Multi-scale Treatment Strategy for Cardiovascular Diseases. Sci Rep, 2016, 6: 19809.
13 Mei Y, Wang Y, Chen H, et al. Recent Progress in CRISPR/Cas9 Technology. J Genet Genomics, 2016, 43(2): 63-75.
Constellation Pharmacology and Researches on Traditional Chinese Medicine
Xie Weidong1, Jiang Xin1, Fan Lei2, Xu Chenke1, Zhao Yunan3, Du Lijun4
(1. Shenzhen Key Laboratory of Health Science and Technology, Division of Life Science & Health, Graduate School at Shenzhen, Tsinghua University, Shenzhen 518055, China; 2. School of Pharmacology and Pharmaceutical Sciences, Tsinghua University, Beijing 100084, China; 3. Laboratory of Pathological Sciences, Basic Medical College, Nanjing University of Traditional Chinese Medicine, Nanjing 210046, China; 4. Laboratory of Molecular Pharmacology and Pharmaceutical Science, School of Life Science, Tsinghua University, Beijing 100084, China)
Constellation pharmacology is a cell-based high-content phenotypic-screening platform that investigate effects of drug cabal in cells with key signaling proteins which define specific cell types and further integrate into cell constellation with pharmacological functions. Constellation pharmacology emphasizes onorganic combinations and whole connections between different subtype cells with pathophysiological significance, in which drug cabal with different molecular targets can produce specific synergic pharmacological effects in the cell constellation. The utilization of constellation pharmacology will promote therapeutic effects, while reduce untoward effects and drug tolerances. Constellation pharmacology can be applied in the field of pharmacological evaluation of complicated compounds in traditional Chinese medicines at the level of cells, and have much flexibility and innovative vitality in the research and development of traditional Chinese medicines. Therefore, constellation pharmacology may proactively promote the research and development of novel traditional Chinese medicine.
Constellation pharmacology, synergic action, traditional Chinese medicines, cellular experiments
10.11842/wst.2016.06.013
R965.1
A
(责任编辑:马雅静,责任译审:朱黎婷)
2016-05-25
修回日期:2016-06-14
* 国家自然科学基金委面上项目(81373460):基于ceRNA与miRNA“网络对话”研究胰岛细胞炎症“微环境”与功能及探索抗糖尿病药物新策略,负责人:谢伟东。
** 通讯作者:杜力军,本刊编委,教授,主要研究方向:药理学。
