维持性血液透析患者高磷血症的相关因素分析
2016-03-01丁红莲汪裕伟杨沿浪
丁红莲,汪裕伟,杨沿浪
(1.皖南医学院附属弋矶山医院,安徽 芜湖 241000;2.池州市人民医院,安徽 池州 247000)
维持性血液透析患者高磷血症的相关因素分析
丁红莲1,2,汪裕伟1,杨沿浪1
(1.皖南医学院附属弋矶山医院,安徽 芜湖241000;2.池州市人民医院,安徽 池州247000)
摘要:目的调查该院维持性血液透析(MHD)患者的血磷状况,对其相关影响因素做出临床分析,为血磷控制提供科学依据。方法比较该院透析中心88例MHD患者的血磷、钙、钙磷乘积、甲状旁腺素、碱性磷酸酶及血清白蛋白的检测数值,按照透析频次、透析器超滤系数、是否服用降磷药物等进行分组,对高磷血症的影响因素进行相关性分析。结果88例MHD患者中高磷血症发生率为62.5%,血磷与年龄、碱性磷酸酶呈负相关,与血清白蛋白、甲状旁腺素呈正相关,透析频次高组较透析频次低组血磷水平低,高通量透析器治疗组较低通量透析器治疗组血磷水平低,服用含钙磷结合剂治疗高磷血症有效,碳酸钙组与醋酸钙组之间无显著统计学差异。结论MHD患者高磷血症患病率高,应进一步指导患者低磷饮食、加强透析频次、改善透析方式、规范使用磷结合剂,以此全方位加强对血磷的控制。
关键词:高磷血症;维持性血液透析;相关因素;分析
慢性肾脏病(chronic kidney disease,CKD)目前已经成为全球公共卫生问题,血液透析(hemodialysis,HD)治疗的患者人数呈递增趋势,而矿物质代谢紊乱(高磷血症、高钙血症、高甲状旁腺激素)已成为MHD患者猝死的独立危险因素[1]。研究证实高磷对血钙、全段甲状旁腺素(iPTH)、1,25(OH)2D3、成纤维细胞生长因子23(FGF23)等都有重要的调节作用,因此在慢性肾脏病-矿物质及骨代谢异常(chronic kidney disease-mineral and bone disorder,CKD-MBD)发病机制中扮演了关键角色[2]。本文旨在比较我院透析中心88例MHD患者的血磷、钙、钙磷乘积、甲状旁腺素、碱性磷酸酶及血清白蛋白的检测数值,重点阐述高磷血症的相关临床影响因素,为指导防治提供科学依据。
1资料与方法
1.1对象与分组回顾性分析我院透析中心2014年1—9月行MHD治疗的CKD患者88例,其中男性55例,女性33例,年龄17~85岁(56±15岁),透析龄2~113月(47±31月)。CKD临床病因诊断:慢性肾小球肾炎31例,高血压肾病22例,糖尿病肾病17例,急进性肾小球肾炎2例,狼疮性肾炎3例,梗阻性肾病2例,慢性肾盂肾炎2例,先天性多囊肾2例,不明病因7例。血液透析使用费森尤斯4008B、金宝AK95、日机装DBB27透析机,使用透析器型号如下:Nipro SUREFLUX-130G LC GA空心纤维透析器(超滤系数18 mL·h-1·mmHg-1)、Nipro FB-150U LC GA空心纤维透析器(超滤系数37 mL·h-1·mmHg-1、Bello BLS 814 SD透析器(超滤系数61 mL·h-1·mmHg-1),均采用碳酸氢盐透析,透析液钙浓度1.5 mmol·L-1,钾浓度2.0 mmol·L-1,每周透析2~3次,每次3.5~4 h。
2结果
本研究观察患者血磷(6.08±1.96)mg·dL-1、钙(9.13±1.06 )mg·dL-1、钙磷乘积(55.43±18.78) mg2·dL-2、甲状旁腺素(413.99±471.26)ng·L-1、碱性磷酸酶(111.29±92.04) IU·L-1以及血清白蛋白(37.64±4.75)g·L-1,其中血磷>5.5 mg2·dL-1(1.78 mmol·L-1)者占62.5%,血钙<8.4 mg·dL-1(2.10 mmol·L-1)者占18.2%,钙磷乘积>55 mg2·dL-2者占50.0%,甲状旁腺素>300 ng·L-1者占42.5%。在对血磷水平与年龄、血清白蛋白、碱性磷酸酶、甲状旁腺素之间相关性分析发现,血磷水平与年龄、碱性磷酸酶呈负相关,与白蛋白、甲状旁腺素呈正相关。见表1。
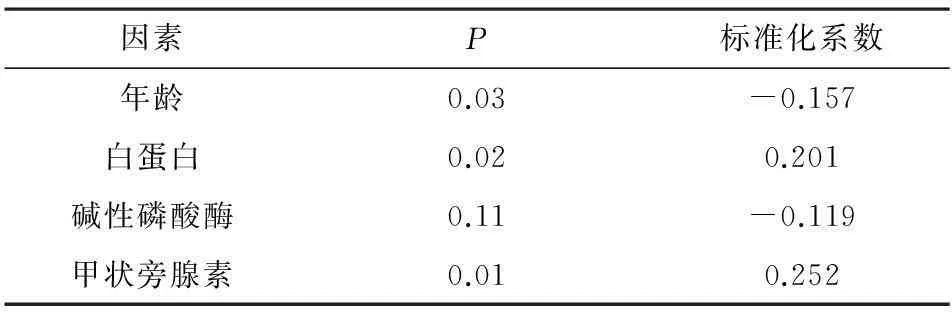
表1 血磷水平和临床参数相关性分析
在对不同透析频次分组的血磷水平观察发现,透析频次高组血磷值低于透析频次低组,但两组之间差异无统计学意义(P>0.05)。见表2。
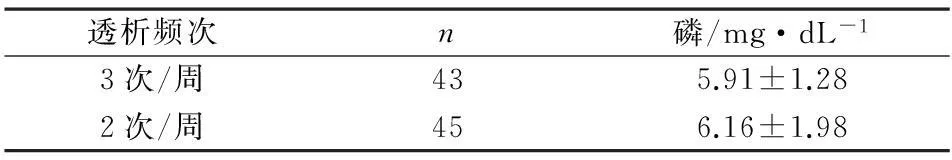
表2 不同透析频次患者的血磷水平
在对按使用不同通量透析器分组的患者血磷水平观察发现,使用高通量透析器治疗组血磷值低于高通量透析器治疗组。见表3。
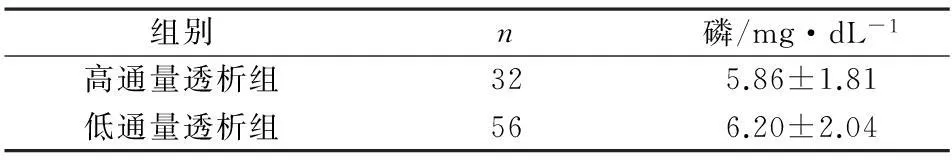
表3 使用不同通量透析器患者的血磷水平
在对服用不同含钙磷结合剂及未服用降磷药物患者的血磷水平观察发现,服药组血磷水平低于未服药组,碳酸钙组与醋酸钙组无显著统计学差异。见表4。
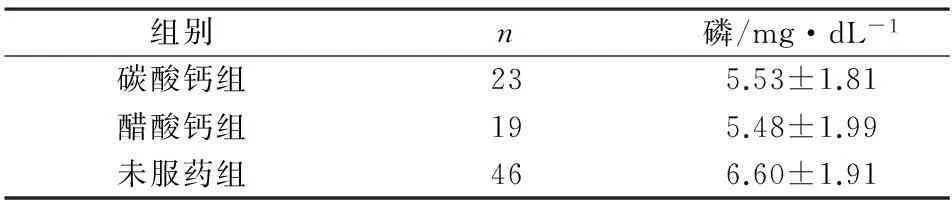
表4 按使用含钙磷结合剂类型分组及
3讨论
MHD患者体内有毒物质潴留,引起活性维生素D相对或绝对不足、小肠功能受损、钙吸收减少,加上肾小球率过率降低、肾脏排磷明显减少、磷的摄入增高、透析清除有限等原因而普遍存在高磷血症[3]。大量临床研究证实高血磷与肾功能持续恶化、心血管疾病、继发性甲状旁腺功能亢进(secondary hyperparathyroidism,SHPT)和骨代谢紊乱均密切相关,这些并发症直接或间接导致CKD患者病死率增加[4],其危害性在MHD患者中则更为突出。Floege等[5]回顾性分析了7 970例MHD患者的临床资料,结果发现血磷水平和病死率呈U型曲线关系,血磷水平为3.5~5.5 mg·dL-1(1.13~1.78 mmol·L-1)时病死率最低,高于或低于此范围,病死率明显增加。
目前全球均存在MHD患者高磷血症突出的问题。当前大量的临床研究表明高磷血症的控制率、知晓率非常不理想,严重影响患者的预后[6]。2012年的DOPPS研究显示,较之欧美发达国家,我国血液透析患者高磷血症的患病率更高,达到57.4%[7],本透析中心的最新统计数据为62.5%,高于国内平均值。而依据K/DOQI指南建议,MHD患者的血磷目标值为3.5~5.5 mg·dL-1(1.13~1.78 mmol·L-1),血钙目标值为8.4~9.5 mg·dL-1(2.10~2.37 mmol·L-1),钙磷乘积目标值小于55 mg2·dL-2,甲状旁腺素目标值为150~300 ng·L-1,所以我们的防治工作显得尤为重要。
本研究发现血磷的水平与年龄呈负相关,老年组总体血磷水平优于非老年组,这可能与老年患者进食量较少、对自身健康关注性高且医嘱依从性较好有关。正常成人每日饮食摄磷量约1 000~1 800 mg·d-1,而K/DOQI指南推荐的饮食摄磷量为800 mg·d-1,所以饮食控制一直是控制高血磷最基本的措施,也是极为重要的措施。由于磷的摄入量与蛋白质的摄入量呈正相关,过分限制磷的摄入会导致低蛋白血症,而血清白蛋白由肝脏合成,是反映患者体内蛋白质储存最重要、最常用的生化参数,营养不良是MHD患者预后差的强烈指标[8]。由表1可以看出,本透析中心非老年组血清白蛋白值(39.3±4.3)g·L-1高于老年组(35.8±4.6)g·L-1,说明老年MHD患者在限磷饮食基础上应科学地摄入蛋白质。
CKD患者高磷血症、低钙血症及维生素D的合成减少共同导致了甲状旁腺素水平的升高,而高血磷直接影响甲状旁腺的基因表达、细胞增殖及甲状旁腺激素分泌,引起SHPT[9]。SHPT不仅可以导致骨骼的严重损害,而且可以引起皮肤瘙痒、贫血、神经系统损害及心血管疾病,并参与尿毒症患者体内微炎症状态的形成。本透析中心甲状旁腺素达标率不理想(仅为33%),与血磷的水平呈一定的正相关性,故降磷的同时应注重甲状旁腺素的合理控制。
本研究组数据表明,MHD患者的透析频次越高,使用的透析器通量越高,血磷的控制相对较好。有研究证实,常规血液透析方式对磷的清除有限[10],通过调整透析方式可以增加透析中磷的清除,如增加透析频次[11]、高通量血液透析[12]。我院透析中心的数据显示,目前行每周三次透析治疗的患者仅占研究组的48.9%,使用高通量透析器的患者为36.4%,这与地区的经济水准及医保政策关系密切,在患者经济条件许可下应鼓励加强透析频次、改善透析方式,以此加强对高磷血症的控制。
目前治疗高磷血症的药物主要为磷结合剂,分为含铝磷结合剂、含钙磷结合剂、非铝非钙磷结合剂三大类。本研究组患者使用的含钙磷结合剂为碳酸钙及醋酸钙,从表4可以看出,服药组的血磷水平低于未服药组,而碳酸钙组与醋酸钙组之间无显著统计学差异。需要注意的是,虽然含钙磷结合剂降磷效果确切、运用广泛,是目前治疗MHD患者高磷血症的一线药物,但易导致钙负荷过多,特别是与活性维生素D合用时更容易发生,使患者出现血管和其他部位转移性钙化[13],所以在用药过程中需加强监测血磷、血钙水平,及早使用低钙透析液。含铝磷结合剂由于其骨及神经毒性现临床已不再使用[14],非铝非钙磷结合剂譬如新型磷结合剂碳酸镧、盐酸司维拉姆等虽然降磷效果确切,临床观察不良反应小,但因价格昂贵本透析中心暂无患者使用。
综上所述,MHD患者血磷控制达标率低,应重视高磷血症的防治工作,通过指导患者科学限磷饮食、加强透析频次、改善透析方式、规范使用磷结合剂等多项措施加强对血磷的控制。
参考文献:
[1]郭劲,马春荣,余蕾,等.高通量血液透析及高通量血液透析滤过对骨及矿物质代谢的影响[J].安徽医药,2014,18(2):319-321.
[2]王梅.慢性肾脏病患者高磷血症的治疗[J].肾脏病与透析肾移植杂志,2014,3(3):247-248.
[3]王海燕 主编. 肾脏病学[M].3版.北京:人民卫生出版社,2008: 1922.
[4]魏青,汤日宁,刘必成.慢性肾脏病患者高磷血症的危害性研究进展[J].中华实用诊断与治疗杂志,2014,28(11):1041-1043.
[5]Floege J,Kim J,Ireland E,et al.Serum iPTH,calcium and phosphate,and the risk of mortality in a European hemodialysis population[J].Nephrol Dial Transplant,2011,26(6):1948-1955.
[6]Panichi V,Bigazzi R,Paoletti S,et al.Impact of calcium,phosphate,PTH abnormalities and management on mortality in hemodialysis:results from the RISCAVID study[J].J Nephrol,2010,23(5):556-562.
[7]Kong X,Zhang L.Mineral and bone disorder in Chinese dialysis patients:a multicenter study[J].BMC Nephrology,2012,13(1):116-122.
[8]焦春红.血液透析充分性评估[J].国际移植与血液净化杂志,2010,5(3):18-19.
[9]张景红,宦红娣.维持性血液透析患者高磷血症的控制[J].中国血液净化,2009,8(10):533-535.
[10] 周文祥,郑文彬,黄小妹,等.维持性血液透析患者钙磷乘积与营养状态的关系[J].中国血液净化,2009,8(5):253-255.
[11] 李月红,王梅.北京市2007年慢性维持性血液透析患者钙磷代谢分析[J].中国血液净化,2010,9(2):112-115.
[12] Schneider A,Drechsler C,Krane V,et al.The effect of high-flux hemodialysis on hemoglobin concentrations in patients with CKD:results of the MINOXIS study[J].Clinical Journal of the American Society of Nephrology,2012,7(1):52-59.
[13] 陈楠,史浩.慢性肾脏病高磷血症治疗-新型磷结合剂碳酸镧研究进展[J] .中华内科杂志,2012,51(9):742-744.
[14] 吴燕.慢性肾脏病降磷治疗的选择[J].肾脏病与透析肾移植杂志,2014,23(3):250-251.
1.2研究方法所有患者空腹抽取静脉血标本,血清生化检测采用日本奥林巴斯AU5400血生化自动分析仪,血清钙、磷、碱性磷酸酶及血清白蛋白采用比色法测定,正常值:血磷2.6~4.5 mg·dL-1(0.84~1.45 mmol·L-1),血钙8.8~10.8 mg·dL-1(2.20~2.70 mmol·L-1),校正钙公式:校正钙(mg·dL-1)=血清总钙(mg·dL-1)+0.8×[4-血清白蛋白(g·dL-1)],钙磷乘积<55 mg2·dL-2,碱性磷酸酶20~190 IU·L-1,血清白蛋白35~52 g·L-1,血清甲状旁腺素使用西门子全段甲状旁腺激素测定试剂盒,采用化学发光法测定,正常值为11.0~67.0 ng·L-1。
1.3统计学分析应用SPSS 11.0统计软件进行数据处理。计量资料用均数±标准差表示,组间比较采用t检验,相关分析采用直线相关分析,P<0.05有统计学意义。
收稿日期:(2015-04-11,修回日期:2015-05-25)
通讯作者:汪裕伟,男,主任医师,硕士生导师,研究方向:慢性肾脏疾病诊治, E-mail:wangyuwei921@sina.com
doi:10.3969/j.issn.1009-6469.2016.01.045
