转录因子BACH2在冠心病患者外周血单个核细胞中的表达及意义①
2016-02-24单圣帅王博远林吉斌李大主
单圣帅 王博远 凯 山 林吉斌 林 静 李大主
(华中科技大学同济医学院附属协和医院心内科,武汉430022)
·临床免疫学·
转录因子BACH2在冠心病患者外周血单个核细胞中的表达及意义①
单圣帅王博远凯山林吉斌林静②李大主
(华中科技大学同济医学院附属协和医院心内科,武汉430022)
[摘要]目的:研究转录因子BACH2在冠心病(CAD)患者外周血单个核细胞中的表达水平,并探讨其在冠心病发病中的意义及作用机制。方法:采用密度梯度离心法分离急性冠脉综合征(ACS)、稳定型心绞痛(SA)和正常对照组(NS)三组受试者外周血单个核细胞(PBMC);采用RT-PCR和Western blot法检测不同组别PBMC中BACH2及TLR4的表达量;采用ELISA法检测不同组别血清ox-LDL及TH1,TH2,TH17 和 Treg细胞各自标志性细胞因子(IFN-γ,IL-4,IL-17 和 TGF-β1)的水平。组间差异的比较使用方差齐性分析,各变量之间的相关性使用直线回归分析。结果:ACS组病人PBMC中的BACH2表达显著下调,TLR4表达显著上调。ACS组血清ox-LDL及IFN-γ、IL-4、IL-17水平较SA组和NC组显著升高,而TGF-β1显著降低。CAD患者PBMC中的BACH2表达量与TLR4表达水平显著负相关;BACH2表达量与IFN-γ、IL-4和IL-17水平负相关,与TGF-β1水平显著正相关。结论:冠心病患者循环中的BACH2表达降低;CAD病人循环中高浓度的ox-LDL可能通过激活TLR4抑制BACH2的表达,进而造成CD4+T细胞亚群分化和发育失调以及炎症因子分泌紊乱,从而导致冠心病的发生和发展。
动脉粥样硬化(Atherosclerosis,AS)是一种慢性炎症性疾病,多种炎症细胞(如CD4+T细胞、单核-巨噬细胞)和炎症因子在其中发挥重要作用[1]。Toll样受体(Toll-like receptors,TLRs)特别是Toll样受体4(Toll-like receptor4,TLR4)识别并接受氧化性低密度脂蛋白(oxidized low density lipoprotein,ox-LDL)的刺激,导致抗原提呈细胞的激活,以及作为T细胞的共刺激信号促进T细胞激活,激活的T细胞产生炎症因子网络,并进一步激活多种免疫细胞,引发并促进AS炎症反应[1-3]。新近研究发现,B淋巴细胞转录抑制剂BTB和CNC同源类似物2(B lymphoid transcription repressor BTB and CNC homology 2,BACH2)是CD4+T细胞分化和发育的关键调节因子,它通过维持免疫激活与免疫耐受之间的平衡防止炎症性疾病的产生[4]。BACH2与哮喘、克罗恩病、乳糜泻、白癜风、多发性硬化、肺炎等多种免疫性和炎症性疾病有关[5-10]。BACH2是否也参与AS的炎症反应目前尚不清楚。本研究通过检测BACH2及TLR4在冠心病患者PBMC中的表达,以及循环中的ox-LDL及冠心病相关炎症因子(IFN-γ,IL-4,IL-17和TGF-β1)的水平,探讨BACH2在AS发病中的意义及可能的作用机制。
1材料与方法
1.1主要试剂RT-PCR试剂盒购自TakaRa公司;PCR引物由北京擎科新业生物技术有限公司引物合成;检测人源性IFN-γ,IL-4,IL-17,TGF-β 1酶联免疫吸附试验(Enzyme-linked immunosorbent assay,ELISA)试剂盒购自RayBiotech公司;ox-LDL ELISA试剂盒购于上海Westang Biotech公司;淋巴细胞分离液购于Axis-Shield公司;用于蛋白质免疫印迹法(Western blot)的anti-BACH2抗体购于Aviva Systems Biology公司;anti-TLR4抗体购于eBioscience公司。
1.2方法
1.2.1研究对象挑选2013年11月至2014年9月在武汉协和医院心内科住院病人共110例,根据纳入标准和排除标准分三组:急性冠脉综合征(Acute Coronary Syndrome,ACS)组35例,稳定型心绞痛(Stable Angina,SA)组35例和正常对照组(Normal Control,NC)40例。ACS及SA的纳入标准采用新近中华医学会心血管病学分会制定的冠心病诊断指南,NC组选取正常体检人群。纳入的三组受试者需满足以下条件:排除患有其他急慢性炎症性疾病;未使用抗炎药物及免疫抑制剂;无肿瘤性疾病;无急慢性肾衰竭及肝功能衰竭。
1.2.2样本采集所有受试者于入院24 h内采集外周血10 ml并置于肝素抗凝的无菌试管中,采集后立即离心取上层血清-80℃保存备用,血清标本保存不超过30 d。
1.2.3密度梯度离心法分离外周血单个核细胞(PBMC) 将采集的肝素抗凝静脉血离心去上层血清后,使用PBS稀释并转移到含淋巴细胞分离液上。按照密度梯度离心法获得PBMC。
1.2.4RT-PCR检测不同组别PBMC中BACH2及TLR4的mRNA表达按RT-PCR试剂盒提供方法进行,反转录后PCR,β-actin为内参(所用引物见表1)。采用 2-ΔΔCt算法分析结果。
1.2.5Western blot检测不同组别PBMC中BACH2及TLR4的蛋白质表达提取PBMC总蛋白并使用BCA法测蛋白浓度。每孔上样50ug蛋白质,蛋白变性后10 % SDS-PAGE电泳、转膜并封闭,加一抗(anti-BACH2 1∶500,anti-TLR4 1∶200)孵育后再加入二抗孵育。最后加入荧光检测试剂,UVP凝胶成像系统进行图像分析。
1.2.6ELISA法检测不同组别血清ox-LDL及细胞因子IFN-γ、IL-4、IL-17、TGF-β1的浓度根据说明书检测不同组别血清ox-LDL及IFN-γ、IL-4、IL-17、TGF-β1的浓度。
2结果
2.1不同组别的临床特点三组受试者的年龄、性别、高血压病史、糖尿病史、吸烟史及脂质代谢紊乱病史无明显差异。ACS组病人的既往发病史及PCI史比其他组更常见。ACS组、SA组两组的药物使用情况相似且比阴性对照组更常见(表2)。
表1PCR引物
Tab.1PCR primers

PrimersForward(5'-3')Reverse(5'-3')BACH2ATGCACAAGCTAACCTCAGATCACTAGGTATAATCTTTCCTGTLR4TACAAAATCCCCGACAACCTCCGCTGCCTAAATGCCTCAGGGβ-actinATCTGGCACCACACCTTCTACGAGGCGTACAGGGATAGCAC
2.2临床生化指标检测结果包括总胆固醇、LDL、HDL、甘油三酯、血糖、白细胞计数和血肌酐水平(表3)。不同组别的LDL、HDL、甘油三酯、血糖水平无显著差异。ApoA1 和ApoB在三组受试者中有差异。与SA和NC相比,ACS组的白细胞计数有轻度升高。
2.3BACH2在不同组别PBMC中的表达RT-PCR表明,和NS组相比,ACS和SA组PBMC中的BACH2 mRNA表达量显著下降(NC;1.00±0.02,ACS;0.265±0.06,SA;0.552±0.115,P<0.001)。而且,和SA组相比,ACS组也有显著下降(P<0.001)(图1A)。Western blot结果与RT-PCR相似,ACS组BACH2蛋白质的表达显著减少(P<0.001,ACS vs NCP<0.001,SA vs NCP<0.001)。ACS组与SA组相比亦显著减少(ACS vs SAP<0.001)(图1B)。
2.4TLR4在不同组别PBMC中的表达RT-PCR表明,ACS和SA组TLR4 mRNA表达明显增加(ACS;1.85±0.65,SA;1.52±0.34,NC;1.00±0.00,P<0.05),ACS和SA组相比亦有显著差别(P<0.05)(图2A)。Western blot表明,ACS组病人TLR4蛋白表达显著增高(ACS vs NCP<0.001),ACS和SA组相比亦有显著差别(ACS vs SAP<0.05)(图2B)。
2.5PBMC中的BACH2与TLR4之间的相关性直线回归分析表明,在全部受试者PBMC中,BACH2与TLR4的表达量之间存在显著负相关,具有统计学意义(r2= 0.93,P<0.000 1) (图3)。
表2不同组别的临床特点[n(%)]
Tab.2Baseline clinical characteristics of the three groups of subjects[n(%)]

CharacteristicsNC(n=40)SA(n=35)ACS(n=35)PvalueAge(Years)56.75±8.6657.71±9.3459.49±8.62NSFemalegender(%)15(37.5)12(34.3)12(34.3)NSRiskfactorsHypertension11(27.5)14(40)17(48.6)NSDiabetes4(10.0)7(20.0)9(25.7)NSSmoking11(27.5)9(25.7)15(42.86)NSDyslipidaemia7(17.5)9(25.7)11(31.4)NSFamilyhistoryofCAD5(12.5)8(22.9)11(31.4)NSCurrentmedicationAspirin6(15.0)10(28.6)1)16(45.7)<0.05(0.014)β-Blockers3(7.5)7(20.0)1)15(42.9)<0.05(0.001)ACEinhibitors4(12.5)8(22.86)1)12(33.33)<0.05(0.039)Statins4(10.0)11(31.4)1)15(42.9)<0.05(0.005)CCB3(7.5)6(17.1)1)11(31.4)<0.05(0.027)ClinicalhistoryPreviousACS-4(11.4)2)6(17.1)<0.031PreviousPCI-2(5.7)2)5(14.29)<0.040
Note:1)SA vs NC;2)SA vs ACS.
2.6不同组别血清中炎症因子(pg/ml)的含量ELISA结果表明,ACS组的IFN-γ分泌量显著升高(ACS 48.64±2.548,NC 28.54±1.718,SA 39.96± 1.815;ACS vs NCP<0.0001,ACS vs SAP=0.007 1)。ACS组的IL-4 和IL-17水平亦显著升高(IL-4:ACS 9.033±0.672,NC 6.206±0.337,SA6.918±0.306 1;ACS vs NCP=0.000 4,ACS vs SAP=0.005 6。IL-17:ACS 178.6± 5.475,NC 98.65±2.614,SA 131.9 ± 5.197;ACS vs NCP<0.000 1,ACS vs SAP<0.0001)。然而,ACS组的TGF-β1水平显著降低(ACS 89.72±1.949,NC 103.3±2.045,SA 7.16±1.757;ACS vs NCP<0.000 1,ACS vs SAP=0.006 0)(图4)。
表3不同组别的临床生化指标检测结果
Tab.3Biochemical indicators of the three groups of patients
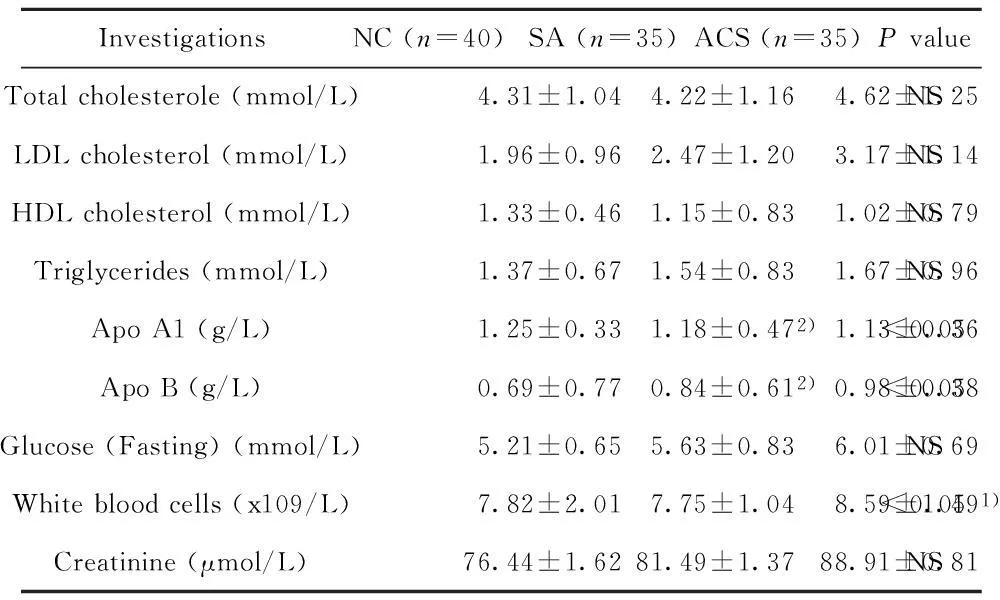
InvestigationsNC(n=40)SA(n=35)ACS(n=35)PvalueTotalcholesterole(mmol/L)4.31±1.044.22±1.164.62±1.25NSLDLcholesterol(mmol/L)1.96±0.962.47±1.203.17±1.14NSHDLcholesterol(mmol/L)1.33±0.461.15±0.831.02±0.79NSTriglycerides(mmol/L)1.37±0.671.54±0.831.67±0.96NSApoA1(g/L)1.25±0.331.18±0.472)1.13±0.36<0.05ApoB(g/L)0.69±0.770.84±0.612)0.98±0.38<0.05Glucose(Fasting)(mmol/L)5.21±0.655.63±0.836.01±0.69NSWhitebloodcells(x109/L)7.82±2.017.75±1.048.59±1.491)<0.05Creatinine(μmol/L)76.44±1.6281.49±1.3788.91±0.81NS
Note:1)ACS vs NC and SA;2)SA vs NC.

图1 不同组别PBMC中BACH2的表达Fig.1 Expression levels of BACH2 on PBMC in NC,SA and ACS groupsNote: A.RT-PCR analysis of BACH2 mRNA expression levels in three groups.B.Western blot analysis of BACH2 protein level in three groups.Gray levels were normalized against β-actin (ACS vs NC P<0.001,ACS vs SA P<0.001,SA vs NC P<0.001).

图2 不同组别的PBMC中的TLR4表达Fig.2 Measurement of TLR4 expression levels on PBMC in three groups
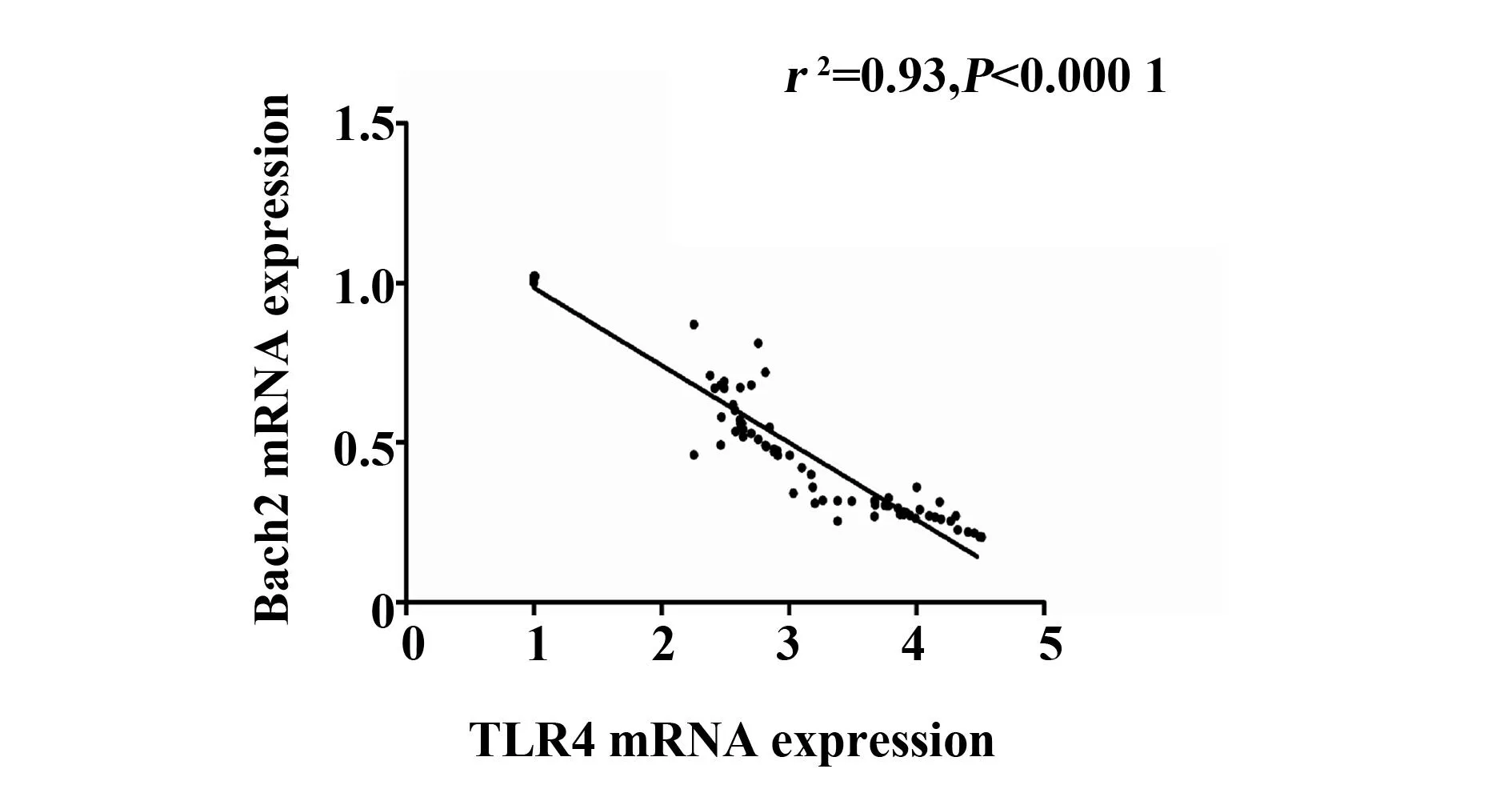
图3 PBMC中的BACH2与TLR4之间的相关性Fig.3 Correlation between expression levels of BACH2 and TLR4 in all subjects

图4 不同组别血清中炎症因子的含量Fig.4 Serum levels of Th1 (IFN-γ),Th2 (IL-4),Th17 (IL-17) and Treg (TGF-β1) cytokines among groups

图5 转录因子BACH2与炎症因子的相关性Fig.5 Correlation between expression levels of BACH2 and pro-inflammatory and anti-inflammatory cytokines in all subjects of three groups
2.7BACH2与炎症因子的相关性直线回归分析表明,在所有受试者中,BACH2与IFN-γ(r=-0.62,P<0.000 1),IL-4(r=-0.32,P=0.007 3)和IL-17(r=-0.52,P<0.000 1)负相关,与抑炎因子TGF-β1(r=0.74,P<0.000 1)显著正相关,具有统计学意义(图5)。
2.8不同组别血清ox-LDL(μg/ml)的浓度ACS组血清ox-LDL 显著升高(ACS 32.35±0.701,SA 22.23±0.642 0,NC 15.28±0.427 1,ACS vs NCP<0.000 1 ;ACS vs SAP<0.000 1)。SA组与NC组相比,ox-LDL亦显著升高(P<0.000 1),见图6。
2.9BACH2与ox-LDL的相关性直线回归分析表明,PBMC中的BACH2表达量与血清ox-LDL浓度显著负相关,具有统计学意义(r=-0.78,P<0.000 1),见图7。
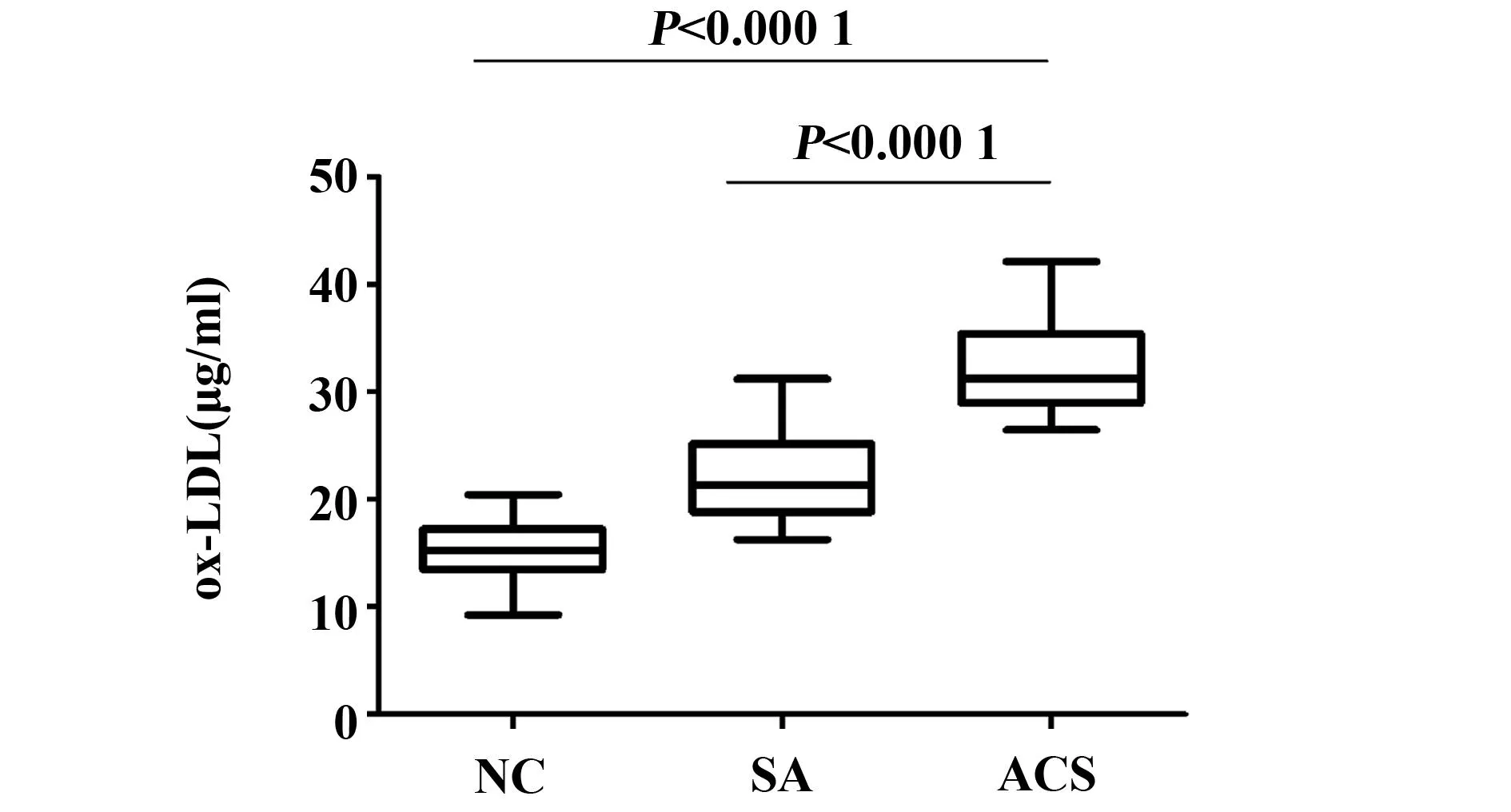
图6 不同组别血清ox-LDL的浓度Fig.6 Circulating concentrations of ox-LDL in threegroups

图7 PBMC中的BACH2表达量与血清ox-LDL浓度的相关性Fig.7 Correlation between expression levels of BACH2 in PBMC and concentrations of ox-LDL in serum in all subjects of three groups
3讨论
CD4+T细胞亚群通过促进或抑制AS的炎症反应参与AS发生发展[11]。TH1细胞引发的促炎反应在AS中发挥关键作用,而TH2和TH17细胞在AS中的作用目前还存在争议,Treg通过产生抑制炎症的细胞因子在防止AS方面发挥关键作用[11]。然而,CD4+T细胞在CAD炎症反应中的调控机制目前尚不清楚。
新近研究发现,转录因子BACH2是CD4+T细胞分化和发育的关键调节因子,BACH2通过抑制效应程序稳定Treg细胞介导的免疫稳态[4]。具有效应细胞特异性功能的Map3k8,以及Gata3、Irf4、Nfil3和Ahr,分别对TH1、TH2和TH17细胞分化具有重要作用[12-16],BACH2通过抑制这些基因的表达,从而对TH1、TH2和TH17细胞的分化发挥关键作用[4]。BACH2敲除的小鼠T细胞显示出自发激活,并引起TH1/TH2型细胞因子产生增加,而Treg细胞表现出Foxp3表达量减少,细胞数量减少,进而导致严重的肺部慢性炎症病变[10]。因此,BACH2在维持免疫稳态防止炎症性疾病方面发挥重要作用。BACH2是否也参与了AS的炎症反应,目前尚未见报道。我们的研究发现,与正常人群相比,CAD患者循环中的BACH2表达显著降低。这是我们首次发现转录因子BACH2与AS相关,这表明BACH2可能参与了AS的炎症反应。
为了探讨BACH2是否调控了CD4+T细胞在CAD的炎症反应,我们检测了CAD和正常人群体内CD4+T细胞亚群分泌的标志性炎症因子IFN-γ(Th1)、IL-4 (Th2)、IL-17(Th17)和TGF-β1(Treg)的水平。我们发现,ACS病人循环水平的IFN-γ、IL-4、IL-17显著升高,而TGF-β1显著降低。这与文献报道的结果是一致的。直线回归分析显示,BACH2表达量与IFN-γ、IL-4和IL-17的分泌量呈负相关,而与TGF-β1的分泌量呈显著正相关,提示BACH2可能通过调控CD4+T细胞的分化和发育及相关炎症因子的分泌,进而在冠心病发病过程中发挥重要作用。
研究证实,ox-LDL是AS发生发展的关键危险因素[17]。为了进一步探讨BACH2与AS危险因素之间的关系,本研究组检测了CAD患者和正常人群血清ox-LDL。我们发现,与正常人群相比,CAD患者血清ox-LDL浓度显著升高。直线回归分析表明,PBMC中的BACH2表达量与ox-LDL浓度显著负相关。这提示ox-LDL可能通过抑制BACH2的表达发挥致AS作用。但是,ox-LDL是通过何种方式抑制BACH2的表达还需探讨。
TLR4是ox-LDL致AS作用的重要配体,TLR4识别并接受ox-LDL的刺激,导致单核-巨噬细胞和T细胞激活,促进炎症因子产生,引发AS炎症反应[2]。因而我们推测,ox-LDL有可能通过TLR4抑制BACH2的表达。我们检测了CAD和正常人群PBMC中的TLR4的表达。结果表明,ACS病人循环中的TLR4表达显著上调。直线回归分析显示,PBMC中的BACH2量与TLR4显著负相关。提示ox-LDL可能是通过TLR4抑制了BACH2的表达。
综上所述,CAD患者循环中高浓度的ox-LDL可能通过激活TLR4抑制BACH2的表达,进而造成下游的CD4+T细胞亚群分化和发育失调以及相关炎症因子分泌紊乱,从而导致CAD的发生和发展。上述发现不仅证实了BACH2与AS的相关性,还为进一步阐明BACH2在AS炎症中的作用和机制提供依据,为冠心病防治提供了潜在的新靶点,因而具有重要的临床意义。
参考文献:
[1]Hansson GK,Robertson AK,Soderberg-Naucler C.Inflammation and atherosclerosis[J]. Annu Rev Pathol,2006,1:297-329.
[2]Chávez-Sánchez L,Garza-Reyes MG,Espinosa-Luna JE,etal.The role of TLR2,TLR4 and CD36 in macrophage activation and foam cell formation in response to oxLDL in humans[J].Hum Immunol,2014,75(4):322-329.
[3]Wang L,Li D,Yang K,etal.Toll-like receptor-4 and mitogen-activated protein kinase signal system are involved in activation of dendritic cells in patients with acute coronary syndrome[J].Immunology,2008,125(1):122-130.
[4]Roychoudhuri R,Hirahara K,Mousavi K,etal.BACH2 represses effector programs to stabilize T(reg)
-mediated immune homeostasis[J].Nature,2013,498(7455):506-510.
[5]Ferreira MA,Matheson MC,Duffy DL,etal.Identification of IL6R and chromosome 11q13.5 as risk loci for asthma[J].Lancet,2011,378(9795):1006-1014.
[6]Franke A,Mcgovern DP,Barrett JC,etal.Genome-wide meta-analysis increases to 71 the number of confirmed Crohn′s disease susceptibility loci[J].Nat Genet,2010,42(12):1118-1125.
[7]Jin Y,Birlea SA,Fain PR,etal.Genome-wide association analyses identify 13 new susceptibility loci for generalized vitiligo[J].Nat Genet,2012,44(6):676-680.
[8]Hellenthal G,Pirinen M,Sawcer S,etal.Genetic risk and a primary role for cell-mediated immune mechanisms in multiple sclerosis[J].Nature,2011,476(7359):214-219.
[9]Dubois PC,Trynka G,Franke L,etal.Multiple common variants for celiac disease influencing immune gene expression[J].Nat Genet,2010,42(4):295-302.
[10]Kim EH,Gasper DJ,Lee SH,etal.Bach2 regulates homeostasis of Foxp3+regulatory T cells and protects against fatal lung disease in mice[J].J Immunol,2014,192(3):985-995.
[11]Tse K,Tse H,Sidney J,etal.T cells in atherosclerosis[J].Int Immunol,2013,25(11):615-622.
[12]Watford WT,Hissong BD,Durant LR,etal.Tpl2 kinase regulates T cell interferon-gamma production and host resistance to Toxoplasma gondii[J].J Exp Med,2008,205(12):2803-2812.
[13]Zheng W,Flavell RA.The transcription factor GATA-3 is necessary and sufficient for Th2 cytokine gene expression in CD4 T cells[J].Cell,1997,89(4):587-596.
[14]Rengarajan J,Mowen KA,Mcbride KD,etal.Interferon regulatory factor 4 (IRF4) interacts with NFATc2 to modulate interleukin 4 gene expression[J].J Exp Med,2002,195(8):1003-1012.
[15]Kashiwada M,Cassel SL,Colgan JD,etal.NFIL3/E4BP4 controls type 2 T helper cell cytokine expression[J].EMBO J,2011,30(10):2071-2082.
[16]Veldhoen M,Hirota K,Westendorf AM,etal.The aryl hydrocarbon receptor links TH17-cell-mediated autoimmunity to environmental toxins[J].Nature,2008,453(7191):106-109.
[17]Koenig W,Karakas M,Zierer A,etal.Oxidized LDL and the risk of coronary heart disease:results from the MONICA/KORA Augsburg Study[J].Clin Chem,2011,57(8):1196-1200.
[收稿2015-06-13]
(编辑许四平)
[关键词]冠心病;转录因子BACH2;Toll样受体4;炎症因子
Expression of transcription factor BACH2 and its significance on PBMC in patients with coronary artery disease
SHANSheng-Shuai,WANGBo-Yuan,KaiShan,LINJi-Bin,LINJing,LIDa-Zhu.DepartmentofCardiology,UnionHospital,TongjiMedicalCollege,HuazhongUniversityofScienceandTechnology,Wuhan430022,China
[Abstract]Objective:To investigate the expression of transcription factor BACH2 on PBMC in patients with coronary artery disease(CAD) and discuss its significance and role.Methods: The circulating levels of BACH2 and TLR4 in PBMC were evaluated by RT-PCR and Western blot separately.Serum levels of signature cytokines of T-helper cells,cytokines and ox-LDL were evaluated by ELISA.The data among groups were analyzed by one-way ANOVA.Correlation between variables were subjected to linear regression analysis.Results: The expression level of BACH2 down-regulated and TLR4 up-regulated significantly in PBMCs of ACS patients had significantly higher concentrations of serum ox-LDL,cytokines of TH1 cells,TH2 cells and TH17 cells and low level of cytokine of Treg cells.Negative correlation exists significantly between BACH2 and TLR4 in patients with CAD and between BACH2 and IFN-γ,IL-4 and IL-17,and between BACH2 and ox-LDL in serum.However,positive correlation exists significantly between BACH2 and TGF-β1.Conclusion: Increased serum concentrations of ox-LDL probably down-regulated the expression of BACH2 in ACS patients by activating TLR4 on PBMC,resulting in promoting production of pro-inflammatory cytokines and suppressing production of anti-inflammatory cytokine and then might cause ACS.
[Key words]Coronary artery disease;Transcription factor BACH2;TLR4;Inflammatory cytokines
通讯作者及指导教师:李大主(1963年-),男,教授,博士生导师,主要从事动脉粥样硬化发病机制的研究,E-mail:lidazhuhp@sohu.com。
作者简介:单圣帅(1985年-),男,在读博士,主要从事动脉粥样硬化发病机制的研究,E-mail:shanshengshuai@163.com。
中图分类号R392.12
①本文为国家自然科学基金资助项目(No.81370406)。
②陕西省人民医院心内科,西安710068。
文献标志码A
文章编号1000-484X(2016)01-0069-06
doi:10.3969/j.issn.1000-484X.2016.01.015
