吡格列酮治疗脂肪肝伴2型糖尿病的代谢指标变化及肝功能观察
2016-02-23刘雪梅王巧云
李 伟 刘雪梅 王巧云
吡格列酮治疗脂肪肝伴2型糖尿病的代谢指标变化及肝功能观察
李 伟1刘雪梅2王巧云2
目的观察吡格列酮治疗脂肪肝伴2型糖尿病对患者代谢指标及肝功能的影响。方法选择我院2013年5月至2016年2月收治的非酒精性脂肪肝伴2型糖尿病患者85例作为研究对象,随机分为观察组(n=44)与对照组(n= 41)。两组均在二甲双胍治疗基础上,观察组联合盐酸吡格列酮片治疗,对照组联合格列美脲片治疗,均为16周。比较两组治疗前后血糖控制指标(FPG、2 h PG)、代谢指标(LDL、TG、HOMA-IR)、肝功能指标(AST、ALT)、Leptin、肝脏脂肪含量及不良反应发生率。结果治疗前,两组各项指标差异无统计学意义(P>0.05);治疗后,两组AST、ALT无明显变化(P>0.05);FPG、2 h PG、LDL、TG、HOMA-IR、Leptin、肝脏脂肪含量均较治疗前降低(P<0.05)。观察组治疗后均显著低于对照组(P<0.05)。治疗期间观察组、对照组不良反应发生率分别为13.6%、7.3%,差异无统计学意义(P>0.05)。结论吡格列酮在脂肪肝伴2型糖尿病患者中的应用可强化对胰岛素抵抗的改善,更大幅度降低FPG、2 h PG,并改善LDL、TG等代谢指标、抑制Leptin表达,缓解脂肪肝病情,安全性高,值得借鉴。
脂肪肝;2型糖尿病;吡格列酮;肝功能;代谢
非酒精性脂肪肝(nonalcoholic fatty liver disease, NAFLD)为多种因素共同作用的结果,主要包括遗传、代谢、环境等因素。有研究[1]发现NAFLD与代谢、糖尿病有较大联系,NAFLD合并2型糖尿病的几率较升高。有研究指出[2],NAFLD合并2型糖尿病为冠心病发病的重要危险因素之一。噻唑烷二酮类药物可调节机体糖脂代谢,目前已经在NAFLD合并2型糖尿病患者的治疗中应用。本研究经我院医学伦理委员会批准,以我院收治的85例非酒精性脂肪肝伴2型糖尿病患者为例,观察吡格列酮治疗脂肪肝伴2型糖尿病对患者代谢指标及肝功能的影响,现报道如下。
资料与方法
一、一般资料
1.纳入标准
①符合1999年WHO所制定的2型糖尿病诊断标准[3];②符合《非酒精性脂肪性肝病诊疗指南(2010年修订版)》[4]中相关诊断标准;③患者对研究知情,且自愿知情签署知情同意书。
2.排除标准
①合并各种肝硬化、药物性肝病、病毒性肝炎者;②合并严重心、肺、肾、脑等脏器障碍者;③合并血液系统疾病者;④合并胆道梗阻或自身免疫性疾病者;⑤合并各种急慢性感染性疾病者;⑥合并Graves病、结缔组织病及肿瘤者。
3.分组资料
选择我院2013年5月至2016年2月收治的非酒精性脂肪肝伴2型糖尿病患者85例作为研究对象,随机分为观察组(n=44)与对照组(n=41)。观察组男20例、女24例;年龄39~58岁,平均(45.0±6.7)岁;体重指数(BMI)23.3~26.7 kg/m2,平均(25.6±0.8)kg/m2;空腹血糖水平(FPG)7.3~9.6 mmol/L,平均(8.3±0.7)mmol/L;餐后2 h血糖含量(2 h PG)11.3~12.8 mmol/L,平均(12.0±0.5)mmol/L;低密度脂蛋白(LDL)3.0~4.3 mmol/L,平均(3.8±0.5)mmol/L。对照组男18例、女23例;年龄37~56岁,平均(45.3±6.9)岁;BMI 23.5~26.9 kg/m2,平均(25.8±0.7)kg/m2;FPG 7.2~9.8 mmol/L,平均(8.4±0.8)mmol/L;2 h PG 11.4~13.0 mmol/L,平均(12.2±0.6)mmol/L;LDL 2.9~4.5 mmol/L,平均(3.7± 0.6)mmol/L。两组性别、年龄、BMI、FPG、2 h PG、LDL等基线资料的差异无统计学意义(P>0.05),具有可比性。
二、方法
两组治疗期间均予以脂肪肝常规干预:控制饮食、加强运动、控制血脂及积极治疗原发病,若肝功异常的脂肪性肝炎则行护肝治疗,应用二甲双胍(中美上海施贵宝制药有限公司生产,批准文号:国药准字H20023370,规格:0.5 g*10片*2板)降糖治疗,口服,第1周500 mg/次、1次/d,第2~6周500 mg/次、2次/d,6周后结合患者血糖实际控制情况调整用药剂量,但不可超过1.5 g/d。在此基础上观察组应用盐酸吡格列酮片(江苏恒瑞医药股份有限公司生产,批准文号:国药准字H20040631,规格:15 mg*7s)治疗,晨服,15 mg/次;对照组应用格列美脲片(江苏万邦生化医药股份有限公司生产,批准文号:国药准字H20010575,规格:2 mg*12s)治疗,晨服,1 mg/次。两组治疗时间均为16周。
三、观察指标
1.血糖控制指标
治疗前后检测两组患者FPG及2 h PG,应用葡萄糖氧化酶法测定。
2.代谢指标
治疗前后检测两组患者以下代谢指标:LDL、甘油三酯(TG)及胰岛素抵抗指数(HOMA-IR)。LDL与TG应用全自动生化分析仪测定,HOMA-IR=FBG×Fins/22.5;其中Fins采用放射免疫法测定。
3.肝功能指标
治疗前后检测两组患者以下肝功能指标:谷草转氨酶(AST)、谷丙转氨酶(ALT)。应用全自动生化分析仪测定。
4.脂肪肝疗效指标
治疗前后检测两组患者血浆瘦素(Leptin)、肝脏脂肪含量。其中Leptin采用放射免疫法测定。肝脏脂肪含量采用计算机断层摄影(仪器Marconi Mx8000型)检测,具体采用校正CT测试管法。首先模仿人体肝脏脂肪浓度配制溶液,得到相应CT值。于治疗前后对两组患者行断层扫描,分别取肝顶、肝右叶下缘、肝门头侧、肝门尾侧4个平面,以4项平均值作为最终CT值数据。根据所得肝脏脂肪含量与CT值的关系图(肝脏脂肪含量越高CT值越低)获得患者脂肪含量数据。
5.不良反应
记录两组治疗期间的不良反应发生情况。
四、统计学方法
采用统计学软件SPSS 19.0对研究数据进行处理,计量资料以表示,采用t检验;计数资料以%表示,采用χ2检验,P<0.05为差异有统计学意义。
结果
一、血糖控制指标
治疗前,两组FPG、2 h PG比较,差异无统计学意义(P>0.05)。治疗后,两组FPG、2 h PG均显著降低,差异具有统计学意义(P<0.05);观察组的FPG、2hPG均低于对照组,差异有统计学意义(P<0.05)。见表1。
二、肝功能指标
治疗前,两组AST、ALT比较,差异无统计学意义(P>0.05);治疗后两组AST、ALT均无明显变化(P>0.05);见表2。
三、脂肪肝疗效指标
治疗前,两组的Leptin、肝脏脂肪含量比较,差异无统计学意义(P>0.05);治疗后,两组Leptin、肝脏脂肪含量均减小(P<0.05),观察组的Leptin、肝脏脂肪含量均小于对照组(治疗前<0.05);见表3。
表1 两组治疗前后血糖控制指标的比较(,mmol/L)
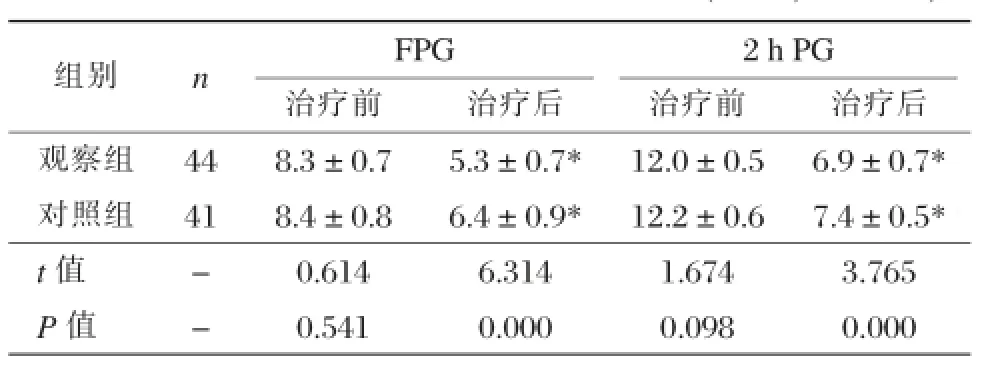
表1 两组治疗前后血糖控制指标的比较(,mmol/L)
注:*与本组治疗前比较,P<0.05。
组别n F P G 2 h P G治疗前治疗后治疗前治疗后观察组4 4 8 . 3 ± 0 . 7 5 . 3 ± 0 . 7 * 1 2 . 0 ± 0 . 5 6 . 9 ± 0 . 7 *对照组4 1 8 . 4 ± 0 . 8 6 . 4 ± 0 . 9 * 1 2 . 2 ± 0 . 6 7 . 4 ± 0 . 5 * t值-0 . 6 1 4 6 . 3 1 4 1 . 6 7 4 3 . 7 6 5 P值-0 . 5 4 1 0 . 0 0 0 0 . 0 9 8 0 . 0 0 0
表2 两组治疗前后肝功能指标的比较(,U/L)
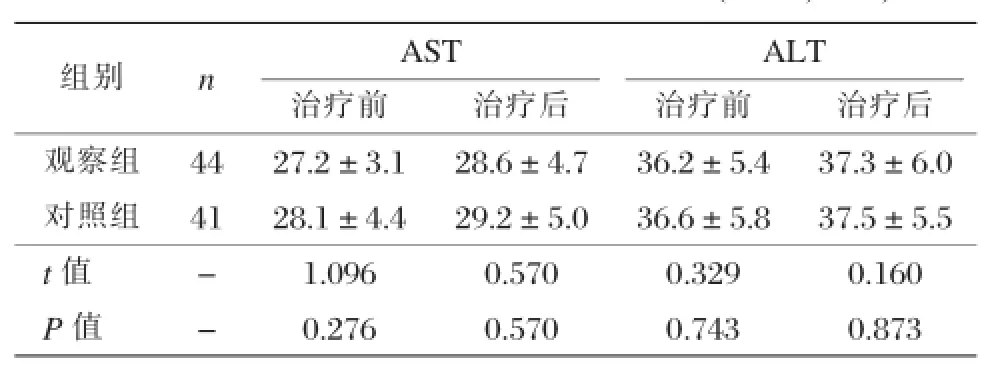
表2 两组治疗前后肝功能指标的比较(,U/L)
治疗前治疗后治疗前治疗后观察组4 4 2 7 . 2 ± 3 . 1 2 8 . 6 ± 4 . 7 3 6 . 2 ± 5 . 4 3 7 . 3 ± 6 . 0对照组4 1 2 8 . 1 ± 4 . 4 2 9 . 2 ± 5 . 0 3 6 . 6 ± 5 . 8 3 7 . 5 ± 5 . 5 t值-1 . 0 9 6 0 . 5 7 0 0 . 3 2 9 0 . 1 6 0 P值-0 . 2 7 6 0 . 5 7 0 0 . 7 4 3 0 . 8 7 3 A S T A L T组别n
表3 两组治疗前后脂肪肝疗效指标的比较()
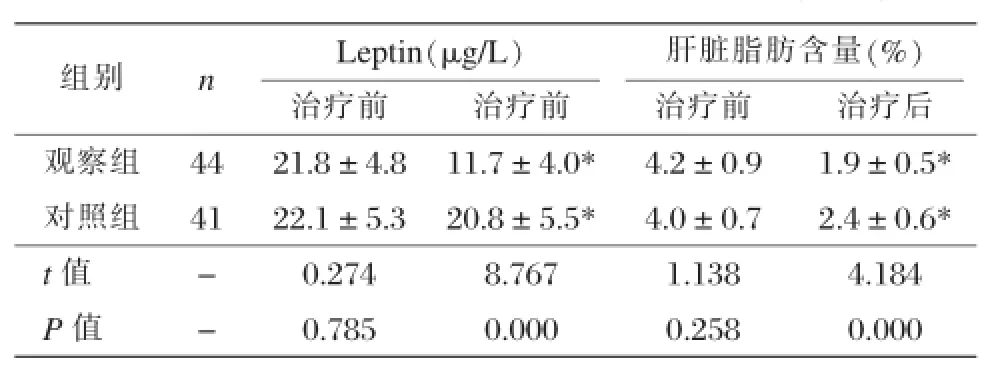
表3 两组治疗前后脂肪肝疗效指标的比较()
注:*与本组治疗前比较,P<0.05。
治疗前治疗前治疗前治疗后观察组4 4 2 1 . 8 ± 4 . 8 1 1 . 7 ± 4 . 0 * 4 . 2 ± 0 . 9 1 . 9 ± 0 . 5 *对照组4 1 2 2 . 1 ± 5 . 3 2 0 . 8 ± 5 . 5 * 4 . 0 ± 0 . 7 2 . 4 ± 0 . 6 * t值-0 . 2 7 4 8 . 7 6 7 1 . 1 3 8 4 . 1 8 4 P值-0 . 7 8 5 0 . 0 0 0 0 . 2 5 8 0 . 0 0 0 L e p t i n(μ g / L)肝脏脂肪含量(%)组别n
四、脂代谢指标
治疗前,两组LDL、TG、HOMA-IR比较,差异无统计学意义(P>0.05);治疗后,两组LDL、TG、HOMA-IR均显著降低(P<0.05),观察组LDL、TG、HOMA-IR显著低于对照组(P<0.05)。见表4。
五、不良反应发生情况
治疗期间观察组出现4例上呼吸道感染、1例头痛、1例轻度低血糖,不良反应发生率为13.6%(6/44);对照组出现1例低血糖、1例恶心呕吐、1例头痛,不良反应发生率为7.3%(3/41),差异无统计学意义(χ2=0.895,P=0.344)。
讨论
脂肪肝发病机制非常复杂,目前尚无统一说法,一般认为机体在能量供应充分前提下会将剩余能量储存于脂肪组织中。由于脂肪组织储脂能力有限,当超过其限度就会引起脂肪细胞功能失常,引起葡萄糖耐量异常。此时机体脂肪分解速度大于合成速度,释放大量脂肪酸,经血液循环送至肝脏、肌肉等非脂肪组织,造成肝脏脂肪的过量堆积而形成脂肪肝[5-6]。脂肪细胞功能失常后机体糖脂代谢异常,因而脂肪肝患者易合并2型糖尿病。
表4 两组治疗前后脂代谢指标的比较()
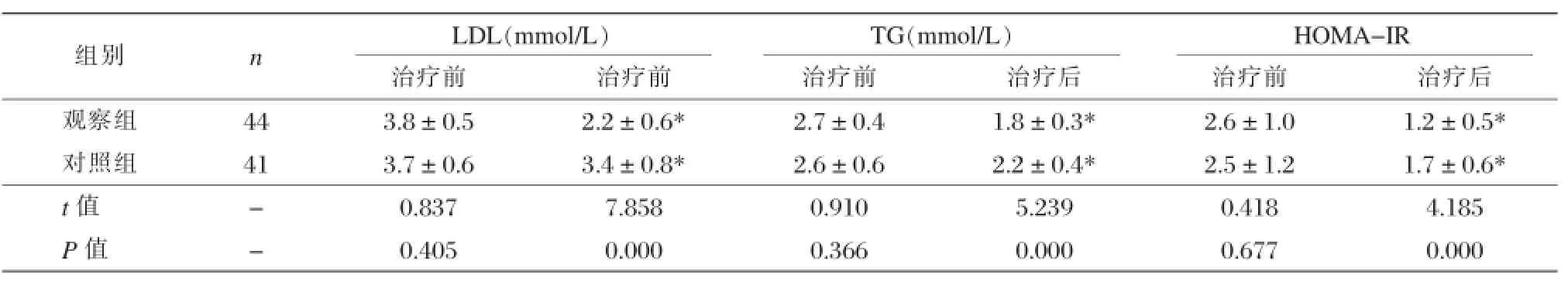
表4 两组治疗前后脂代谢指标的比较()
注:*与本组治疗前比较,P<0.05。
组别n L D L(m m o l / L)T G(m m o l / L)H O M A -I R治疗前治疗前治疗前治疗后治疗前治疗后观察组4 4 3 . 8 ± 0 . 5 2 . 2 ± 0 . 6 * 2 . 7 ± 0 . 4 1 . 8 ± 0 . 3 * 2 . 6 ± 1 . 0 1 . 2 ± 0 . 5 *对照组4 1 3 . 7 ± 0 . 6 3 . 4 ± 0 . 8 * 2 . 6 ± 0 . 6 2 . 2 ± 0 . 4 * 2 . 5 ± 1 . 2 1 . 7 ± 0 . 6 * t值-0 . 8 3 7 7 . 8 5 8 0 . 9 1 0 5 . 2 3 9 0 . 4 1 8 4 . 1 8 5 P值-0 . 4 0 5 0 . 0 0 0 0 . 3 6 6 0 . 0 0 0 0 . 6 7 7 0 . 0 0 0
二甲双胍为双胍类代表性药物,可提高糖尿病患者的血糖耐受性,降低基础及餐后血糖水平。同时抑制肝糖产生及肠对糖分的吸收,强化外周糖的摄取与利用。本研究两组患者均应用二甲双胍,结果显示两组FPG、2 h PG均大幅降低,表明二甲双胍能明显降血糖,治疗2型糖尿病效果显著。在此基础上,观察组与对照组分别应用盐酸吡格列酮片及格列美脲片,结果显示治疗后观察组LDL、TG、HOMA-IR等代谢指标与Leptin、肝脏脂肪含量等脂肪肝指标下降幅度与对照相相比均更大,提示盐酸吡格列酮片的应用在改善脂代谢、胰岛素抵抗方面疗效更佳,更利于脂肪肝病情的缓解。有研究提出[7-8],肥胖与胰岛素抵抗之间有密切关系,脂肪肝患者之所以出现糖脂代谢异常,与产生胰岛素抵抗致组织的胰岛素敏感性降低有关。盐酸吡格列酮片组经治疗后HOMAIR下降幅度大于格列美脲片组。患者胰岛素抵抗得到明显缓解,机体对胰岛素敏感性随之提高。二甲双胍也有改善胰岛素抵抗的作用,因而二药联合可强化药物对胰岛素的抵抗作用,最终促进血糖水平的降低,这也是观察组FPG、2 h PG降至更低的重要机制。
吡格列酮为噻唑烷二酮类降糖药,其特点是改善胰岛素抵抗[9],作用机制复杂。随着盐酸吡格列酮片的应用,发挥PPAR-γ激动剂作用,激活肝细胞、脂肪中的过氧化物酶体增殖物激活受体γ(PPAR-γ),对胰岛素应答相关基因的转录进行调节,促进机体外周组织及肝脏对胰岛素敏感性的提高[1 0]。此外,吡格列酮可促进脂肪细胞分化,改善脂代谢。而激活PPAR-γ之后,调节脂肪细胞的分化与分布,抑制Leptin分泌,降低Leptin水平,能使高瘦素血症得到明显改善,减轻NAFLD病变程度。Leptin为人体脂肪组织所分泌的多肽类激素,主要负责调解人体能量平衡,过量Leptin会可使高胰岛素血症及炎症反应加剧,且其与NAFLD的发生、发展关系密切,因而本研究应用Leptin评价患者脂肪肝治疗效果。有国外研究[11]发现,血浆Leptin与TG有较大关联,NAFLD患者血浆Leptin、TG水平大幅增高。肝组织中Leptin受体功能减弱,致Leptin生理效应下降,即存在瘦素抵抗,引起肝脏脂类输出减少,诱发脂代谢紊乱,脂肪在肝脏大量蓄积。脂肪细胞可以看成是内分泌器官,产生TNF-α等炎性因子,肝脏脂肪含量的增加会加重炎症反应而增大心血管疾病风险。本组结果显示,经盐酸吡格列酮片治疗后患者Leptin水平由(21.8±4.8)μg/L降低至(11.7±4.0)μg/L,肝脏脂肪含量由(4.2±0.9)%减小至(1.9±0.5)%,改善幅度均优于格列美脲片治疗组,提示患者脂代谢异常及脂肪肝堆积情况得到更佳缓解。
大量临床研究均显示[12-13],吡格列酮具有肝功能改善作用,可有效降低脂肪肝患者的ALT及AST。尚涛等[14]的研究也表明,吡格列酮也改善糖尿病脂肪肝患者的肝损伤。本研究中两组患者入组时均未出现明显肝损伤,治疗后两组AST及ALT等肝功能指标也无明显变化,因而未能凸显其对脂肪肝伴2型糖尿病患者肝功能的影响,为研究不足之处。另外,两组的不良反应发生率分别为13.6%、7.3%,无显著差异,且症状均较轻,未影响治疗,提示两种药物均有较高安全性。
综上所述,吡格列酮联合二甲双胍治疗脂肪肝伴2型糖尿病可强化对胰岛素抵抗的改善,更大幅度降低患者FPG、2 h PG,改善LDL、TG并抑制Leptin表达,对脂肪肝病情的缓解有益,且安全性高,值得借鉴。
[1]白雪梅,梁萍,张晶.伴有高血压的非酒精性脂肪肝患者的糖耐量特点分析[J].实用医学杂志,2016,32(6):914-915.
[2]刘春花,左涛,王静凤,等.乳清酸诱导的大鼠非酒精性脂肪肝与糖耐量异常和高血压关系的研究[J].营养学报,2013,35(1):23-26.
[3]中华医学会糖尿病学分会.中国2型糖尿病防治指南(2013年版)[J].中华糖尿病杂志,2014,6(7):447-498.
[4]中华医学会肝病学分会脂肪肝和酒精性肝病学组.NAFLD诊疗指南[J].胃肠病学,2010,6(19):483-487.
[5]杨文,于晓红,王玉柱,等.糖尿病和糖代谢异常/糖耐量异常与非酒精性脂肪肝的相关研究[J].胃肠病学和肝病学杂志,2014, 23(4):438-440.
[6]牛明佳,铉绪敏,陈兰兰,等.2型糖尿病合并非酒精性脂肪性肝病相关因素的研究[J].医学临床研究,2013,30(6):1146-1148.
[7]张凤平.非酒精性脂肪肝与胰岛素抵抗和糖耐量异常的关系[J].山东医药,2011,51(9):78-79.
[8]刘晓琳,明雅南,张静怡,等.非酒精性脂肪性肝病不同表型的代谢组学研究[J].肝脏,2015,20(2):95-100.
[9]呙劲松,陈艳.吡格列酮对糖耐量异常合并非酒精性脂肪肝患者血浆瘦素水平及胰岛素抵抗的影响[J].中南医学科学杂志, 2014,42(4):379-381.
[10]姚远涛,沙卫红,王启仪,等.血清超敏C反应蛋白评估非酒精性脂肪肝临床风险的前瞻性研究[J].现代消化及介入诊疗,2011, 16(2):82-86.
[11]Anton I,Kovacs K,Hollo G,et al.Effect of DGAT1,leptin and TG gene polymorphisms on some milk production traits in different dairy cattle breeds in Hungary[J].Archiv Fur Tierzucht,2012,55 (4):307-314.
[12]刘亚军,侯健红.吡格列酮对2型糖尿病或糖耐量减低患者内脏脂肪代谢活性影响的观察[J].中国糖尿病杂志,2015,23(2):127-130.
[13]黎叶飞,盛臻强,王毅,等.吡格列酮对代谢综合征糖耐量异常患者血管内皮功能的影响[J].南通大学学报(医学版),2012,32(6): 446-448.
[14]尚涛,杜玉茗,姚庆春,等.吡格列酮联合丹参对糖尿病脂肪肝患者糖、脂代谢及肝损伤的影响[J].吉林中医药,2013,33(4):374-375.
2016-06-28)
(本文编辑:白岚)
10.3969/j.issn.1672-2159.2016.06.014
716000延安大学附属医院1内分泌科;2超声诊断科
