染色体核型联合芯片技术在反复缺陷儿妊娠史夫妇再生育咨询中的应用体会
2016-02-13郭彩琴王峻峰唐叶刘俊肖建平
郭彩琴 王峻峰 唐叶 刘俊 肖建平
(南京医科大学附属无锡妇幼保健院 产前诊断中心,江苏 无锡 214000)
染色体核型联合芯片技术在反复缺陷儿妊娠史夫妇再生育咨询中的应用体会
郭彩琴 王峻峰 唐叶 刘俊 肖建平*
(南京医科大学附属无锡妇幼保健院 产前诊断中心,江苏 无锡 214000)
目的 联合应用染色体核型分析及芯片检测,对一例反复缺陷儿妊娠史有再生育需求夫妇进行产前诊断与遗传咨询,为有效预防出生缺陷提供诊疗思路。方法 夫妇双方及本次妊娠胎儿进行G显带染色体核型分析,采用微阵列比较基因组杂交(array-based comparative genomic hybridization, array-CGH)技术排除致病性染色体微缺失微重复。结果 丈夫核型为46,XY,t(5;6)(p13;p25),孕妇核型正常,胎儿染色体核型46,XN,结合第二胎猫叫综合征(Cri-du-Chat syndrome,CDCS)引产史,考虑为父源性CDCS;array-CGH检测未发现致病性拷贝数变异(Copy number variation, CNV);孕妇继续妊娠并顺产健康男婴,随访至今无异常。结论 细胞与分子遗传学方法相结合合理应用,可为反复缺陷儿妊娠史夫妇查找病因,减少再发风险,改善妊娠结局,达到优生优育的目的。
核型分析;微阵列比较基因组杂交;产前诊断;遗传咨询
先进的分子诊断技术为产前诊断提供了有效的检测手段,但针对不同患者特点制定有效的产前诊断策略仍是亟待解决的难题。本研究应用染色体核型分析联合微阵列比较基因组杂交(array-based comparative genomic hybridization, array-CGH),为一对两次缺陷儿妊娠史夫妇进行再孕后产前诊断与遗传咨询,为有效预防出生缺陷提供了思路。
1 资料与方法
1.1 一般资料 孕妇,29岁,因“停经19+3周,两胎缺陷儿孕产史”要求行产前诊断由外院转入。夫妻二人体格、智力发育无异常;非近亲结婚;孕产史:1-0-1-0。婚后3个月首次受孕,未定期产前检查,2012年1月足月顺产一活男婴,3900g,出生后40天因先天性心脏病(右心室发育不良?)夭折,未行尸体解剖。2012年12月再次妊娠,外院定期产检并于停经20周行产前诊断提示“猫叫综合征(CDCS)”后引产。本次2014年1月意外受孕,未孕前准备。1.2 检测方法
1.2.1 染色体核型分析 经孕妇知情同意后抽取第2、3胎胎儿羊水、脐带血及夫妻双方外周血,按常规方法进行羊水、淋巴细胞培养及中期染色体制备,G显带分析。
1.2.2 比较基因组杂交芯片 采用Topuer试剂盒(Gene Tech,上海)抽提羊水全基因组DNA,Agilent Human Genome CGH Microarray 44K芯片(Agilent Technologies,美国)进行比较基因组杂交,DNA标记和芯片杂交由北京博奥医学检验所完成。运用Agilent芯片扫描仪获取荧光图像,通过Agilent DNA Analytics软件Z-scoring方法进行数据分析。
2 结果
2.1 染色体核型分析 丈夫核型为46,XY,t(5;6)(p13;p25),为部分5p接到6p的单相平衡易位(图1);孕妇核型正常。第二胎胎儿获得了父亲的1条异常5号与正常的6号,核型为46,XX,del(5)(p15)pat(图2),导致5p部分单体即CDCS。本胎胎儿则获得了父亲正常的5、6 号染色体,核型结果为46,XN(图3)。
2.2 array-CGH分析 因本胎是两次不良孕产史后的珍贵儿,核型结果无异常后,为排除微缺失、微重复,胎儿羊水进行array-CGH检测。基因芯片分析显示5p13、6p25位点(图4、5)未发现CNV,5号染色体的CNV也在染色体良性拷贝数变异数据库(Database of Genomic Variants, DGV)范围内,其他染色体区域未见明显异常。

图1 丈夫染色体核型 箭头示易位染色体
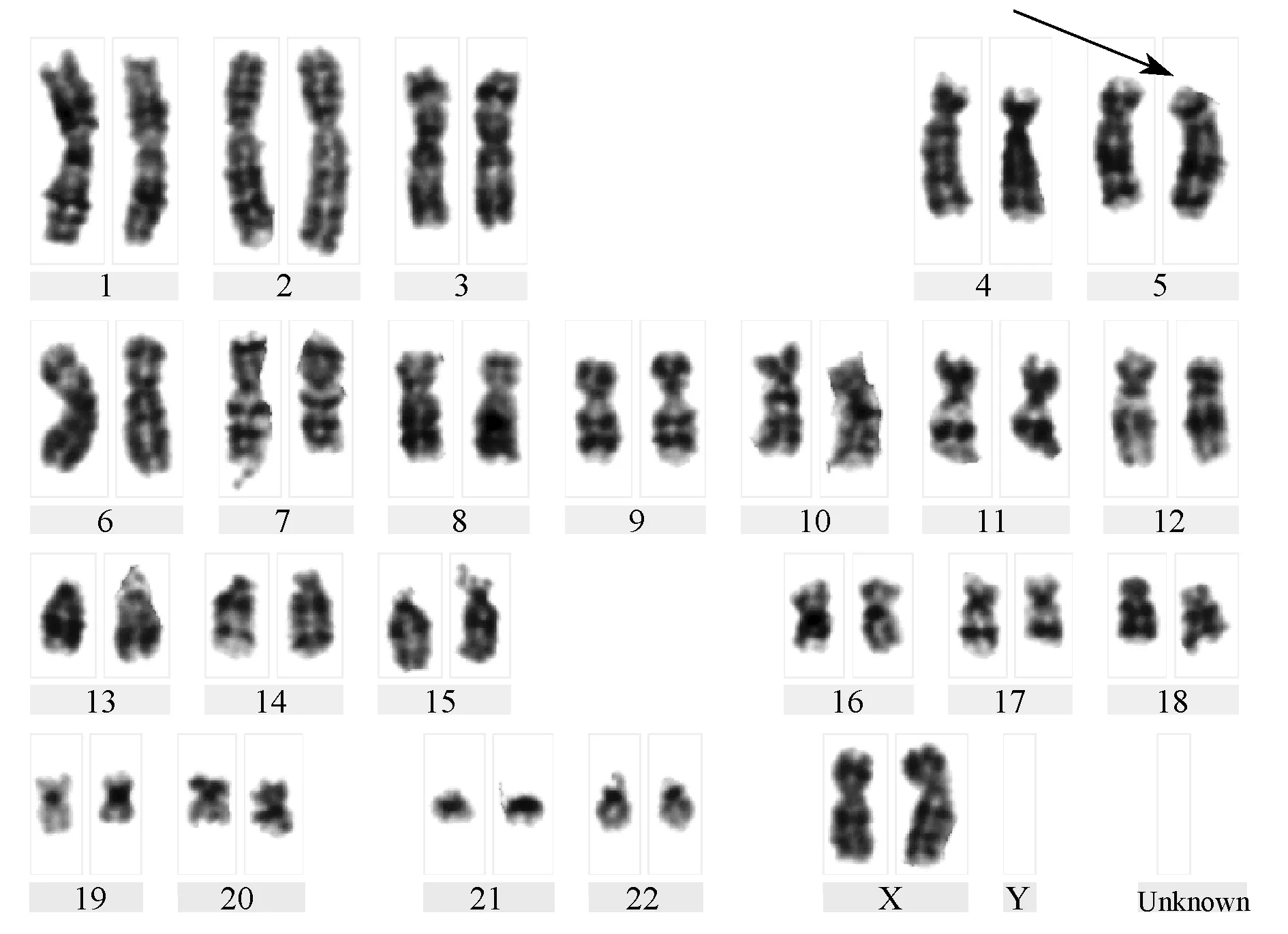
图2 第2胎胎儿染色体核型 箭头示5P-

图3 本胎胎染色体核型

图4 本胎胎儿5号染色体基因芯片图

图5 本胎胎儿6号染色体基因芯片图
图左侧为相应染色体模式图;右侧偏离0基线的片段为染色体异常位置,负值为缺失,正值为重复
2.3 咨询及随访
2.3.1 第一次咨询 (孕19+3周)孕妇就诊时已孕19+3周,考虑本次意外受孕,两次缺陷儿妊娠史,且第二胎“猫叫综合征”引产胎儿为染色体异常(5P-),建议行羊膜腔穿刺同时夫妇双方外周血染色体检查,羊水标本除核型分析外-80℃保存备进一步检测。结果:丈夫核型46,XY t(5;6)(p13;p25),孕妇核型正常,胎儿染色体核型46,XN(320-400条带)。同期超声筛查报告示胎儿三尖瓣少量反流,未见明显心脏结构异常。
2.3.2 第二次咨询 (孕23周)考虑患者有反复缺陷儿妊娠史、第一次妊娠新生儿可疑右心发育不良夭折、本次胎儿三尖瓣少量反流等情况,本次妊娠前无孕前准备,告知常规染色体核型分析的局限性,不排除围孕期不良因素暴露增加子代染色体新发突变位点增加微重复及微缺失风险,建议动态随访胎儿心脏血流及结构的同时行羊水芯片检测,患方同意。芯片检查结果:未发现致病性拷贝数变异(copy number variation, CNV)。
2.3.3 第三次咨询 (孕27周)结合孕妇病史及检查结果,再次超声复查胎儿心脏三尖瓣反流无明显增多,心脏结构未见明显异常,建议继续妊娠,同时告知后续产检注意事项及随访要点。
2.3.4 妊娠结局及随访 孕40+5周自然分娩一男婴,3950g,Apgar评分10-10分,留脐带血高分辨染色体复查核型未见异常,心脏彩超检查未示明显结构异常。现随访满20个月,子代生长发育状况良好。
3 讨论
传统的G显带核型分析费用低廉,分辨率约5Mb,可检测大部分染色体非整倍体与易位、倒位等结构异常而被广泛应用,但报告周期较长且很难检测出5Mb以下的亚显微染色体异常,尤其是微缺失微重复[1]。随着分子遗传学的发展,array-CGH等技术因具有检测周期短、定位准确、高分辨高敏感度等特点,最高分辨率可达100~200kb,能检测染色体的微缺失微重复,在染色体微小结构改变的检测中具有明显优势[2],已被逐步应用到产前诊断中,但仍不能检测出平衡易位、低比例嵌合体、多倍体等畸变且价格相对昂贵尚不能大范围推广。
本研究中,由于第一次缺陷儿可疑虑右心发育不良未作遗传学病因分析遗憾夭折,第二次妊娠虽然羊水染色体核型诊断为猫叫综合征,但未对夫妇双方进行溯源排查。CDCS又称5p-综合征,由5号染色体短臂缺失所致,发病率约1/50 000[3]。患儿临床表型复杂,包括生长发育迟缓、头面部畸形、哭声奇特、智力障碍以及皮纹改变等症状,因多数患儿哭声微弱似猫叫而得名[4]。患者染色体核型有多种,其中约8.75%源于父母的平衡易位[5]。因此本次妊娠产前诊断前首先对夫妇双方染色体核型分析,结果提示,胎儿父亲为5p、6p平衡易位携带者,由此有理由推测,上胎CDCS胎儿获得了父亲短臂部分缺失的一条5号和一条正常的6号染色体,导致5p部分单体的非平衡易位。理论上,本次怀孕胎儿获得正常配子的几率为1/18[6]。在其产前诊断与遗传咨询中,核型分析可排除父源性平衡易位所致的部分单体或三体。幸运的是,本次妊娠胎儿羊水核型分析未见明显异常。由于本次为意外怀孕,孕22周系统筛查提示胎儿三尖瓣反流,结合首次妊娠病史,对羊膜腔穿刺保存的备用羊水行array-CGH检测,可排除不良环境暴露致染色体新发突变位点致病性CNV可能。结果胎儿5、6号染色体易位位点处未发现异常,其他染色体也未发现致病性CNV。超声动态随访三尖瓣反流无进行性加重及其他异常,孕妇继续妊娠并足月分娩,新生儿脐带血行高分辨染色体核型分析复查结果同羊水,跟踪随访男婴生长发育正常从而获得了良好的妊娠结局。因此,针对此类患者,先采用传统的核型分析排查大片段的部分三体或单体及平衡易位,再用array-CGH等分子遗传方法排查新发微缺失微重复,不仅减轻了患者负担而且降低了染色体微小病变致病的风险,是较为经济合理的诊疗方案。
由于亲代染色体异常是复发性胎停、流产及缺陷儿妊娠的重要因素,因此对反复妊娠缺陷儿的孕妇,需先行夫妻双方染色体检查,做好孕前咨询以减少再次妊娠围孕期不良因素暴露可能。缺陷儿妊娠及分娩史是再次妊娠侵入性产前诊断的指征之一。对亲代染色体异常的孕妇,在侵入性操作获得胎儿标本后,应首选行染色体核型分析排除染色体数目及大片段异常。考虑患者反复缺陷儿妊娠史,为避免后续可能需标本作进一步分子诊断,冰冻保存部分羊水标本备用,减少二次取样风险。本研究中,将细胞遗传与分子遗传学检测有效结合,较全面地排查遗传学病因、合理指导胎儿去留,但孕期需同时动态超声监测排除脏器异常,综合考虑予以合理建议指导妊娠。分娩后仍需定期跟踪随访婴幼儿生长发育状况。
综上所述,本研究中,父母染色体核型分析具有重要价值,不仅帮助明确了反复缺陷儿妊娠史的病因,更有利于评估再发风险。对平衡易位家系,遗传咨询中告知夫妻双方受孕后及时产前诊断非常重要。除核型检查外,还留有充足时间进行芯片检测。将细胞与分子遗传学技术合理运用,才能更经济有效排查遗传学致病性可能。对反复缺陷儿妊娠史的夫妇,需孕前咨询减少围孕期不良因素接触,孕前检查排除可能的病因;孕期则需定期产检,综合运用超声及遗传学检查方法动态监测,合理指导妊娠;分娩后仍需随访婴幼儿状况反馈妊娠结局。通过产前诊断与遗传咨询方案的完善,真正为出生缺陷二级干预及优生优育奠定基础。
[1] 杨世伟,王大为,秦玉明. 先天性心脏病分子遗传学研究进展[J].心脏杂志,2011,23:542-545.
[2] 武彬彬,胡朝晖.微阵列比较基因组杂交技术在产前诊断中的应用[J/CD].中华临床医师杂志(电子版),2013,7:2631-2634.[3] Fang J S, Lee K F, Huang C T, et al. Cytogenetic and molecular characterization of a three-generation family with chromosome 5p terminal deletion[J]. Clin Genet, 2008,73:585-590. [4] 罗福薇,罗彩群,谢建生,等.微阵列比较基因组杂交技术分析一例猫综合征患儿的基因组拷贝数变异[J].中华医学遗传学杂志,2013,30:443-446.
[5] Mainardi PC1, Perfumo C, Calì A, et al. Clinical and molecular characterization of 80 patients with 5p deletion: genotype-phenotype correlation[J]. J Med Genet. 2001,38:151-158.[6] 陆国辉,徐湘民. 临床遗传咨询[M]. 北京:北京大学出版社,2007:41-44,50.
编辑:宋文颖
Objective To provide prenatal diagnosis and genetic counseling for a pregnant couple with defective pregnancies by the combination of karyotype and chip testing and then to provide clinical thinking for effectively preventing birth defects. Method G-banding was performed to analyze the karyotypes of the three family members, and then array-based comparative genomic hybridization (array-CGH) was applied to investigate micro deletions and duplications. Results G-banding analysis revealed that the husband was a balanced translocation carrier of 46,XY,t(5;6)(p13;p25)and the pregnant woman was normal. Accordingly, the second fetus induced for Cri-du-Chat syndrome (CDCS) was considered to result from balanced paternal translocation. The current fetus was with normal karyotype of 46,XN and pathogenic copy number variations(CNV)weren’t found by array-CGH. Therefore, the pregnant woman continued pregnancy and gave birth to a healthy baby boy by vaginal delivery. The boy had no abnormalities during follow-up. Conclusions By rational application of cellular and molecular genetic methods, not only the causes could be investigated for the couples with defective pregnancies but also recurrent risk would be reduced, and then pregnancy outcomes would be improved eventually.
karyotype analysis;array-based comparative genomic hybridization;prenatal diagnosis;genetic counselling
10.13470/j.cnki.cjpd.2016.04.009
R714.55
A
2016-6-18)
*通讯作者:肖建平,E-mail:jianpingx999@126.com
