黄曲霉毒素B1半抗原分子设计与抗原合成及抗体特性研究进展
2016-02-09王亚楠王晓斐牛琳琳张海棠王自良
王亚楠,王晓斐,牛琳琳,雷 壮,张海棠,王自良,*
(1.河南科技学院动物科技学院,河南新乡 453003;2.动物病毒病防控与药残分析河南省高校重点学科开放实验室,河南新乡 453003;3.河南科技学院新科学院,河南新乡 453003)
黄曲霉毒素B1半抗原分子设计与抗原合成及抗体特性研究进展
王亚楠1,2,王晓斐3,牛琳琳1,2,雷 壮1,2,张海棠1,2,王自良1,2,*
(1.河南科技学院动物科技学院,河南新乡 453003;2.动物病毒病防控与药残分析河南省高校重点学科开放实验室,河南新乡 453003;3.河南科技学院新科学院,河南新乡 453003)
本文综述了国内外半抗原分子设计方法、基本要求、应遵循原则、抗原合成方法等方面的研究进展,尤其是对黄曲霉毒素B1(AFB1)半抗原分子设计与抗原合成及抗体特性进行了详尽阐述,旨在为AFB1制备AFB1及其他小分子半抗原高质量的抗体提供新的方法和思路。
黄曲霉毒素B1,半抗原分子设计,抗原合成,抗体特性
黄曲霉毒素(aflatoxins,AF)是由黄曲霉(Aspergillusflavu)和寄生曲霉(Aspergillusparasiticus)经过聚酮途径所产生的含有二呋喃环和氧杂萘邻酮结构相似的一组有毒次生代谢产物,主要污染玉米、大米等粮食作物和花生、棉籽、坚果等油料作物及其制品[1]。目前已发现AF有20种,自然条件下产生的AF主要包括B1、B2、G1、G24种[2]。AF对人体健康具有致癌性、致突变性、致畸形性和致免疫抑制性等毒性作用,尤其是AFB1毒性最强,是氰化钾的10倍,砒霜的68倍,被国际癌症研究组织(IARC)确定为I类致癌物[3]。由于AFB1毒性较大,污染广泛,在AF总量中所占比例较高(50%以上),世界上大多数国家对食品中AFB1残留限量标准都做出了明确的规定[4],我国现行的《GB 2761-2011 食品中真菌毒素限量》标准严格规定了AFB1的限量标准[5]。
食品中AFB1分析方法主要有理化分析和免疫分析两种,目前各国主要采用理化分析方法,包括高效薄层色谱法(HPTLC)[6]、高效液相色谱法(HPLC)[7]、液相色谱-串联质谱法(LC/MS-MS)[8]、荧光分光光度法(FS)[9]、微柱筛选法(MCS)[10]、傅立叶变换红外光谱(FTIR)[11]等。但由于受仪器设备、技术人员、样品处理、操作场地、经济成本等方面的制约,理化分析方法的应用受到了限制[12]。免疫分析方法由于具有选择性强、灵敏度高、快速简便、样品筛检量大、可现场操作等优势,已成为AFB1检测研究的热点课题[13]。由于AFB1是小分子化合物,不具有免疫原性,无法直接诱导机体等产生特异性抗体,只有通过半抗原分子结构改造,再与大分子蛋白质载体结合合成抗原,通过T细胞表位诱导激活B细胞,由B细胞成熟为浆细胞分泌产生特异性抗体,而高灵敏度、高特异性抗体的产生依赖于半抗原分子设计和抗原合成[14]。本文对AFB1半抗原分子设计与抗原合成及抗体特性研究进展进行了综述,旨在为食品AFB1污染残留更加灵敏、特异的免疫学检测方法建立提供参考。
1 半抗原分子设计方法、基本要求与遵循原则
半抗原免疫分析(hapten immunoassay,HIA)是以抗原与对应抗体的特异性识别和可逆性结合反应为基本原理的分析方法,迄今已在农药[15]、兽药[16]、生物毒素[17]、重金属离子[18]、特殊化合物[19]等食品污染残留检测方面发挥了重要作用。HIA的研究内容主要包括半抗原分子设计和抗原合成、灵敏性和特异性抗体制备与鉴定、免疫分析方法建立与验证三部分,其中半抗原分子设计和抗原合成是基础,灵敏性和特异性抗体制备是核心,免疫分析方法建立是目的[20]。
1.1 半抗原分子设计方法
半抗原分子设计方法的研究内容包括半抗原分子结构与潜在免疫特性分析、活性位点的选择、活性基团的引入、连接臂的选择等。
半抗原分子结构与潜在免疫特性分析。半抗原潜在免疫特性的高低与半抗原分子结构的复杂性呈正相关,其复杂性是指半抗原分子结构中是否含有苯环及数目、杂环及数目、分支结构及数目,通常结构较复杂的半抗原易于诱导动物产生抗体,而结构过于简单的半抗原较难诱导动物产生抗体[21-22]。Szurdoki等[23]研究表明,半抗原分子结构中具有苯环则制备抗体的成功率为1/3,而不含苯环的成功率仅为1/11。因此,对半抗原分子结构(如分子大小、构型、极性、电子云密度、特征结构等)与潜在免疫特性(如活性位点、活性基团、前体物及代谢物、异构体等)分析非常重要,目前主要通过网络数据库和各种文献进行信息收集与分析,HaptenDB[24]数据库有1087种半抗原、25种载体蛋白及2021种条目供选择,查阅网站为http://www.imtech.res.in/raghava/haptendb/及http://bioinformatics.uams.edu/raghava/haptendb/(Mirror site);http://cdb.ics.uci.edu网站[25]可查阅4.1×106种商品化的化合物及8.2×106种同分异构体;http://bioinformatics.charite.de/superhapten网站[26]可查阅7500种半抗原及其25000种类似物。
活性位点的选择。一般情况下,小分子半抗原中含有多个可供选择的活性位点,正确选择活性位点对合成高质量的小分子半抗原至关重要,直接影响着产生抗体的效价、亲和性和特异性[27]。因为不同的活性位点会导致分子中电子分布的改变,从而使小分子半抗原的电化学性质改变,进而改变其免疫活性,影响产生抗体的效价和亲和性[28];由于不同的活性位点会导致分子的空间结构不同,从而暴露的抗原决定簇也不同,进而影响产生抗体的特异性[29];再者,选择活性位点时,应远离半抗原的特征结构部分,使半抗原的特征分子结构部分充分暴露而得以充分识别,避免破坏特征结构部分或载体蛋白对特征结构部分产生屏蔽作用,所制备的抗体不能识别半抗原。因此,对于具有多个活性位点的小分子半抗原,可尝试利用多个位点分别合成多种人工抗原,然后通过比较筛选出最好的人工抗原用于抗体制备。
活性基团的引入。活性基团的引入主要包括五个路径,一是利用半抗原自身分子结构中含有可供偶联利用的活性功能基团,如氨基(-NH2)、羧基(-COOH)、羟基(-OH)、羰基(-CO-)、巯基(-SH)等,不同的功能基团可选择不同的偶联方法,与载体蛋白偶联制备抗原;二是利用半抗原分子结构上已有的非活性基团,通过改造产生相应的活性功能基团,如硝基(-NO2)还原引入-NH2、醛基(-CHO)肟化引入-COOH等,王自良等[30]在设计苯巴比妥(Phenobarbital,PB)半抗原时,将PB分子上的对位-NO2还原为对位-NH2,之后通过重氮化反应将PB与载体蛋白偶联合成抗原,制备出了高效价、敏感、特异的抗体;三是根据小分子化合物结构上存在的活性位点,通过化学反应引入活性功能基团;四是选择小分子化合物的前体物或代谢物作为半抗原,Liu等[31]在选择呋喃唑酮(Furazolidone)半抗原时,使用其代谢产物3-氨基-2-恶唑烷酮(3-amino-2-oxazolidone,AOZ)作为半抗原;五是重新合成半抗原,Sun等[32]在制备克百威(Carbofuran)抗体时,以呋喃酚为起始原料,经光气酰氯化,再与4-氨基丁酸反应,制备了带有羧基的半抗原。
连接臂的选择。半抗原分子设计时,常在特征结构和载体蛋白之间引入一定长度的连接分子即连接臂,连接臂的选择包括连接臂的长度与结构的确定。关于连接臂长度的确定,Tuomola等[33]和Jung等[34]研究提出,连接臂的最适长度为3~6个碳原子,连接臂太短不利于半抗原的充分暴露,而连接臂太长又会因疏水作用而造成烷基链的折叠,导致半抗原分子被载体蛋白所掩盖,不利于抗原递呈细胞(antigen-presenting cell,APC)对其的识别,但这一结论有待进一步证实[35]。关于连接臂结构的确定,Bruun等[36]和Kolosova等[37]研究认为,连接臂以含末端活性基团的链环烃为宜,不应含有其它高免疫活性的结构如芳环、共轭双键或杂环等,以减少所产生的抗体对连接臂的过度识别而降低对目标分子的识别能力。
1.2 半抗原分子设计应满足的基本要求
不管采用任何路径,在半抗原分子设计时,均应符合以下四点基本要求,一是与待测靶标物在分子结构、空间构象、电子分布和疏水性上应尽可能相似,以便于机体对特征结构进行识别[38];二是半抗原与载体蛋白之间引入的间隔臂应是具有一定长度的碳链,且间隔臂自身不诱导机体产生“桥抗体”[39];三是改造后的半抗原分子末端需有可直接与载体蛋白偶联的活性基团,且活性基团的存在对待测靶标物分子的电子分布没有影响;四是半抗原与载体偶联后仍应保留待测物分子的基本特征结构[40]。
1.3 半抗原分子设计应遵循原则
在进行半抗原分子设计时,应遵循四点原则,一是由于抗原的免疫原性与半抗原分子空间结构的复杂程度呈正相关,应引入不饱和的立体结构,增加结构复杂性,进而增强免疫原性[41];二是引入间隔臂位置应远离半抗原的特征结构,尽量避免对特异性抗原决定簇的干扰,提高抗体的亲和性和特异性[42];三是引入间隔臂长度应适宜,间隔臂太短,则载体的空间位阻影响机体的免疫系统对半抗原特征结构的识别;间隔臂太长,则可能因氢键、疏水作用或其它作用力使半抗原发生折叠而不被机体的免疫系统识别[43]。四是引入反应条件应温和,简单易行,改造产物产率高,且易分离纯化。
2 抗原合成方法
抗原合成方法的研究包括载体的选择、偶联方法的选择、反应条件的选择和偶联率的选择等。
2.1 载体的选择
小分子半抗原与载体偶联合成人工抗原,通过载体效应诱导机体免疫应答,产生针对小分子半抗原的特异性抗体[44]。用于小分子半抗原免疫检测的人工抗原包括免疫抗原和包被抗原两种,在合成人工抗原选择载体时,应考虑两个方面,一是载体的种类,常用的载体有蛋白质和聚合物两类,载体蛋白钥孔血蓝蛋白(keyhole limpet hemocyanin,KLH)、牛血清蛋白(bovine serum albumin,BSA)、卵清蛋白(ovalbumin,OVA)、人血清蛋白(human serum albumin,HSA)、兔血清白蛋白(rabbit serum albumin,RSA)等,其中KLH免疫活性最好,但价格昂贵;BSA性质稳定,价廉易得,免疫活性较好,应用最为普遍。聚合物包括多肽聚合物和大分子聚合物,常见的多肽聚合物有多聚赖氨酸、二软脂酰赖氨酸、多聚谷氨酸和多聚氨基酸等,大分子聚合物有羧甲基纤维素、聚乙烯比咯烷酮等,但在人工抗原合成的实际工作中,载体的选择仍以蛋白质为主,聚合物应用较少[45]。二是免疫抗原和包被抗原应使用不同的载体,且尽可能引入不同的连接臂,以提高抗原抗体反应的灵敏性和特异性。
2.2 偶联方法的选择
根据半抗原的分子结构上具有的活性基团性质或通过活性位点引入的活性基团性质,采用不同的化学反应方法实现与载体蛋白分子的氨基或其他基团的偶联合成抗原[46]。半抗原分子结构上存在或引入的活性基团主要包括氨基(-NH2)、羧基(-COOH)、羟基(-OH)、羰基(-CO-)、巯基(-SH)等,常用的偶联方法见表1。
2.3 偶联条件的选择
偶联过程其实质就是半抗原化合物、偶联剂、载体蛋白在一定条件下的化学反应过程,主要考虑三个方面的反应条件,一是参与反应各物质的初始摩尔浓度;二是反应的溶液体系及pH要求,若半抗原化合物溶于水,偶联反应可在水相中进行;若半抗原化合物难溶或不溶于水,偶联反应应在水、有机溶剂混合的有机相中进行,此时应选择既能使半抗原溶解又保持载体蛋白呈可溶状态,并对载体蛋白的生物活性没有影响的有机溶剂,如吡啶、1,4-二氧六环、丙酮、二甲基甲酰胺;三是偶联反应的温度和时间要求。
2.4 偶联率的选择
偶联率是影响人工抗原免疫效果的重要因素之一,适宜的偶联率有助于提高抗体的亲和力和特异性,但不同半抗原化合物的最佳偶联率目前学界尚未定论。过去一些学者曾经认为偶联率越大越好,但Gefen等[68]和Peterson等[69]的研究结果表明,较大的偶联率并不能得到预期的免疫效果,原因在于载体上覆盖过多的半抗原时,不利于载体与淋巴细胞的结合,减弱载体效应,半抗原与载体蛋白最佳偶联率应为(10~20)∶1。Singh等[70]在制备农药莠去津(atrazine)抗体时研究发现,偶联率为15∶1时抗体的效价和特异性最高,而不是20∶1和40∶1,认为低偶联率的人工抗原引起的免疫反应较慢,但可获得亲和力高、特异性强的抗体。因此,为取得比较理想的免疫效果,应根据不同半抗原的特征结构通过筛选确定最佳偶联率。
3 AFB1半抗原分子设计与抗原合成及抗体特性
AFB1属多环不饱和双呋喃香豆素内酯类化合物,含有一个与基本毒性有关的双呋喃环结构和致癌性有关的氧杂萘邻酮结构(见图1),根据其分子结构上存在的活性基团和活性位点,AFB1半抗原分子设计与抗原合成方法主要有肟化活泼酯法、氨甲基化法、混合酸酐法、环氧化物法、半缩醛法、烯醇醚衍生物法等。人工抗原制备所选用的载体蛋白主要是牛血清白蛋白(BSA)、钥孔戚血蓝蛋白(KLH)两种等。
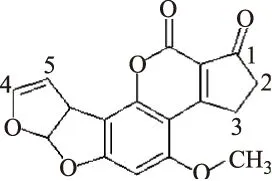
图1 AFB1分子结构式Fig.1 Molecular structure of AFB1
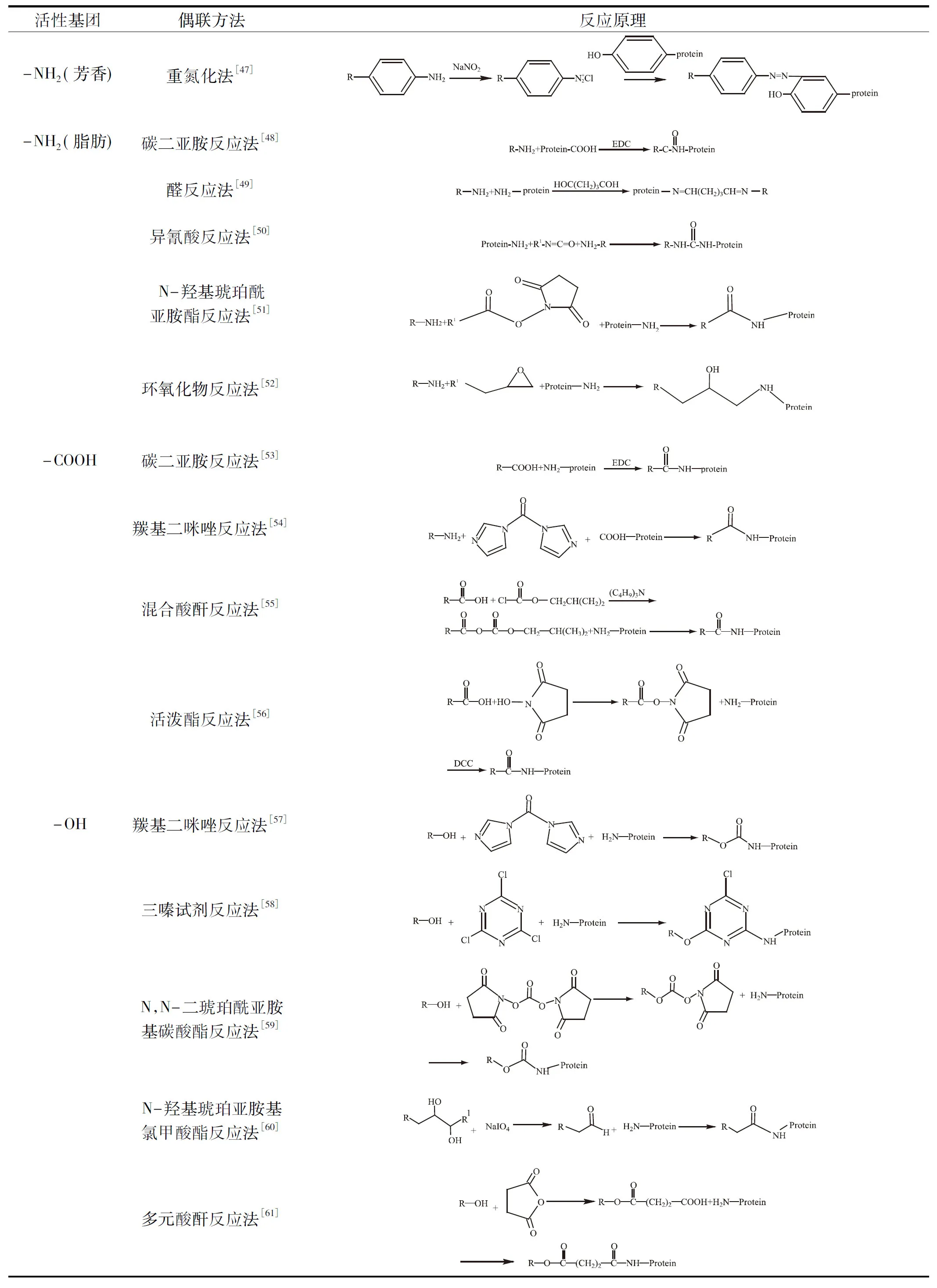
表1 制备小分子半抗原人工抗原常用的偶联方法Table 1 Common coupling methods for preparation of artificial antigen of small molecule antigen
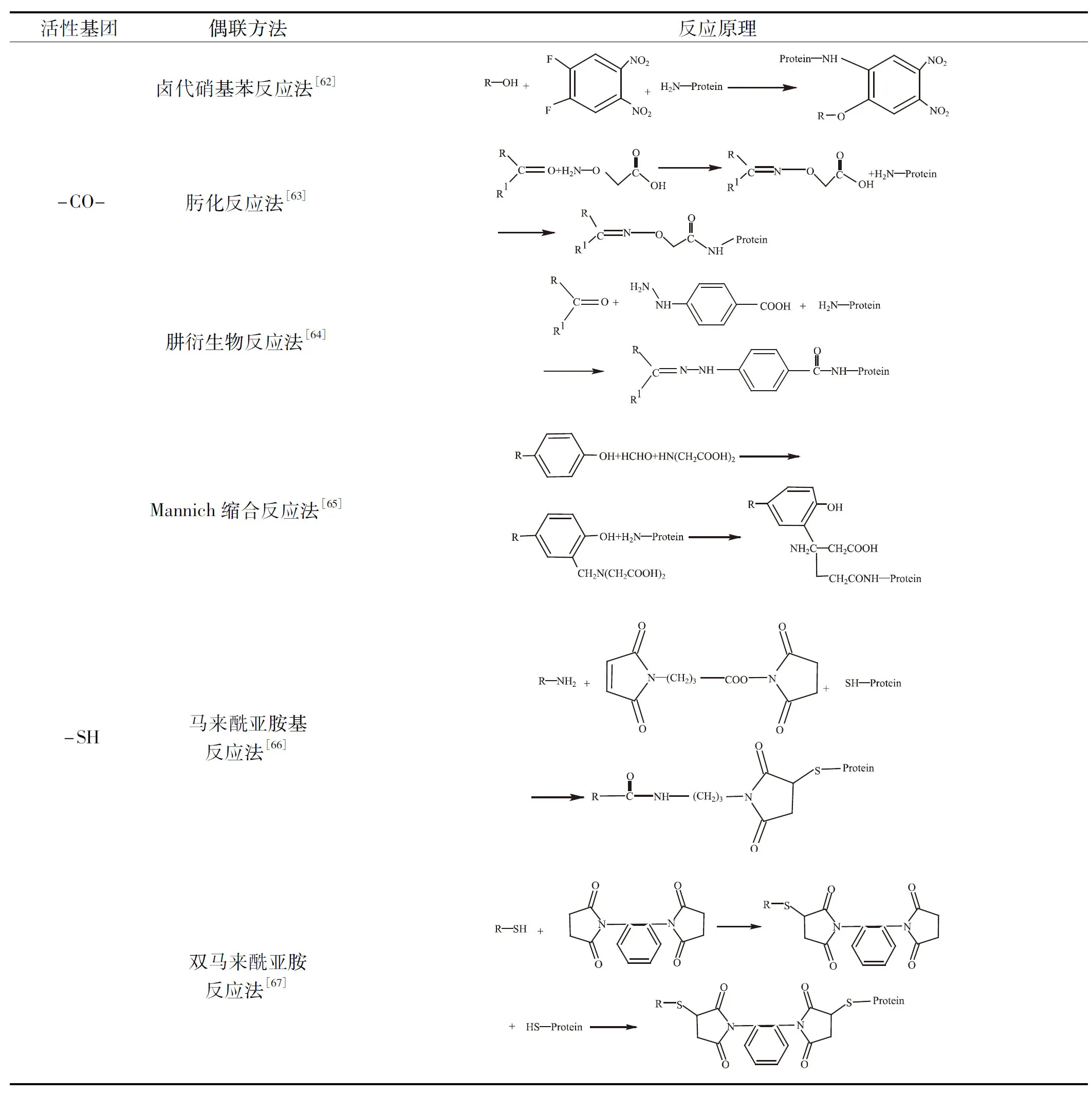
续表
3.1 肟化活泼酯法
AFB1的环戊烯酮环上存在有羰基活性基团(1位),以甲醇水溶液为溶剂,以吡啶为催化剂,以羧甲基羟胺半盐酸盐(CMO)为半抗原肟化剂,在加热回流条件下,AFB1的羰基与CMO的氨基缩合形成N-O-甲基羧酸(-COOH),使AFB1肟化为AFB1O。之后采用活泼酯法合成人工抗原,使用双功能偶联剂1-乙基-3-(3-二甲基氨丙基)碳二亚胺(EDC)在水溶液中或使用是N,N″-二环己基碳二亚胺(DCC)在有机溶液中将AFB1O中的-COOH与载体蛋白的-NH2以单酰胺键(-CONH-)的形式实现偶联,合成路线见图2。该方法Chu等[71]于1977年建立,AFB1O的产率为73%~83%,之后Kolosova等[72]和Cervino等[73]对该方法进行了完善,AFB1O的产率提高到90%以上,获得了抗AFB1高效价、敏感、特异的抗体。孙清等[74]和谢珲等[75]采用该方法分别获得了代表性杂交瘤细胞株2A4和3B9,制备出了高质量的mAb,尤其是2A4株mAb对AFB1的半数抑制浓度(IC50)为0.066 μg/mL,与其他AF无交叉反应。Zhang等[76]对该方法进一步优化,筛选出了灵敏性高、识别谱广的杂交瘤细胞株1C11,所分泌的mAb对AFB1、AFB2、AFG1和AFG2的IC50分别可达1.2、1.3、2.2、18.0 pg/mg。
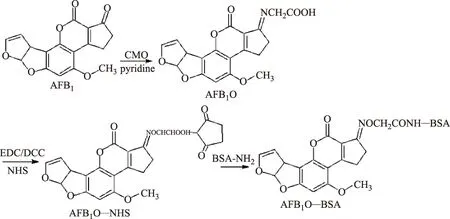
图2 肟化活泼酯法合成AFB1人工抗原路线Fig.2 Synthesis scheme of AFB1-BSA artificial antigen by oximation and active ester method
3.2 氨甲基化法
AFB1的环戊烯酮环上有两个α-活泼氢(2位),在微酸性条件下(pH4.0),以28%乙醇水溶液为反应体系,α-活泼氢、甲醛及载体蛋白氨基酸上的氨基三者可以发生氨甲基化反应,又称曼尼希(Mannich)反应,以Mannich碱的形式实现AFB1与载体蛋白的偶联,合成路线见图3。该方法韦耀鹏等[77]于1992年建立,步骤简单,操作方便,但产物产率不高。Fuentes等[78]和Zhou等[79]进一步完善实验方案,研究结果表明,载体蛋白经阳离子化处理后,可显著提高抗原的免疫活性,在合成人工抗原时,首先用偶联剂EDC将载体蛋白BSA进行阳离子化(cBSA),再利用Mannich反应制备人工抗原AFB1-cBSA。Urusov等[80]的实验结果表明,AFB1-cBSA免疫动物后取得了较好的免疫效果,对AFB1多克隆抗体(pAb)敏感性较高,IC50为1.6 ng/mL,但其特异性需要进一步提高。
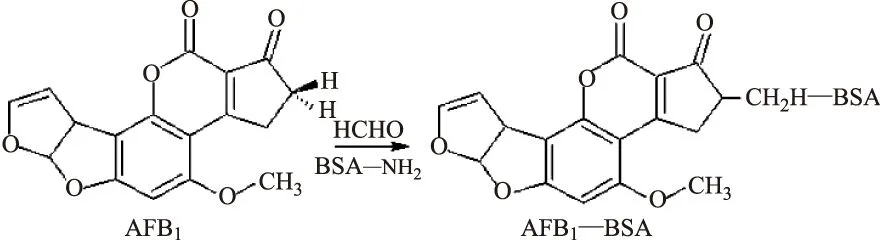
图3 氨甲基化法合成AFB1人工抗原路线Fig.3 Synthesis scheme of AFB1-BSA artificial antigen by aminomethylation method
3.3 混合酸酐法
AFB1经代谢形成AFB2a与AFQ1,在AFB2a的双呋喃环结构上存在一个羟基(-OH)活性基团(2位),在AFQ1的环戊烯酮环结构上同样存在一个-OH活性基团,首先,以四氢呋喃为溶剂,与酸酐反应形成半酯化合物AFB2a-HS,之后,以四氢呋喃为溶剂,在三正丁胺和氯甲酸异丁酯作用下,以单酰胺键的形式实现与载体蛋白的偶联,合成路线见图4、图5。Lau等[81]1981年建立了AFB2a-BSA合成方法,随后该课题组成员Gaur等[82]进行了完善,研究结果表明,AFB2a-BSA为抗原制备的抗体可100%识别AFB1。Fan等[83]1984年首先合成AFQ1-BSA人工抗原,制备出兔源pAb,并建立了间接竞争ELISA检测方法,对AFB1的IC50为2.95 ng/mL,检测限为2 ng/mL,与其他化合物交叉反应均大于1000 ng/mL。

图4 混合酸酐法法合成AFB2a-BSA人工抗原路线Fig.4 Synthesis scheme of AFB2a-BSA artificial antigen by mixed anhydride method
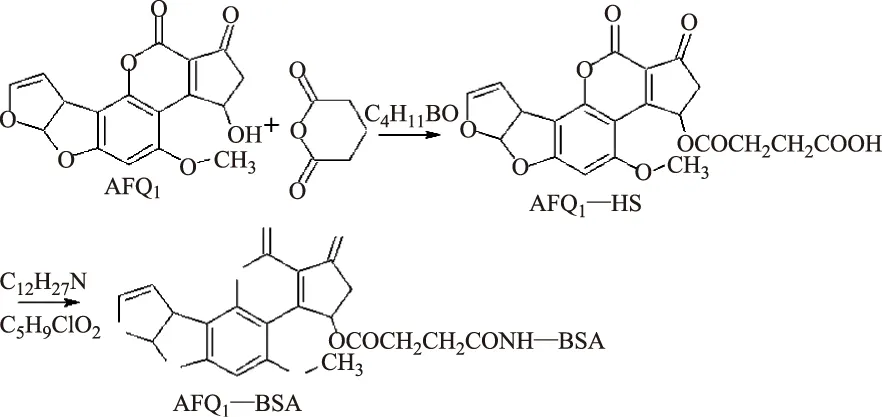
图5 混合酸酐法合成AFQ1-BSA人工抗原路线Fig.5 Synthesis scheme of AFQ1-BSA artificial antigen by mixed anhydride method
3.4 半缩醛法
AFB2a为是AFB1的代谢产物,又是AFB1的半缩醛形式,以丙酮为溶剂,在H2SO4作用下AFB1可转化为AFB2a,AFB2a的醛基(-CHO-)与载体蛋白的氨基(-NH2)生成不稳定的希夫氏碱(schiff-base),在还原剂硼氢化钠(NaBH4)的还原作用下,酰胺键双键(-C=N-)被还原成单键(-C-N-),生成稳定的AFB2a-Protein复合物,合成路线见图6。Ashoor等[84]1975年建立了该方法,Kononenko等[85]运用该方法制备免疫抗原,免疫动物后获得的pAb与AFB1、AFB2的交叉反应率均为100%,与AFG1、AFG2的0.4%。肖智等[86]运用该方法制备了杂交瘤细胞3A12,所分泌的单克隆抗体(mAb)对AFB1、AFB2、AFG1和AFG2的交叉反应率分别为100%、7.8%、22.2%和0.6%,对AFB1的IC50为6.1 ng/mL,检测限为0.6 ng/mL。
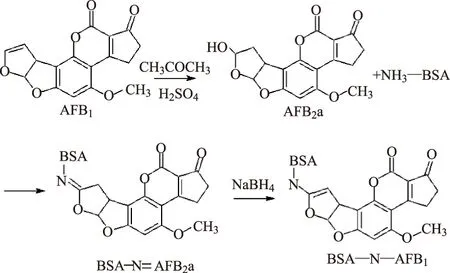
图6 半缩醛法合成AFB1-BSA人工抗原路线Fig.6 Synthesis scheme of AFB1-BSA artificial antigen by hemiacetal method
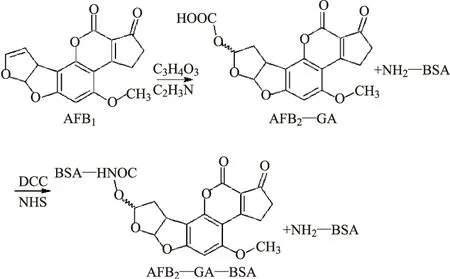
图7 烯醇醚衍生物法合成AFB1-BSA人工抗原路线Fig.7 Synthesis scheme of AFB1-BSA artificial antigen by enol ether derivative method
3.5 烯醇醚衍生物法
AFB1与AFG1的双呋喃环结构上存在活性位点,即双呋喃环中外侧呋喃环氧原子临位位点,利用该位点,通过添加乙醇酸(Glycolic Acid,GA)连接臂,获得了一种新的黄曲霉毒素烯醇醚衍生物AFB1-Glycolic Acid(AFB1-GA)和AFG1-Glycolic Acid(AFG1-GA),利用衍生物的羧基与载体蛋白偶联制备完全抗原,合成路线见图7、图8。Cervino等[87]于2007年建立了该方法,反应简单,操作简便,但对反应试剂纯度及反应条件要求较高,所制备的pAb和mAb与其他AF化合物存在较强的交叉反应,抗体的特异性有待进一步提高。

图8 烯醇醚衍生物法合成AFG1-BSA人工抗原路线Fig.8 Synthesis scheme of AFG1-BSAartificial antigen by enol ether derivative method
3.6 环氧化物法
该方法是以二氯甲烷为溶剂,AFB1双呋喃环双键被过氧化物氧化形成AFB1环氧化物(4位、5位),AFB1环氧化物可与载体蛋白的一级胺发生反应形成二级胺,在反应过程中,环被打开,在环氧化合物上形成一个β-羟基,以单酰胺的形式与载体蛋白偶联,这是AFB1致癌过程中的主要反应[88],也是合成AFB1抗原的途径之一,合成路线见图9。Martin等[89]于1977年报道该方法,Groopman等[90]进行了改进,制备出mAb杂交瘤细胞株2B11,抗体亚类为IgM,能较好识别AFB1、AFB2,所建立得免疫吸附测定柱层析系统对AFB1的检测限达到5 ng/mL。但由于反应需要较高的碱性环境(pH11~12),且AFB1环氧化物活性较高,易于和水及氧化剂形成副产物而影响产率,该方法目前已不常用。

图9 环氧化物法合成AFB1-BSA人工抗原路线Fig.9 Synthesis scheme of AFG1-BSA artificial antigen by epoxide reaction method
4 展望
近年来,国内外学者国对半抗原分子设计及人工抗原合成进行了大量的实践探索,总结了一些规律和方法,但就AFB1半抗原分子设计与抗原合成而言,仍停留在经验设计层面,多采用试错法(trial-and-error assays)进行,最终是通过动物实验来验证半抗原分子设计与抗原合成的合理性,存在较大的盲目性和偶然性。随着免疫学、计算科学、量子化学、分子动力学等学科理论的发展,以及分子模拟技术、计算机辅助技术、网络数据库分析技术等在半抗原分子设计与抗原合成中的应用,以半抗原分子结构复杂程度与潜在免疫特性分析、活性位点的选择、活性基团的引入和连接臂的选择为主要研究内容的半抗原分子设计与抗原合成理论逐渐丰富与完善,可实现半抗原分子设计与抗原合成的可控性、预见性,必将推动我国食品小分子污染物免疫检测方法的快速发展。
[1]Gnonlonfin G J,Hell K,Adjovi Y,et al. A review on aflatoxin contamination and its implications in the developing world:a sub-Saharan African perspect[J]. Critical reviews in food science and nutrition,2013,53(4):349-365.
[2]Bala P,Gupta D,Sharma Y P. Mycoflora and natural aflatoxin contamination in dried quince seeds from Jammu,India[J]. Journal of environmental biology,2016,37(1):101-106.
[3]Ding X,Wu L,Li P,et al. Risk Assessment on Dietary Exposure to Aflatoxin B1in Post-Harvest Peanuts in the Yangtze River Ecological Region[J]. Tcxins,2015,7(10):4157-4174.
[4]Sun D,Gu x,Li j,et al. Quality Evaluation of Five Commercial Enzyme Linked Immunosorbent Assay Kits for Detecting Aflatoxin B1in Feedstuffs[J]. Asian Australasian Journal of Animal Sciences,2015,28(5):691-696.
[5]马海华,孙楫舟,甄彤,等. 我国国家标准和行业标准中黄曲霉毒素测定方法综述[J]. 食品工业科技,2016,37(6):360-366.
[6]Kotinagu K,Mohanamba T,Kumari L R. et al. Assessment of aflatoxin B1in livestock feed and feed ingredients by high-performance thin layer chromatography[J]. Veterinary world,2015,8(12):1396-1399.
[7]Siahi Shadbad M R,Ansarin M,Tahavori A,et al. Determination of aflatoxins in nuts of Tabriz confectionaries by ELISA and HPLC methods[J]. Advanced Pharmaceutical Bulletin,2012,2(1):123-126
[8]Kongkapan J,Poapolathep S,Isariyodom S,et al. Simultaneous detection of multiple mycotoxins in broiler feeds using a liquid chromatography tandem-mass spectrometry[J].Journal of Veterinary Medical Science,2016,78(2):259-264.
[9]Cigic I k,Prosen H. An overview of conventional and emerging analytical methods for the determination of mycotoxins[J]. International Journal of Molecular Sciences,2009,10(1):62-115.
[10]肖志军,李培武,张文,等. 粮油黄曲霉毒素B1高效快速检测微柱的研制[J]. 中国油料作物学报,2006,28(3):335-341.
[11]Mcmullin D,Mizaikoff B,Krska R. Advancements in IR spectroscopic approaches for the determination of fungal derived contaminations in food crops[J]. Analytical and Bioanalytical Chemistry,2015,407(3):653-660.
[12]Mak A C,Osterfeld S J,Yu H,et al. Sensitive giant magnetoresistive-based immunoassay for multiplex mycotoxin detection[J]. Biosensor and Bioelectronics,2010,25(7):1635-1639.
[13]Siahi Shadbad M R,Ansarin M,Tahavori A,et al. Determination of aflatoxins in nuts of Tabriz confectionaries by ELISA and HPLC methods[J]. Advanced Pharmaceutical Bulletin,2012,2(1):123-126.
[14]Gefen T,Vaya J,Khatib S,et al. The effect of haptens on protein-carrier immunogenicity[J]. Immunology,2015,144(1):116-126.
[15]Rajesh K,Rana KV,Suri CR. Characterization of Hapten-Protein Conjugates:Antibody Generation and Immunoassay Development for Pesticides Monitoring[J]. Bionanoscience,2013,3(3):137-144.
[16]Kim NG,Kim MA,Park YI,et al. Magnetic nanoparticle based purification and enzyme-linked immunosorbent assay using monoclonal antibody against enrofloxacin[J]. Journal of Veterinary Science,2015,16(4):431-437.
[17]Urusov AE,Zherdev AV,Petrakova AV,et al. Rapid Multiple Immunoenzyme Assay of Mycotoxins[J]. Toxins,2015,7(2):238-254.
[18]Kuang H,Xing C,Hao C,et al. Rapid and Highly Sensitive Detection of Lead Ions in Drinking Water Based on a Strip Immunosensor[J]. Sensors,2013,13(4):4214-4224.
[19]Tian W,Xie HQ,Fu H,et al. Immunoanalysis Methods for the Detection of Dioxins and Related Chemicals[J]. Sensors,2012,12(12):16710-16731.
[20]Gefen T,Vaya J,Khatib S,et al. The effect of haptens on protein-carrier immunogenicity[J]. Immunology,2015,144(1):116-126.
[21]Walter FM,Stocklein,AW,Burkhard M,et al. Diphenylurea hapten sensing with a monoclonal antibody and its Fab fragment:Kinetic and thermodynamic investigations[J]. Analytica Chimica Acta,1998,362(1):101-111.
[22]Josten A,Meusel M,Spener F. Microbial transglutaminase-mediated synthesis of hapten-protein conjugates for immunoassays[J]. Analytical Biochemistry,1998,258(2):202-208.
[23]Szurdoki F,Bekheit H K M,Marco M P,et al. Synthesis of hapten and conjugates for enzyme mmunoassay for analysis of the herbicide Vromacil[J]. J Agri Food Chem,1992,40(8):1459-1465.
[24]Singh MK,Srivastava S,Raghava GP,et al.Hapten DB:a comprehensive database of haptens,carrier proteins and anti-hapten antibodies[J]. Bioinformatics,2006,22(2):253-255.
[25]Chen J,Swamidass SJ,Dou Y,et al. Chem DB:a public database of small molecules and related hemoinformatics resources[J]. Bioinformatics,2005,21(22):4133-4 139.
[26]Salimi N,Fleri W,Peters B,et al. Design and utilization of epitope-based databases and predictive tools[J]. Immunogenetics,2010,62(4):185-196.
[27]Singh KV,Kaur J,Varshney GC,et al. Synthesis and characterization of hapten-protein conjugates for antibody production against small molecules[J]. Bioconjugate Chemistry,2004,15(1):168-173.
[28]Pedersen MK,Sorensen NS,Heegaard PM,et al. Effect of different hapten-carrier conjugation ratios and molecular orientations on antibody affinity agaigst a peptide antigen[J]. Journal of Immunological Methods,2006,311(1-2):198-206.
[29]Xu ZL,Xie GM,Li YX,et al. Production and characterization of a broad-specificity polyclonal antibody for o,o-diethyl organophosphorus pesticides and a quantitative structure-activity relation-ship study of antibody recognition[J]. Analytica Chimica Acta,2009,647(1):90-96.
[30]王自良,王建娜,张海棠,等. 苯巴比妥单克隆抗体的研制及竞争ELISA血药浓度监测方法的建立[J]. 中国药学杂志,2006,41(23):1826-1830.
[31]Liu Y,Peng D,Huang L,et al. Application of a modified enzyme-linked immunosorbent assay for 3-amino-2-oxazolidinone residue in aquatic animals[J]. Analytica Chimica Acta,2010,664(2):151-157.
[32]Sun X,Du S,Wang X,et al. A label-free electrochemical immunosensor for carbofuran detection based on a sol-gel entrapped antibody[J]. Sensors,2011,11(10):9520-9531.
[33]Tuomola M,Harpio R,Knuuttila P.Production and characterization of monoclonal antibodies against a very small hapten,3-methylindole[J].Journal of Immunological Methods,2000,240(2):111-124.
[34]Jung F,Gee S J,Harrison R O,et al.Use of immunochemical techniques for the analysis of pesticides[J]. Pesticide Science,1989,26(3):303-317.
[35]Moreno MJ,Abad A,Montoya A. Production of monoclonal antibodies to the N-methylcar-bamate pesticide propoxur[J]. Journal of Agricultural and Food Chemistry,2001,49(1):72-78.
[36]Bruun L,Koch C,Jakobsen MH,et al. Characterization of monoclonal antibodies raised against different structures belonging to the s-triazine group of herbicides[J]. Analytica Chimica Acta,2001,436(1):87-101.
[37]Kolosova AY,Park JH,Eremin SA,et al. Fluorescence polarization immunoassay based on a monoclonal antibody for the detection of the organophosphorus pesticide parathion-methyl[J]. Journal of Agricultural and Food Chemistry,2003,51(5):1107-1114.
[38]Chipinda I,Hettick J M,Siegel P D. Haptenation:chemical reactivity and protein binding[J]. Journal of Allergy,2011,4:1-11.
[39]Peterson E C,Gunnell M,Che Y,et al. Using hapten design to discover therapeutic monoclonal antibodies for treating methamphetamine abuse[J]. Journal of Pharmacology and Experimental Therapeutics,2007,322(1):30-39.
[40]Peterson E C,Owens S M. Designing immunotherapies to thwart drug abuse[J]. Molecular Interventions,2009,9(3):119-124.
[41]Poljak R. X-ray crystallographic studies of immunoglobulins. Contemporary Topics in Molecular Immunology. 1973;2:1-26.
[42]Meulenberg E P. Immunochemical methods for ochratoxin A detection:a review[j]. Toxins,2012,4(4):244-266.
[43]Liang Y,Liu X J,Yu X Y,et al. Synthesis of three haptens for the class-specific immunoassay of O,O-dimethyl organophosphorus pesticides and effect of hapten heterology on immunoassay sensitivity[J]. Analytica chimica acta,2008,615(2):174-183.
[44]Fasciglione GF,Marini S,Bannister JV,et al. Hapten-carrier interactions and their role in the production of monoclonal antibodies against hydrophobic haptens[J]. Hybridoma,1996,15(1):1-9.
[45]Jones LH. Recent advances in the molecular design of synthetic vaccines[J]. Nature Chemistry,2015,7(12):952-960.
[46]Peterson E C,Hambuchen M D,Tawney R L,et al. Simple radiometric method for accurately quantitating epitope densities of hapten-protein conjugates with sulfhydryl linkages[J]. Bioconjugate chemistry,2014,25(12):2112-2115.
[47]Li X,Wang W,Wang L,et al. Rapid determination of phenylethanolamine A in biological samples by enzyme-linked immunosorbent assay and lateral-flow immunoassay[J]. Analytical and Bioanalytical Chemistry,2015,407(25):7615-7624.
[48]Kriechbaum M,List M,Himmelsbach M,et al. Peptide coupling between amino acids and the carboxylic acid of a functionalized chlorido-gold(I)-phosphane[J]. Inorganic Chemistry,2014,53(19):10602-10610.
[49]Hong S H,Kim K R,Oh D K. Biochemical properties of retinoid-converting enzymes and biotechnological production of retinoids[J]. Applied Microbiology Biotechnology,2015,99(19):7813-7826.
[50]Grange R L,Evans P A. Metal-free metathesis reaction of C-chiral allylic sulfilimines with aryl isocyanates:construction of chiral nonracemic allylic isocyanates[J]. Journal of the American Chemical Society,2014,136(34):11870-11873.
[51]Luo L,Xu Z L,Yang J Y,et al. Synthesis of novel haptens and development of an enzyme-linked immunosorbent assay for quantification of histamine in foods[J]. Journal of Agricultural and Food Chemistry,2014,62(51):12299-12308.
[52]Morgan K M,Ellis J A,Lee J,et al. Thermochemical studies of epoxides and related compounds[J]. Journal of Organic Chemistry,2013,78(9):4303-4311.
[53]Liu L,Xing C,Yan H,et al. Development of an ELISA and immunochromatographic strip for highly sensitive detection of microcystin-LR[J]. Sensors,2014,14(8):14672-14685.
[54]Kaminski K,Rapacz A,Luszcki J J,et al. Design,synthesis and biological evaluation of new hybrid anticonvulsants derived from N-benzyl-2-(2,5-dioxopyrrolidin-1-yl)propanamide and 2-(2,5-dioxopyrrolidin-1-yl)butanamide derivatives[J]. Bioorganic and Medicinal Chemistry,2015,23(10):2548-2561.
[55]贾国超,职爱民,李梦琴,等. 氟罗沙星残留检测间接竞争ELISA试剂盒的研制[J]. 中国农业科学,2014,47(11):2251-2261.
[56]Zhang T,Xue H,Zhang B,et al. Determination of folic acid in milk,milk powder and energy drink by an indirect immunoassay[J]. Journal of Science and Food Agricultrue,2012,92(11):2297-2304.
[57]王玲玲,职爱民,杨艳艳,等. 抗百菌清单克隆抗体的研制与鉴定[J]. 中国农业科学,2013,46(7):1509-1515.
[58]娄忠良,王鹏,孟子晖,等. 1,3,5-三乙酰基六氢均三嗪的小分子合成反应机理研究[J]. 有机化学,2010,30(7):1059-1062.
[59]Mercader J V,Esteve FA,Agullo C,et al. Antibody generation and immunoassay development in diverse formats for pyrimethanil specific and sensitive analysis[J]. Analyst,2012,137(23):5672-5279.
[60]Dubey RD,Alam N,Saneja A,et al. Development and evaluation of folate functionalized albumin nanoparticles for targeted delivery of gemcitabine[J]. International Journal of Pharmaceutics,2015,492(1-2):80-91.
[61]王迪,杨署明,刘潇威,等. 莱克多巴胺免疫亲和柱的制备与应用研究[J]. 分析测试学报,2010,29(8):812-816.
[62]尹静梅,张瑞,贾颖萍,等. 芳香硝基化合物环氧制备芳胺的研究进展[J]. 化学研究,2010,21(1):96-101.
[63]Bvzova N A,Zvereva E A,Zherdev A V,et al. Pretreatment-free immunochromatographic assay for the detection of streptomycin and its application to the control of milk and dairy products[J]. Analytical Chimica Acta,2011,701(2):209-217.
[64]Wu C M,Chen C H,Dayananda K,et al. Sensitivity evaluation of rhodamine B hydrazide towards nitric oxide and its application for macrophage cells imaging[J]. Analytical Chimica Acta,2011,708(1-2):141-148.
[65]Gao Y,Yang M,Peng C,et al. Preparation of highly specific anti-zearalenone antibodies by using the cationic protein conjugate and development of an indirect competitive enzyme-linked immunosorbent assay[J]. Analyst,2012,137(1):229-236.
[66]李萍,马亚茹,李刚,等. 恶性疟原虫环子孢子蛋白四肽重复序列单克隆抗体的制备[J]. 中国生物制品学杂志,2015,28(10):1039-1043.
[67]Desilva B S,Wilson G S. Synthesis of bifunctional antibodies for immunoassays[J]. Methods,2000,22(1):33-43.
[68]Gefen T,Vaya J,Khatib S,et al. The effect of haptens on protein-carrier immunogenicity[J]. Immunology,2015,144(1):116-126.
[69]Peterson EC,Hambuchen MD,Tawney RL,et al. Simple radiometric method for accurately quantitating epitope densities of hapten-protein conjugates with sulfhydryl linkages[J]. Bioconjugate Chemistry,2014,25(12):2112-2115.
[70]Singh KV,Kaur J,Varshney GC,et al. Synthesis and characterization of hapten-protein conjugrtes for antibody production against small molecules[J]. Bioconjugate Chemistry,2004,15(1):168-173.
[71]Chu F S,Ueno I. Production of Antibody Against Aflatoxin B1[J]. Applied and Environmental Microbiology,1977,33(5):1125-1128.
[72]Kolosova A Y,Shim W B,Yang Z Y,et al. Direct competitive ELISA based on a monoclonal antibody for detection of aflatoxin B. Stabilization of ELISA kit components and application to grain samples[J]. European Journal of Human Genetics,2006,12(1):13-23.
[73]Cervino C,Weber E,Knopp D,et al. Comparison of hybridoma screening methods for the efficient detection of high-affinity hapten-specific monoclonal antibodies[J]. Journal of Immunological Methods,2008,329(1-2):184-193.
[74]孙清,李谷丰,邓乾民,等. 高灵敏黄曲霉毒素B1酶联免疫试剂盒的研制及应用[J]. 环境化学,2015,34(10):1845-1853.
[75]谢珲,章先,王歆,等. 黄曲霉毒素B1单克隆抗体的制备及间接竞争ELISA检测技术研究[J]. 微生物学通报,2015,42(10):2033-2040.
[76]Zhang D,Li P,Zhang Q,et al. Production of ultrasensitive generic monoclonal antibodies against major aflatoxins using a modified two-step screening procedure[J]. Analytica Chimica Acta,2009,636(1):63-69.
[77]韦耀鹏,陆善新,顾旭辉,等. 黄曲霉毒素B1抗原制备的新方法及抗体特性的初步研究[J]. 肿瘤防治研究,1992,19(2):78-79.
[78]Fuentes M,Palomo J,Mateo C,et al. Optimization of the modification of carrier proteins with aminated haptens[J]. Journal of Immunological Methods,2005,307(1-2):144-149.
[79]Zhou Y,Wu J,Yu W,et al. Preparation for aflatoxin B1-cationized bovine serum albumin based on Mannich-type reaction[J]. Journal of Immunological Methods,2007,328(1-2):79-88.
[80]Urusov A E,Petrakova A V,Vozniak M V,et al. Rapid Immunoenzyme Assay of Aflatoxin B1Using Magnetic Nanoparticles[J]. Sensors,2014,14(11):21843-21857.
[81]Lau H P,Gaur P K,Chu F S. Preparation and characterization of aflatoxin B2a-hemiglutarate and its use for the production of antibody against aflatoxin B1[J]. Journal of Food Safety,3(1):1-13.
[82]Gaur P K,Lau H P,Pestka J J,et al. Production and characterization of aflatoxin B2a antiserum[J]. Applied and Environmental Microbiology,1981,41(2):478-482.
[83]Fan T S,Zhang G S,Chu F S. Production and characterization of antibody against aflatoxin Q1[J]. Applied and Environmental Microbiology,1984,47(3):526-532.
[84]Ashoor S H,Chu F S. Reduction of aflatoxin B2a with sodium borohydride[J]. Journal of Agricultural and Food Chemistry,1975,23(3):445-447.
[85]Kononenko G,Burkin A,Soboleva N. Comparative Characterization of Immune Reagents Based on Hemiacetals of Aflatoxin B1and Sterigmatocystine[J]. Applied Biochemistry and Microbiology,2002,38(5):487-492.
[86]肖智,李培武,张奇,等. 高特异性黄曲霉毒素B1单克隆抗体的制备及特性研究[J]. 中国油料作物学报,2011,33(1):66-70.
[87]Cervino C,Knopp D,Weller M G,et al. Novel aflatoxin derivatives and protein conjugates[J]. Molecules,2007,12(3):641-653.
[88]Lin J K,Miller J A,Miller E C. 2,3-Dihydro-2-(guan-7-yl)-3-hydroxy-aflatoxin B1,a major acid hydrolysis product of aflatoxin B1-DNA or-ribosomal RNA adducts formed in hepatic microsome-mediated reactions and in rat liverinvivo[J]. Cancer Research,1977,37(12):4430-4438.
[89]Martin C N,Garner R C. Aflatoxin B-oxide generated by chemical or enzymic oxidation of aflatoxin B1causes guanine substitution in nucleic acids[J]. Nature,1977,267(5614):863-865.
[90]Groopman J D,Trudel L J,Donahue P R,et al. High-affinity monoclonal antibodies for aflatoxins and their application to solid-phase immunoassays[J]. Proceeding of the National Academy of Science of the United States of America,1984,81(24):7728-7731.
Research progress in hapten molecule design and immunogen synthesis and antibody characteristics of aflatoxin B1
WANG Ya-nan1,2,WANG Xiao-fei3,NIU Lin-lin1,2,LEI Zhuang1,2,ZHANG Hai-tang1,2,WANG Zi-liang1,2,*
(1.The Animal Science and technology College,Henan Institute of Science and Technology,Xinxiang 453003,China; 2.Animal Viral Disease Control and Residual Analysis Henan Higher Education Key Discipline Open Laboratory,Xinxiang 453003,China; 3.School of Xinke,Henan Institute of Science and Technology,Xinxiang 453003,China)
To provide new methods and ideas of preparation of high quality antibodies for aflatoxin B1(AFB1)and other small molecule hapten,the domestic and foreign research progress on molecular design method,the basic requirements,principles to be followed and antigen synthesis methods were reviewed in this paper,in particular,the AFB1hapten molecule design,antigen synthesis and antibody characteristics were described in detail.
aflatoxin B1;hapten molecule design;antigen synthesis;antibody characteristics
2016-07-08
王亚楠(1989-), 女, 硕士研究生, 研究方向:食品安全免疫检测,E-mail:792176339@qq.com。
*通讯作者:王自良(1966-), 男, 博士, 教授, 研究方向:免疫学与抗体工程,E-mail:wangziliang66@126.com。
“十二五”国家科技支撑计划项目(2014BAD13B05)。
TS201.1
A
1002-0306(2016)23-0367-10
10.13386/j.issn1002-0306.2016.23.061
