鲈鱼肠道Lactobacillussakei LY1-6对荧光假单胞菌抑制作用研究
2016-02-09马欢欢吕欣然孙梦桐白凤翎励建荣
马欢欢,吕欣然,林 洋,孙梦桐,白凤翎,*,励建荣
(1.渤海大学食品科学与工程学院,辽宁省食品安全重点实验室,生鲜农产品贮藏加工及安全控制技术国家地方联合工程研究中心,辽宁锦州 121013;2.北京林业大学生物科学与技术学院,北京 100083)
鲈鱼肠道LactobacillussakeiLY1-6对荧光假单胞菌抑制作用研究
马欢欢1,吕欣然2,林 洋1,孙梦桐1,白凤翎1,*,励建荣1
(1.渤海大学食品科学与工程学院,辽宁省食品安全重点实验室,生鲜农产品贮藏加工及安全控制技术国家地方联合工程研究中心,辽宁锦州 121013;2.北京林业大学生物科学与技术学院,北京 100083)
目的:从海鱼肠道中筛选对荧光假单胞菌具有较强抑制作用的乳酸菌。方法:采用牛津杯琼脂扩散法筛选菌株,通过生理生化反应和16S rRNA测序进行菌株生物学鉴定,利用蛋白酶、pH和温度等因素对抑菌活性进行分析,采用扫描电镜分析乳酸菌无细胞上清液(CFS)对荧光假单胞菌细胞结构的完整性影响。结果:从鲈鱼肠道中筛选出对荧光假单胞菌具有较强抑制活性的菌株LY1-6,经生理生化和16S rRNA测序鉴定为清酒乳杆菌(Lactobacillussakei)。菌株LY1-6 CFS经胃蛋白酶处理后其抑菌活性完全丧失,经中性蛋白酶、木瓜蛋白酶、胰蛋白酶和碱性蛋白酶处理后其抑菌活性分别丧失了38.22%、38.00%、22.48%和18.46%。在pH2.5~5.0具有抑菌活性,并具有良好的热稳定性,初步结果表明LY1-6 CFS中抑菌活性物质可能为细菌素。扫描电镜结果表明经LY1-6 CFS处理使荧光假单胞菌细胞结构被破坏并溶解。结论:来自鲈鱼肠道的清酒乳杆菌LY1-6对荧光假单胞菌具有较强抑制作用,其抑菌活性物质为细菌素类,作用机制为破坏细胞的完整性,可作为控制水产品中荧光假单胞菌腐败生物保鲜的出发菌株。
荧光假单胞菌,清酒乳杆菌LY1-6,海水鱼肠道,筛选,水产品保鲜
荧光假单胞菌(Pseudomonasfluorescens)可引起低温条件下的奶类、蛋类、肉类和鱼类等食品的腐败变质[1]。刘永吉等[2]从冷却猪肉中分离鉴定形成生物被膜能力较强的菌株Pseudomonasfluorescens113,证实是引起肉类腐败的特定腐败菌。崔方超等[3]从冷藏大菱鲆体表分离获得导致鱼体腐败的特定腐败菌菌株P001,经鉴定为Pseudomonasfluorescens。在低温贮藏条件下,控制水产动物和肉禽乳类食品中荧光假单胞菌具有重要应用价值。
对水产食品而言,生物防腐保鲜技术具有安全、无残留和无损伤的优势,一般采用动植物提取物和微生物菌体及其代谢产物控制食品中致病和腐败微生物的生长繁殖。Küçükgülmez等[4]研究表明虾壳中提取的壳聚糖对荧光假单胞菌具有较强的抑菌作用。赵前程等[5]采用果胶的酶解物可使冷藏大菱鲆鱼肉贮藏期从1周延长至2周。Rong等[6]利用Lactobacillusplantarum1.19可使罗非鱼生鱼片的贮藏期从24 h延长到48 h。陈桂芳等[7]通过添加3 μL/mL肉桂油以抑制荧光假单胞菌群体感应的方式延缓冷藏大菱鲆鱼汁的腐败,使贮藏时间延长48 h。
传统发酵食品是拮抗性乳酸菌的重要来源,Liu等[8]从牦牛酸奶中筛选出对PseudomonasfluorescensAS1.1802具有较强抑制作用的菌株LactobacillusplantarumQ7。高鹏等[9]从酸菜中分离获得LactobacillusplantarumHLJ-174,能有效抑制Pseudomonasfluorescens的生长。天然鱼类肠道也栖息着对细菌具有拮抗活性的乳酸菌,Kaynar等[10]从红鲷鱼肠道中分离获得菌株LactobacillusxylosusHC9对目标菌BacillusmegateriumP4具有较强的抑制作用。缪璐欢等[11]从鲤鱼肠道中分离筛选出对EscherichiacoliO157∶H7具有较强拮抗活性的菌株Lactobacillussakei和Lactobacillusplantarum。然而,从鲈鱼肠道中分离拮抗性乳酸菌的研究偏少,对海洋鱼类中乳酸菌资源还有待于开发。
大菱鲆是我国重要的海产养殖经济鱼类,由于缺乏有效的冷鲜保藏技术,目前主要以鲜售为主,限制了产业的发展。本文从鲈鱼、刀鱼、牙鲆、大菱鲆等海水鱼肠道中分离筛选出对荧光假单胞菌具有较强拮抗作用的乳酸菌菌株,并对其拮抗性能进行研究,旨在为冷藏大菱鲆防腐保鲜提供优良生物防腐菌株资源。
1 材料与方法
1.1 材料与仪器
鲈鱼、刀鱼、牙鲆、大菱鲆 辽宁省锦州市金凌商场。
指示菌:单核细胞增生李斯特菌(Listeriamonocytogenes)ATCC19115、铜绿假单胞菌(Pseudomonasaeruginosa)ATCC9027、哈维氏弧菌(Vibrioharveyi)ATCC BB-170 美国典型菌种保藏中心;金黄色葡萄球菌(Staphylococcusaureus)CMCC26003、蜡样芽孢杆菌(Bacilluscereus)CMCC63301 医学微生物菌种保藏管理中心;嗜冷杆菌(Psychrobactersp.)MCCC1A00052 中国实验室微生物菌种购买保藏中;荧光假单胞菌(Pseudomonasfluorescens)P001、温和气单胞菌(Aeromonassobria)L002 分离自大菱鲆。
MRS琼脂培养基、LB肉汤、LB营养琼脂 北京奥博星生物技术有限公司;细菌基因组DNA快速抽提试剂盒、DNA marker-D、Taq PCR Master mix 上海生工生物工程有限公司;乳酸菌生理生化鉴定管 杭州天和微生物试剂有限公司;胃蛋白酶(15000 U/g)、胰蛋白酶(250000 U/g)、木瓜蛋白酶(200000 U/g)、中性蛋白酶(200000 U/g)、碱性蛋白酶(200000 U/g) 华蓝化学有限公司。
DL-CJ-2N型超级洁净工作台 东联哈尔(北京)仪器制造有限公司;赛福智能生化培养箱 宁波海曙赛福实验仪器厂;BMM-408YS显微镜 上海浍统光学仪器有限公司;5804R冷冻高速离心机 德国Eppendorf公司;Mastercycler pro梯度PCR仪 德国艾本德股份有限公司;DYY-8C电泳仪 北京市六一仪器厂;Cheimdox XRS 凝胶成像仪 美国Bio-Rad公司;GI54DS立式高压蒸汽灭菌锅 致微(厦门)仪器有限公司;E-1045镀金仪、S-4800扫描电镜 日本日立公司。
1.2 实验方法
1.2.1 海鱼肠道中乳酸菌的分离 分别称取10.00 g鲈鱼、刀鱼、牙鲆和大菱鲆的肠道,剪成长约2 cm片段,置于装有90 mL无菌水的三角瓶中,充分震荡,静置10 min。吸取100 μL在1% CaCO3MRS琼脂平板上涂布,37 ℃培养48 h,挑选有溶钙圈的白色菌落进行纯化。挑取纯化培养后的单个菌落进行过氧化氢酶实验和革兰氏染色初筛乳酸菌菌株。
1.2.2 指示菌菌悬液制备 将-80 ℃保存的8株指示菌以0.5%的接种量于10 mL LB肉汤培养基中30 ℃培养12 h,活化3代,用无菌生理盐水进行梯度稀释使其菌悬液最终浓度为106CFU/mL,后置于4 ℃冰箱备用。
1.2.3 抗荧光假单胞菌乳酸菌的筛选 取初筛乳酸菌菌株培养24 h的菌悬液10 mL,经4 ℃ 8000 r/min离心10 min,吸取上清液经 0.45 μm滤器过滤获得乳酸菌无细胞上清液(cell free supernatant,CFS)。参照等[12]利用牛津杯琼脂扩散法应用菌株CFS对荧光假单胞菌进行抑菌实验。
1.2.4 乳酸菌菌株抑菌谱测定 利用从鲈鱼、刀鱼、牙鲆和大菱鲆的肠道中筛选出的乳酸菌菌株CFS对8株指示菌按1.2.3方法进行抑菌实验。
1.2.5 乳酸菌菌株鉴定
1.2.5.1 生理生化鉴定 参照《乳酸细菌分类鉴定及实验方法》和《伯杰氏细菌鉴定手册》(第八版)中乳酸菌的鉴定方法进行生理生化实验[13-15]。
1.2.5.2 16S rRNA鉴定 吸取1.0 mL乳酸菌菌株12 h菌悬液加入1.5 mL EP管中,4 ℃ 12000 r/min离心5 min,采用DNA快速抽提试剂盒提取菌株DNA,以16S rDNA通用引物进行PCR扩增。正向引物为27 f(5′-AGAGTTTGATCCTGGCTCAG-3′),反向引物为1492 r(5′-TACGGYTACCTTTGTT ACGACTT-3′),引物由上海生工生物技术公司合成。PCR扩增反应体系为DNA模板1.0 μL、Taq PCR Master mix 12.5 μL、dd H2O 9.5 μL、上游引物1.0 μL、下游引物1.0 μL,总体积25 μL。PCR扩增反应程序:94 ℃预变性2 min,94 ℃变性1 min,60 ℃退火1 min,72 ℃延伸90 s,72 ℃保持10 min,循环30次,4 ℃保温。
PCR产物经1.0%琼脂糖凝胶电泳,观察凝胶成像系统的扩增效果并照相。将扩增成功的PCR产物送至上海生物工程股份有限公司进行测序。测序结果经校对后与NCBI上GeneBank数据库中的己有序列进行BLAST比对分析,运用MEGA 5.0软件构建菌株系统发育进化树。
1.2.6 乳酸菌生长与抗荧光假单胞菌活性曲线分析 取200 μL乳酸菌菌悬液接种于10 mL MRS液体培养基中,37 ℃静置培养。每隔4 h取样测定菌悬液OD600值和pH,并按照1.2.3测定菌株CFS的抑菌活性。
1.2.7 影响乳酸菌CFS抑制荧光假单胞菌的因素 酶敏感实验:将乳酸菌CFS分别用1.0 mol/L NaOH和1.0 mol/L HCl调至酶的最佳pH(胃蛋白酶pH2.0、胰蛋白酶pH7.5、木瓜蛋白酶pH7.0、中性蛋白酶pH7.0和碱性蛋白酶pH10.0),添加蛋白酶使其在乳酸菌CFS中的终浓度为1.0 mg/mL,37 ℃水浴中孵育2 h,将蛋白酶处理后的CFS pH调至初始值,同时以乳酸菌CFS作对照,参照1.2.3进行抑菌实验。
pH实验:用1.0 mol/L NaOH和1.0 mol/L HCl将乳酸菌CFS pH分别调至2.5、3.5、4.0、4.5、5.0、5.5、6.0和6.5,同时用相同方法相对应pH MRS液体培养基作对照,按1.2.3方法进行抑菌实验。
热稳定性实验:取乳酸菌CFS分别经40、60、80、100和121 ℃处理30 min,同时以菌株CFS作对照,按1.2.3方法进行抑菌实验。
1.2.8 乳酸菌CFS处理荧光假单胞菌细胞扫描电镜分析 参考Hovnanyan等[16]的方法并稍作修改。取1 mL含有106CFU/mL荧光假单胞菌菌悬液4 ℃12000 r/min离心5 min,弃上清液,菌体生理盐水洗涤3次,每次5 min,后加入乳酸菌CFS,未添加CFS为对照,30 ℃静置培养12 h。4 ℃ 12000 r/min离心5 min 收集荧光假单胞菌菌体。将菌体在2.5%戊二醛溶液中4 ℃过夜,用0.1 mol/L pH7.2 PBS 洗涤2次,每次5 min洗去残留的戊二醛。分别用40%、70%、90%、100%乙醇对菌体细胞进行脱水处理15 min,将菌体滴加在盖玻片上,自然晾干,喷金,扫描电镜观察。
1.2.9 实验数据处理 实验均重复测定3次,数据采用平均值±标准差表示。采用SPSS 18.0软件对数据进行统计学分析,采用Origin 8.0软件进行绘图。
2 结果与讨论
2.1 乳酸菌菌株的分离
从鲈鱼、刀鱼、牙鲆和大菱鲆鱼肠道中筛选出具有溶钙圈、过氧化氢酶阴性和革兰氏染色阳性的49株乳酸菌,四种海鱼肠道的乳酸菌菌株数分别为15、13、12和9,以海鱼中文名称首字母和分离顺序进行命名。
2.2 拮抗性乳酸菌的筛选
利用牛津杯琼脂扩散法从49株菌株中筛选出7株对荧光假单胞菌具有较强抑制活性的菌株,抑菌直径均大于12.00 mm,分别为YP1-6、YP4-5、LP2-4、DY1-3、DY3-2、LY2-4和LY1-6。图1中A为5株乳酸菌CFS对荧光假单胞菌的抑菌效果,从中可以看出菌株LY1-6和DY3-2的抑菌圈较大,YP1-6次之,YP4-5和LY1-3抑菌圈较小。B图为7株乳酸菌CFS对荧光假单胞菌的抑菌结果,从中可看出菌株LY1-6的CFS抑菌效果最好,抑菌直径为18.90 mm,因此,选取菌株LY1-6进行下一步研究。
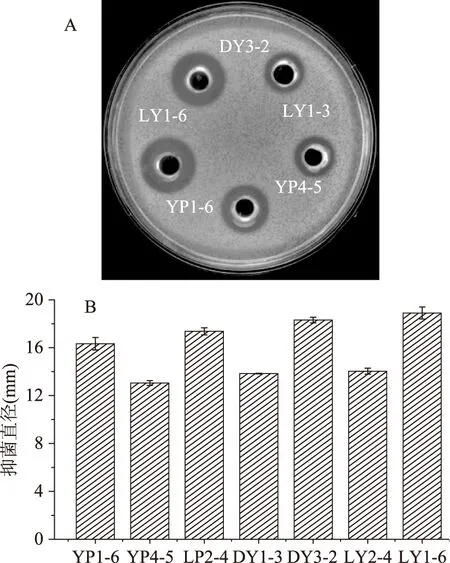
图1 乳酸菌对荧光假单胞菌的抑制作用和效果Fig.1 Antagonistic effect of LAB on P. fluorescens
2.3 乳酸菌抑菌谱测定
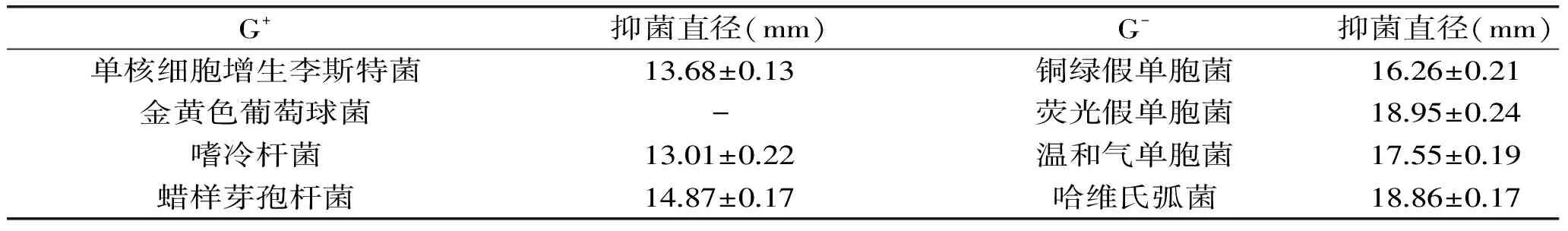
不同来源的乳酸菌代谢过程中形成的抑菌活性物质抑菌谱不同。表1是筛选菌株LY1-6 CFS对8株指示菌的抑菌结果,从中可看出菌株LY1-6对革兰氏阳性菌(G+)抑菌效果较差,抑菌直径均低于15 mm;菌株LY1-6 CFS对革兰氏阴性菌(G-)抑菌效果较好,抑菌直径均高于15 mm,其中对荧光假单胞菌和哈维氏弧菌的抑菌效果最好,抑菌直径分别为18.95 mm和18.86 mm。结果表明,菌株LY1-6 CFS中抑菌活物质不具较广的抑菌谱,而对G-细菌具有较强的抑制作用。
表1 菌株LY1-6对革兰氏阳性菌和革兰氏阴性菌抑菌结果
Table 1 Results of strain LY1-6 against gram positive bacteria and gram negative bacteria
G+抑菌直径(mm)G-抑菌直径(mm)单核细胞增生李斯特菌1368±013铜绿假单胞菌1626±021金黄色葡萄球菌-荧光假单胞菌1895±024嗜冷杆菌1301±022温和气单胞菌1755±019蜡样芽孢杆菌1487±017哈维氏弧菌1886±017
注:“-”为无抑菌作用。
表2 菌株LY1-6生理生化鉴定结果
Table 2 Physiological and biochemical test results of strain LY1-6

项目LY1-6项目LY1-6项目LY1-6阿拉伯糖+麦芽糖+葡萄糖酸盐-纤维二糖-甘露醇-乳糖-七叶灵-甘露糖+木糖-果糖+松三糖-鼠李糖-半乳糖+蜜二糖+山梨醇-葡萄糖+棉籽糖-蔗糖+
注:“+”表示阳性;“-”表示阴性。
2.4 乳酸菌菌株鉴定
2.4.1 生理生化鉴定 表2为筛选菌株LY1-6生理生化鉴定结果,依照文献[13]可初步判定菌株LY1-6为乳杆菌属的Lb.sakei。
2.4.2 分子生物学鉴定 图2为菌株LY1-6 PCR反应产物经1%琼脂糖凝胶电泳分离结果,从中可看出菌株在1500 bp左右出现荧光条带。PCR产物经测序分析菌株LY1-6 16S rRNA基因序列长度为1459 bp。

图2 菌株LY1-6的16S rRNA基因扩增电泳图Fig.2 PCR amplification of 16S rRNA gene of strain LY1-6
菌株同源性分析及系统发育树建立:将菌株LY1-6的测序结果通过MEGA5.05软件与GenBank数据库中乳杆菌属标准菌株的基因序列进行比对,结果如图3所示,菌株LY1-6与3株标准菌株Lb.sakei在同一分支上,且四株菌的同源性很高,可确定菌株LY1-6为Lb.sakei。
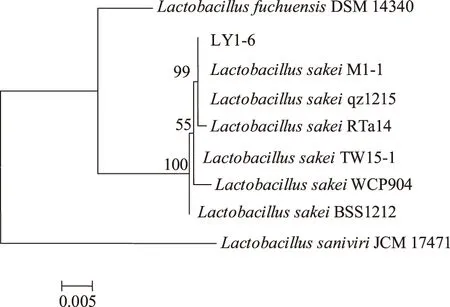
图3 菌株LY1-6的系统发育树Fig.3 The phylogenetic tree for sequences of strain LY1-6
2.5 乳酸菌生长与拮抗活性曲线
乳酸菌在生长过程中形成乳酸等酸性物质和一些拮抗性代谢产物,对霉菌、细菌等微生物生长具有抑制作用[17]。图4为菌株LY1-6经37 ℃静置培养48 h的生长曲线及对荧光假单胞菌抑菌活性的动态变化结果。从中可以看出,随着培养时间的延长pH呈现逐步下降趋势,在16 h呈水平发展。从培养至8 h LY1-6 CFS表现出对荧光假单胞菌的生长具有的抑菌作用,培养12 h细胞生长进入稳定期,当细菌培养到24 h时抑菌活性达到最大值,后期呈稳定状态。结果表明乳酸菌生长至稳定期时,其拮抗性代谢产物已经形成。因此,选择24 h为菌株LY1-6抑菌活性研究的最佳时间。
2.6 影响乳酸菌CFS抑制荧光假单胞菌的因素
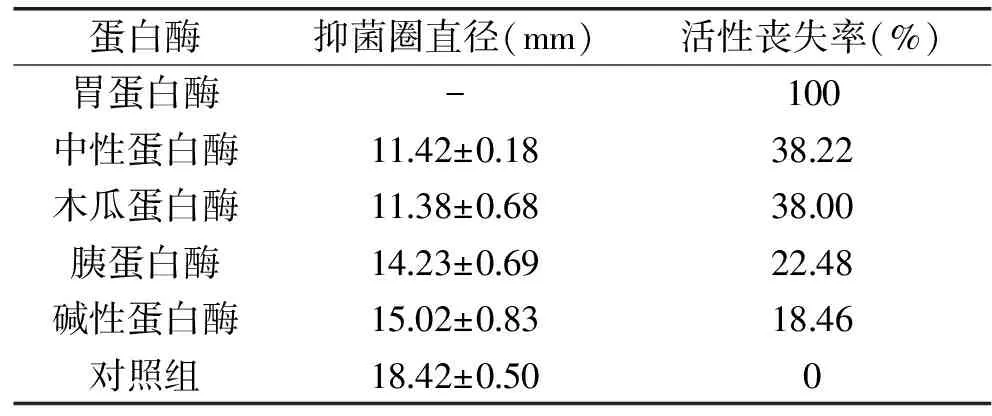
2.6.1 酶敏感性实验 乳酸菌代谢产物中的抑菌活性物质包括乳酸菌素、罗伊氏菌素和双乙酰等代谢产物,蛋白酶敏感性测定是影响抑菌活性物质的主要因素之一[17]。表3是LY1-6 CFS经胃蛋白酶、中性蛋白酶、木瓜蛋白酶、胰蛋白酶和碱性蛋白酶处理后对荧光假单胞菌抑菌结果,从中可以看出,经蛋白酶处理后抑菌活性出现不同程度的降低或丧失。胃蛋白酶处理后抑菌活性完全丧失,表明菌株LY1-6 CFS中抑菌物质对胃蛋白酶具有较强的敏感性。经中性蛋白酶、木瓜蛋白酶、胰蛋白酶和碱性蛋白酶处理后抑菌活性分别丧失了38.22%、38.00%、22.48%和18.46%,表明LY1-6对这4种蛋白酶具有不同程度的敏感性。缪璐欢等[11]研究发现Lactobacillusplantarum代谢产生具有抑制大肠杆菌O157∶H7的细菌素,经胃蛋白酶处理后抑菌活性丧失,可初步判定其抑菌物质中有蛋白类物质。
表4 不同pH对菌株CFS抑菌活性的影响
Table 4 Effects of pH on the anti-bacterial activity of CFS

组别抑菌圈直径(mm)2535455055CFS2265±0172049±0211568±0141132±023-MRS1618±0541298±027---
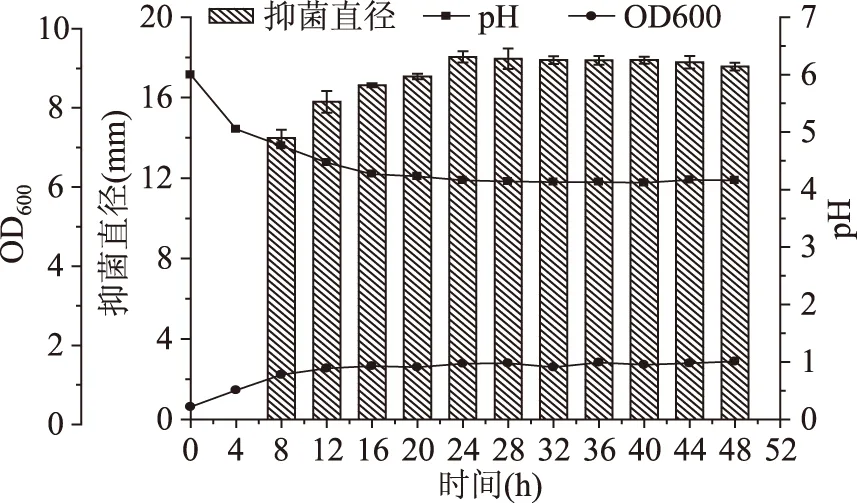
图4 菌株LY1-6的生长及拮抗活性曲线Fig.4 The growth and antagonistic activity curve of strain LY1-6
注:“-”为无抑菌作用。
表3 蛋白酶处理对菌株CFS抑菌活性的影响
Table 3 Effects of proteases treatment on the anti-bacterial activity of CFS
蛋白酶抑菌圈直径(mm)活性丧失率(%)胃蛋白酶-100中性蛋白酶1142±0183822木瓜蛋白酶1138±0683800胰蛋白酶1423±0692248碱性蛋白酶1502±0831846对照组1842±0500
注:“-”为无抑菌作用。
2.6.2 pH实验 pH是影响乳酸菌CFS抑菌活性的主要因素,表4是不同pH下菌株LY1-6 CFS和MRS对荧光假单胞菌的抑制作用结果。从中可以看出,抑菌直径随pH上升呈现下降趋势。当pH2.5~3.5时,两组实验中均具有抑菌作用;当pH4.5~5.0时,菌株LY1-6 CFS对荧光假单胞菌仍具有抑制作用,对照组抑菌活性完全丧失;当pH5.5~6.5时,抑菌活性均已完全丧失(表中未列出)。结果表明,菌株LY1-6 CFS中抑菌活性物质部分来自酸环境,同时还存在其他抗菌成分。
2.6.3 热稳定性实验 温度是影响乳酸菌CFS抑菌活性的主要因素,从图5可以看出,40、60、80、100和121 ℃处理30 min后的菌株LY1-6 CFS抑菌直径呈平稳状态,结果表明,菌株LY1-6 CFS中的抑菌活性物质具有良好的热稳定性。Gómez等[18]从鳕鱼、沙丁鱼和虹鳟鱼等水产品中分离获得产细菌素Pediococcusacidilactici、Lactococcuspiscium和Lactobacillussakei等乳酸菌菌株,乳酸菌CFS经65、75、100和121 ℃处理后仍具有良好的热稳定性。

图5 热处理对菌株CFS抑菌活性的影响Fig.5 Effects of thermal treatment on the anti-bacterial activity of CFS
2.7 乳酸菌CFS处理荧光假单胞菌细胞扫描电镜分析
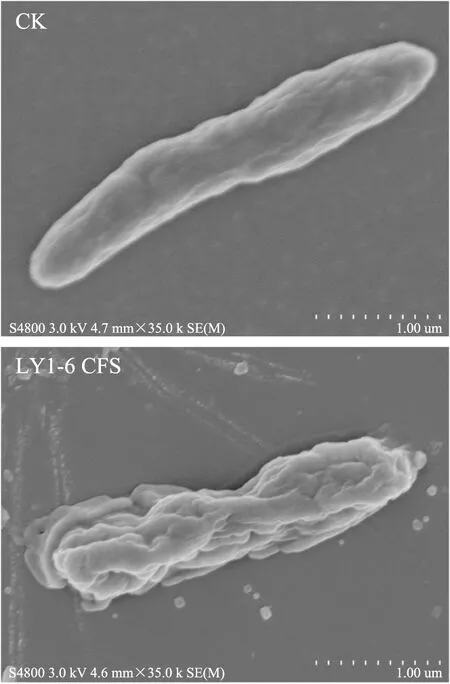
图6 LY1-6 CFS对荧光假单胞菌细胞结构的影响Fig.6 Effect of LY1-6 CFS on the cells structure of P. fluorescens
拮抗性乳酸菌通过形成酸性物质、拮抗性次级代谢产物等以破坏细胞膜的完整性杀伤受试细菌,从而达到抑菌和杀菌的作用效果[19]。图6为LY1-6 CFS对荧光假单胞菌细胞进行处理,通过观察受试细胞的超微结构的变化,分析其拮抗作用方式。从中可以看出,对照组的荧光假单胞菌细胞形态完整,胞膜平滑,两端圆钝。当加LY1-6 CFS时,荧光假单胞菌细胞的完整性破坏,细胞膜出现褶皱并溶解。表明菌株LY1-6 CFS对荧光假单胞菌细胞膜具有破坏作用,从而抑制荧光假单胞菌的生长,结果与Necima等[17]的研究一致。
3 结论
乳酸菌是传统乳酸发酵食品的主体微生物类群,也来自哺乳动物、鸟类和低等脊椎动物的肠道。本文从海鲈鱼肠道中分离对荧光假单胞菌具有较强拮抗作用的菌株Lb.sakeiLY1-6,研究发现其抑菌作用对酸性环境具有良好的耐受性并对热处理稳定,初步判断抑菌活性物质可能为蛋白类细菌素。本研究一方面拓展了拮抗性乳酸菌的生物资源,另一方面利用来源和应用相似相容原则,针对引起大菱鲆腐败的特定腐败菌荧光假单胞菌进行抑菌作用研究。利用该菌株研发一种生物防腐剂,为控制海产品冷藏保鲜过程中荧光假单胞菌导致的腐败变质和延长冷藏产品的货架期奠定基础。
[1]Zhou Z J,Zhang L,Sun L.Pseudomonasfluorescens:Fur is required for multiple biological properties associated with pathogenesis[J]. Veterinary Microbiology,2015,175(1):145-149.
[2]刘永吉,谢晶,赵丽珺. 董韩博冷却猪肉及托盘表面细菌生物被膜分析和肉源荧光假单胞菌的鉴定与被膜研究[J]. 现代食品科技,2016,32(6):1-10.
[3]崔方超,李婷婷,刘明爽,等. 大菱鲆荧光假单胞菌的群体感应现象及不同碳源培养下的腐败特性研究[J]. 现代食品科技,2015,31(12):49-55.
[4]Küçükgülmez A,Gülnaz O,Celik M,et al. Antimicrobial activity of the chitosan extracted from metapenaeus stebbingi shell wastes[J]. Journal of Polymers and the Environment,2011,20(2):431-437.
[5]赵前程,王丹,谢智芬,等. 果胶酶解物对大菱鲆鱼肉保鲜效果的研究[J]. 食品科技,2008,33(3):243-245.
[6]Rong C,Qi L,Chen S,et al. Application of lactic acid bacteria(LAB)in freshness keeping of tilapia fillets as sashimi[J]. Journal of Ocean University of China,2015,14(4):675-680.
[7]陈桂芳,李学鹏,王彦波,等. 肉桂油对大菱鲆荧光假单胞菌腐败能力的抑制作用[J]. 食品工业科技,2016,37(8):313-317.
[8]Liu H,Zhang L,Yi H,et al. Identification and characterization of plantaricin Q7,a novel plantaricin produced byLactobacillusplantarumQ7[J]. LWT-Food Science and Technology,2016,71:386-390.
[9]高鹏,韩金志,陆兆新,等.广谱抗菌乳酸菌的分离鉴定及细菌素的提取和纯化[J]. 2015. http://www.cnli.net/kcms/detail/11.2206.TS.20151126.1411.030.html
[10]Kaynar P,Beyatli Y. Antagonistic activities ofBacillusspp. strains isolated from the fishes[J]. Journal of Applied Biological Sciences,2012,6(3):77-81.
[11]缪璐欢,杜静芳,马欢欢,等. 淡水鱼肠道中抗大肠杆菌O157∶H7乳酸菌的筛选及抑菌作用研究[J]. 食品与发酵工业,2015,41(10):7-13.
[13]凌代文,东秀珠.乳酸细菌分类鉴定及实验方法[M].北京:中国轻工业出版社,1999.
[14]东秀珠,蔡妙英.常见细菌系统鉴定手册[M].北京:科学出版社,2001.
[15]Budanan R E,Gibbonr N E. 伯杰细菌鉴定手册[M].北京:中国科学出版社,1984:477-478.
[16]Hovnanyan K O,Marutyan S,Pepoyan A,et al. Transmission and scanning electron microscopy of contacts between bacterial and yeast cells in biofilms on different surfaces[J]. Open Access Library Journal,2015,59(4):423-435.
[17]Tatiana M,Alzbeta M,L’ubomir V. Production of antimicrobial substances by lactic acid bacteria[J]. Chem Listy,2016,110:179-184.
[18]Gómez-Sala B,Muoz-Atienza E,Sánchez J,et al. Bacteriocin production by lactic acid bacteria isolated from fish,seafood and fish products[J]. European Food Research and Technology,2015,241(3):341-356.
[19]Necima G,Olfa B B,Hani K,et al. Isolation and characterization of large spectrum and multiple bacteriocin-producingEnterococcusfaeciumstrain from raw bovine milk[J]. Journal of Applied Microbiology,2015,118(2):343-55.
Inhibitory activity of Lactobacillus sakei LY1-6 from perch intestine against Pseudomonas fluorescens
MA Huan-huan1,LV Xin-ran2,LIN Yang1,SUN Meng-tong1,BAI Feng-ling1,*,LI Jian-rong1
(1.College of Food Science and Technology,Bohai University;Food Safety Key Lab of Liaoning Province; National & Local Joint Engineering Research Center of Storage,Processing and Safety Control Technology for Fresh Agricultural and Aquatic Products;Jinzhou 121013,China; 2.College of Biology Science and Technology,Beijing Forest University,Beijing 100083,China)
Objective:To isolate lactic acid bacteria(LAB)from marine fish intestine with strong antagonistic activity againstPseudomonasfluorescens. Methods:LAB strains with inhibitory activity againstP.fluorescenswere screened using the method of Oxford cup agar diffusion. The strains were identified by biochemical tests and 16S rRNA sequence analysis. The antibacterial substance was determined using protease sensitivity test,pH test and heat-treated test. The integrity of cell structure ofP.fluorescenstreated with cell-free supernatants(CFS)of produced by LY1-6 was observed by scanning electron microscope. Results:Strain LY1-6 with outstanding inhibitory activity againstP.fluorescenswas screened from ocean perch intestine,and was identified asLactobacillussakei. The inhibitory activity of LY1-6 CFS was completely lost by treated with pepsin,meanwhile,when treated with neutral protease,papaya protease,trypsin and alkaline protease,the inhibitory activity lost 38.22%,38.00%,22.48% and 18.46% respectively. The inhibitory substance was effective within pH2.5~5.0 and stability after thermal treatment,which was preliminary determined as bacteriocins. The scanning electron microscope images revealed that the integrity of cell ofP.fluorescenstreated with LY1-6 CFS was damaged and dissolved. Conclusion:LactobacillussakeiLY1-6 with strong inhibitory activity againstP.fluorescenswas screened from ocean perch intestine. Moreover,its antibacterial substance was determined as bacteriocins. The mechanism of action was destruction the integrity of cell.Lb.sakeiLY1-6 biological preservative can be used as starting strain for the control ofP.fluorescensin aquatic products spoilage.
Pseudomonasfluorescens;LactobacillussakeiLY1-6;marine fish intestine;screening;seafood preservative
2016-07-04
马欢欢(1991-),女,硕士研究生,研究方向:食品安全与质量控制,E-mail:mahuanhuan14@163.com。
*通讯作者:白凤翎(1964-),男,博士,教授,研究方向:食品安全与质量控制和食品微生物学,E-mail:baifling@163.com。
辽宁省科技厅攻关项目(2015103020);泰山学者蓝色产业领军人才团队支撑计划项目(鲁政办字(2015)19号。
TS201.3
A
1002-0306(2016)23-0150-06
10.13386/j.issn1002-0306.2016.23.020
