食品级肉豆蔻酸异丙酯微乳的制备研究
2016-02-09马新辉赵晓涵曹献英
马新辉,殷 欣,赵晓涵,高 健,舒 杨,陈 健,曹献英
(海南大学食品学院,海南海口 570228)
食品级肉豆蔻酸异丙酯微乳的制备研究
马新辉,殷 欣,赵晓涵,高 健,舒 杨,陈 健*,曹献英*
(海南大学食品学院,海南海口 570228)
本文以肉豆蔻酸异丙酯为原料,筛选出肉豆蔻酸异丙酯空白微乳的最佳配方。首先采用伪三元相图法,以微乳区面积为指标,筛选出表面活性剂和助表面活性剂;探究表面活性剂与助表面活性剂质量之比Km值与亲水亲油平衡值(HLB值)对微乳形成的影响,然后以离心和染色实验来判断微乳的稳定性和构型。结果表明:当以肉豆蔻酸异丙酯作为油相,吐温80复配司盘80作为复合表面活性剂,无水乙醇为助表面活性剂(表面活性剂∶助表面活性剂∶IPM=4∶2∶4),且Km=2∶1,HLB=7.5时,形成的微乳液稳定性最好。此条件下,油包水型微乳的最大载水量为15.3%。因此可以说明伪三元相图法制备肉豆蔻酸异丙酯方法方便可行。
伪三元相图,Km值,HLB值,微乳区面积
微乳液是表面活性剂、助表面活性、油和水按照一定比例混合后自发形成的均一透明溶液[1]。它具有以下特点:粒径小且均一,粒径在10~100 nm之间;热力学稳定,低速离心30 min不分层;制备简单;粘度小。近年来,微乳化技术获得快速的发展,已广泛应用于石油工业[2]、材料制备[3]、农药保存[4]、中医制药[5-6],但在食品中的应用还相对较少。
近年来,食品级微乳液克服了溶解性小和生物利用率低的难题,已成为生物活性物质的载体[7]。食品级微乳液的难题是表面活性剂的毒性问题。目前,常用的食品级表面活性剂有大豆卵磷脂[8-9]、山梨醇酐单油酸酯[10](吐温)、聚氧乙烯山梨醇酐单油酸酯(司盘)、蔗糖脂肪酸酯[11]等。研究表明,复配表面活性剂乳化效果比单一表面活性剂乳化效果好,微乳区域面积较大,稳定性好[12]。常用的助表面活性剂有乙醇[13]和丙三醇[14]。
伪三元相图法[15-16]是研究微乳的主要手段之一,我们可以通过微乳相面积的大小来判断微乳的相对稳定程度。本实验选用肉豆蔻酸异丙酯作为油相,吐温和司盘复配作为表面活性剂,通过伪三元相图筛选出表面活性剂和助表面活性剂;并探究不同亲水亲油值(HLB值)、表面活性剂与助表面活性剂的质量比(Km值)对微乳区域面积的影响,旨在为肉豆蔻酸异丙酯为油相的微乳体系在食品中的应用奠定基础。
1 材料与方法
1.1 材料与仪器
肉豆蔻酸异丙酯(IPM),聚氧乙烯山梨醇酐单油酸酯80(吐温80),聚氧乙烯山梨醇酐单油酸酯20(吐温20),山梨醇酐单油酸酯80(司盘80),无水葡萄糖,丙三醇,无水乙醇,聚乙二醇400(PEG 400)等均为分析纯;去离子水 实验室自制。
label dancer混匀器 上海微川精密仪器有限公司;EL602电子天平 梅特勒-托利多仪器有限公司;Master-S15UVF超纯水机 上海和泰仪器有限公司。
1.2 实验方法
1.2.1 伪三元相图的绘制 采用加水滴定法绘制伪三元相图。将表面活性剂(S)、助表面活性剂(COS)以及油相的混合物按一定比例混匀,然后逐滴滴加去离子水来绘制微乳体系的伪三元相图。将肉豆蔻酸异丙酯和表面活性剂[17]按1∶9、2∶8、3∶7、4∶6、5∶5、6∶4、7∶3、8∶2、9∶1(w/w)总量为10 g各3份,每份均在室温25 ℃下混匀,逐滴滴加去离子水,观察体系由澄清至浑浊的现象,记录形成微乳区临界点时的各组百分比。以复合表面活性剂为伪三元相图的一个顶点、油相、水相各为1个顶点。据各组分在临界点时所占总量的百分比来确定,用origin7.5将各临界点连成曲线,绘制伪三元相图。
1.2.2 表面活性剂的筛选 无水乙醇作为助表面活性剂,分别选用吐温20、吐温80与司盘80复配的表面活性剂,每组采用1.2.1中的加水滴定法制备微乳,并绘制伪三元相图,根据最大载水量(即微乳区面积大小,下同)选择合适的表面活性剂。
1.2.3 助表面活性剂的筛选 吐温80和司盘80复配的表面活性剂为复合表面活性剂,分别选用乙醇、丙三醇、PEG400作为助表面活性剂,每组采用1.2.1中的加水滴定法制备微乳并绘制伪三元相图,根据最大载水量选择助表面活性剂。
1.2.4 HLB值的确定 以吐温80和司盘80复配成不同HLB值的复合表面活性剂,根据表面活性剂的复配原则[18],复配的质量如下:
表1 复合表面活性剂组成及HLB值
Table 1 Surfactant consistence and their HLB

HLB6065707580吐温801722273237司盘809085807570
以复配的表面活性剂作为乳化剂,无水乙醇作为助表面活性剂,每组采用1.2.1中的加水滴定法制备微乳并绘制伪三元相图,根据微乳区域面积的大小选择合适的HLB值。
1.2.5 Km值的确定 将1.2.2中确定的表面活性剂与1.2.3中确定的助表面活性剂按质量比分别为1∶1、2∶1、3∶1、4∶1进行复配,每组按1.2.1方法制备微乳并绘制伪三元相图,根据微乳区面积大小选择合适的Km值。
1.2.6 微乳的稳定性 取适量微乳样品,置于离心机中,以4000 r/min的速度离心30 min,观察微乳性状的变化。以5%葡萄糖溶液作为水相,IPM作为油相,司盘80/吐温80作为表面活性剂,乙醇为助表面活性剂,绘制伪三元相图,观察微乳区域面积。以0.9%氯化钠溶液[19-20]作为水相,IPM作为油相,司盘80/吐温80作为表面活性剂,乙醇为助表面活性剂,绘制是伪三元相图,观察微乳区域面积。
1.2.7 微乳构型的鉴定 取相同体积的微乳液2份,分别加入亚甲基蓝染料和苏丹红染料溶液各2滴,静置观察,根据红色染料和蓝色染料的扩散速度判断微乳的构型[21]。
2 结果与讨论
2.1 表面活性剂的确定
采用不同表面活性剂制备微乳,其结果如图1所示。图1a、图1b分别是吐温80/司盘80和吐温20/司盘80为表面活性剂、乙醇为助表面活性剂时微乳体系的拟三元相图,其中阴影区域代表微乳区,空白部分为非微乳区,(图2~图4同)。由图1可以看出,当IPM为油相、乙醇为助表面活性剂时,吐温80/司盘80微乳区域面积较大,这可能是因为吐温80的亲水性高于吐温20,在与司盘80复配的过程中仍然具有较高的水增溶性;此时,表面活性剂与助表面活性剂形成的体系水溶性较好。因此,选择吐温80/司盘80复配作为复合表面活性剂。
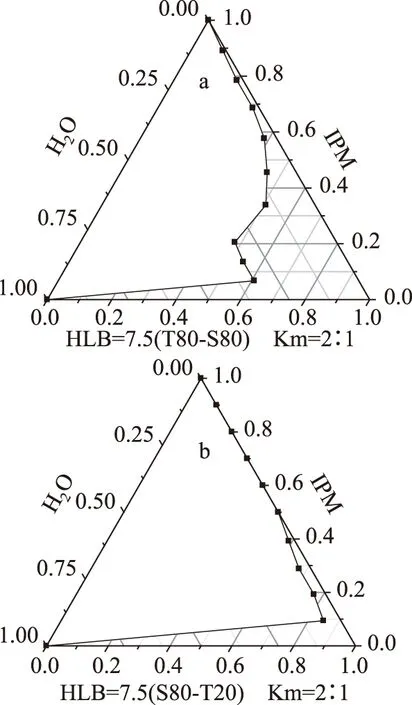
图1 不同表面活性剂时微乳体系伪三元相图(n=3)Fig.1 Pseudo-ternary phase diagram of microemulsion with different surfactant(n=3)
2.2 助表面活性剂的筛选
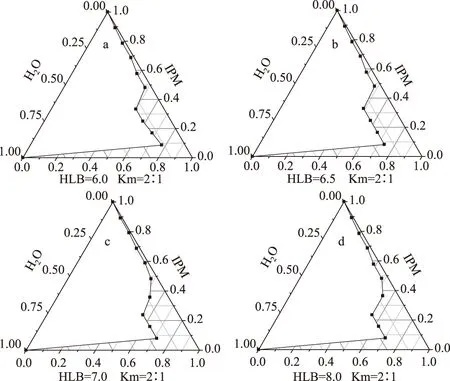
图2 不同HLB值时微乳体系伪三元相图(n=3)Fig.2 Pseudo-ternary phase diagram of microemulsion with different HLB(n=3)
适宜的助表面活性剂可以插在表面活性剂分子之间,形成混合吸附层从而促进微乳的形成。采用丙三醇和PEG400作为助表面活性剂时,只有个别点可以形成微乳,难以绘制微乳区域。从图1可以看出,采用无水乙醇作为助表面活性剂时,微乳区域面积明显大于丙三醇和PEG400;因此,选择无水乙醇作为助表面活性剂。

图3 不同Km值时微乳体系伪三元相图(n=3)Fig.3 Pseudo-ternary phase diagram of microemulsion with different Km(n=3)
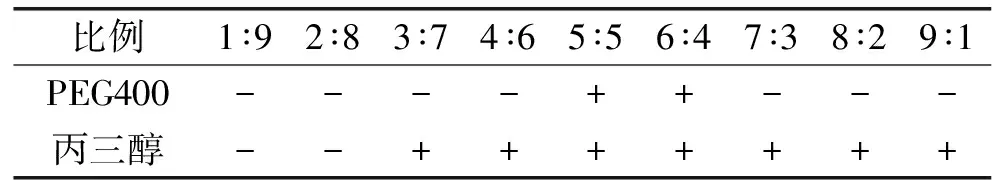
比例1∶92∶83∶74∶65∶56∶47∶38∶29∶1PEG400----++---丙三醇--+++++++
注:比例代表复合表面活性剂与油相的比例;-代表未形成微乳;+代表有微乳形成,但含水量小于体系的1%。
2.3 微乳相图的影响因素
2.3.1 HLB值对相图的影响 表面活性剂分子结构中,既含有亲水基团又含有亲油基团,使用表面活性剂分子的亲水亲油值(即HLB值)来衡量分子的亲水性和亲油性的强弱,将表面活性剂的分子结构、性能和用途连接起来。以司盘80和吐温80复配出不同HLB值的乳化剂,考察了复合乳化剂的HLB值对微乳区域和稳定性的影响,结果见图2a~图2d。从图2可以看出,HLB=6.0、6.5、7.0、7.5复合表面活性剂,微乳区域面积呈现增加趋势。与图1a对比可知,在HLB值=7.5时,微乳区域面积最大;当HLB=8.0时,微乳区域面积反而减小。研究表明,不同油相形成微乳时所需要的HLB值是和油相本身的HLB值一致的。因此,推测肉豆蔻异丙酯的HLB在7.5左右。
2.3.2 Km值对微乳区形成的影响 以无水乙醇为助表面活性剂,肉豆蔻酸异丙酯为油相,HLB=7.5的吐温80和司盘80复配的表面活性剂,制备不同Km值的微乳体系并绘制伪三元相图,结果见图3a~图3c。与图1a对比可知,当Km值从1∶1、2∶1、3∶1、4∶1时,即助表面活性剂增加时,微乳区域面积先增加后减少,且在Km=2∶1,微乳区域面积最大。这说明无水乙醇作为助表面活性剂,并不是越多越好。助表面活性剂可以降低表面张力,调节表面活性剂的HLB值,增加界面膜的强度。当乙醇含量较低时,乙醇存在于界面膜上。随着乙醇的增加,水相和油相的连接更加紧密,微乳的稳定性增加;而过量的无水乙醇溶于水相,从而打破油相和水相的界面膜,破坏微乳的形成。从图3a~图3c中还可以看出,一定范围内,Km值越大,即无水乙醇含量越小时,越有可能形成微乳;当表面活性剂含量较大时,极易形成微乳液,Km值对微乳形成的影响减小,推测可知表面活性剂含量极高时,对水无限增溶。
2.4 微乳的稳定性
以肉豆蔻酸异丙酯为油相、乙醇为助表面活性剂、吐温80/司盘80为表面活性剂,分别以5%葡萄糖和0.9% NaCl为水相,绘制三元相图见图4a、图4b。
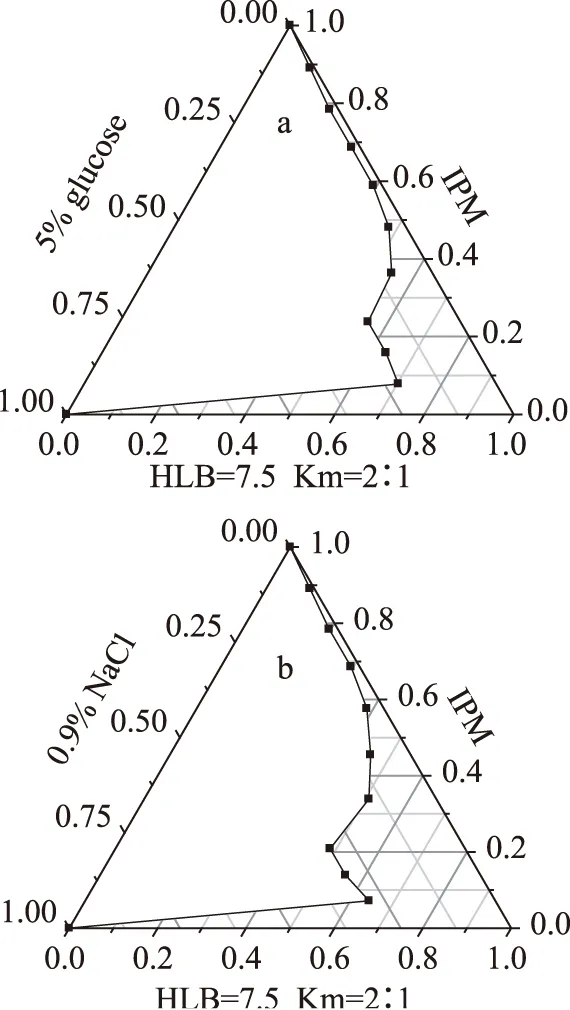
图4 不同水相时微乳体系伪三元相图(n=3)Fig.4 Pseudo-ternary phase diagram of microemulsion with different water(n=3)
从图4a可以看出,5%葡萄糖溶液形成的微乳区域面积变小,这可能是因为葡萄糖分子量较大,容易造成分子聚集,形成粒径100 nm以上的微粒从而破乳;图4b与图1a对比可知,0.9% NaCl溶液并没有对微乳区域面积造成影响,这可能是因为NaCl分子量较小,未引起颗粒聚集而破乳。
制备的微乳液在4000 r/min下离心30 min,均无分层,证明微乳液的稳定性良好。
2.5 微乳的构型
苏丹红是油溶性染料,在油相中扩散较快;亚甲基蓝为水溶性染料,在水相中扩散较快。两种染料分别加入微乳,若蓝色的扩散速度大于红色的扩散速度,则为水包油型微乳;反之,则为油包水型微乳。经染色实验,可以判断出HLB=7.5,Km=2∶1的临界点处,当表面活性剂与油相IPM的质量比分别为4∶6,5∶5,6∶4,微乳为油包水型,最大含水量分别为3.8%、9.1%、15.3%;当吐温80和司盘80复配的表面活性剂与助表面活性剂无水乙醇的质量比分别为7∶3、8∶2、9∶1,微乳为水包油型,最大含水量分别为31.5%、32.4%、32.4%。
3 结论
以肉豆蔻酸异丙酯为油相制备微乳时,选用无水乙醇作为助表面活性剂,选用吐温80/司盘80复合作为表面活性剂;肉豆蔻酸异丙酯/吐温80-司盘80/乙醇/水体系,当HLB值=7.5时,微乳区域面积最大,推测肉豆蔻酸异丙酯的HLB在7.5附近;葡萄糖可以减少肉豆蔻酸异丙酯/吐温80-司盘80/乙醇/水微乳体系的载水量,氯化钠对微乳体系影响较小。肉豆蔻酸异丙酯/吐温80-司盘80/乙醇/水微乳体系中,当表面活性剂、助表面活性剂与油相IPM的质量比分别为4∶2∶4时,形成的油包水型微乳的最大载水量为15.3%。
[1]Chiappisi L,Noirez L,Gradzielski M. A journey through the phase diagram of a pharmaceutically relevant microemulsion system[J]. Journal of Colloid and Interface Science,2016,473:52-59.
[2]吴珣,鲁长波,谷晓昱. 正构醇的碳链长度对柴油微乳液组成和性能的影响[J]. 石油化工,2011,40(10):1068-1072.
[3]郑建东,杨慧慧,温志远. TX-100反相微乳液体系稳定性的研究[J]. 应用化工,2010(5):675-678.
[4]陈圆,张龙,李佳佳,等. 生物相容型氯氰菊酯农药微乳剂的制备与性质研究[J]. 湖北农业科学,2013(6):1312-1314.
[5]杨蒙蒙,张琰,刘新友,等. 中药挥发油微乳与伪三元相图的研究[J]. 中药材,2011(8):1288-1292.
[6]Ma Q,Davidson P M,Zhong Q. Antimicrobial properties of microemulsions formulated with essential oils,soybean oil,and Tween 80[J]. International Journal of Food Microbiology,2016,226:20-25.
[7]Ravanfar R,Tamaddon A M,Niakousari M,et al. Preservation of anthocyanins in solid lipid nanoparticles:Optimization of a microemulsion dilution method using the Placket-Burman and Box-Behnken designs[J]. Food Chemistry,2016,199:573-580.
[8]张奕,蔡建周,魏建业,等. 卵磷脂/正丙醇/肉豆蔻酸异丙酯/水微乳体系的相结构研究[J]. 分析测试学报,2014(1):7-12.
[9]鲁莹,蒋雪涛,曾仁杰. 卵磷脂微乳的制备与理化性质考察[J]. 药学学报,2000,35(1):52-55.
[10]赵嘉敏,陈中,林伟锋. 吐温-80制备食品级微乳的稳定性评价[J]. 食品与发酵工业,2011(3):75-78.
[11]钱伟,张春枝,吴文忠. O/W型微乳法制备纳米植物甾醇酯[J]. 安徽农业科学,2009(8):3771-3772.
[12]赵姗,范青. 复合乳化剂对微乳成乳区域的影响[J]. 大连医科大学学报,2008(4):325-328.
[13]吴芳,田一农,解新安,等. 食品级Tween 80微乳对红茶茶汤沉淀控制作用的研究[J]. 食品工业科技,2014(9):264-268.
[15]田进军,薛艳,候振健. 伪三元相图法制备O/W型蜂胶微乳[J]. 食品与机械,2011(3):127-129.
[16]Wei B,Wang L,Wang Y,et al. In situ growth of manganese oxide on 3D graphene by a reverse microemulsion method for supercapacitors[J]. Journal of Power Sources,2016,307:129-137.
[17]Rakesh Kumar S K V R. Evaluation and Optimization of Water-in-Oil Microemulsion Using Ternary Phase Diagram and Central Composite Design[J]. Journal of Dispersion Science and Technology,2015.
[18]白静,冯彩霞,杨青松,等. Span80-Tween60/液体石蜡/AM/AA反相微乳液体系稳定性研究[J]. 当代化工,2012(9):919-921.
[19]颜秀花.β-胡萝卜素微乳制剂的研究[D]. 无锡:江南大学,2008.
[20]Xu Z,Jin J,Zheng M,et al. Co-surfactant free microemulsions:Preparation,characterization and stability evaluation for food application[J]. Food Chemistry,2016,204:194-200.
[21]刘安刚,李引乾,孙娇,等. 氟苯尼考纳米乳的制备及品质评价[J]. 西北农业学报,2011(5):44-49.
Preparation of food grade isopropyl myristate microemulsion
MA Xin-hui,YIN Xin,ZHAO Xiao-han,GAO Jian,SHU Yang,CHEN Jian*,CAO Xian-ying*
(Department of food college,Hai Nan University,Haikou 570228,China)
In this research,the purpose was to screen out the best formulation of isopropyl myristate(IPM). Firstly,surfactants,co-surfactants,the quality ratio of them(Km)and hydrophilic lipophilic balance(HLB)values were determined by using the pseudo-ternary phase diagrams and the area of microemulsions(MEs)as the index. And the stability and configuration of MEs were measured by centrifugation and dyeing. The results showed that the stability of MEs was well when the IPM as the oil phase,Tweeen80 combined with Span80 as the composite surfactant,ethanol as the co-surfactant(IPM∶Tweeen80 conbined with Span80∶ethanol=4∶4∶2),Km=2∶1 and HLB=7.5. Under this condition,the maximum amount of water contained in the water-in-oil MEs was 15.3%. So it was possible and convenient for the pseudo-ternary phase diagrams to prepare MEs.
pseudo-ternary phase diagrams;Km;HLB;microemulsion area
2016-06-06
马新辉(1993-),男,硕士研究生,研究方向:食品科学,E-mail:15993613885@163.com。
*通讯作者:陈健(1985-),男,博士,讲师,研究方向:天然产物的加工与利用,E-mail:chenjian19850702@163.com。 曹献英(1962-),女,博士,教授,研究方向:食品质量与安全,E-mail:cxying_02@163.com。
国家自然科学基金项目(31501497)。
TS255.4
A
1002-0306(2016)23-0049-04
10.13386/j.issn1002-0306.2016.23.001
