犬血浆中托芬那酸高效液相色谱检测法的建立
2016-02-07李龙飞李宇琛吴天兴夏良友曹杰王双卜仕金
李龙飞,李宇琛,吴天兴,夏良友,曹杰,王双,卜仕金
(1.扬州大学兽医学院,江苏扬州 225009;2.江苏省动物重要疫病与人兽共患病防控协同创新中心,江苏扬州 225009)
犬血浆中托芬那酸高效液相色谱检测法的建立
李龙飞1,2,李宇琛1,2,吴天兴1,2,夏良友1,2,曹杰1,2,王双1,2,卜仕金1*
(1.扬州大学兽医学院,江苏扬州 225009;2.江苏省动物重要疫病与人兽共患病防控协同创新中心,江苏扬州 225009)
为了建立高效液相色谱(HPLC)法测定地犬血浆中托芬那酸的含量,采用Agilent ZORBAX Eclipse Plus C18(250 mm×4.6 mm,5 μm)色谱柱,流动相使用甲醇∶乙腈∶0.05 M醋酸钠(pH=4.6)为36.5∶36.5∶27,流速为0.7 mL/min,柱温为35 ℃,检测波长为290 nm。结果: 托芬那酸的血浆药物浓度在0.05~10.0 μg/mL范围内,线性关系良好(r=0.9993);最低检出限为0.025 μg/mL;定量限为0.05 μg/mL,平均回收率为85%,批内和批间系数分别小于11%和6%。本方法简便准确、快速可靠,适用于犬血浆中托芬那酸的药动学和相对生物利用度研究。
高效液相色谱;托芬那酸;犬血浆
托芬那酸(TA),N(2-甲基-3-氯苯基)-邻氨基苯甲酸是一种非甾体抗炎药物(NSAID),结构与甲氯芬酸类似[1]。非甾体抗炎药主要用于人类和动物的止痛和缓解肌肉骨骼疾病,对于治疗滑膜炎、关节炎、痛风具有较强作用。它的主要作用原理为抑制环氧化酶,减少花生四烯酸向前列腺素转化,从而抑制炎症介质前列腺素的合成。此外,托芬那酸还能够抑制β-葡萄糖醛酸酶、血清中血栓素B2和缓激肽诱导的肿胀。TA的甘氨酸及葡萄糖醛酸结合物形式通过尿液排泄(90%),没有严重的特异性的毒性反应在兽医临床上具有非常广阔的市场前景[2]。目前,对于托芬那酸血药浓度测定方法国内报道的很少,通过研究,提供一种简单、快速、准确的犬血浆中托芬那酸的含量的测定方法,可用于该药物的药动学和相对生物利用度的研究。
1 材料
1.1 药品与试剂 托芬那酸标准品:含量100%,批号:BP 907-F67029,货号Y0000154,由青岛农业大学郝智慧教授馈赠;甲醇、乙腈,均为色谱纯,美国TEDIA公司;醋酸,醋酸钠,均为色谱纯,德国CNW公司;超纯水。
1.2 仪器 高效液相色谱仪:Agilent1260型高效液相色谱仪,Agilent公司;色谱柱:ZORBAX Eclipse Plus C18(250 mm×4.6 mm,5 μm),Agilent公司UPH-11-20T型优普超纯水制造系统:成都超纯科技有限公司;RE-52旋转蒸发器:上海亚荣生化仪器厂;N-EVAPTM112型干浴氮吹仪(美Organo-mation公司KS-250D超声仪:宁波科生仪器厂;WH-1微型漩涡混合仪:上海沪西分析仪器厂有限公司;TGL-16C型高速离心机:上海安亭科学仪器厂。KS-250D超声仪:宁波科生仪器厂;WH-1微型漩涡混合仪:上海沪西分析仪器厂有限公司;TGL-16C型高速离心机:上海安亭科学仪器厂。
2 方法
2.1 血浆中托芬那酸测定方法的建立
2.1.1 色谱条件 色谱柱:ZORBAX Eclipse Plus C18(250 mm×4.6 mm,5 μm);流动相:甲醇∶乙腈∶0.05 M 醋酸钠(pH 4.6)=36.5∶36.5∶27,流速:1 mL/min;柱温:35 ℃;进样量:20 μL;紫外检测波长:λ为290 nm。
2.1.2 标准工作液的制备 精密称取托芬那酸标准品100 mg于100 mL容量瓶中,用乙腈溶解并定容到刻度线,及配成浓度为1000 μg/mL托芬那酸标准储备液,-20 ℃下保存。经流动相稀释成0.5、1、2、5、10、20、100 μg/mL标准工作液备用。
2.1.3 血浆样品的制备与保存 犬卧姿保定后经前肢静脉采血,采血完毕后解除保定,在规定范围内自由活动,每次采血量约2~3 mL,给动物补充适量的5%葡萄糖生理盐水。血样采集后置于肝素浸润并烘干的10 mL离心管内,3500 r/min离心10 min。血浆分离后于-20 ℃下保存备用。
2.1.4 血浆样品处理 将冷冻保存的血浆室温下自然解冻,吸取180 μL血浆,然后分别加入浓度为0.5、1、2、5、10、20、100 μg/mL托芬那酸标准工作液20 μL,涡旋2 min,分别配成0.05、0.1、0.2、0.5、1、2、10 μg/mL的血浆标准溶液,将200 μL的血浆标准溶液置于5 ml离心管中,加入2 mL乙腈去蛋白,混合涡旋3 min。超声10 min,4 ℃ 12000 r/min离心10 min,取上清于45 ℃氮气吹干。加入200 μL流动相溶解氮气吹干后残渣,混合涡旋3 min,12000 r/min离心10 min,取上清25 μL进样供HPLC分析。
2.1.5 标准曲线的制备 取7支5 mL塑料指形管,将冷冻保存的血浆室温下自然解冻。分别加入空白犬血浆180 μL,然后分别加入浓度为0.5、1、2、5、10、20、100 μg/mL标准工作液20 μL,按2.1.4项方法处理,并进行HPLC分析。采用外标法计算,以托芬那酸峰面积(As)与对血药浓度(C)进行加权线性回归,得回归方程,每个浓度重复3次。
2.1.6 检测限和定量限 按照“2.1.4”项处理血浆样品进样检测, 当仪器信噪比(S/N) =3 时, 对应样品中的含药浓度即为检测限;当仪器信噪比(S/N) =10时, 对应的样品中的含药浓度即为定量限。
2.1.7 回收率和精密度 取空白血浆180 μL,加入托芬那酸标准工作液(0.5、10、100 μg/mL)20 μL,制成低、中、高3个质量浓度(0.05、1、10 μg/mL)的血浆样品, 每一浓度5个样品并测定,按2.1.4项下方法处理后进行测定,以测定值与加入值之比计算回收率, 并计算批内精密度。连续 3 d 配制并测定托芬那酸浓度,考察批间精密度。
2.1.8 稳定性试验 对浓度水平为0.05、1、5 μg/mL的5个平行稳定性样品执行分析,从而评估犬血浆中托芬那酸的稳定性。按照标准曲线制备方法分别制备上述3个浓度的空白血浆添加样品后立刻对样品执行分析,以得到第0天数据;在室温(约22 ℃)下放置4、8 h后执行样品分析,在冻存(约-20 ℃)一周后执行样品分析,在冻存(约-20 ℃)一个月后执行样品分析,在三个冻融循环之后执行样品分析。将稳定性样品中检出的托芬那酸浓度与理论加标浓度做比较。
3 结果
3.1 血浆中托芬那酸检测方法的确立
3.1.1 标准曲线 托芬那酸的血浆药物浓度在0.05~10.0 μg/mL范围内,血浆药物浓度与峰面积比值呈良好的线性关系(R2=0.999)。以峰面积
为横坐标,血药浓度为纵坐标,典型的标准曲线方程为:y=63.65x+0.6054。
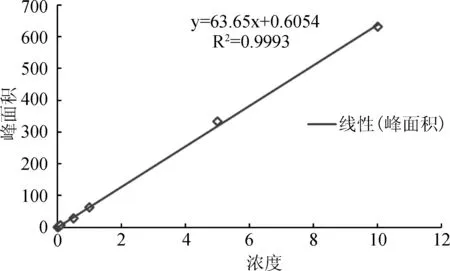
图1 托芬那酸标准曲线图
3.1.2 检测限和定量限 取信噪比S/N≥3时浓度为最低检测限,该方法检测限为0.025 μg/mL;根据精密度和准确度试验结果,取信噪比S/N≥10时浓度为最低定量限为0.05 μg/mL。
3.1.3 精密度和回收率 血浆中托芬那酸HPLC测定方法的结果表明,空白血浆添加样品在0.05~10.0 μg/mL范围内,批内和批间系数分别小于11%和6%,精密度良好;空白血浆中托芬那酸添加浓度在0.05、1和10 μg /mL时的回收率均在85%以上,回收率稳定。
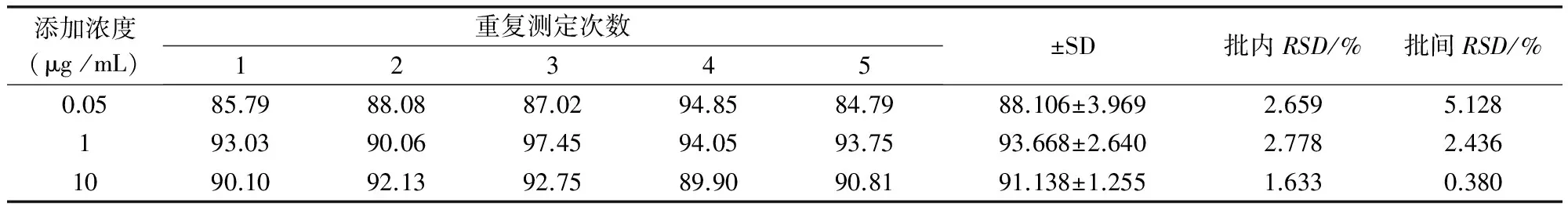
表1 血浆中空白添加托芬那酸相对回收率及精密度(n=5)
SD:标准偏差,RSD:相对标准偏差,n:平行数
3.1.4 稳定性试验 对于犬血浆中的托芬那酸而言,于-20 ℃条件下冻存时能够保持稳定1个月,在3个冻融循环之后仍可保持稳定,于室温条件(约22 ℃)下储存时可保持稳定达4 h。
3.1.5 专属性考察 在所建立的色谱条件下,分别得到托芬那酸标准品图谱、空白血浆样品的图谱、空白血浆加入标准品后的图谱。由图2-图4(横坐标为保留时间min,纵坐标为峰面积mAU)可知,空白血浆中内源性物质不干扰托芬那酸的测定,保留时间为9.14 min。
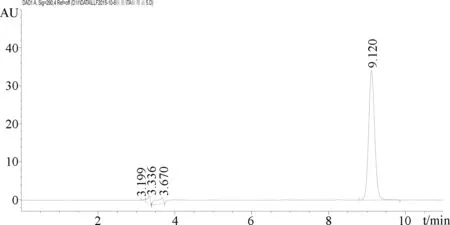
图2 托芬那酸(5 μg/mL)标准品色谱图
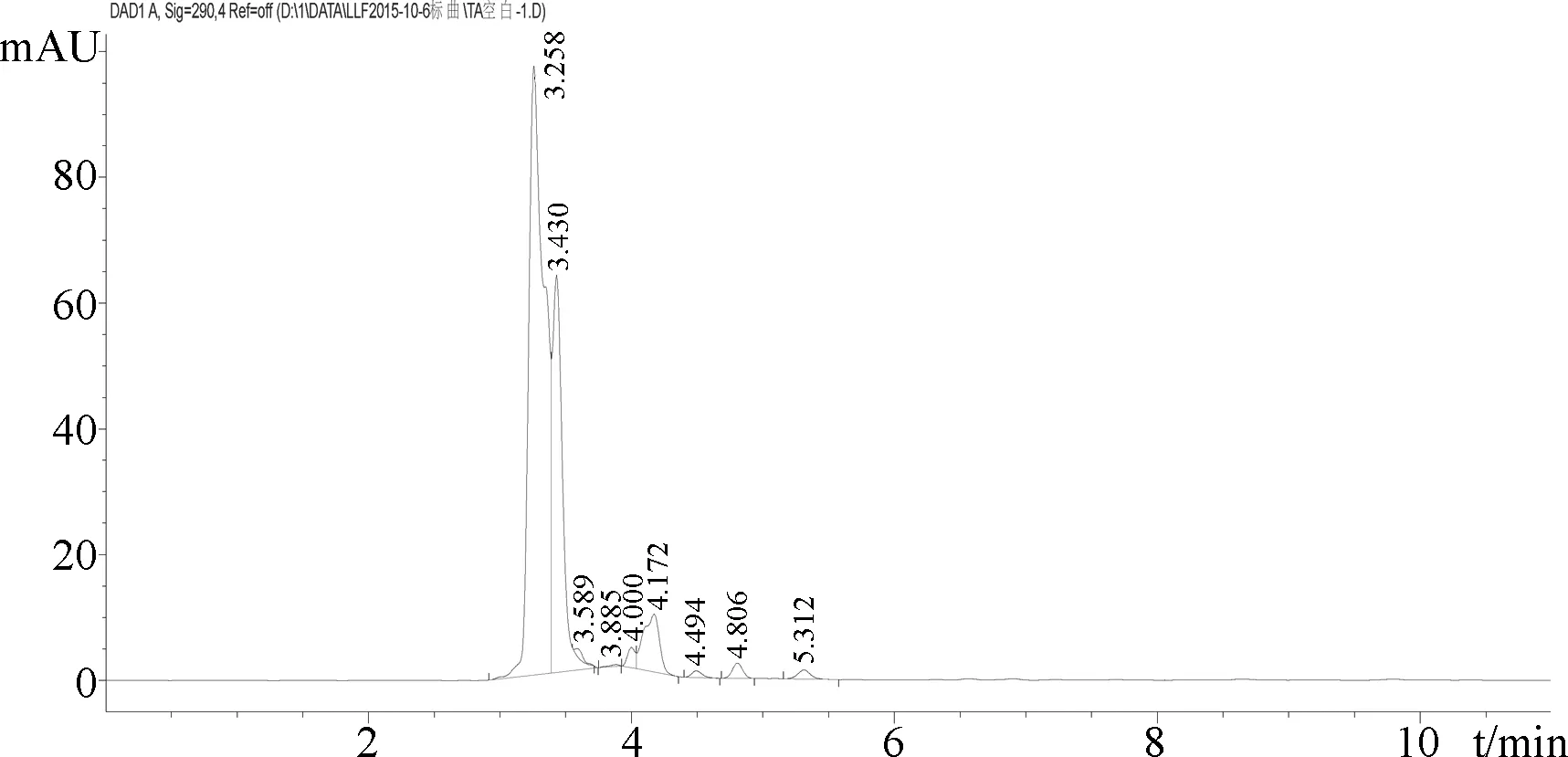
图3 空白犬血浆色谱图
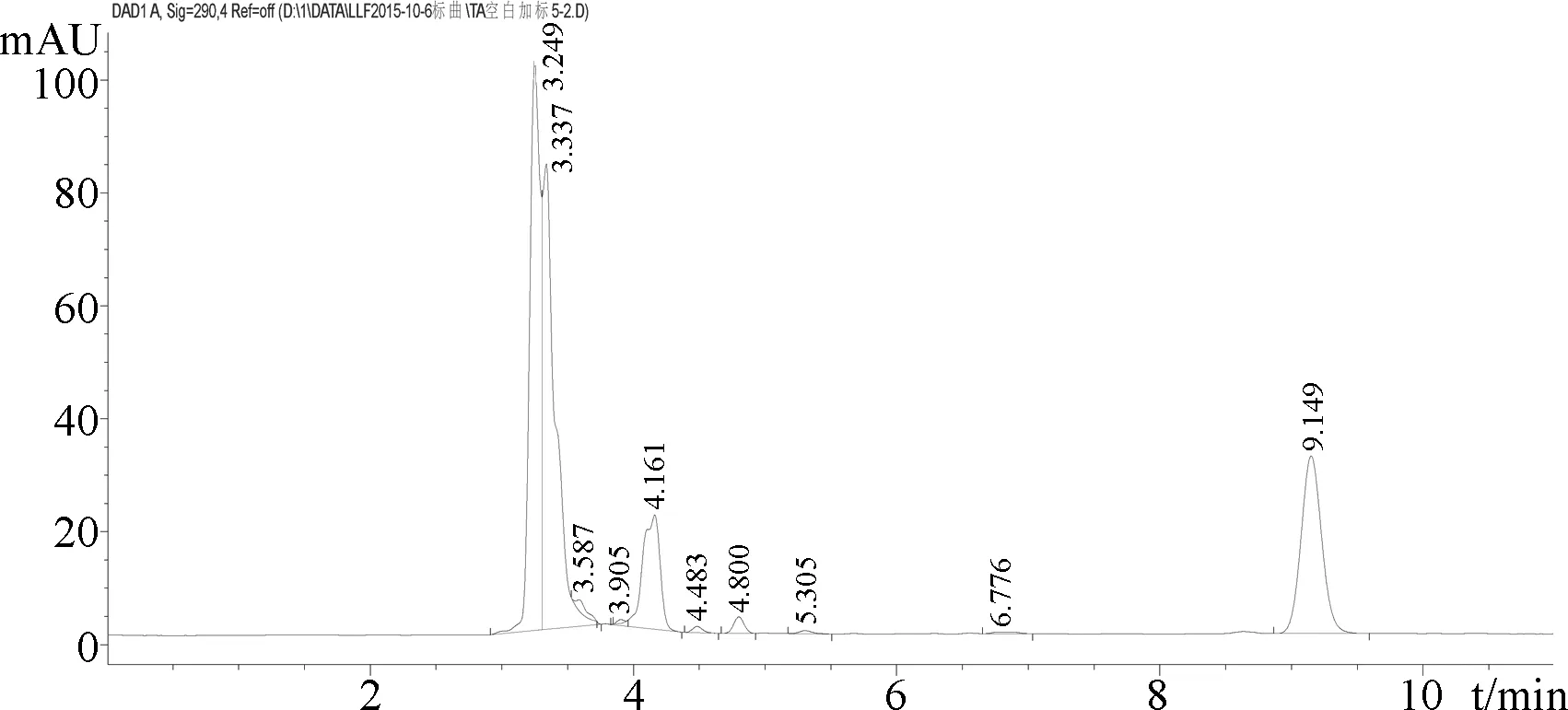
图4 空白血浆添加托芬那酸标准品(5 μg/mL)色谱图
4 讨论
高效液相色谱法 (HPLC)发展迅速已成为血药浓度检测的最佳方法之一,其优点是适用范围广,快速准确,操作简便,样品用量少,可同时测定多种药物及其活性代谢物或化合物,检测灵敏度高,一般检出限可达ng级。为此,本文建立了犬血浆中托芬那酸的高效液相色谱检测方法[3]。
托芬那酸因其良好的止痛和抗炎作用已被广泛应用于不同动物[4]。目前,国外已有托芬那酸在狗、牛、羊、大鼠、犬、人体内的药代动力学研究报道[5-8]。M.F.LANDONI等[6]用pH 3.0的枸橼酸缓冲液酸化血浆样品,用二乙醚提取,建立了牛血浆中托芬那酸浓度的HPLC检测方法。P.K.Sidhu等[8]用pH 3.0的枸橼酸缓冲液酸化血浆样品,氯仿萃取,建立了山羊血浆中托芬那酸浓度的HPLC检测方法。胡婷等[9]综述了托芬那酸在大鼠,牛,羊,犬猫等物种血液、尿液等体液中的HPLC检测方法。本试验参考上述文献报道,用乙腈替代了二乙醚或氯仿,建立了犬血浆中托芬那酸浓度的HPLC检测方法。乙腈作为蛋白沉淀剂,其一可以降低水的介电系数,其二可以使大分子表面的水层脱水,相互聚集,从而使蛋白从水中析出[10];乙腈还是良好的溶剂,托芬那酸在溶液中性质稳定,不易析出。通过高效液相色谱紫外检测器检测托芬那酸的最大吸收波长发现,在波长220和290 nm附近吸收峰最大,但由于在波长220 nm附近其他杂峰干扰明显,在波长290 nm托芬那酸吸收峰分
离明显,无杂峰干扰,故波长定为290 nm。根据托芬那酸的弱酸性,流动相PH的选择参考托芬那酸的PKa=4.1和综上文献,在PH=4.6处可保证托芬那酸的酸性官能团以单一的形式存在,从而保证了峰形的尖锐性和对称性;醋酸盐缓冲液的加入可使溶液变温和,减少对色谱柱的损坏。
本试验研究建立提取方法和色谱条件下,待测物附近无内源性物质干扰托芬那酸的测定,标准曲线在0.025~10.0 μg/mL范围内线性关系良好(R2>0.999),最低检测限和定量限分别为0.025 μg/mL和0.05 μg/mL;空白血浆中托芬那酸添加浓度在0.05、1和5 μg /mL时回收率均在85%以上。本实验建立的血浆样品中托芬那酸提取、净化和检测方法可用于托芬那酸注射在犬体内药动学研究时血药浓度测定要求。
[1] 范莹,苏勍. 托芬那酸原料药中残留溶剂顶空气相色谱测定方法的建立[J]. 实用医药杂志,2014,01:54-55.
[2] 李忠生,冯秀娟,王智群. 托芬那酸肌注后在犬体内的药物代谢动力学研究[J]. 畜牧与兽医,2016,02:67-70.
[3] 周旭平,陆彦,张中文,沈红,吴国娟. 血浆中连翘酯苷高效液相色谱检测方法的建立[J]. 中国畜牧医,2009,09:26-28.
[4] 付海宁,王巧玲,殷生章. 托芬那酸的药理毒理研究[J]. 中国兽药杂志,2010,44(8):52-56[5] Kruszewska H, Zareba T, Tyski S. Search of antimicrobialactivity of selected non-antibiotic drugs[J]. Acta Poloniae Pharmaceutica, 2002, 59: 436-439
[6] Landonib M F, Cunningham F M, Lees P. Pharmacokinetics and pharmacodynamics of tolfenamic acid in calves[J]. Research in Veterinary Science, 1996, 61: 26-32
[7] Jaussaud P, Guieu D, Bellon C,etal. Pharmacokinetics of tolfenamic acid in the horse[J]. Equine Vet J Suppl, 1992, 11: 69-72
[8] Sidhu P.K, Landoni M.F,Lees P. pharmacokinetics and pharmacodynamics interactions of tolfenamic acid and marbofloxacin in goats[J]. Research in Veterinary Science, 2006, 80, 79-90
[9] 胡婷,彭涛,邓晓军. 非甾体抗炎药残留检测方法研究进展[J]. 中国兽药杂志,2010,44(8):42-47
[10]汪芳,李冰,周绪正,等. 犬血浆中塞拉菌素含量的高效液相色谱-荧光检测方法的建立[J]. 畜牧兽医学报,2011,09:1346-1350.
(编辑:陈希)
Determination of Tolfenamic Acid in Dog by High Performance Liquid Chromatography
LI Long-fei1,2,LI Yu-chen1,2,WU Tian-xing1,2,XIA Liang-you1,2,CAO Jie1,2,WANG Shuang1,2,BU Shi-jin1*
(1.VeterinaryMedicineCollege,YangzhouUnivercity,Yangzhou225009,China;2.JiangsuCo-innovationCenterforPreventionandControlofImportantAnimalInfectiousDiseasesandZoonoses,Yangzhou225009,China)
To establish an HPLC method for quantification of tolfenamic acid in dog. The separation was performed on an Agilent ZORBAX Eclipse Plus C18(250 mm×4.6 mm,5 μm). Mobile phase: methanol∶acetonitrile∶0.05 M sodium acetate (pH=4.6) was 4.6∶36.5∶27.The column temperature was 35 ℃ and the detection wavelength was set at 290 nm.The velocity was 0.7 mL/min. Results: A good linear correlation was observed within the range of 0.05~10.0 μg/mL for tolfenamic acid (r=0.9993), the minimum detection limit was 0.025 μg/mL, limit of quantitation was 0.05 μg/mL; The average recovery was 85%. Within-run and between-run analysis less than 11% and 6% respectively. The method is simple,accurate and rapid.It could be suitable for dogs tolfenamic acid in plasma pharmacokinetic experiments.
HPLC; tolfenamic acid; dog plasma
江苏高校优势学科建设工程资助项目(PAPD);扬州大学“新世纪人才工程”资助项目
李龙飞,硕士研究生,从事兽药药理方面研究。
卜仕金。E-mail:pushijin@aliyun.com
2016-03-31
A
1002-1280 (2016) 06-0052-04
S859.79
