肿瘤退缩分级标准的对比及其在直肠癌诊治中的应用进展
2016-02-06谭伊诺陈海燕丁克峰
谭伊诺 陈海燕 丁克峰
•述评•
肿瘤退缩分级标准的对比及其在直肠癌诊治中的应用进展
谭伊诺 陈海燕 丁克峰

丁克峰教授、主任医师、博士生导师。现任浙江大学医学院附属第二医院院长助理、肿瘤外科副主任、大肠外科病区主任、浙江大学肿瘤研究所副所长。中国抗癌协会理事,中国抗癌协会大肠癌专业委员会副主任委员,中国医师协会结直肠外科委员会常委兼副秘书长,浙江省抗癌协会肿瘤转移专业委员会主任委员等职务。长期从事大肠癌综合诊治和大肠癌腹腔镜微创治疗方面的工作,率先在国内提出并开展腹腔镜辅助结直肠癌快速康复治疗模式,规范MDT模式,协助制定全国《大肠癌诊治规范》,推动我院成为“全国结直肠癌多学科综合治疗先进技术示范推广工程”首批示范医院之一。主要从事肿瘤转移和肿瘤耐药机制研究,主持并完成国家自然科学基金课题5项,卫生部课题1项,省部级课题10余项,主持临床研究3项,发表SCI及国内核心期刊论文50余篇。
随着新辅助治疗在直肠癌中的规范化推广,肿瘤退缩分级(TRG)标准逐渐引起广泛关注和重视。多项研究证实TRG与直肠癌患者新辅助治疗反应、生存预后有一定相关性,在患者生存预测、随访和临床诊疗策略等方面均有应用前景,甚至也有报道考虑将其纳入临床试验替代终点。但是目前TRG标准各异,尚未统一化、规范化,故本文旨在对目前常见TRG标准进行汇总对比,并进一步探讨其在直肠癌诊治中的临床应用。
直肠肿瘤;预后;肿瘤退缩分级;临床试验
随着新辅助治疗在多种肿瘤特别是直肠癌诊疗中的普及和应用,肿瘤对新辅助治疗的病理反应情况也引起广泛关注。新辅助治疗后病理反应往往和肿瘤恶性程度、患者生存预后等密切相关,也可能影响患者后续的治疗策略。肿瘤退缩分级(tumor regression grade,TRG)旨在将新辅助治疗后的肿瘤病理反应进行分级,通常主要针对肿瘤中的纤维化和残余肿瘤的比例来划分等级。虽然目前TRG尚未达成国际统一的标准,但较多研究数据可见TRG将病理反应进行了合理的量化,且其与患者生存预后等有一定相关性。本文旨在回顾总结目前常见的若干TRG标准,并且探讨TRG在直肠癌临床诊治决策中的应用进展。
一、TRG介绍和常见评价标准对比
肿瘤退缩分级也称为病理反应分级,是对新辅助化疗后切除的肿瘤进行病理形态学评估后的分级标准,用于对患者的化疗或靶向药物的疗效做出评估,并且预测患者预后情况。
肿瘤受到新辅助治疗后退缩反应中可见到多种不同的形态学表现,比如坏死、纤维组织增生、炎细胞浸润、细胞泡沫样变性、少量细胞不典型增生等,但不是所有肿瘤退缩均会有各种形态学特征性表现。故当前的TRG评判标准多依赖于肿瘤组织中的纤维化比例以及残存肿瘤比例。目前常见的TRG标准包括有Dworak、Mandard、Rodel及Becker等提出的标准[1-5](表1)。
Mandard标准[3]于1994年提出,用于93例食管鳞癌患者接受顺铂联合放疗的新辅助治疗后的评估。该标准首先对肿瘤大体标本的形态学表现分为三类:(1)明显见残余肿瘤,溃疡型、蕈样型和浸润型等;(2)明显肿瘤退缩;(3)瘢痕表现。在组织形态学上,分为TRG1~5等级,具体分类见表1。TRG分级与患者生存预后有明显相关性,后来的多项文献报道也有相似结果。
Becker标准是2003年根据进展期胃癌接受基于顺铂的新辅助化疗后病理评估提出的标准[1]。此项研究纳入36例患者,该标准建议评估肿瘤治疗前的浸润区域,通过残余肿瘤在原先肿瘤区域所占比例做出分级。以10%和50%为节点,分为TRG 1、2、3等级。并且TRG1a表示完全没有肿瘤残余,TRG1b表示少于10%的肿瘤残余。36例患者中有4例TRG1,9例TRG2,23例TRG3,这个分级与患者的生存情况具有独立相关性。并且在2011年,该研究团队将样本量扩大至480例,再一次证明该TRG标准可用于评估患者预后。
Dworak标准是在1997年由基于17例直肠癌接受氟尿嘧啶联合放疗的新辅助治疗患者的研究中提出的[2],共分为TRG 0~4五个等级。该标准与前面提到的标准不同,TRG0代表肿瘤无退缩,而TRG4则代表无肿瘤细胞残留。虽然最初提出时是只有17例患者的小样本研究,但目前该标准已广泛用于临床上直肠癌的病理反应评估。
Rodel标准类似Dworak标准,也是将直肠癌的疗效反应分为TRG 0~4五个等级[4]:TRG0,无明显退缩;TRG1,退缩<25%;TRG2,退缩25%~50%;TRG3,退缩>50%;TRG4,完全退缩。
其他关于直肠癌新辅助化疗后TRG的分类标准还有斯隆-凯特琳癌症纪念医院(MSKCC)提出的标准[6],美国癌症分期联合委员会(American Joint Committee On Cancer,AJCC)提出的标准[7],以及Wheeler等[5,8]提出的特定于直肠癌的肿瘤退缩分级RCRG标准,详细分级情况见表1。
二、TRG在直肠癌诊治中的应用
(一)TRG在预后评估中的预测作用
目前关于TRG与直肠癌患者预后的相关性方面有较多文献报道,但结论并非完全统一。有研究表明TRG并不是预后影响因素[9],但目前大部分均提示TRG分级对于患者生存预后有独立预测作用,往往TRG疗效反应佳的患者预后较好,较少发生局部复发、远处转移,总生存也更长。有一个Meta分析汇总了14个研究中的3 105例患者数据,其中有484例患者获得病理完全缓解(pathologic complete response,pCR),获得pCR的患者有较好的5年无病生存率(83.3% vs 65.6%),多因素回归分析后也提示pCR是独立预后影响因素[10]。也有其他类似大型分析报道提示经过多因素回归后pCR仍为独立预后因子[11]。
(二)TRG分级对于临床决策的影响
对于直肠癌新辅助放化疗后出现较好的病理反应,比如TRG分级较良好的、pCR或者临床评估完全缓解(clinical complete remission,cCR)的患者,是否仍采用传统的直肠癌根治手术方法,这值得很多临床医生去考虑及深入研究。有临床试验试图对新辅助治疗疗效反应较好的患者采取比较保守的手术方式,比如局部切除[12],甚至暂不手术而采取观察等待的措施[13-14]。例如在2013年Habr-Gama等[13]报道了一项局部进展期直肠癌患者的研究,对于行常规新辅助放化疗后通过直肠镜下未见肿块,影像评估同样阴性,即获得cCR的患者,研究者推荐患者采取观察等待的策略,每2~6个月规律体检和复查影像。若10周后有可疑残余病灶则行局部切除,切除后病理若为ypT0期,则继续观察等待并规律随访。所有观察等待策略的患者随访1年仍无疾病进展或复发证据,则定义为持续cCR。所有其余患者,即未获得cCR的患者,则补充根治性手术。最终有69例患者完成新辅助放化疗并规律随访12个月以上。总的中位随访时间达到53个月。其中有51%的患者能获得持续cCR,这部分患者的3年生存率为94%。这样的生存数据可与根治性手术相当,与此同时,这些患者的生活质量明显提高,手术相关的风险和创伤远远降低。因此,在全身状况较差或者年老患者中可尝试将TRG纳入临床决策考虑因素中。
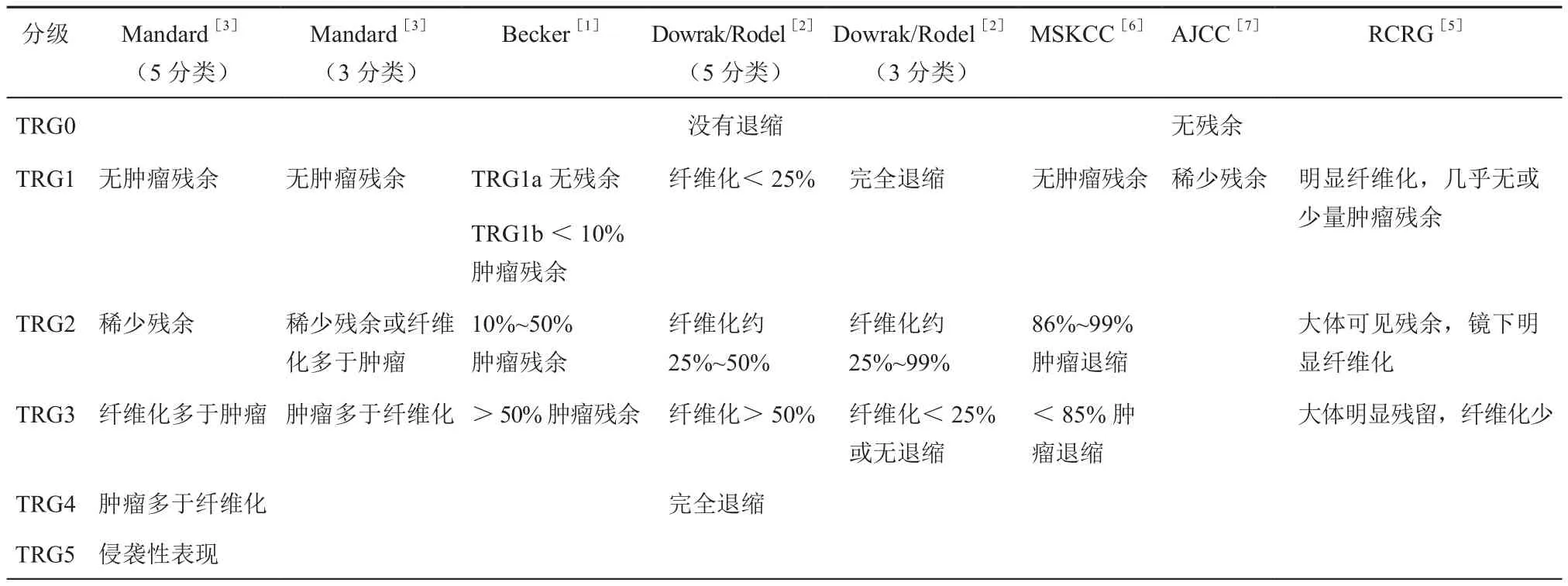
表1 目前多种TRG分级的汇总对比
TRG另外一方面的应用是在术后辅助治疗的策略选择上。欧洲一项临床研究(EORTC22921)中[15],亚组分析提示对于术前新辅助放化疗疗效较好的患者更有可能从术后辅助化疗中获益。可惜的是,研究未采用TRG对新辅助治疗疗效进行明确分级评估。
(三)TRG与临床研究的替代终点
随着目前医疗领域的快速发展,各种临床试验不断推出,对于直肠癌相关研究,大多以无疾病生存期(disease free survival,DFS)、总生存期(overall survival,OS)等为主要研究终点[16-17],但漫长的随访不仅增加人力物力,也延缓了优质临床诊疗措施的推广,故目前急需有效的替代终点以缩短研究时间。美国国立卫生研究院早在2001就提出相关建议和要求[18],明确一个合格的替代终点必须符合两点要求:(1)替代终点和真实终点的结果需吻合;(2)治疗措施对于替代终点的影响和真实终点的影响也需要吻合[19]。在研究治疗措施结束后不久就能测量出的替代终点则是所有研究者都期待的,在直肠癌的临床试验中较多纳入考虑的指标有根治性切除率、阴性环周切缘、原发灶的退缩率、pCR等[17]。虽然有多个Ⅲ期随机对照的结果表明pCR与局部控制率有一定相关性,EORTC22921研究和FFCD9203研究中也均可见5-Fu联合放疗后pCR率从3%增长到11.7%和13.7%,随访后可见局部复发率降低,但pCR率的增加并未带来DFS和OS的显著延长[20-21]。其他研究也尚未明确证实pCR可作为直肠癌临床研究中的有效的替代终点[22-24]。目前大多患者的病理反应仍是基于肿瘤对于放化疗的敏感性,故目前在临床试验中将pCR作为明确的研究终点仍缺乏有力数据。
在大多临床决策和临床研究中,将病理分级纳入考量仍以pCR为主,这个层面就是“全或无”的选择,而不是连续等级变量-TRG分级,究其原因,可能一方面是由于pCR是保证患者生存安全的基础,也符合伦理规范,另一方面则是TRG目前的各种分级系统尚未统一,尚无大规模研究对比各种分级系统的优劣,故在临床中应用仍以pCR为重点。
(四)TRG在随访中的作用
结直肠癌术后辅助治疗的临床试验中常以2年DFS为随访结局终止[25],但在直肠癌中,特别是新辅助放化疗相关的临床试验中可见到术后2年后复发的病例也不在少数。例如德国一项临床研究CAO/ARO/AIO-94研究中发现在长达10年的随访中,每年均有患者陆续地出现局部复发。而在一项对297例接收新辅助治疗的直肠癌患者长达10年的随访中发现,44例(15%)获得pCR的患者中,前2年的随访中无一例复发,最终这44例患者中只有1例患者发生了复发,故在TRG评估中获得pCR的患者可以考虑缩短术后随访时间至2年[26]。
三、挑战和展望
目前TRG分级标准越来越多的被病理科医生和临床医生关注和重视,也不断有文章强调在常规病理报告中纳入TRG分级等描述以辅助临床决策。但是目前仍缺乏统一的TRG分级标准和标准化取材流程规范,甚至肿瘤侵袭性征象、退缩表现的定义等也较难量化,在不同病理学家判定间难以获得较高一致性。欧洲直肠癌共识会议建议对于直肠癌取材至少5个蜡块,若大体检查未见明显肿瘤则建议全肿瘤区域均包埋检查。根据常规病理阅片经验可见,若有残余肿瘤,大多位于肿块外周部位,故若肿块不全部包埋切片,则可能遗漏残余肿瘤而造成假阴性。
总而言之,当前众多报道的TRG分级均提示和患者预后有相关性,在直肠癌临床诊治中也有一定作用,对于临床决策的影响已经日渐明显,但目前仍有不少待解决问题,TRG分级标准众多亟待尽早统一,不同病理学家的评判差异存在,需要尽量量化标准以减少评判差异,且其对于临床决策的选择甚至诊治指南的修订仍需要更多大样本临床试验证实。
[1]Becker K,Mueller JD,Schulmacher C,et al.Histomorphology and grading of regression in gastric carcinoma treated with neoadjuvant chemotherapy[J].Cancer,2003,98(7):1521-1530.
[2]Dworak O,Keilholz L and Hoffmann A.Pathological features of rectal cancer after preoperative radiochemotherapy[J].Int J Colorectal Dis,1997,12(1):19-23.
[3]Mandard AM,Dalibard F,Mandard JC,et al.Pathologic assessment of tumor regression after preoperative chemoradiotherapy of esophageal carcinoma.Clinicopathologic correlations[J].Cancer,1994,73(11):2680-2686.
[4]Rodel C,Martus P,Papadoupolos T,et al.Prognostic signifcance of tumor regression after preoperative chemoradiotherapy for rectal cancer[J].Journal of clinical oncology:official journal of the American Society of Clinical Oncology,2005,23(34):8688-8696.
[5]Wheeler JM,Warren BF,Mortensen NJ,et al.Quantification of histologic regression of rectal cancer after irradiation:a proposal for a modifed staging system[J].Diseases of the colon and rectum,2002,45(8):1051-1056.
[6]Quah HM,Chou JF,Gonen M,et al.Pathologic stage is most prognostic of disease-free survival in locally advanced rectal cancer patients after preoperative chemoradiation[J].Cancer,2008,113(1):57-64.
[7]Zhang LN,Xiao WW,Xi SY,et al.Pathological Assessment of the AJCC Tumor Regression Grading System After Preoperative Chemoradiotherapy for Chinese Locally Advanced Rectal Cancer[J].Medicine,2016,95(3):e2272.
[8]Wheeler JM,Dodds E,Warren BF,et al.Preoperative chemoradiotherapy and total mesorectal excision surgery for locally advanced rectal cancer:correlation with rectal cancer regression grade[J].Diseases of the colon and rectum,2004,47(12):2025-2031.
[9]Pucciarelli S,Toppan P,Friso ML,et al.Complete pathologic response following preoperative chemoradiation therapy for middle to lower rectal cancer is not a prognostic factor for a better outcome[J].Diseases of the colon and rectum,2004,47(11):1798-1807.
[10]Maas M,Nelemans PJ,Valentini V,et al.Long-term outcome in patients with a pathological complete response after chemoradiation for rectal cancer:a pooled analysis of individual patient data[J].The Lancet Oncology,2010,11(9):835-844.
[11]Patel UB,Taylor F,Blomqvist L,et al.Magnetic resonance imagingdetected tumor response for locally advanced rectal cancer predicts survival outcomes:MERCURY experience[J].Journal of clinical oncology:official journal of the American Society of Clinical Oncology,2011,29(28):3753-3760.
[12]Pucciarelli S,De Paoli A,Guerrieri M,et al.Local excision after preoperative chemoradiotherapy for rectal cancer:results of a multicenter phase II clinical trial[J].Diseases of the colon and rectum,2013,56(12):1349-1356.
[13]Habr-Gama A,Sabbaga J,Gama-Rodrigues J,et al.Watch and wait approach following extended neoadjuvant chemoradiation for distal rectal cancer:are we getting closer to anal cancer management?[J].Diseases of the colon and rectum,2013,56(10):1109-1117.
[14]Maas M,Beets-Tan RG,Lambregts DM,et al.Wait-and-see policy for clinical complete responders after chemoradiation for rectal cancer[J].Journal of clinical oncology:official journal of the American Society of Clinical Oncology,2011,29(35):4633-4640.
[15]Bosset JF,Collette L,Calais G,et al.Chemotherapy with preoperative radiotherapy in rectal cancer[J].The New England journal of medicine,2006,355(11):1114-1123.
[16]Kockerling F,Raymond MA,Altendorf-Hofmann A,et al.Infuence of surgery on metachronous distant metastases and survival in rectal cancer[J].Journal Of Clinical Oncology,1998,16(1):324-329.
[17]Glynne-Jones R,Mawdsley S,Pearce T,et al.Alternative clinical end points in rectal cancer--are we getting closer?[J].Annals of oncology:official journal of the European Society for Medical Oncology /ESMO,2006,17(8):1239-1248.
[18]De Gruttola VG,Clax P,DeMets DL,et al.Considerations in the evaluation of surrogate endpoints in clinical trials:Summary of a National Institutes of Health Workshop[J].Controlled Clinical Trials,2001,22(5):485-502.
[19]Buyse M and Molenberghs G.Criteria for the validation of surrogate endpoints in randomized experiments[J].Biometrics,1998,54(3):1014-1029.
[20]Bosset JF,Calais G,Mineur L,et al.Preoperative radiation(PreopRT)in rectal cancer:Effect and timing of additional chemotherapy(CT)5-year results of the EORTC 22921 trial[J].Journal Of Clinical Oncology,2005,23(16):247S-247S.
[21]Conroy T,Bonnetain F,Chapet O,et al.Preoperative(preop)radiotherapy(RT)+5FU/folinic acid(FA)in T3,4 rectal cancers:Preliminary results of the FFCD 9203 randomized trial[J].Journal Of Clinical Oncology,2004,22(14):276S-276S.
[22]Sauer R,Becker H,Hohenberger W,et al.Preoperative versus postoperative chemoradiotherapy for rectal cancer[J].New England Journal Of Medicine,2004,351(17):1731-1740.
[23]Gerard J,Bonnetain F,Conroy T,et al.Preoperative concurrent chemoradiotherapy(CT-RT)improves local control in T3-4 rectal cancers.Results of the FFCD 9203 randomized trial[J].Ejc Supplements,2005,3(2):170.
[24]Bosset J-F,Collette L,Calais G,et al.Chemotherapy with preoperative radiotherapy in rectal cancer[J].New England Journal Of Medicine,2006,355(11):1114-1123.
[25]Sargent DJ,Patiyil S,Yothers G,et al.End points for colon cancer adjuvant trials:observations and recommendations based on individual patient data from 20,898 patients enrolled onto 18 randomized trials from the ACCENT Group[J].Journal of clinical oncology :official journal of the American Society of Clinical Oncology,2007,25(29):4569-4574.
[26]Guillem JG,Chessin DB,Cohen AM,et al.Long-term oncologic outcome following preoperative combined modality therapy and total mesorectal excision of locally advanced rectal cancer[J].Annals of surgery,2005,241(5):829-836;discussion 836-828.
Criteria of tumor regression grade and its application in diagnosis and treatment of rectal cancer
TanYinuo,Chen Haiyan,Ding Kefeng.Department of Surgical Oncology,The Second Affliated Hospital of Zhejiang Medical University,Hangzhou 310009,China
Ding Kefeng,Email:dingkefeng@zju.edu.cn
Along with the neoajuvant treatment popularized in rectal cancer treatment,tumor regression grade(TRG)has gradually attracted broad attention.Several studies have validated that TRG correlated well with neoajuvant treatment response and prognosis of patients,thus TRG has broad application prospect in prognosis prediction,follow-up and clinical decision,some other researches began to consider it as a surrogate endpoint in clinical trials.However,different systems of TRG couldn′t be unified and standardized.This review was to make a comparison of several popular systems of TRG and explore the clinical application of TRG in rectal cancer treatment.
Rectal neoplasms;Prognosis;Tumor regression grade;Clinical trial
2016-07-19)
(本文编辑:杨明)
10.3877/cma.j.issn.2095-3224.2016.06.001
2014年中国国家卫生行业公益性基金项目(No.201402015);国家自然科学基金项目(No.81272455,81472664);浙江省重点研发项目(No.2016CG1360721)
310009 杭州,浙江大学医学院附属第二医院肿瘤外科
丁克峰,Email:dingkefeng@zju.edu.cn
谭伊诺,陈海燕,丁克峰.肿瘤退缩分级标准的对比及其在直肠癌诊治中的应用进展[J/CD].中华结直肠疾病电子杂志,2016,5(6):458-462.
