碳纳米管负载二氧化钛的制备及其对甲基橙的光催化降解
2016-02-05王文一王恩霞霍腾波朱刘勇山伯晋连伟涛李银山
王文一,王恩霞,霍腾波,朱刘勇,山伯晋,连伟涛,李银山
(1.天津工业大学材料科学与工程学院,天津 300387;2.天津工业大学省部共建分离膜与膜过程国家重点实验室,天津 300387)
碳纳米管负载二氧化钛的制备及其对甲基橙的光催化降解
王文一,王恩霞,霍腾波,朱刘勇,山伯晋,连伟涛,李银山
(1.天津工业大学材料科学与工程学院,天津 300387;2.天津工业大学省部共建分离膜与膜过程国家重点实验室,天津 300387)
采用溶胶-凝胶法,以钛酸四丁酯为前驱体,羧基化多壁碳纳米管(oCNTs)为载体,乙醇为溶剂,冰醋酸为抑制剂,成功制备了TiO2纳米粒子负载碳纳米管的复合光催化剂(TiO2/oCNTs).通过XRD、TEM、UV等测试手段对复合材料进行了表征.结果表明:经450℃煅烧3 h后制备的TiO2/oCNTs复合体系中,纳米TiO2呈现锐钛矿且均匀包覆在碳纳米管表面.oCNTs的存在能够有效改变复合材料的表面性质,以实现TiO2对紫外光的敏感性.当TiO2和oCNTs的质量比为1∶0.03、TiO2/3%oCNTs催化剂使用量为0.8 g/L时,对20 mg/L甲基橙溶液紫外灯照射1 h,甲基橙溶液的降解率达到99%,而同等条件下纯TiO2对甲基橙的降解率不到50%,说明oCNTs能够有效提高TiO2对甲基橙的光催化活性.TiO2/3%oCNTs光催化剂对甲基橙进行5次循环降解,降解率保持在95%左右.
多壁碳纳米管;纳米二氧化钛;甲基橙;溶胶-凝胶法;光催化;降解
近几年,环境污染已经成为一个严重的全球性问题,有害有机物的光催化降解对环境保护非常重要,因此受到了学者们的广泛关注[1-5].纳米TiO2由于具有光催化活性高、热稳定性好、氧化能力强、无毒、廉价及无二次污染等独特的优点[6-13],成为备受人们青睐的一种绿色环保型光催化剂.TiO2为N型半导体材料,带隙宽为3.2 eV[12].当TiO2受到波长小于380 nm的紫外光照射时,价带的电子获得光子能量跃迁到导带,激发电离出电子的同时产生正电性的空穴,形成电子/空穴对,与吸附溶解在其表面的O2和H2O反应形成很高活性的·O2-和·OH自由基[5-10].·OH自由基的氧化能力是在水体中存在的氧化集中最强的,能氧化大部分的有机污染物和无机污染物,而且对反应物几乎无选择,在光催化氧化中起着决定性的作用[14-15].为了增强TiO2在可见光照射下的催化活性,可以掺杂一些金属或非金属物质,已经成功合成的如TiO2-SiO2-Ag[2]、Mn/TiO2[7]和MWCNT-TiO2[6],常见的合成方法之一为溶胶凝胶法[10].
碳纳米管(CNT)是1991年Lijim发现的一种新型碳结构.理想碳纳米管是由六边形碳原子组成的石墨烯片层卷成的无缝、中空的管腔结构[7].因为碳纳米管具有极大的比表面积、极高的化学稳定性、独特的电子结构、纳米级中空管腔和优良的吸附性能,被认为是一种理想的催化剂载体.很多学者进行深入研究发现,在光催化过程中,多壁碳纳米管(MWCNTs)能够作为TiO2的一种良好的光敏剂,这是由于光诱导电子能够很容易地从MWCNTs转移到TiO2的导带,导带的空洞可以中和羟基离子,而且在催化过程中,碳管还可以和金属离子起协同作用[6].
由于文献[6]中所述MWCNT-TiO2是将MWCNT直接加入到溶有无水乙醇的钛酸丁酯溶液中,在溶液中碳管分散性并不是很好,钛酸丁酯与MWCNT的结合也并不好.相比之下,本文直接用超声细胞粉碎器对羧基化多壁碳纳米管(oCNTs)进行粉碎处理,使得羧基化多壁碳纳米管有更多端口出现,使其更容易与钛酸丁酯结合,更易于TiO2负载到oCNTs上.同时,本文采用溶胶凝胶法制备了不同组分的TiO2/oCNTs复合光催化剂,并在紫外光照射下对甲基橙进行催化降解,分析其催化降解机理,考察此复合光催化剂的催化活性.
1 实验部分
1.1 实验药品和仪器
药品:钛酸丁酯,冰醋酸,无水乙醇,AR级,天津市科密欧化学试剂有限公司产品;羧基化多壁碳纳米管,质量分数>95%,长度0.5~2 μm,成都市有机化学所产品;盐酸,分析纯,国药集团化学试剂有限公司产品;甲基橙,天津市天新精细化工开发有限公司产品;氮气,天津市静海县环宇制氧有限公司产品.
仪器:ME204E型精密电子分析天平,梅特勒-托利多有限公司产品;DH-101型恒温电热鼓风干燥箱,SK-G06123K型真空/气氛管式电炉,天津市中环实验电炉有限公司产品;DZF-6050型真空干燥烘箱,巩义市予华仪器有限公司产品;KQ2200型双频数控超声波清洗器,昆山市超声仪器有限公司产品;H2050R型离心机,长沙市湘仪离心机仪器有限公司产品;H7650型透射电子显微镜,DMax-2500型X射线衍射仪,日本日立公司产品;光化学反应器,氙灯光源,北京中教金源科技有限公司产品;UV-Vis DRS TU-1810型双光束紫外可见分光光度仪,北京普析通用仪器有限责任公司产品.
1.2 TiO2/oCNTs复合材料的制备
首先对羧基化碳管(oCNTs)进行超声震荡粉碎处理1 h;取100 mL无水乙醇置于500 mL烧杯中,加入1 mL冰醋酸,在剧烈搅拌下缓慢将0.1 mol钛酸丁酯滴入,搅拌1 h得透明黄色溶液A.再将处理后的oCNTs加入到A中搅拌3 h.配制无水乙醇、蒸馏水和浓硝酸的混合液为B,然后在磁力搅拌下将B溶液缓慢地滴到A溶液中,滴定之后再继续搅拌2 h,然后将溶液在室温下放置24 h形成凝胶,置于烘箱中于80℃干燥并研磨备用,最后在450℃下将研磨后的样品煅烧3 h.煅烧后即得TiO2/oCNTs复合材料.其中,分散在溶胶凝胶中的TiO2和oCNTs分别以1∶0,1∶0.01,1∶0.03,1∶0.05,1∶0.07的质量比来制备不同组分的TiO2/oCNTs复合材料.
1.3 结构和性能表征
(1)结构表征:采用透射电子显微镜来观察所制备的TiO2/oCNTs复合材料样品的外观形貌,取样品0.001 0 g粉末溶于20 mL无水乙醇中进行超声处理;采用X射线衍射仪来定性分析所制备的TiO2/oCNTs复合材料样品的晶相,CuKa射线,管电压150 kV,管电流3 mA,扫描速率8°/min,扫描范围10°~80°;利用紫外漫反射光谱分析TiO2/oCNTs复合材料样品的红移情况和吸光性,取样品0.1%溶于20 mL无水乙醇中进行超声处理,样品在空气中的能带波长为200~900 nm.根据公式(1)计算能带:

式中:Eg为能带间隙(eV);λ为波长(nm).
(2)光催化降解甲基橙:将光催化剂加入到250 mL含有20 mg/L甲基橙的溶液中,调节pH为3.64,暗中超声0.5 h,然后在黑暗中搅拌0.5 h,为了建立光催化剂的吸附平衡(甲基橙在溶液中的浓度和TiO2/oCNTs复合物表面上的浓度都不再发生改变时的状态),用最大照射波长大约470 nm左右300 W的氙灯照射,每隔10 min取样,离心分离,取上部清液,用UVVis分光光度计检测甲基橙的吸光度(检测波长465 nm),根据光照前后溶液吸光度的变化,计算甲基橙的降解率,并以此评价复合材料的光催化活性.测试TiO2/oCNTs复合光催化剂(TiO2∶oCNTs=1∶0.03)对甲基橙进行5次循环降解的效果和催化剂回收的情况,即对每次催化后的光催化剂进行回收,重复以上实验过程多次.降解率计算公式为:
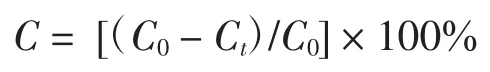
式中:C为甲基橙的降解率;C0为光照前甲基橙溶液的浓度;Ct为光照时间t时甲基橙溶液的浓度.
2 结果与讨论
2.1 X射线衍射(XRD)分析
图1所示为TiO2、oCNTs和TiO2/oCNTs复合材料经450℃煅烧后的X射线衍射图.

图1 TiO2、oCNTs和TiO2/oCNTs复合材料的XRD图Fig.1 XRD patterns of TiO2,oCNTs and TiO2/oCNTs composite samples
由图1可以看出,2θ在 25.28°(101)、37.80°(004)、48.05°(200)和53.89°(105)处,TiO2/1%oCNTs、TiO2/3%oCNTs、TiO2/5%oCNTs和TiO2/7%oCNTs皆形成TiO2锐钛矿,没有金红石和板钛矿的晶相结构,且它们的晶相衍射峰突出.在复合材料的光谱范围内,没有多壁碳纳米管的特征衍射峰,可能是由于二氧化钛锐钛矿型主峰位置处(2θ=25.28°)和羧基化碳纳米管的特征衍射峰(2θ=26.23°)是重叠的,这与两者质量分数之间的差别大有关.观察图1可以发现,当oCNTs相对于TiO2的质量分数增加时,会出现衍射峰宽化,这说明TiO2和oCNTs之间的界面是紧密连接的[12].
2.2 透射电子显微镜(TEM)分析
图2所示为TiO2、oCNTs和TiO2/oCNTs复合材料的外部形态和微观结构的TEM图.

图2 TiO2、oCNTs和TiO2/oCNTs复合材料表面形貌的投射电镜图Fig.2 TEM images of TiO2,oCNTs and TiO2/oCNTs composites surface morphology
由图2(a)可看出,TiO2粒子是紧密排列的六面体型的晶体结构,平均粒子直径为10 nm左右.图2(b)为未经粉碎处理的碳纳米管,可以看出碳纳米管是团聚纠缠到一起的.粉碎后的羧基化碳管比较短,如图2(c)所示,其表面杂质几乎都是分离的,而且会有较多的端口出现,增加了碳管的比表面积.图2(d)—图2(g)为不同组分TiO2/oCNTs的表面形貌图,可以看出,二氧化钛和羧基化碳纳米管之间是紧密接触的,且羧基化碳纳米管的表面被TiO2纳米粒子均匀覆盖,这也是TiO2/oCNTs复合材料的XRD图中,oCNTs的衍射峰不存在的原因,进一步说明TiO2和oCNTs之间的界面可以抑制光生电子-空穴对的再结合,从而可以提高复合材料的光催化活性.当碳纳米管的质量分数增加时,碳纳米管表面沉积的二氧化钛纳米粒子随之增加,这可能是由于二氧化钛的溶胶浓度增加了.图2中,部分二氧化钛纳米粒子会随机团聚在碳纳米管的表面,说明碳纳米管起到生长和沉淀中心的作用.
2.3 UV-vis漫反射的分析
图3所示为TiO2、oCNTs和TiO2/oCNTs复合材料的UV-Vis光谱图.

图3 TiO2、oCNTs和TiO2/oCNTs复合材料的紫外漫反射图Fig.3 UV-Vis spectra of TiO2,oCNTs and TiO2/oCNTs composites
由图3可以看出,纯的TiO2在200~400 nm的紫外光区域有较强的吸收性能,在400~800 nm的可见光区域对光的吸收强度显著减弱.掺杂适量的碳纳米管后,TiO2/oCNTs复合材料在350 nm处的吸光度明显高于纯TiO2,并且在400~800 nm的可见光区域也有比较稳定的吸收.TiO2/oCNTs光催化剂在可见光区域的波长大约是462 nm,而纯TiO2的波长是385 nm,说明TiO2/oCNTs复合材料产生了红移.由此可知,TiO2和oCNTs之间是紧密接触的,oCNTs可以改变TiO2的电子结构,电荷从TiO2的价带运输到了导带,在能带间隙产生能量,进而发生红移的现象.与纯TiO2相比,TiO2/oCNTs复合材料光催化剂对可见光的吸收提高,催化活性有所增加.由此说明,oCNTs的加入可以有效地改善TiO2复合光催化剂在紫外光下的吸收能力.
从紫外反射能谱图中计算TiO2、oCNTs及TiO2/ oCNTs的能带,如表1所示.由表1可以看出,TiO2的能带间隙是3.22 eV,而掺杂了oCNTs后,TiO2/oCNTs复合材料的吸收边缘发生了红移,TiO2/oCNTs的能带间隙逐渐减少.复合材料的能带间隙减少是由于碳管的存在,oCNTs可以作为一个转移电子的通道,抑制电子-空穴对的再结合,因而掺杂了oCNTs的TiO2在紫外光下其催化活性有所提高.

表1 oCNTs、TiO2和TiO2/oCNTs复合材料的能带间隙Tab.1 Band gap energy of oCNTs,TiO2and TiO2/oCNTs composites
2.4 不同催化剂对甲基橙的降解效果
图4所示为将0.2g光催化剂溶于250 mL、20 mg/L的甲基橙溶液中考察oCNTs、TiO2和TiO2/oCNTs在紫外光下对甲基橙的降解.

图4 催化剂类型对甲基橙光催化降解的影响Fig.4 Effect of catalyst type on photocatalytic degradation of methyl orange
由图4可以看出,oCNTs在紫外光下对甲基橙没有降解效果,TiO2在紫外光下对甲基橙的降解效果也不理想,紫外光照射60 min后甲基橙降解率不到50%.而在相同时间内,TiO2/1%oCNTs、TiO2/3%oCNTs、TiO2/ 5%oCNTs和TiO2/7%oCNTs对甲基橙的降解率分别达到90%、99%、96%、94%,几乎全部降解,相对于纯TiO2,复合光催化剂对甲基橙的降解率平均提升了40%左右,说明碳管的添加可以有效地提高TiQ2的光催化活性.作为TiO2催化剂的载体,oCNTs利用其独特的管腔结构,提高了TiO2表面氧与有机物的浓度,发挥了oCNTs作为优良导体的优势,促进了光生电子和光生空穴的分离,并使光生电子向催化剂表面转移,有效抑制了电子-空穴对的泯灭作用,提高了光催化效率.光催化活性升高的顺序是:oCNTs<TiO2<TiO2/ 1%oCNTs<TiO2/7%oCNTs<TiO2/5%oCNTs<TiO2/3%oCNTs.当TiO2∶oCNTs=1∶0.03时,即TiO2/3%oCNTs复合光催化剂对甲基橙的降解效果最佳.不同组分复合光催化剂之间光催化活性有所差异是因为如果添加过量oCNTs会造成oCNTs之间缠结团聚,对于TiO2的负载造成影响,从而会有一部分电子-空穴对复合,降低TiO2的催化活性.
2.5 用量对甲基橙降解效果的影响
图5所示为不同浓度TiO2/3%oCNTs催化剂对甲基橙的降解效果.

图5 催化剂用量对光催化降解的影响Fig.5 Effect of catalyst dosage on photocatalytic
由图5可以看出,当光催化剂质量浓度从0.4 g/L增加到0.8 g/L时,甲基橙的降解率逐渐增大;当质量浓度在0.8 g/L以上时,甲基橙的降解率下降.由此说明,光催化活性可以通过增加催化剂用量进行提高,但过量的催化剂渗透到溶液里会阻止光催化的进行[12].
2.6 光催化剂的回收利用
催化剂的回收是判断光催化剂的实际应用效果和发展多相光催化氧化技术处理废水的关键步骤之一.本文用TiO2/3%oCNTs光催化剂对甲基橙进行了多次降解.图6所示为TiO2/3%oCNTs光催化剂对甲基橙循环降解5次的降解效果.
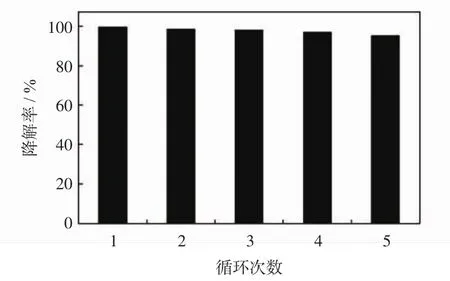
图6 光催化剂对甲基橙的循环催化降解Fig.6 Recycle and reuse of photocatalysts for photocatalytic degradation of methyl orange
由图6可以看出,TiO2/3%oCNTs光催化剂对甲基橙进行了5次降解后,对甲基橙的降解率依然保持在95%左右.
3 结论
本文成功制备了TiO2/oCNTs光催化剂,并对其进行XRD、TEM和UV-Vis的表征.结果表明:
(1)oCNTs能够有效地抑制TiO2电子-空穴对的再结合,有效改善TiO2光催化剂在可见光下的催化活性.
(2)用0.2 gTiO2/3%oCNTs光催化剂降解20 mg/L的甲基橙溶液,在光照1 h后,甲基橙的降解率可以达到99%左右.
(3)光催化剂循环降解5次后,对甲基橙的降解率依然在95%左右.
[1]SCHNEIDER J,MATSUOKA M,TAKEUCHI M,et al.Understanding TiO2photocatalysis:Mechanisms and materials[J]. Chem Rev,2014,114:9919-9986.
[2]LIU C,YANG D,JIAO Y,et al.Biomimetic synthesis of TiO2-SiO2-Ag nanocomposites with enhanced visible-light photocatalytic activity[J].ACS Appl Mater Interfaces,2013,38(5):24-3832.
[3]CHEN Y F,HUANG W X,HE D L,et al.Construction of heterostructured g-C3N4/Ag/TiO2mcrospheres with enhanced photocatalysis performance under visible-light irradiation[J]. ACS Appl Mater Interfaces,2014,14(6):405-14414.
[4]UIIAH K,YE S,JO S B,et al.Optical and photocatalytic properties of novel heterogeneous PtSe2-graphene/TiO2nanocomposites synthesized via ultrasonic assisted techniques[J]. Ultrason Sonochem,2014,21:1849–1857.
[5]孙晓锋,李驰,夏修阳,等.半纤维素/TiO2复合凝胶的光催化降解性能[J].化工学报,2016,67(5):2070-2077. SUN X F,LI C,XIA X Y,et al.Photocatalytic degradation property of hemicellulose/TiO2composite gel[J].CIESC Journal,2016,67(5):2070-2077(in Chinese).
[6]GUI M M,CHAI S P,XU B Q,et al.Preparation and characterization of nanostructured MWCNT-TiO2composite materials for photocatalytic water treatment applications[J].Mater Res Bull,2008,43:958-967.
[7]PARK E,LE H,CHIN S,et al.Synthesis and enhanced photocatalytic activity of Mn/TiO2mesoporous materials using the impregnation method through CVC process[J].Porous Mater,2012,19:877-881.
[8]徐延明,赵明,李坚,等.氨基酞菁-二氧化钛可见-近红外光催化剂的制备及其性能 [J].化工学报,2016,67(5):1915-1921. XU Y M,ZHAO M,LI J,et al.Visible near-infrared amino phthalocyanine-titaniumdioxidephotocatalyst:Preparationandperformance[J].CIESC Journal,2016,67(5):1915-1921(in Chinese).
[9]SARKAR D,GHOSH C K,MUKHERJEE S,et al.Three dimensional Ag2O/TiO2type-II(p-n)nanoheterojunctions for superior photocatalytic activity[J].ACS Appl Mater Interfaces,2013(5):331-337.
[10]LEONG K H,MONASH P,IBRAHIM S,et al.Solar photocatalytic activity of anatase TiO2nanocrystals synthesized by non-hydrolitic sol-gel method[J].Sol Energ,2014,101:321-332.
[11]AN H,PAN L N,CUI H,et al.Electrocatalytic performance of Pdnanoparticles supported on TiO2-MWCNTs for methanol,ethanol,and isopropanol in alkaline media[J].J Electroanal Chem,2015,741:56-63.
[12]AAZZAM E S.Visible light photocatalytic degradation of thiophene using Ag-TiO2/multi-walled carbon nanotubes nanocomposite[J].Ceram Int,2014,40:6705-6711.
[13]LEE S T,PARK S J.TiO2photocatalyst for water treatment applications[J].J Ind Eng Chem,2013,19:1761-1769.
[14]LI W,WANG F,FENG S S,et al.Sol-Gel design strategy for ultradispersed TiO2nanoparticles on graphene for high-performance lithium Ion batteries[J].Am Chem Soc,2013,135:18300-18303.
[15]刘冰,付荣荣,高善民,等.Ti3+自掺杂的TiO2(A)/TiO2(R)/ In2O3纳米异质结的制备与可见光催化性能[J].无机化学学报,2016,32(2):223-232. LIU B,FU R R,GAO S M,et al.Preparation of Ti3+self doped TiO2(A)/TiO2(R)/In2O3nanoheterojunctions with enhanced visible light driven photocatalytic properties[J].Chin J Inorg Chem,2016,32(2):223-232(in Chinese).
Preparation of carbon nanotubes supported titanium dioxide and its photocatalytic degradation for methyl orange
WANG Wen-yi,WANG En-xia,HUO Teng-bo,ZHU Liu-yong,SHAN Bo-jin,LIAN Wei-tao,LI Yin-shan
(1.School of Materials Science and Engineering,Tianjin Polytechnic University,Tianjin 300387,China;2.State Key Laboratory of Separation Membranes and Membrane Processes,Tianjin Polytechnic University,Tianjin 300387,China)
By using sol-gel method with tetrabutyl titanate as precursor,carboxylic multi walled carbon nanotubes(oCNTs)as carrier,ethanol as solvent,acetic acid as inhibitor,the composite photocatalyst of TiO2nanoparticles supported on carbon nanotubes(TiO2/oCNTs)was synthesized successfully.The prepared TiO2/oCNTs nanocomposite materials were characterized through X-ray diffraction(XRD),transmission electron microscopy(TEM),and UV-vis spectra (UV-vis)etc.The results showed that in the TiO2/oCNTs composite prepared by calcination at 450℃for 3 hours,Nano TiO2was anatase and even coated on the surface of oCNTs.The existence of oCNTs can effectively change the surface properties of the composite in order to realize the sensitivity of TiO2to UV light.When the TiO2and oCNTs were dispersed in the solution with the mass ratios of 1∶0.03,and the amount of the TiO2/oCNTs catalyst was 0.8 g/L,the methyl orange solution was 20 mg/L,which was lighted under UV radiation for 1 h,the degradation rate of the methyl orange in the photocatalyst′s experimental was about 99%.At the same conditions,the degradation rate of pure TiO2for methyl orange was below 50%.This indicated that the oCNTs can improve the photocatalytic activity of TiO2towards methyl orange.Methyl orange was cyclic degradated with five times by the TiO2/3%oCNTs photocatalyst when the mass ratios of TiO2and oCNTs is 1∶0.03,its degradation rate remained at 95%,catalyst recovery reached 95%.
carboxylic multi walled carbon nanotubes(oCNTs);titanium dioxide nanoparticles;methyl orange;sol-gel method;photocatalytic;degradation
TQ426;O643.36
A
1671-024X(2016)06-0050-05
10.3969/j.issn.1671-024x.2016.06.009
2016-10-09
国家自然科学基金资助项目(21206120);化学工程联合国家重点实验室开放课题(SKL-ChE-14A03)
王文一(1978—),男,博士,副教授,主要研究方向为碳纳米管改性及其复合.E-mail:wenyi-wang@hotmail.com
