机器人辅助全腹腔镜下根治性膀胱切除加原位回肠新膀胱术
2016-01-27陈光富张鹏张旭马鑫李宏召孙圣坤朱捷杨国强黄双艾青
陈光富 张鹏△ 张旭 马鑫 李宏召 孙圣坤 朱捷 杨国强 黄双 艾青
1中国人民解放军总医院泌尿外科 100853 北京
△共同第一作者
机器人辅助全腹腔镜下根治性膀胱切除加原位回肠新膀胱术
陈光富1张鹏1△张旭1马鑫1李宏召1孙圣坤1朱捷1杨国强1黄双1艾青1
1中国人民解放军总医院泌尿外科 100853 北京
△共同第一作者
[摘要]目的:总结采用da Vinci S机器人系统完成机器人辅助全腹腔镜根治性膀胱切除(totally robotic-assisted laparoscopic radical cystectomy, tRARC)加原位回肠新胱术的临床技术经验和疗效。方法:回顾分析2012年3月~2015年7月接受机器人辅助腹腔镜根治性膀胱切除加原位回肠新膀胱术的膀胱尿路上皮癌患者9例。均为男性,平均年龄54(37~64)岁。术前肿瘤活检病理诊断为浸润性或高级别膀胱尿路上皮癌,术前检查均未发现有其他邻近脏器浸润、盆腔淋巴结转移或远处转移,临床分期均低于T3N0M0。9例患者全部为全麻下行tRARC加腔内原位回肠新膀胱术。 结果:9例患者手术均获成功。手术平均时间520(360~780)min;平均出血量555 (300~1 200)ml;平均淋巴结清扫数目为13(4~23)枚。术后2~3 d下地活动,3~4 d肠功能恢复,术后平均住院时间20(10~32)d。患者术后1个月行膀胱造影确定无吻合口漏后拔除尿管和双侧输尿管支架管。术后随访时间平均28(1~41)个月,入组所有病例肾功能均正常,尿控较满意,无肾积水。结论:根据初期的手术操作过程和随访结果,tRARC加原位新膀胱术在临床上是可行的。更多的操作经验、规范的手术流程和长期和随机的对照研究将有助于对这一技术进行评估和推广。
[关键词]机器人;全腹腔镜;膀胱切除术;原位新膀胱术
机器人辅助腹腔镜根治性膀胱切除加尿流改道术的临床可行性已得到广泛认可,其具有手术创伤更小、手术视野暴露更清晰、术中出血少、术后恢复快、术者操作舒适感强等优势,尤其是在狭小骨盆中进行根治性膀胱切除术和前列腺癌根治术,可以实现更加精细的解剖,更易于保留神经,保护控尿结构,达到根治肿瘤、保留性功能和完全控尿的完美结合。2012年3月~2015年7月我们对9例膀胱尿路上皮癌患者行机器人辅助全腹腔镜下根治性膀胱全切除(totally robotic-assisted laparoscopic radical cystectomy, tRARC)加腔内原位回肠新膀胱术,手术效果满意,现报告如下。
1资料与方法
1.1临床资料
本组9例,全部为男性,年龄37~64岁,平均54岁。体质指数23.6~29.1 kg/m2,平均27.4 kg/m2。麻醉评分1~2分。术前肿瘤活检病理诊断为浸润性或高危的非肌层浸润性膀胱尿路上皮癌,术前检查均未发现有其他邻近脏器浸润、盆腔淋巴结转移或远处转移,临床分期均低于T3N0M0。患者术前3 d流质饮食,术前1 d禁食,口服抗生素,术前清洁灌肠。
1.2手术方法
气管内插管全身麻醉,取头低脚高截石位,倾斜25~50°。da Vinci S系统床旁机械臂系统位于患者双下肢之间。助手立于患者左右两侧,器械护士立于患者右前方。手术区皮肤消毒(含会阴部)。
于脐上1 cm处作长12 mm纵形皮肤切口为镜头孔,采用气腹针建立气腹,将12 mm套管置入腹腔,气腹压力保持在1.862 kPa(14 mm Hg)。以耻骨联合为中心,以其至镜头孔的距离为半径作一弧线,在弧线上于距镜头孔右、左侧各8 cm及左侧16 cm位置各作一8 mm皮肤切口,作为第1、2、3机械臂孔,于第1臂孔外下8 cm作10 mm切口为第1辅助孔,必要时于第2、3臂孔间略上方作5 mm切口为第2辅助孔。腹腔镜监视下将套管置入上述各位点。各套管分别置入30°镜头、单极弯剪(第1臂孔)、双极钳(第2臂孔)、无创环钳(第3臂孔)、吸引器(第2辅助孔)及辅助器械(第1辅助孔)。术中第1和第2臂为主要操作臂,第3臂起到牵拉周围组织的作用。助手通过2个辅助孔协助手术。
tRARC采用顺行切除的方法。在骼内外动脉分叉处找到输尿管,向下游离至膀胱壁外,Week夹夹闭剪断,预置待用。在靠盆壁的无血管区分离两侧膀胱壁,夹闭并离断膀胱上动脉(图1A)。在膀胱直肠凹陷内,靠近底部横行切开腹膜,找到并完全分离输精管和精囊腺,将精囊腺和输精管壶腹保留在膀胱上(图1B)。用第3臂将精囊向上牵拉,暴露并横行切开Denonvillier筋膜。分离直肠前壁直至前列腺尖部(图1C)。助手自第1辅助孔置入ligsure靠近膀胱夹闭、切断膀胱侧韧带。沿腹膜返折切开腹膜分离膀胱前间隙。打开盆底筋膜,紧贴前列腺用剪刀锐性分离两侧前列腺侧韧带,将两侧神经血管束(neurovascular bundle, NVB)从前列腺分离并保留,从两侧分离至前列腺尖部。分离阴茎背深静脉复合体和前列腺尖部,用2-0可吸收线作8字形缝扎阴茎背深静脉复合体(图1D)。在阴茎复合体近前列腺处剪断前列腺尖部, 离断尿道(图1E)。置入标本袋将标本完整装入袋中,拉紧开口并将其放入腹腔内。盆腔内用无菌生理盐水冲洗并观察有无损伤直肠前壁。术中将尿道和两侧输尿管残端送冷冻病理检查均未见肿瘤组织。
常规标准盆腔淋巴结清扫范围包括髂血管外组、内组淋巴结以及闭孔组淋巴结。后期我们采用扩大盆腔淋巴结清扫,清扫范围包括腹主动脉、髂总血管、骼内外血管和闭孔神经周围淋巴脂肪组织,外侧缘至生殖股神经生殖支,近端至主动脉分叉处,远端至骨盆面。靠近神经、血管处宜尽量应用冷剪刀或双极电钳,避免造成生殖神经和闭孔神经的损伤。将清扫下的双侧淋巴结做好标记,装入标本袋中。
采用完全体内制作新膀胱或回肠输出道。腹腔内放入标有自制刻度的烟卷引流管,距回盲部12 cm处取回肠段54 cm,距远端22 cm和44 cm处分别缝合标记线。Endo-GIA(6TB45, ETHICON)直线闭合切割器截取肠管和部分肠系膜。远端及近端肠管重叠交错备肠吻合用,截取回肠置于备吻合肠管后方。将重叠部分回肠段对系膜缘分别作1 cm切口并先后放入2个Endo-GIA上下齿,闭合完成两端肠管侧侧吻合(图1F)。再分别使用2个Endo-GIA闭合开放的肠管断端,恢复回肠肠管连续性。系膜切缘和闭合肠管远端可间断缝合关闭数针。近端保持10 cm完整的回肠作为Studer新膀胱输出道,其余肠管排成U型并于靠拢侧在胸导管的引导下沿近肠系膜缘1 cm处切开(图1G)。2-0可吸收线先间断对位再连续缝合回肠新膀胱后壁。将22 cm标记线处提起拉至尿道残端处,在此处将肠管与尿道残端下方的组织固定,注意防止肠系膜扭转或张力过大,必要时可减小手术床的倾斜角度。在F18尿管引导下于肠管最低位与尿道残端行双针法连续缝合:2个3-0,5/8弧单荞缝线,分别取10 cm,两线尾相互打结,做成1个双头针缝合线(图1H)。尿道吻合结束后,将两侧输尿管分别于末端Studer输出道行粘膜对粘膜吻合,输尿管内置入F7单J管,并将其用4-0可吸收线固定于新膀胱内壁防止脱出(图1I)。将双侧单J管自尿道拉出,注意不要将其脱离输尿管吻合口。新膀胱内留置气囊尿管,注水试验吻合口有无渗漏,如有明显渗漏的吻合处可行8字缝合修补。自第1辅助孔放置乳胶引流管,自脐上穿刺点做3~4 cm切口取出标本。
2结果
本组9例手术均获成功,术中未出现并发症或中转开放。手术时间360~780 min,平均520 min;出血量300~1 200 ml,平均555 ml,其中术后输血3例。术后2~3 d下地活动,3~4 d肠功能恢复。术后6~31 d拔除盆腔引流管,平均13 d。患者术后第2天起每4~6 h时冲洗新膀胱1次,直至拔除尿管,术后1个月行膀胱造影,确定无吻合口漏后拔除尿管和双侧输尿管支架管。本组病例无肠瘘和尿瘘并发症发生。术后住院时间10~32 d,平均20 d。
术后病理诊断为膀胱高级别浸润性尿路上皮癌pT1~T3a期, 级别为G2~G3,平均淋巴结清扫13(4~23)枚。平均术后随访28(1~41)个月,所有入组病例肾功能均正常。新膀胱容量280~450 ml,平均385 ml,患者尿控较满意,日间排尿1次/2 h,夜间排尿1次/3 h,除1例患者术后随访仅1月外所有患者术后3个月尿控均满意。
3讨论
根治性膀胱切除术同时行盆腔淋巴结清扫术,是治疗肌层浸润性和高危的非肌层浸润性膀胱癌的金标准[1]。其可以很好的控制局部肿瘤的复发,并且5年的肿瘤特异性生存率可以达到50%~70%。但是由于骨盆的解剖空间狭小,根治性膀胱切除术的并发症发生率和死亡率较高,一直以来都是泌尿外科最复杂的手术之一[2]。
目前,在许多国家机器人手术技术已经逐渐成为膀胱癌治疗的一种主流方式,而机器人辅助的RARC的临床可行性也得到越来越多的认可[3,4]。在我国,中国人民解放军总医院于2009年首次报道了机器人辅助RARC的临床资料[5]。与开放手术或普通腹腔镜手术相比,机器人辅助RARC具有手术创伤更小、手术视野暴露更清晰、术中出血少、术后恢复快、术者操作舒适感强等,且肿瘤治疗效果与开放手术无明显差异[6,7]。近年来,机器人辅助腹腔镜下膀胱癌根治在扩大淋巴结清扫和保留性神经的技术方面又展现出更大的优势,这对于提高肿瘤患者预后和改善患者术后生活质量方面起了推动作用[8,9]。通常,膀胱根治性切除常辅以尿流改道术。近年来,患者对于术后整体生活质量的要求不断提升,在条件允许的情况下,越来越多的患者更愿选择原位新膀胱作为尿流改道术。目前,由于操作难度大,手术时间长,大多数RARC原位新膀胱术的相关报道是通过体外完成[10]。2003年,Beecken等就已报道机器人辅助完全体内原位新膀胱术,该术式可以减轻患者手术切口的疼痛,预防肠管由于长时间暴露于体外引起的功能紊乱,以及减少可能的体液丢失[11~13]。尽管手术操作尤其是在肠道和膀胱重建方面耗时较长,难度较大,但借助da Vinci S机器人系统所具备的高清放大、稳定操作、高度灵活等优点,其在完全体内尿流改道的操作中较单纯腹腔镜具有明显优势。本组9例患者均采用完全体内原位膀胱的手术均获成功,术后未出现严重并发症,平均随访28个月,患者肾功能均正常,且对于术后生活质量均比较满意。
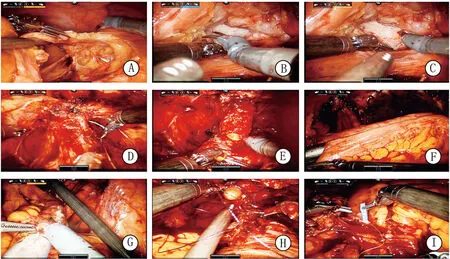
A:游离输尿管及膀胱侧壁;B:游离输精管和精囊腺;C:切开Denonvilliers筋膜;D:缝扎DVC;E:离
断前列腺尖部尿道;F:恢复肠道连续性;G:制作新膀胱;H:尿道新膀胱吻合;I:留置单J管。
图1机器人辅助全腹腔镜下膀胱根治性切除回肠新膀胱术
膀胱根治性切除原位新膀胱术作为肌层浸润性和高危的非肌层浸润性膀胱癌的治疗术式已在近年来被越来越广泛地开展,其良好的术后肿瘤学疗效和满意的术后生活质量已被明确证实。但由于其手术步骤多,操作较为复杂,术后并发症发生率高。我们在借鉴多年的开放膀胱根治性切除原位新膀胱术的经验在前期成功开展了全腹腔镜膀胱根治性切除原位新膀胱术,并在此基础上不断总结经验,对传统技术进行了手术方式和手术技巧的改良,将手术技术移植到机器人辅助腹腔镜上,成功开展并实施了该项术式[14]。因此,良好扎实的开放与腹腔镜膀胱根治性切除及腔内肠道手术技术是开展此项术式的良好保障。
根据初期的手术操作过程和随访结果,tRARC加腔内原位新膀胱术在临床上是可行和安全的。通过既往手术经验的总结,我们认为谨慎的选择病例和提高术者的操作熟练程度可以达到令人满意的短期临床效果。目前,机器人在我国还未广泛普及,各单位对于机器人辅助系统的应用水平也参差不齐,将来还需要长期的大量的临床资料对这一术式进行全面的评估。
[参考文献]
[1]Babjuk M, Burger M, Zigeuner R, et al. EAU guidelines on non-muscle-invasive urothelial carcinoma of the bladder: update 2013. Eur Urol, 2013, 64(4): 639-653.
[2]Lawrentschuk N, Colombo R, Hakenberg OW, et al. Prevention and management of complications following radical cystectomy for bladder cancer. Eur Urol, 2010, 57(6): 983-1001.
[3]Gandaglia G, De Groote R, Geurts N, et al. Oncologic Outcomes of Robot-Assisted Radical Cystectomy: Results of a High--Volume Robotic Center. J Endourol, 2015, Epub ahead of print.
[4]Collins JW, Sooriakumaran P, Sanchez-Salas R, et al. Robot-assisted radical cystectomy with intracorporeal neobladder diversion: The Karolinska experience. Indian J Urol, 2014, 30(3): 307-313.
[5]朱捷,高江平,徐阿祥,等.机器人辅助腹腔镜根治性膀胱切除体外尿流改道术.中华外科杂志,2009,47(16): 1242-1244.
[6]Bochner BH, Dalbagni G, Sjoberg DD, et al. Comparing open radical cystectomy and robot-assisted laparoscopic radical cystectomy: a randomized clinical trial. Eur Urol, 2015, 67(6): 1042-1050.
[7]Abraham JB, Young JL, Box GN, et al. Comparative analysis of laparoscopic and robot-assisted radical cystectomy with ileal conduit urinary diversion. J Endourol, 2007, 21(12): 1473-1480.
[8]Canda AE, Atmaca AF, Altinova S, et al. Robot-assisted nerve-sparing radical cystectomy with bilateral extended pelvic lymph node dissection (PLND) and intracorporeal urinary diversion for bladder cancer: initial experience in 27 cases. BJU Int, 2012, 110(3): 434-444.
[9]Gamboa AJ, Young JL, Dash A, et al. Pelvic lymph node dissection and outcome of robot-assisted radical cystectomy for bladder carcinoma. J Robot Surg, 2009, 3(1): 7-12.
[10]Ahmed K, Khan SA, Hayn MH, et al. Analysis of intracorporeal compared with extracorporeal urinary diversion after robot-assisted radical cystectomy: results from the International Robotic Cystectomy Consortium. Eur Urol, 2014, 65(2): 340-347.
[11]Beecken WD, Wolfram M, Engl T, et al. Robotic-assisted laparoscopic radical cystectomy and intra-abdominal formation of an orthotopic ileal neobladder. Eur Urol, 2003, 44(3): 337-339.
[12]Fahmy O, Asri K, Schwentner C, et al. Current status of robotic assisted radical cystectomy with intracorporeal ileal neobladder for bladder cancer. J Surg Oncol, 2015, 112(4): 427-429.
[13]Shao P, Li P, Ju X, et al. Laparoscopic radical cystectomy with intracorporeal orthotopic ileal neobladder: technique and clinical outcomes. Urology, 2015, 85(2): 368-373.
[14]陈光富,瓦斯里江·瓦哈甫,马鑫,等.完全腹腔镜下根治性膀胱全切除加原位回肠新膀胱术(附3例报告).临床泌尿外科杂志,2012, 27(8):601-604.
论著
Totally robot-assisted laparoscopic radical cystectomy with orthotopic ileal neobladder
ChenGuangfu1ZhangPeng1ZhangXu1MaXin1LiHongzhao1SunSengkun1ZhuJie1YangGuoqiang1HuangShuang1AiQing1
(1Department of Urology, Chinese PLA General Hospital, Beijing 100853, China)
Corresponding author: Zhang Xu, xzhang@foxmail.com; Chen Guangfu, cgf301@foxmail.com
AbstractObjective: To summarize the clinical operative technique and effect of totally robotic-assisted laparoscopic radical cystectomy (tRARC) with orthotopic ileal neobladder by da Vinci surgical system. Methods: From Mar 2012 to July 2015, 9 male patients of bladder urothelial carcinomas underwent tRARC with orthotopic ileal neobladder were enrolled. The mean age was 54 years (ranged from 37-64 years). All patients were diagnosed preoperatively with muscle-invasive or high-grade bladder urothelial carcinomas in cystoscopic biopsy. There were no adjacent organ infiltration found, pelvic lymph node metastases or distant metastasis on preoperative examinations, and the clinical stage were all below T3N0M0. General anesthesia was administered for tRARC with intracorporeal orthotopic ileal neobladder to all patients. Results: All 9 cases were successful. The average operation time was 520min (ranged from 360-780 min) with average blood loss of 555ml (300 to 1 200 ml), and the average number of lymph nodes was 13 (ranged from 4 to 23). All patients resumed ambulation on postoperative 2 to 3 days, and bowel function recovered on either postoperative day 3 or 4. The average length of hospital stay was 20d (ranged from 10-32 d). One month after operation a cystogram was performed to confirmed watertight healing. During the follow up of 3-43 months (mean 30 months ). All of the patients have normal renal functions and satisfactory urinary continence without hydronephrosis. Conclusions: According to the initial surgery procedure and the results of the initial operation, the tRARC with intracorporeal orthotopic ileal neobladder by da Vinci surgical system is feasible in clinic. More operational experience, standard surgical procedures, long-term and randomized controlled studies will be helpful to evaluate and promote the technology.
Key wordsrobotics; cystectomy; intracorporeal orthotopic ileal neobladder
基金项目:国家高技术研究发展计划(863计划)(2012AA021100)
[文章编号]2095-5146(2015)05-257-04
[中图分类号]R737.14
[文献标识码]A
收稿日期:2015-09-12
通讯作者:张旭,xzhang@foxmail.com;陈光富:cgf301@foxmail.com
