舌下特异性免疫治疗对于多种过敏原过敏儿童变应性鼻炎的疗效
2016-01-22法明
法 明
(南通大学附属常州儿童医院耳鼻喉科,江苏 南通 226000)
舌下特异性免疫治疗对于多种过敏原过敏儿童变应性鼻炎的疗效
法明
(南通大学附属常州儿童医院耳鼻喉科,江苏南通226000)
[摘要]目的:研究单一粉尘螨舌下特异性免疫治疗在单一过敏和多重过敏患者中的疗效。方法:研究入组65例4~15岁患有变应性鼻炎患儿,且临床病史显示其临床症状主要由尘螨引起且合并另外过敏原过敏。将患儿随机分为两组,治疗组35例,对照组30例,治疗组所有患儿均接受粉尘螨滴剂联合药物治疗1年。每12周随访并评估患儿的鼻炎症状与用药评分、VAS评分、皮肤点刺试验结果。结果:治疗组30例患儿与对照组22例患儿均完成1年治疗。SLIT组与对照组患儿的鼻炎症状评分,对症用药评分和VAS评分在52周治疗后均显著减少(均P<0.05),SLIT组尘螨皮肤反应等级在52周治疗后下降(均为P<0.05),对照组尘螨皮肤反应等级治疗后大于治疗前(P>0.05)。组间比较,SLIT组鼻炎症状评分在24周、36周、52周均低于对照组,差异有统计学意义(均为P<0.05)。SLIT组对症用药评分和VAS评分在36周和52周低于对照组,差异有统计学意义(均为P<0.05)。SLIT组尘螨皮肤反应等级在52周低于对照组,差异有统计学意义(均为P<0.05)。结论:本研究显示单一尘螨制剂SLIT治疗在多重过敏患者可以获得在单一过敏患者中同样的疗效,明显优于对症药物治疗。
[关键词]疗效;舌下特异性免疫治疗;单一变应原制剂;单一过敏;多重过敏
[收稿日期:2015-06-24编校:郑英善]
舌下特异性免疫治疗(Sublingual immunotherapy,SLIT)已经成为儿童变应性鼻炎和过敏性哮喘常见的治疗方法,能够明显减轻过敏症状和减少药物使用。但无论是国外还是国内流行病学研究均显示,大部分过敏性疾病患儿在皮肤点刺试验(skin prick test,SPT)和(或)血清学检测中显示其对多种过敏原过敏[1-4]。多重过敏的现实情况让临床医师在选择特异性免疫治疗所用变应原制剂的种类时感到难以抉择。欧洲的医生认为多重过敏的患者不一定在临床上会对多种过敏原表现出过敏症状,因此选用单一过敏原提取物的变应原制剂。而美国医生则倾向于使用混合变应原混合制剂来治疗多重过敏患者[4-5]。近期国外研究显示[2,6-8],单一花粉在多种过敏原过敏季节性鼻炎患者中安全有效,单一尘螨SLIT对多种过敏原过敏常年性鼻炎患者有效[9]。本课题组前期研究证实标准化粉尘螨舌下特异性免疫治疗在单一过敏和多重过敏的儿童变应性鼻炎和哮喘中具有同等疗效[10],本研究在此基础上进一步探讨单一标准化粉尘螨制剂对于多种过敏变应性鼻炎临床疗效,探讨过敏状态与疗效的关系。
1材料与方法
1.1基本信息:本研究是前瞻性随机对照研究,选自2010年6月~9月来南通大学附属常州耳鼻喉科65例儿童患者,年龄4~15岁。入组标准:①变应性鼻炎1年不合并哮喘[7-8];②SPT结果显示患者对粉尘螨(Dermatophagoides farinae,D.f.)和(或)屋尘螨(Dermatophagoides pteronyssinus,D.p.)点刺阳性,并且至少合并另外一种过敏原过敏,点刺分级2+以上;③呼出峰流速PEF(%预计值)≥ 70%。④具有良好依从性。排除标准:①以前开展过ASIT;②有免疫系统疾病或免疫异常。所有患儿入组前进行1个月药物治疗观察依从性,确认有良好依从性后,再入组。入组患儿随机分为两组,SLIT组35例,对照组30例,SLIT组患儿采用SLIT 1年联合药物治疗;对照组采用仅药物治疗。患儿诊断和治疗参照儿童变应性鼻炎诊断和治疗指南(2010年,重庆)[11]和变应性鼻炎国内专家共识[12-13]。
1.2治疗方案
1.2.1SLIT组:患儿使用舌下含服粉尘螨滴剂1~4号(商品名:畅迪,浙江我武生物科技股份有限公司),服用方法是滴于舌下,含1~3 min后吞咽,1次/d,固定时间用药。其中前1~3周服用递增剂量,第1周使用1号(总蛋白浓度1 μg/ml),第2周使用2号(总蛋白浓度10 μg/ml),第3周使用3号(总蛋白浓度100 μg/ml),每周第1天~第7天依次服用1、2、3、4、6、8、10滴。第4周至治疗结束服用4号(总蛋白浓度333 μg/ml),每次服用3滴。在治疗期间需接受随访和复诊,患者的首次用药在医院进行。在治疗期间同时使用的药物治疗按照ARIA[11]方案和变应性鼻炎国内专家共识进行药物治疗[13]。如果出现不良事件,由医生进行评估并指导剂量调整或延迟。
1.2.2对照组:患儿药物使用按照ARIA和变应性鼻炎国内专家共识的阶梯治疗方案进行升级或降级治疗[13],进行至少1年的患者跟踪随访。
1.3临床评估:分别在患者治疗前、治疗第52周评估患者在过去1周中鼻炎症状、用药情况并进行视觉模拟评分(visual analogue score,VAS)。对患者回访前1周内的鼻部典型症状(喷嚏、流涕、鼻塞、鼻痒)进行评估,评分标准为:无症状=0分,轻微=1分、中度=2分、重度=3分,鼻部四个症状的总分即为鼻部症状总分(total nasal symptoms score,TNSS)。研究过程中,患者在医生指导下使用以下缓解药物进行治疗:抗组胺药物,口服或鼻喷激素类药物,白三烯拮抗剂和长效β激动剂(long-acting β-agonist,LABA)。医生根据每次随访时患者的症状进行对症药物调整,同时评估随访前1周内药物使用情况,记录每天平均药物分数(total medication score,TMS):抗组胺=1分,吸入/鼻喷激素=2分,口服激素=3分,白三烯拮抗剂=1分,LABA=1分。
每次随访时,患者使用0~10 cm的VAS尺进行自我症状评估,记录VAS评分。
1.4皮肤点刺试验:在治疗前和治疗后对患者进行皮肤点刺试验。在患者前臂内侧使用标准化试剂进行13个过敏原的皮肤点刺实验,包括屋尘螨、粉尘螨、热带无爪螨、狗毛、猫毛、美洲大蠊、德国小蠊、Blatella germanica、Artemisia vulgaris、Ambrosia artemisifolia、混合草花粉 mixed grasses、混合树花粉mixed trees、mould mix I and mould mix IV,记录每个结果。风团直径≥3 mm为阳性反应。根据阳性风团面积与组胺风团面积比值,阳性过敏原皮肤反应分为4级:1级1%~49%;2级50%~99%;3级100%~199%;4级≥200%。尘螨皮肤反应级别为屋尘螨和粉尘螨阳性等级的平均值。
1.5统计分析:使用SPSS12.0软件进行数据处理和分析。计量资料基线比较采用两样本t检验,组内不同时间点的两两比较采用多元方差分析;数据不成正态分布或者方差不齐时组间比较采用非参数检验Mann-Whitney U或者Wilcoxon秩和检验(Wilcoxon rank sum test),P<0.05为差异具有统计学意义。
2结果
2.1各组患者的入组基线水平比较:65例患儿中52例患儿完成1年研究,13例脱落,SLIT组5例患儿和对照组8例患儿脱落。SLIT组患儿30例,男19例,女11例,年龄(6.56±2.89)岁,过敏原个数(3.68±1.33)个;对照组患儿22例,男16例,女6例,年龄(7.23±2.78)岁,过敏原个数(3.89±1.24)个,两组患儿在年龄、性别、鼻炎总评分、用药评分、VAS,尘螨皮肤反应级别和过敏个数差异均无统计学意义(P>0.05)。整个研究中,无严重的系统性不良事件报道。
2.2鼻炎症状:与治疗前相比,SLIT组和对照组鼻炎症状评分都在治疗52周显著下降(P<0.05)。组间比较显示,两组患儿鼻炎症状评分在52周差异有统计学意义(Z=-9.123,P>0.05)。
表1鼻炎症状评分比较[分,中位数(25分位数;75分位数)]
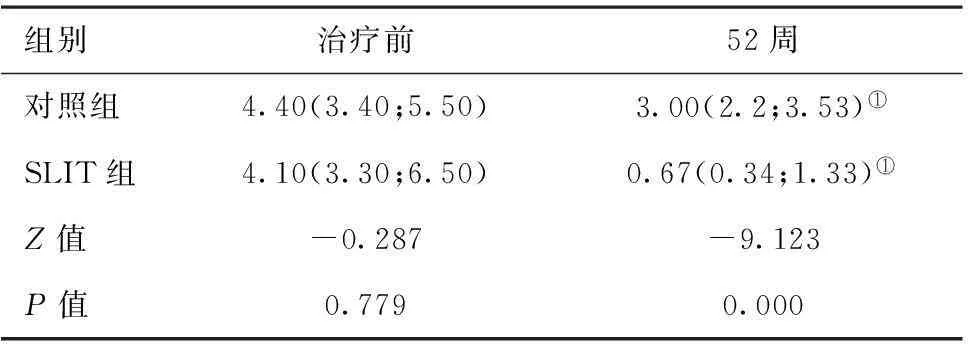
组别治疗前52周对照组4.40(3.40;5.50)3.00(2.2;3.53)①SLIT组4.10(3.30;6.50)0.67(0.34;1.33)①Z值-0.287-9.123P值0.7790.000
注:与治疗前比较,①P<0.05
2.3用药评分:与治疗前比较,SLIT组和对照组的用药评分都在52周显著下降(P<0.05)。组间比较显示,52周随访时SLIT组对症用药评分低于对照组,差异有统计学意义(Z=-6.249,P<0.05)。见表2。
2.4VAS评分:与治疗前相比,SLIT组和对照组VAS评分都在治疗52周显著下降(P<0.05)。组间比较显示,52周SLIT组患儿鼻炎症状低于对照组,差异有统计学意义(Z=-7.332,P<0.05)。见表3。
2.5皮肤反应级别:与治疗前比较,在52周SLIT组尘螨皮肤反应等级显著降低(Z=-6.164,P<0.05),对照组尘螨皮肤反应等级大于治疗前,差异有统计学意义(Z=-2.111,P<0.05),在52周,SLIT组尘螨皮肤反应等级低于对照组,差异有统计学意义(Z=-5.826,P<0.05)。见表4。
2.6安全性:SLIT组和对照组55例患者中,3例患儿出现轻度不良反应,无中重度不良反应出现,其中1例患儿出现咳嗽,给予缓解药物后消失。1例患儿出现轻度局部皮疹,1例患儿出现舌下黏膜瘙痒感,未经处理后消失。
表2对症用药评分比较[分,中位数(25分位数;75分位数)]

组别治疗前52周对照组2.15(1.33;2.77)1.11(0.73;1.88)①SLIT组1.60(1.30;3.00)0.00(0.00;0.00)①Z值-0.088-6.249P值0.8260.000
注:与治疗前比较,①P<0.05
表3VAS评分比较[分,中位数(25分位数;75分位数)]

组别治疗前52周对照组3.50(3.25;4.41)2.52(1.33;3.13)①SLIT组370(2.23;4.45)0.36(0.09;0.73)①Z值-0.418-7.332P值0.8220.000
注:与治疗前比较,①P<0.05
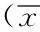
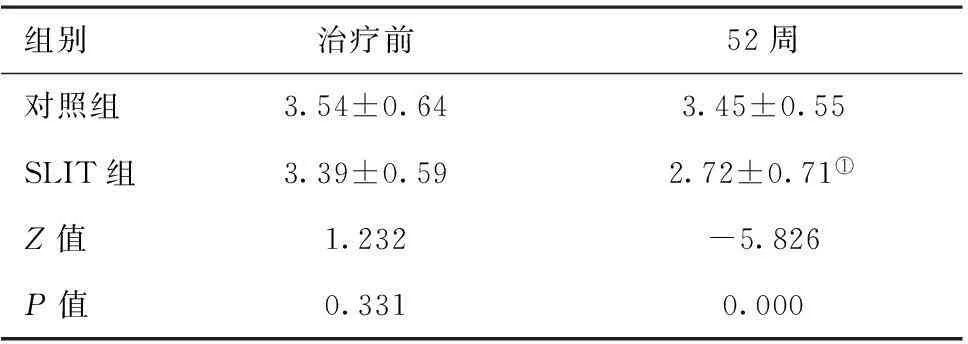
组别治疗前52周对照组3.54±0.643.45±0.55SLIT组3.39±0.592.72±0.71①Z值1.232-5.826P值0.3310.000
注:与治疗前比较,①P<0.05
3讨论
舌下特异性免疫治疗是目前过敏性疾病唯一可能对因治疗的方法,也已经成为针对过敏性疾病的临床常见治疗方法。研究显示,SLIT能够明显减轻鼻炎、哮喘症状和药物使用并具有长期疗效与预防作用。国内外大部分过敏性疾病患儿在皮肤点刺试验(skin prick test,SPT)和(或)血清学检测中显示其对多种过敏原过敏,但目前中国获得SFDA批准,符合GMP生产要求,标准化的SLIT疫苗只有粉尘螨的滴剂[1-4]。因此,多重过敏患者是否适合采用单一粉尘螨制剂进行治疗成为临床医生的难题之一。探讨单一制剂在多重过敏患者中临床疗效这一问题对临床实践具有重要的临床意义,同时也为今后舌下特异性免疫治疗机理研究提供临床依据。
近期国外研究显示[2,6-8],单一花粉在多种过敏原过敏季节性鼻炎患者中安全有效,单一尘螨SLIT对多种过敏原过敏常年性鼻炎患者有效[9]。国内,陈伯亚等研究显示,多种过敏患者在SLIT治疗1年时鼻炎症状改善不如单一过敏患者,但SLIT治疗2年时,两组疗效一致[14]。对于儿童AR,本课题组已经发表了对SLIT 1年观察(每4周随访1次,共13次),单一过敏患儿和多种过敏患儿的鼻部症状、对症药物,VAS评分,点刺风团等级明显低于治疗前,两组组间比较显示,除了在入组时和第20周多种过敏组对症用药评分高于单一过敏组,两组其他观察指标在13次随访中差异均无统计学意义[10],此结果与陈伯亚结果相似,多种过敏患者起效可能略慢于单一过敏组,但长期治疗结果是相同的。但由于受入组时多种过敏患儿对症用药积分已经高于单一过敏患儿和此类文献不是随机研究影响,多种过敏进行单一粉尘螨SLIT起效时间是否有差异还需要更多研究观察。
本研究采用随机对照研究方法对65例AR患儿进行1年观察显示,SLIT组和对症用药组患儿的鼻部症状,对症用药和患儿VAS评分在治疗1年后均低于治疗前,说明两种治疗方法都能改善患者症状,减少用药,减少AR对患儿的困扰。但仅仅SLIT组治疗1年后,皮肤点刺风团等级低于治疗前,而对症治疗组治疗后尘螨皮肤风团等级大于治疗前,说明SLIT 1年已经开始改善患儿过敏体质,单纯对症治疗没有类似疗效,可能过敏还有加重的趋势。SLIT组与对症治疗组两组组间比较显示,SLIT组患儿鼻炎症状明显低于对症治疗组,对症用药评分和VAS评分明显低于对症治疗组,尘螨皮肤反应等级在52周低于对症治疗组均说明,SLIT联合对症用药的疗效要明显优于单纯使用对症药物,并且减轻机体对于尘螨反应强度,预示着有可能已经开始改变过敏性疾病自然进程。在整个研究中两组患儿其他临床指标均相同,显示多种过敏患儿使用单一粉尘螨滴剂具有明显疗效。
由于粉尘螨与户尘螨的致敏蛋白具有高度同源性和交叉抗原性,因此本研究与前期研究一样将粉尘螨和或户尘螨皮肤点刺试验有阳性反应的患者视为单一过敏患者,这种分组方法在其他研究中也有报道[9]。本项研究中多种过敏患者除尘螨之外的过敏原阳性率为:热带五爪螨83 %、狗毛23%、德国小蠊17%、猫毛13%,与前期研究多种过敏组患儿过敏类似。
本研究表明单一粉尘螨制剂SLIT治疗对于主要由尘螨引起的多重过敏的患儿均有显著疗效,而这种疗效可能与患者的过敏状态无关,后续研究需要从免疫机理上获得更多证据,如IgG4[15]。
参考文献4
[1]Calderón MA,Cox L,Casale TB,et al.Multiple-allergen and single-allergen immunotherapy strategies in polysensitized patients: Looking at the published evidence[J].J Allergy Clin Immunol,2012,129(4):929.
[2]Malling HJ,Montagut A,Melac M,et al.Efficacy and safety of 5-grass pollen sublingual immunotherapy tablets in patients with different clinical profiles of allergic rhinoconjunctivitis[J]. Clin Exp Allergy,2009,39(3):387.
[3]Craig TJ,King TS,Lemanske RF Jr,et al.Aeroallergen sensitization correlates with PC(20) and exhaled nitric oxide in subjects with mild-to-moderate asthma[J].J Allergy Clin Immunol,2008,121(3): 671.
[4]J Li,B Sun,Y Huang,et al.A multicentre study assessing the prevalence of sensitizations in patients with asthma and/or rhinitis in China[J].Allergy,2009,64(7): 1083.
[5]G Ciprandi,I Cirillo.Monosensitization and polysensitization in allergic rhinitis[J].European Journal of Internal Medicine,2011,22(6):e75.
[6]G Ciprandi,G Cadario,C Valle,et al.Sublingual Immunotherapy in Polysensitized Patients: Effect on Quality of Life[J].J Investig Allergol Clin Immunol,2010,20(4): 274.
[7]HG Ciprandi,G Cadario,G M.Di Gioacchino,et al.Sublingual immunotherapy in children with allergic Polysensitization[J].Allergy Asthma Proc,2010,31(3):227.
[8]H.Nelson,M.Blaiss,H.Nolte,et al.Efficacy and safety of the SQ-standardized grass allergy immunotherapy tablet in mono- and polysensitized subjects[J].Allergy,2013,68(2): 252.
[9]J-E Lee,Y-S Choi,M-S Kim,et al.Efficacy of sublingual immunotherapy with house dust mite extract in polyallergen sensitized patients with allergic rhinitis[J].Ann Allergy Asthma Immunol,2011,107(1):79.
[10]Peng Li,Qi Li,Zhenghua Huang,et al.Efficacy and safety of house dust mite sublingual immunotherapy in monosensitized and polysensitized children with respiratory allergic diseases[J]. International Forum of Allergy & Rhinology,2014,4(10):1.
[11]中华耳鼻咽喉头颈外科杂志编辑委员会鼻科组,中华医学会耳鼻咽喉头颈外科学会鼻科学组、小儿组,中华儿科杂志编辑委员会.儿童变应性鼻炎诊断和治疗指南(2010年,重庆) [J].中华耳鼻咽喉头颈外科杂志,2011,46(1):7.
[12]顾之燕,董震.变应性鼻炎的诊治原则和推荐方案(2004年,兰州)[J].中华耳鼻咽喉头颈外科杂志,2005,49(3):166.
[13]中华耳鼻咽喉头颈外科杂志编委会鼻科组,中华医学会耳鼻咽喉头颈外科学分会鼻科学组.变应性鼻炎国内专家共识 [J].中华耳鼻咽喉头颈外科杂志,2011,46(12):976.
[14]陈伯亚,龙自铭,黄燕君,等.舌下含服粉尘螨滴剂治疗单一和多重过敏变应性鼻炎患者的临床疗效评估[J].中华耳鼻咽喉头颈外科杂志,2013,48(7):549.
[15]黎敏.标准化免疫治疗对哮喘儿童屋尘螨特异性IgG4和肺功能的影响[J].吉林医学,2013,34(21):42.
