医保目录中西药复方制剂3 350例安全问题分析与思考
2016-01-19孙小霞林志健董百惠朱春胜张晓朦
孙小霞,张 冰,林志健,董百惠,朱春胜,王 雨,张晓朦
医保目录中西药复方制剂3 350例安全问题分析与思考
孙小霞,张冰*,林志健,董百惠,朱春胜,王雨,张晓朦
[摘要]目的对《国家基本医疗保险、工伤保险和生育保险药品目录》(2009年版,本文简称《医保目录》)中西药复方制剂近30年来存在的安全问题进行分析,探讨该类制剂发生ADR/ADE的原因,并提出相关建议,指导临床合理用药。方法采用回顾性研究方法,检索和查阅中西药复方制剂的ADR/ADE文献及CFDA药品不良反应信息通报,应用统计学方法对资料进行整理和分析。结果共检索到最新版医保目录中西药复方制剂(包括同一药品的不同剂型)的ADR/ADE 3 350例,涉及药物品种39种,其中详细案例1 470例。由于该类制剂自身的特殊性,不良反应的发生率高,危害涉及人体多个器官及系统。此外,说明书信息不完善,使用过程存在超剂量、用药时间长、联合用药等问题,增加了该类制剂出现不良反应的风险。结论应对中西药复方制剂的安全问题引起高度重视,开展相关药品监管工作,增加药品安全性、有效性的基本评价,为临床安全、合理用药提供参考依据。
[关键词]中西药复方制剂;安全问题;合理用药
[Abstract]ObjectiveTo analyze the existing safety problems of Chinese-western medicine compound preparations in the latest edition of medical insurance directory in order to investigate the causes of ADR/ADE and provide suggestions and references for the supervision and policy-making as well as the rational use of drugs.MethodsBased on the related literature retrieval of domestic periodicals and the adverse drug reactions information bulletin of CFDA,which were analyzed by retrospective study method and statistic method.ResultsTotally 3 350 ADR/ADE cases about Chinese-western medicine compound preparations (including the same drug in different dosage forms) in medical insurance directory were retrieved,of which 1 470 detailed ADR/ADE cases were induced by 39 kinds of Chinese-western medicine compound preparations.Due to the particularity of the drugs,it led to high incidence of adverse reactions and harmful to multiple organs and systems.In addition,imperfect instruction information,overdose,long duration,combination use of drugs could increase the risk of adverse reactions.ConclusionWe should pay more attention to the safety problems of Chinese-western medicine compound preparations,promote related supervision measures and increase the basic evaluation of drug safety and effectiveness so as to provide reference for the safety of clinic and the rational use of drugs.
收稿日期:2015-01-26
通信作者*
DOI:10.14053/j.cnki.ppcr.201510037
Analysis and consideration of the safety problem of 3 350 cases about Chinese-western medicine compound preparations in medical insurance directorySUN Xiao-xia,ZHANG Bing*,LIN Zhi-jian,DONG Bai-hui,ZHU Chun-sheng,WANG Yu,ZHANG Xiao-meng (School of Chinese Pharmacy,Beijing University of Chinese Medicine,Beijing 100029,China)
Key words:Chinese-western medicine compound preparations;Security issues;Rational drug use
0引言
中西药复方制剂是我国当前药品注册分类中“中药、天然药物和化学药品组成的复方制剂”的简称,包括中药和化学药品,天然药物和化学药品,以及中药、天然药品和化学药品三者组成的复方制剂[1-3]。近年来,随着中西药复方制剂在临床的广泛应用,用药安全问题频繁暴露,引起公众的高度关注。在2012年中成药报告数排名前20名的品种中,其中有3个是中西药复方制剂[4]。另外,如2010年,中西药复方制剂维C银翘片就因严重ADR被国家药品监督管理局收入《药品不良反应信息通报》[5-6],2013年国家药监部门发布了珍菊降压片的不良反应信息通报[7],提醒公众关注中西药复方制剂的品种安全性问题,以降低用药风险。医保目录是保障我国群众经济安全用药、推进我国医疗卫生体制改革的重要组成部分之一,又有保险费用作为资金支持,要保障患者的用药需求,目录品种会较为丰富,可供选择的中西药复方制剂种类也较多。因此,本文以医保目录所收载的中西药复方制剂为例进行相关分析,共收集到该类制剂近30年的ADR/ADE案例3 350例,对其中1 470例详细案例进行重点分析,并对医保目录中中西药复方制剂现存的安全问题进行分析,探讨引发该类制剂ADR/ADE的原因,以加强对中西药复方制剂的科学监管,指导临床合理用药,保障公众的用药安全。
1资料与方法
1.1资料
1.1.1资料来源以《国家基本医疗保险、工伤保险和生育保险药品目录》(2009年版)收载的中西药复方制剂品种(72种)为例,检索近30年来国内期刊收载的ADR/ADE文献报道。
1.1.2检索策略以“药品名称”和“例/例报告”或“致”或“引起”或“过敏”或“不良反应”或“副作用”或“中毒”为检索词,系统检索 “中国期刊全文数据库(CNKI)”、“万方数据知识服务平台”、“中文科技期刊数据库(VIP)” (1984-2014年)的文献资料。以“药品名称”为检索词,查阅国家食品药品监督管理总局(CFDA)网站上发布的《药品不良反应信息通报》。
1.1.3文献筛选根据文献报告将最新版医保目录中西药复方制剂的ADR/ADE案例入选,排除涉嫌转载或重复的案例。
1.2方法采用回顾性研究方法,对收集到的文献资料进行系统整理与分析,录入数据信息,主要包含发表时间及例数、患者基本情况(性别、年龄、既往病史及过敏史情况)、ADR/ADE涉及的中西药复方制剂的情况,应用SAS 9.30软件对获得的数据进行统计分析。
2结果
2.1文献资料共检索到医保目录中西药复方制剂的ADR/ADE 3 350例,其中详细案例1 470例,共698篇文献,来自225种国内期刊,涉及的药物品种共39种(54.17%),包括24种口服制剂(33.33%)、5种注射剂(6.94%)、10种外用制剂(13.89%)。依据药物功能不同可分为9类:降血压类、降血糖类、心血管类、抗感冒类、止咳化痰平喘类、跌打损伤类、消化系统类、外用类、其他类等。其中ADR/ADE涉及案例居前10位的中西药复方制剂品种情况,见表1。

表1 ADR/ADE涉及案例居前10位的中西药复方制剂品种
2.2患者的基本情况
2.2.1患者年龄、性别分布1 470例ADR/ADE中,患者年龄、性别分布情况见表2。其中男773例,女662例;年龄最小者为16 d,最大者为91岁,中青年者占59.46%,60岁以上者占14.49%。
2.2.2患者的既往疾病史和过敏史情况1 470例ADR/ADE案例中,既往有疾病史的病例为430例(29.25%),疾病史包括糖尿病、心血管疾病、肾病、肝病、胃病、癫疒间病、银屑病、精神病及手术史等。患者的过敏史情况,既往有过敏史者57例(3.88%),其中含磺胺类过敏8例、青霉素过敏9例、先锋霉素过敏1例、扑尔敏过敏1例、过敏体质5例;无过敏史者354例(24.15%);不详1 056例(72.03%)。
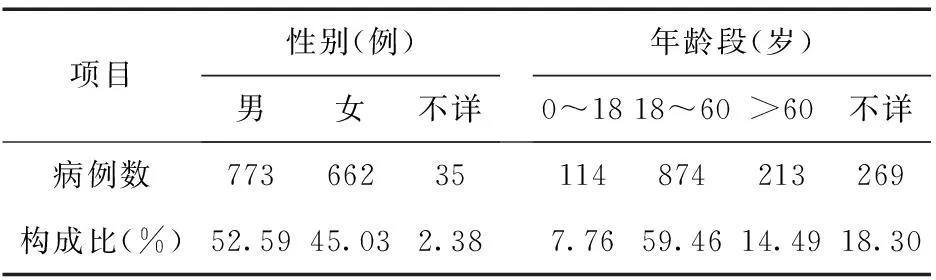
表2 患者的年龄、性别分布
2.3ADR/ADE涉及的中西药复方制剂
2.3.1ADR/ADE发生的例数及时间分布1 470例ADR/ADE案例中,不良反应出现最快的时间是在用药15 s后,最久的时间是在用药2年后,其中发生不良反应的时间多集中在用药1~14 d内,共475例(32.31%),其次为1 h~1 d内,共170例(11.56%),再次为10~60 min,共156例(10.61%),见表3。

表3 ADR发生的例数及时间分布
2.3.2不同给药途径致ADR/ADE的分布1 470例ADR/ADE案例中,注射给药占较大比例,包括静脉滴注和肌肉注射2类,共606例(41.22%);其次为口服给药,共513例(34.90%)。见表4。
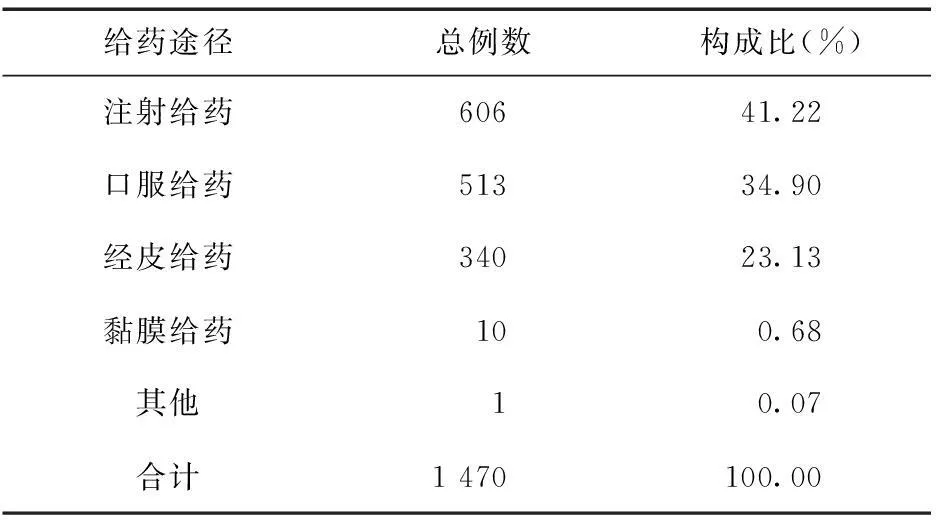
表4 不同给药途径致ADR/ADE的分布
2.3.3ADR/ADE中的药物联用情况1 470例ADR/ADE案例中,有193例(13.13%)单独用药,325例(22.11%)联用其他药物,其中联合用药以抗菌药物(氨基糖苷类、青霉素类、林可霉素类、头孢菌素类、大环内酯类、喹诺酮类)为主,共179例(占12.18%),其他联合的药物为抗炎药、抗感冒药、降血糖药、中成药、中药汤剂、中药注射液等,见表5。

表5 ADR/ADE中的药物联用情况
2.3.4ADR/ADE累及的器官/系统及临床表现ADR/ADE案例累及人体多个器官/系统,临床表现复杂(见表6)。其中以皮肤及附件损害较多,共531例(24.20%);其次为神经系统损害,共333例(15.18%);再次为全身性损害,共309例(14.08%)。
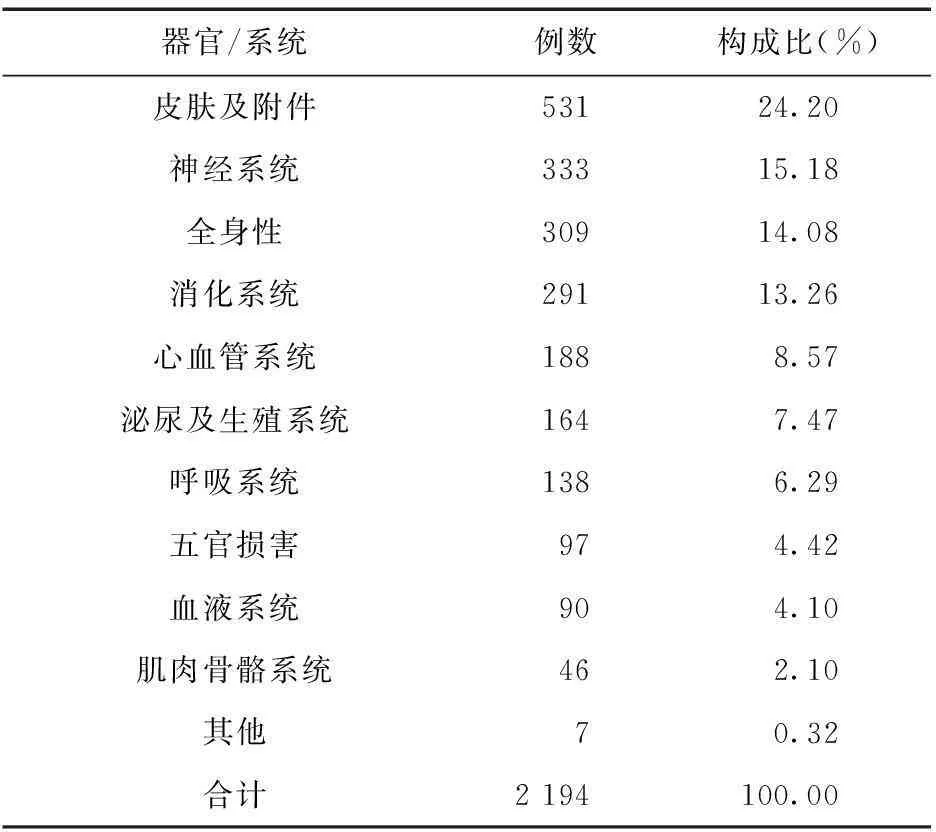
表6 ADR累及器官/系统及临床表现
注:部分案例涉及多个器官/系统
2.3.5ADR/ADE的转归1 470例ADR/ADE案例中,绝大多数患者转归情况良好,见表7。其中好转974例(66.26%),治愈218例(14.83%);发生严重的ADR/ADE 167例(含79例过敏性休克反应),其中持续治疗者16例(1.09%),死亡者33例(2.24%)。其余不详。
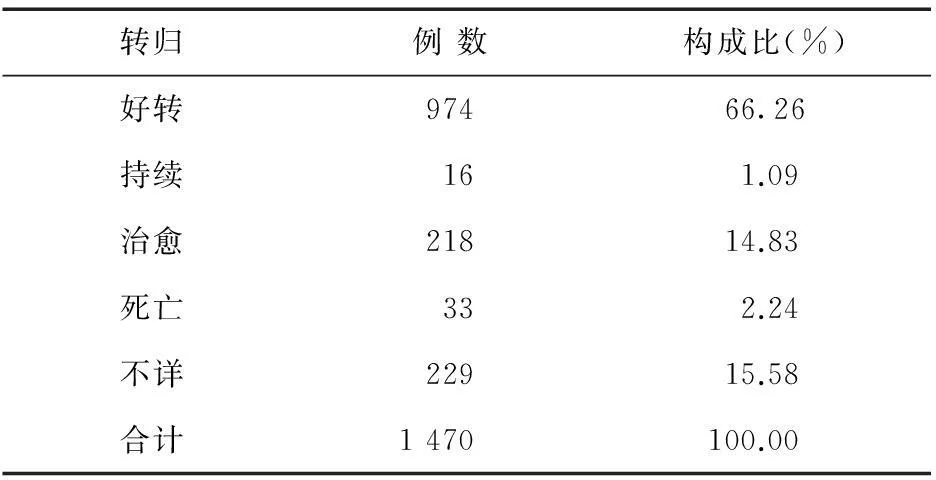
表7 ADR的转归情况
3中西药复方制剂的安全问题分析
目前,国家药品标准中收载的中西药复方制剂品种约有389个[2]。以医保目录(最新版)为例,其中收载中西药复方制剂72个品种。除西藏外,所有省区都有中西药复方制剂的生产企业。其中有16个品种为独家生产,ADR/ADE涉及的中西药复方制剂品种为39种(占54.17%),说明该类制剂的不良反应发生率高,需对该类制剂的临床安全性引起重视。研究结果显示,1 470例中,中西药复方制剂的不良反应累及人体多个器官/系统,主要为皮肤及附件损害(24.20%)、神经系统损害(15.18%)、全身性损害(14.08%)。其中严重过敏性休克反应为79例(5.37%),均发生在给药30 min内,与其他文献报道相似[8]。本研究中涉及的维C银翘片被2010年国家《药品不良反应信息通报》所收载,2004-2010年报道的病例总数达1 885例[5],本次研究又补充了该品种的ADR案例164例,共计2 049例(61.16%),主要累及神经系统、消化系统、皮肤及附件等。随着维C银翘片、珍菊降压片被药监部门的相继通报,引起社会对中西药复方制剂的广泛关注,起到了一定的安全警示作用。因此,应关注患者在使用此类制剂时的临床表现及主要生命指征,做好相关急救措施,尤其重视过敏性休克反应,用药期间一旦出现心慌、胸闷、皮肤瘙痒、恶心等症状,应立即停药给予及时治疗,避免出现严重不良反应。笔者认为,可从以下几方面对中西药复方制剂的安全问题以及合理用药进行探讨。
3.1药物自身因素中西药复方制剂的药学基础研究工作较为薄弱,组方合理性及安全性方面的研究较少,缺乏指导临床合理用药的科学依据。此外,品种的归属界定不确切,以至于个别药品在地方标准升国家标准时,分别被中药国家标准和西药国家标准收载,出现同名异方、异方同名现象及品种类别管理的混乱,导致同一品种在不同制药企业存在质量差异性,增加用药风险[9]。中西药复方制剂的品种较多,处方成分复杂,使其在质量控制方面难以把握,尤其口服制剂和注射剂的质量问题更应引起重视。研究显示,中西药复方制剂的不良反应主要集中在抗感冒类、降血糖类、降血压类、止咳平喘类、消化系统类、跌打损伤类等药物,涉及的剂型有针剂、丸剂、颗粒剂、片剂、胶囊、糖浆剂及一些外用制剂,所含西药成分主要有格列苯脲、氢氯噻嗪、水杨酸甲酯、吲哚美辛、对乙酰氨基酚、马来酸氯苯那敏、盐酸小檗碱、维生素类、矿物质类等。如降压类中西药复方制剂所含的氢氯噻嗪成分,是一种噻嗪类利尿药,使用时可抑制胰岛素的释放,使糖耐量降低,继而升高血糖,如用于治疗兼有高血压和糖尿病史的患者,会加重糖尿病的病情。此外,氢氯噻嗪成分还能干扰肾小管排泄尿酸,引发高尿酸血症,故肝肾功能不全者、痛风患者、糖尿病患者及孕妇均不宜服用。
3.2机体因素不同年龄、性别的个体对于药物的吸收、分布、排泄、代谢不同,所占的ADR/ADE比例也不同。研究结果显示,18~60岁者占59.46%,其次为60岁以上者(占14.49%),与其他文献报道的年龄分布相似[3]。中老年患者在生理、心理方面均处于衰退阶段,用药安全方面存在隐患。如生理上,老年患者大多存在着不同程度系统、器官功能的衰退,对于药物的耐受和代谢能力较成年人弱,对药物剂量的个体差异也较大,使得不良反应的发生率升高。心理上,老年患者对于安全合理用药的意识较差,自我风险管理能力较弱,而且多数患者往往身患数病,求医心切、用药依从性明显,易出现药物的不合理使用情况。在出现ADR/ADE的患者中,既往有疾病史的患者ADR/ADE的发生率相对较高,其临床治疗恢复也较缓慢,易出现严重不良反应。此外,56例有既往过敏史的患者中(占3.82%),主要为青霉素和磺胺类过敏;354例既往无过敏史的患者在用药时也出现不良反应,说明无过敏史的患者在使用该类制剂时也应引起足够重视。因此,临床应用时应仔细阅读药品说明书,重视特殊人群、特殊症状及体质患者的用药问题,关注患者的既往疾病史和过敏史情况,避免不良反应的发生。
3.3用药因素研究表明,1 470例中,不良反应的时间多集中在1~14 d (32.31%),1 h以内者多以过敏反应为主,还有一些不良反应出现在用药14 d以后(8.78%),说明有些药物的不良反应存在迟发的特性。部分案例存在超剂量和疗程久的用药问题,易引起中毒反应,需在用药期间密切观察患者的临床表现,提醒患者定期去医院查血象、肝肾功能等,确保用药安全有效。不同给药途径直接影响着药物在体内的代谢、吸收和药效。上述结果显示,注射给药的ADR发生率最高(41.22%),其次为口服给药(34.90%)、经皮给药(23.13%)、黏膜给药(0.68%),说明给药途径对于药物不良反应的发生与否及严重程度也有影响。此外,联合用药的不良反应发生率有明显增加,主要以联合抗菌药物引发的不良反应为主,共179例(12.18%)。如:青霉素类、头孢菌素类本身易出现不良反应,联合用药又会增加不良反应的发生率。当中西药复方制剂与其他中成药、汤剂、中药注射液合用时,可能因其配伍禁忌、相同成分的剂量叠加而发生不良反应,如含有“天花粉”成分的消渴丸、海珠喘息定片、天麦消渴片等,应避免与含附子、乌头类的中成药或汤剂一起合用;当与其他西药合用时,可能因相同成分的剂量叠加超出单一使用量或不同成分间产生拮抗作用而出现不良反应,如维C银翘片与其他含马来酸氯苯那敏、对乙酰氨基酚的感冒药合用时,由于含同种化药成分,造成剂量增加,出现对肝脏的损害[10]。因此,临床应用时需关注药物之间的合理联用,避免出现不良反应。
3.4药品说明书问题药品说明书是药品安全性、有效性等重要信息的详细说明,是临床医生和患者用药时的重要依据,是合理用药和药物不良反应监测的重要参考资料[11]。中西药复方制剂的药品说明书主要存在缺项、信息不详、条理不清等问题,如:①个别药品的名称和纯中药制剂难于区分,仅看药品通用名称,很难判断其处方所含成分,易被医生和患者混淆,如维C银翘片、复方罗布麻颗粒、复方黄连素片等;②未明确标示用法用量,缺少用药剂量和疗程的相关提示,公众用药时很难将药物剂量严格控制在常规剂量范围内,超剂量或长期服用都会引起严重的药物不良反应;③将不良反应、禁忌证以及药物相互作用等内容写进注意事项,而对于某些在实际用药过程中易发生的问题却未明确说明,如未对所含西药成分的一般注意事项做完整说明,有些西药成分若长期服用易引起在机体内的蓄积;④未强调特殊人群、特殊症状及特殊体质患者的用药问题,许多西药成分对于老年人、妊娠/哺乳期妇女、儿童、运动员、慢性病患者、肝肾功能不全患者都应当谨慎使用;⑤不良反应、禁忌、注意事项等项目内容有缺项、描述简单或根本不提及,通常可见“小儿酌减”、“遵医嘱”、“不详”、“尚不明确”等字样,无法为临床合理用药提供安全信息,存在一定的用药风险;⑥未添加“不能口服”或“不能外用”等明显字样来提醒患者正确用药,避免因误服误用造成的严重不良反应,如一些外用贴剂、膏剂未注明皮肤溃破者禁止贴敷患处,一些患者误用后,易出现皮肤感染、脓疱等不良反应[12-17]。因此,建议在说明书中增加“中西药复方制剂”、“请仔细阅读说明书并按说明使用或在药师指导下购买和使用”等警示语,提醒患者注意。单独列出所含的西药成分,对用法用量进一步细化,标明用药时间、剂量、次数、疗程及使用方法。尤其不良反应、用药禁忌、注意事项、药物相互作用等项目的书写更要全面、细致。
4总结
综上所述,医保目录中中西药复方制剂存在的安全问题应引起高度重视,同时也要关注医保目录之外的其他中西药复方制剂的安全问题及用药风险。中西药复方制剂是一类特殊的药品,不同于纯中药制剂、化学药制剂,需加强该类制剂的监测与通报工作,及时反馈有关此类制剂的ADR信息,提醒公众用药时对其进行充分的效益和风险分析。对已上市的药品说明书进行适时修订,确保该类制剂说明书项目和内容得到及时补充和完善,增加药品安全性、有效性、合理性的基本评价。对该类制剂的用药风险与效益进行科学评估,尤其是含有多种化学成分的非外用品种的合理性、安全性需要进行重新评估。加强社会药房及医院工作人员对中西药复方制剂的认识,多组织培训中西药复方制剂相关法规、合理应用及不良反应防范的专业知识,提高药学服务质量,对患者进行正确的用药指导,保证用药的安全有效。从各个环节着手制定有效的控制措施,以达到控制ADR/ADE的发生,指导临床安全、合理使用药物的目的。中西药复方制剂不仅是中西医结合的发展方向,也是新药研究和开发的一个重要突破点,需要不断地摸索和探讨,使中西药复方制剂更好地为临床服务,保障公众的用药安全。
参考文献:
[1]药品注册管理办法[J].中国新药与临床杂志,2008,10:303-312.

[2]于永江,余伯阳,钱忠直.关于我国中西药复方制剂科学监管的思考[J].中国中药杂志,2011,11:1542-1546.
[3]吴家瑞,董玲,张冰,等.中西药复方制剂不良反应信息数据挖掘研究[J].中国执业药师,2011,12:10-12,15.
[4]国家食品药品监督管理总局.国家食品药品监督管理局发布2012年药品不良反应监测年度报告(EB/OL)(2013-03-14),[2013-03-14].http://www.sfda.gov.cn/WS01/CL0051/79058.html.
[5]国家局提醒关注中西药复方制剂维C银翘片安全性问题[J].中国医药报,2010,9(21):A01.
[6]国家食品药品监督管理局.关注中西药复方制剂维C银翘片的安全性问题[J].中国社区医生,2010,38:9.
[7]国家食品药品监督管理局.关注中西药复方制剂珍菊降压片的用药风险[J].中国医学前沿杂志,2013,4:11.
[8]吴嘉瑞,张冰.清开灵注射剂致过敏性休克流行病学特点研究[J].中药新药与临床药理,2007,1:74-77.
[9]周亚丽,韩峰.中西药复方制剂存在的问题及不良反应分析[J].内蒙古中医药,2011,1:71-72.
[10]朱立平,马秉智,常明.含有明确化学成分中成药的统计与分析[J].中国药学杂志,2007,12:959-960.
[11]药品说明书和标签管理规定[S].国家食品药品监督管理局令第24号,2006:4-5.
[12]徐燕侠,曾艳,孟莉.《新编国家中成药》收载品种中含化学药成分的统计与思考[J].中国药房,2006,5:392-393.
[13]吴嘉瑞,张冰.中药注射剂药物警戒探析(三)[J].中国执业药师,2011,8(5):47-49.
[14]吴嘉瑞,张冰.穿琥宁注射剂致血小板减少62例文献分析[J].药物不良反应杂志,2006,1:24-27.
[15]吴嘉瑞,张冰.中药不良反应评价方法的分析与思考[J].中国执业药师,2009,6(12):3-5.
[16]翟永松,吴嘉瑞,龚慕辛,等.中西药复方制剂的风险管理[J].临床药物治疗杂志,2013,6:27-29,62.
[17]张艳华,赵庆军.中成药说明书内容分析与药学服务[J].实用药物与临床,2014,17(2):252-255.
·短篇报道·
作者单位:1.吉林省珲春市人民医院临床药学室,吉林 珲春
133300;2.吉林大学第一医院药学部,长春 130000
