大黄滴眼液质量标准研究
2016-01-19汪映宇
大黄滴眼液质量标准研究
汪映宇
(苏州市食品药品检验所,苏州215004)
摘要:目的建立大黄滴眼液的质量标准。方法选用TLC法鉴别制剂中大黄有效成分大黄酸;进行pH等项目的检查;选用HPLC法测定芦荟大黄素、大黄酸、大黄素和大黄酚的含量。结果薄层色谱斑点清晰,分离度好。芦荟大黄素在2.532~50.646 μg·mL`(-1)范围内呈良好的线性关系(r=1.000 0),平均回收率为91.8%,RSD为0.79%。大黄酸在3.764~75.280 μg·mL`(-1)范围内呈良好的线性关系(r=1.000 0),平均回收率为99.4%,RSD为1.46%。大黄素在2.608~52.160 μg·mL`(-1)范围内呈良好的线性关系(r=1.000 0),平均回收率为92.4%,RSD为0.87%。大黄酚在2.499~49.989 μg·mL`(-1)范围内呈良好的线性关系(r=0.999 9),平均回收率为92.6%,RSD为0.85%。结论该方法操作简单,结果可靠,可用于大黄滴眼液的质量控制。
关键词:大黄滴眼液;质量标准;薄层色谱;高效液相色谱
doi:10.3969/j.issn.1004-2407.2015.03.007
中图分类号:R282
文献标志码:A
文章编号:1004-2407(2015)03-0241-04
Abstract:ObjectiveTo establish the quality standard for Dahuang Eye Drops.Methods Thin-layer chromatography was used to identify rhein; the pH of this formulation and other items were checked; and the content of aloe-emodin, rhein,emodin and chrysophanol were determined by HPLC. Results The TLC identification was distinct and the spots were clear. The linear range of aloe-emodin was 2.532-50.646 μg·mL`(-1)(r=1.000 0) with an average recovery of 91.8% (RSD=0.79%). The linear range of rhein was 3.764-75.280 μg·mL`(-1)(r=1.000 0) with an average recovery of 99.4% (RSD=1.46%). The linear range of emodin was 2.608-52.160 μg·mL`(-1)(r=1.000 0) with an average recovery of 92.4% (RSD=0.87%). The linear range of chrysophanol was 2.499-49.989 μg·mL`(-1)(r=0.999 9) with an average recovery of 92.6% (RSD=0.85%).Conclusion This method is simple and reliable, so it could be used for the quality control of Dahuang Eye Drops.
收稿日期:(2014-10-23)
Study on the quality standard for Dahuang Eye Drops
WANG Yingyu(Suzhou Institute for Food and Drug Control, Suzhou 215004,China)
Key words: Dahuang Eye Drops; quality standard; TLC; HPLC
大黄滴眼液为苏州市中医医院眼科经验方,由大黄、黄芩素、硼酸、硼砂、羟苯乙酯、氯化钠组成,临床上用于急慢性结膜炎、红眼及对西药过敏的眼疾患者,疗效显著。大黄作为其主药,对多种细菌均有不同程度的抑制作用[1]。由于传统医院制剂存在质量不稳定的缺点[2],且质量标准水平普遍较低[3],为更好地控制大黄滴眼液的质量,本文选用TLC法鉴别制剂中的主药大黄有效成分大黄酸[4],选用HPLC法测定大黄中芦荟大黄素、大黄酸、大黄素、大黄酚的含量,以期建立可行的质量标准,为保证其临床用药安全有效提供依据。
1仪器与试药
1.1仪器拍照系统:CAMAG TLC VISVALIZER(瑞士卡玛公司);HPLC:Waters e2695/waters 2489 UV Detector(美国Waters公司)。
1.2试药大黄滴眼液(批号140312,140324,140331);大黄对照药材(批号200402)、芦荟大黄素对照品(批号201007,质量分数98.0%)、大黄酸对照品(批号200206,质量分数100.0%)、大黄素对照品(批号200110,质量分数100.0%)、大黄酚对照品(批号201118,质量分数99.5%),均由中国药品生物制品检定所提供;盐酸为优级纯(国药集团化学试剂有限公司);磷酸为优级纯(国药集团化学试剂有限公司);水为超纯水;甲醇为色谱纯(SIGMA-ALDRICH);其余试剂均为分析纯。
2方法与结果
2.1性状本品为红棕色澄明液体。
2.2薄层色谱(TLC)鉴别取本品20 mL,加盐酸3 mL,加热回流30 min,冷却,用乙醚振摇提取4次(30,20,10和10 mL),合并乙醚液,挥干,残渣加适量甲醇溶解,并定容至5 mL量瓶中,作为供试品溶液。取阴性样品(不加大黄),按供试品溶液的制备方法,制成阴性对照溶液。另取大黄对照药材0.1 g,加甲醇20 mL,浸泡1 h,滤过,取滤液5 mL,蒸干,残渣加水10 mL使溶解,再加盐酸1 mL,加热回流30 min,冷却,用乙醚振摇提取2次,每次20 mL,合并乙醚液,蒸干,残渣加三氯甲烷1 mL使溶解,作为对照药材溶液。再取大黄酸对照品,加甲醇制成每1 mL含1 mg的溶液,作为对照品溶液。照薄层色谱法[5](《中国药典》2010年版附录 B)实验,吸取上述溶液各5 μL分别点于同一以羧甲基纤维素钠为黏合剂的硅胶H薄层板上,以环己烷-乙酸乙酯-甲酸(12∶3∶0.1)为展开剂,展开,取出,晾干。置于紫外光灯(365 nm)下检视。阴性色谱中,在与对照药材色谱相应的位置上,无斑点。供试品色谱中,在与对照药材色谱相应的位置上,显相同的5个橙黄色荧光主斑点,置于氨蒸气中熏后,斑点变为红色;阴性对照无干扰。
2.3检查参照《中国药典》2010年版一部附录ⅠY要求制定本品的检查项目,包括pH值、可见异物、渗透压浓度、无菌、重金属检查、砷盐检查项。
2.4含量测定
2.4.1色谱条件与系统适用性实验以TURNER 100A C18(250 mm×4.6 mm,5 μm)为填充剂;以甲醇-1 mL·L-1磷酸溶液(75∶25)为流动相;检测波长为254 nm。理论板数按大黄素峰计算应不低于3 000。(流速:1 mL·min-1;柱温:35 ℃;进样量:10 μL)。
2.4.2对照品溶液的制备精密称取芦荟大黄素、大黄酸、大黄素、大黄酚对照品6.46,9.41,6.52和6.28 mg,置于50 mL量瓶中,用甲醇溶解并稀释至刻度,然后再稀释10倍,至各质量浓度为12.662,18.820,13.040和12.497 μg·mL-1,作为混合对照品溶液。
2.4.3供试品溶液的制备精密量取本品20 mL,置于烧瓶中,加盐酸溶液3 mL,加热回流30 min,冷却,用乙醚分4次萃取(30,20,10和10 mL),合并乙醚液,挥干,用甲醇定容至10 mL量瓶中,离心,即得。
2.4.4专属性实验在2.4.1项下色谱条件,芦荟大黄素、大黄酸、大黄素、大黄酚峰形良好,阴性样品对主峰无干扰。见图1。
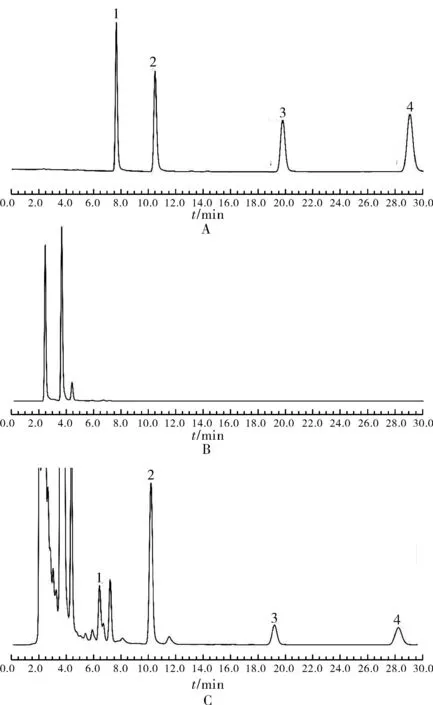
图1HPLC图
A.对照品溶液;B.大黄滴眼液阴性样品溶液;C.大黄滴眼液样品溶液;1.芦荟大黄素;2.大黄酸;3.大黄素;4.大黄酚
Fig.1 HPLC chromatograms
A.control substances;B.negative control;C.sample;1. aloeemodin;2.rhein;3.emodin;4.chrysophanol
2.4.5标准曲线及线性范围分别精密吸取混合对照品溶液配制成相应质量浓度的对照品溶液,分别进样10 μL,记录峰面积,以质量浓度为横坐标、峰面积A为纵坐标,绘制标准曲线,得到回归方程。结果表明,芦荟大黄素、大黄酸、大黄素和大黄酚对照品质量浓度分别在2.532~50.646,3.764~75.280,2.608~52.160和2.499~49.989 μg·mL-1范围内,均呈良好的线性关系。见表1。
表1标准曲线及线性范围
Tab.1 Data of standard curves and linear ranges

成分线性范围/μg·mL-1标准曲线方程相关系数r芦荟大黄素2.532~50.646Y=56040X-337951.0000大黄酸3.764~75.280Y=46331X-393181.0000大黄素2.608~52.160Y=41602X-314051.0000大黄酚2.499~49.989Y=57953X-374230.9999
2.4.6精密度实验精密吸取混合对照品溶液10 μL,按照2.4.1项下色谱条件连续进样6次,记录芦荟大黄素、大黄酸、大黄素、大黄酚的峰面积。结果芦荟大黄素、大黄酸、大黄素和大黄酚峰面积的RSD分别为0.260%,0.293%,0.378%和0.311%。
2.4.7重复性实验分别精密量取同一份大黄滴眼液样品6份,每份20 mL,按照2.4.3项下方法制备供试品溶液,按上述高效液相色谱条件测定。结果芦荟大黄素含量的RSD为2.087%,大黄酸含量的RSD为1.980%,大黄素含量的RSD为1.453%,大黄酚含量的RSD为1.914%。
2.4.8稳定性实验取混合对照品溶液,按2.4.1项下色谱条件分析,分别在0,1,2,4,6,8和12 h进样10 μL,RSD分别为1.208%,0.511%,1.536%和0.668%,表明对照品溶液在12 h内稳定。
2.4.9加样回收率实验取同一批大黄滴眼液6份,精密量取10 mL,分别精密加入混合对照品溶液(芦荟大黄素、大黄酸、大黄素、大黄酚的质量浓度分别为12.662,18.820,13.040和12.497 μg·mL-1)0.6 mL。照2.4.3项下方法制备供试溶液,按2.4.1项下色谱条件测定,计算回收率,结果见表2。
2.4.10样品测定分取3批大黄滴眼液,按照4.3项下方法操作,提取供试品溶液,注入高效液相色谱仪,测定芦荟大黄素、大黄酸、大黄素、大黄酚的色谱峰面积,结果3批样品中芦荟大黄素的含量分别为3.328 2,3.346 6和3.397 6 μg·mL-1;大黄酸的含量分别为19.115 2,19.212 1和19.184 2 μg·mL-1;大黄素的含量分别为4.115 9,4.133 0和4.254 2 μg·mL-1;大黄酚的含量分别为3.647 8,3.674 3和3.744 6 μg·mL-1。
表2加样回收率实验结果
Tab.2 Results of recovery tests

( n=6)
3小结与讨论
在供试品溶液制备中,预实验考察了:加盐酸的量(1,3,5和10 mL);酸化回流时间(30,60和90 min);用乙醚回流和不回流萃取(乙醚回流:考察加乙醚量10,20,30和40 mL和回流时间30,60和90 min);用乙醚萃取的量(20,20,20和10或30,20,20和10 mL)。结果表明,加盐酸3 mL,加热回流30 min,不用乙醚回流,直接用乙醚(30,20,20和10 mL)萃取,提取效率最高。综上所述,本研究制备工艺合理可行,质量标准科学可靠。
大黄滴眼液作为苏州市中医医院眼科经验方,沿用至今,疗效显著,成本低,在临床长期使用中受到广大患者的欢迎,是典型的传统医药制剂。本文采用灵敏度高、重复性好的TLC和HPLC等方法建立和优化了其质量标准,并做了完整的方法学验证,以期确保大黄滴眼液质量的稳定和安全,为临床用药安全有效提供依据。
参考文献:
[1]李广峰.大黄的药理作用及临床应用分析[J].中国医药指南,2013,11(16):317-318.
[2]马尔丽.中国医院制剂的历史、现状和发展策略[J].中国药事,2007,21(9):713-715.
[3]杨雪梅.医院制剂的质量现状和发展趋势[J].中国药事,2007,21(9): 716-717.
[4]王义潮,朱婧怡,崔延堂,等.大黄中大黄酸提取新方法研究[J].西北药学杂志,2011,26(2):84-86.
[5]国家药典委员会.中国药典2010年版[S].一部.北京:中国医药科技出版社,2010:22.
