南极假丝酵母脂肪酶B催化3-(4-氟苯基)戊二酸酐不对称醇解
2016-01-14贾义刚,杨震炯,刘维明等

南极假丝酵母脂肪酶B催化3-(4-氟苯基)戊二酸酐不对称醇解
贾义刚1,杨震炯2,刘维明1,张洋1,黄和1,胡燚1
(1. 南京工业大学材料化学工程国家重点实验室,江苏南京210009;
2. 永康市质量技术监督检测中心,浙江永康321300)
摘要:采用分子模拟技术,研究了南极假丝酵母脂肪酶B(Candida antarctica lipase B,CALB)催化3-(4-氟苯基)戊二酸酐(3-FGA)不对称醇解的分子机制。首先借助力场修改的Autodock 4.2软件将过渡态底物与CALB进行对接,根据对接自由能差异解析了CALB催化3-FGA与不同醇反应的立体选择性差异,得到的S型底物结合能小于R型底物;其次,基于扭转角机制分析发现,S型底物扭转角小于R型底物,从分子水平上揭示了CALB对S型底物选择性优于R型底物的机制。
关键词:南极假丝酵母;脂肪酶; 3-(4-氟苯基)戊二酸酐;分子对接;分子动力学;对映选择性
doi:10.3969/j.issn.1672-3678.2015.04.011
收稿日期:2014-09-06
基金项目:国家高技术研究发展计划(863计划)(2011AA02A209)
作者简介:贾义刚(1989—),男,山东济阳人,硕士研究生,研究方向:生物催化;胡燚(联系人),教授 ,E-mail:huyi@njtech.edu.cn
中图分类号:Q71文献标志码:A
Enantioselective alcoholysis of 3-(4-fluorophenyl)glutaric anhydride catalyzedbyCandidaantarcticalipase B
JIA Yigang1,YANG Zhenjiong2,LIU Weiming1,ZHANG Yang1,HUANG He1,HU Yi1
(1. State Key Laboratory of Materials-Oriented Chemical Enqineering,Nanjing Tech University,Nanjing 210009,China;
2. Quality and Technical Supervision and Inspection Center of Yongkang City,Yongkang 321300,China)
Abstract:We studied enantioselective alcoholysis of 3-(4-fluorophenyl) glutaric anhydride(3-FGA) by Candida antarctica lipase B(CALB) through molecular simulation technology. The transition state substrates were docked with CALB by using Autodock 4.2 whose force file was modified. The enantioselective difference of the alcoholysis of 3-FGA with various alcohols catalyzed by CALB was proved by the differences of binding energy. The binding energy of S-enantiomer was smaller than R-enantiomer. Furthermore,we also found that the torsional angle of S-enantiomer was smaller than R-enantiomer through analyzing the torsional angle mechanism, CALB showed an S-enantiomer enantiopreference from the molecular level.
Keywords:Candida antarctica; lipase; (3-(4-fluorophenyl)glutaric anhydride; molecular docking; molecular dynamics; enantioselectivity
手性3-(4-氟苯基)戊二酸单酯是一种重要的药物中间体,可用于合成抗抑郁药帕罗西汀以及P2X7受体抑制剂[1-3]。酶法因其催化效率高、立体选择性强和反应条件温和等优点而被广泛应用于手性单酯的合成。目前,酶法制备3-氟苯基戊二酸单酯的方法主要是脂肪酶催化3-(4-氟苯基)戊二酸二酯的不对称水解和3-(4-氟苯基)戊二酸酐(3-FGA)的不对称醇解[4-6]。在前期工作中,笔者所在课题组的Liu等就南极假丝酵母脂肪酶B(CALB)催化3-FGA的不对称醇解反应的工艺条件进行了系统研究,在研究中发现,当采用不同链长和结构的醇作为酰基受体与3-FGA反应时,脂肪酶表现出不同的催化性能,如脂肪酶活性和选择性随酰基受体链长增加而降低。然而,目前CALB在采用不同链长的醇作为酰基受体时表现出的对映选择性差异机制尚不清楚,近年来,分子模拟作为一种辅助技术,为酶的催化机制解析提供了强大支持[8-9]。
为此,从分子模拟的角度对3-(4-氟苯基)戊二酸酐的去对称醇解反应进行研究,从分子水平解析酶催化3-FGA去对称醇解的分子机制,揭示酶与不同醇之间的相互作用,对研究醇解反应具有重要的意义。
1材料与方法
1.1分子对接
1.1.1受体酶分子准备
CALB的pdb结构从蛋白质结构数据库RCSB(Protein Data Bank,PDB)获取(PDB ID:1TCA)。首先利用Autodock 4.2删除晶体结构中水分子,添加缺省的H及其原子的部分电荷;为了保证对接过程真实于反应条件,笔者采用过渡态对接,将活性中心的丝氨酸Ser质子化,删除—OH中的H原子,并利用RESP对其电荷分布重新拟合(电荷:-1)。将处理后的结构保存为pdbqt格式,以备下一步对接工作。
1.1.2配体的准备
利用ChemOffice 3D 软件构建过渡态底物。在构建的过渡态底物过程中,将其羰基中的O 原子设置成带一个单位负电荷。进而,利用MM2 模块对底物结构进行能量最小化。用Chimera1.8添加缺省的氢原子及部分原子电荷,并手动删除底物上与酰基受体相连的羰基O原子的H原子,得到分子总电荷为-1,保存为mol2格式,以备下一步工作使用。
1.1.3力场修改
为实现底物与受体CALB活性口袋部位的成功对接,底物与受体必须满足四面体过渡态对接条件。考虑到过渡态对接时,配体分子中羰基的O原子远离Thr40氧负离子,无法形成氢键,因而对配体丝氨酸的OG 与配体CT 的范德华力(vdW) 及范德华势能ε参数进行修正。一方面,通过减小OG与CT的间距来降低OG和CT的范德华作用,另一方面,通过OG 和CT 的相互作用力提高范德华势能ε值,以降低对接势能。本研究最终将丝氨酸OG原子的原子类型改为非键类型,范德华参数修正:ε=2.93×105J、半径σ=0.15 nm;对接过程中,所有配体分子的CT 原子范德华参数修正为ε=1.26×105J、半径σ=0.15 nm;同时,受体与配体分子的O1、O2 原子形成的氢键ε值修正为1.26×105J[10-11]。
1.1.4底物对接
本文采用半柔性对接方式,对接过程中配体小分子的可旋转键由系统自动分配,但受体酶为刚性结构。在对接前,设置4.0 nm×4.0 nm×4.0 nm 大小的搜索网格,其格点步长为0.037 5 nm,盒子中心为Ser105的OG 原子坐标(坐标:-7.320,22.766,16.938),其他参数默认。通过拉马克(Lamakian) 遗传算法获得100个最优的对接构象。根据文献[11]报道,笔者设定一个筛选条件作为构型筛选标准:①丝氨酸的OG原子与羰基的CT原子之间的键长小于0.2 nm;②配体分子必须与“氧负离子洞”形成2个的氢键;③配体分子与His224的咪唑环NE2原子形成1个氢键。
1.2分子动力学模拟
采用Gromacs 4.5.4软件进行分子动力学模拟,具体操作如下:采用Prodrg进行处理对接底物力场参数[12-13]。所有模拟过程均在pH7.0、温度300 K 下,GROMOS96 53a6力场、SPC216水模型、PME(particle mesh Ewald) 算法处理静电作用、远程静电截断值为1.2 nm、远程范德华力的截断值为1.2 nm,进行15 ns动力学模拟。体系采用立方体盒子,每个模拟周围填充1.0 nm 的水分子,模拟体系首先采用1 000 步的能量最小化;之后进行压力与温度平衡模拟500 ps;最后进行分子动力学模拟,放松蛋白,进行非限制性模拟。等压模拟体系下,温度模拟采用V-rescale 算法,耦合常数为0.1 ps。动力学模拟的数据借助OriginPro 8.0处理分析。
2结果与讨论
2.1对接结果分析
与其他脂肪酶一样,脂肪酶CALB活性口袋由底物酰基部分结合的疏水性口袋和醇基部分结合的亲水性口袋两部分组成,CALB对S型底物选择性与底物的醇基部分能否分布在亲水性口袋有关,如图1所示。
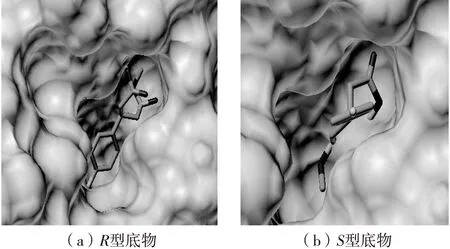
图1 底物(酰基受体甲醇)在活性腔中的分布 Fig.1 Distribution of substate(acyl acceptor methanol) in the active site
利用分子对接,分别将5种不同的手性醇过渡态底物对接到酶的活性口袋,考察其对接结合能数据,结果见表1。由表1可知:CALB对不同底物的S构型优于R型构象,这一现象与之前课题组实验数据报道相一致(表1)。

表1 3-FGA与不同酰基受体的去对称作用及结合能
由表1可知:CALB对3-FGA的S型构象底物具有优先选择性。随着碳链的增长,转化率和对映体消旋(e.e.)值逐渐降低,这可能是由于构成活性口袋的残基对长链底物更易形成空间位阻,使酶不能很好地分布在活性口袋,导致转化率和e.e.值降低。从结合能发现,酰基受体丁醇底物小于丙醇底物,由于空间位阻,使酰基受体1-丁醇的CT原子更靠近Ser105上的OG原子,导致氢键OG—CT=0.16 nm小于酰基丙醇底物形成的氢键OG—CT=0.21 nm,进而结合能低于酰基丙醇底物。同样,林明等[10]在研究洋葱假单胞菌脂肪酶去对称水解N-(2-甲基-6-乙基苯基) 丙氨酸(NEMPA)制备R-NEMPA时认为醇解部分相对较窄,对底物的选择性强,而酰基部分则相对较弱。为了从动态上进一步研究CALB对底物选择性差异,笔者采用分子动力学就底物与口袋动态结合情况进行研究。
2.2动力学分析
根据文献报道,一些研究者认为底物与酶形成复合物的扭转角对酶选择性具有很大影响(图2)。如Jung等[14]研究CALB催化手性3-苯基戊二酸二元酯过渡态底物时发现R型底物与酶形成扭转角为0°(O—H—O 或N—H—O),小于S型底物与酶形成的扭转角60°。因而,笔者又将对接最优构象复合物进行了15 ns的分子动力学模拟。其中,选取了甲醇与乙醇为代表来研究扭转角与选择性的关系。

图2 酶与配体扭转角图 Fig.2 Torsional angle for enzyme and substrate
首先对酰基受体甲醇和乙醇复合物进行Cα均方根偏差(RMSD)15 ns分子动力学模拟发现,整个体系波动较小,且都在5 ns后达到平衡状态,见图3和4。由图3和4可知:甲醇的RMSD约为0.2 nm,乙醇体系的RMSD约为0.18 nm。通过RMSD分析说明,平衡后的复合物的结构构象已趋向稳定、合理。而在扭转角分析中,对于酰基受体甲醇,体系约在5 ns平衡。模拟结果发现,S型构象底物与酶的扭转角度约为90°,而R型底物则为110°。而酰基受体乙醇体系在5 ns平衡后的S型底物扭转角度约为60°,R型底物扭转角为150°(图5),基于两者发现S型底物的扭转角度明显小于R型底物。

图3 酰基受体甲醇RMSD Fig.3 RMSD of acyl acceptor methanol

图4 酰基受体乙醇RMSD Fig.4 RMSD of acyl acceptor ethanol
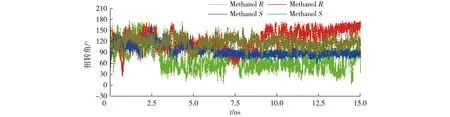
图5 分子动力学模拟酰基受体扭转角 Fig.5 The simulation of torsional angle of acyl acceptor with molecular dynamics
3结论
基于分子模拟技术对CALB催化3-FGA的去对称醇解反应研究,通过结合能差异分析了酶与不同链长的醇去对称醇解的对映选择性差异,发现S型底物结合能小于R型底物。同时通过分子动力学模拟分析了扭转角与不同醇对映选择性的分子机制,证实S型底物与酶形成的复合物扭转角小于R型底物。但是目前的模拟研究并不能证实哪几个氨基酸在选择性中起关键性作用,有必要在今后的研究中引入量子力学及MM-GBSA,对氨基酸的能量效应进行分析,确定对映选择性的关键氨基酸,理性指导优化酶的性能。
参考文献:
[1] Liu L T,Hong P C,Huang H L,et al.Asymmetric syntheses oftrans-3,4-disubstituted 2-piperidinones and piperidines.Tetrahedron:Asymmetry,2001,12(3):419-426.
[2]Risi C D,Fanton G,Pollini G P,et al.Recent advances in the stereoselective synthesis of trans-3,4-disubstituted-piperidines:applications to (-)-paroxetine.Tetrahedron:Asymmetry,2008,19(2):131-155.
[3]Huang X J,Broadbent S,Dvorak C,et al.Pilot-plant preparation of 3,4-dihydropyridin-2-one derivatives,the core structures of P2X7 receptor antagonists.Org Process Res Dev,2010,14(3):612-616.
[4]Yu M S,Lantos I,Peng Z Q,et al.Asymmetric synthesis of (-)-paroxetine using PLE hydrolysis.Tetrahedron Lett,2000,41(30):5647-5651.
[5]Huang X J,Zhu J,Broadbent S.The first asymmetric synthesis of a 4-arylsubstituted 5-carboxy-3,4-dihydropyridin-2-one derivative.Tetrahedron Lett,2010,51(12):1554-1557.
[6]Fryszkowska A,Komar M,Koszelewski D,et al.Studies on enzymatic synthesis of chiral non-racemic 3-arylglutaric acid monoesters.Tetrahedron:Asymmetry,2006,17(6):961-966.
[7]Liu Weiming,Hu Yi,Zhang Yang,et al.Enzymatic desymmetrization of 3-(4-fluorophenyl)glutaric anhydride through enantioselective alcoholysis in organic solvents.Biotechnol Bioeng,2014,19(3):449-455.
[8]Kofke D A,Mihalick B C.Web-based technologies for teaching and using molecular simulation.Fluid Phase Equilib,2002,194-197:327-335.
[9]Bartsch S,Kourist R,Bornscheuer U T.Complete inversion of enantioselectivity towards acetylated tertiary alcohols by a double mutant of aBacillussubtilisesterase.Angew Chem Int Ed,2008,47(8) :1508-1511.
[10]林明,江凌,胡燚,等.基于分子对接的洋葱假单胞菌脂肪酶催化制备R-N-(2-甲基-6-乙基苯基)丙氨酸的分子机制.生物加工过程,2013,11(4):49-54.
[11]张洋,江凌,张红漫,等.基于分子模拟技术研究枯草芽孢杆菌Lip-A对映体选择性反转.生物物理学报,2013,29(11):863-874.
[12]van Aalten D M,Bywate r R,Findlay J B,et al.PRODRG,a program for generating molecular topologies and unique molecular descriptors from coordinates of small molecules.J Comput Aided Mol Des,1996,10(3):255-262.
[13]Schüttelkopf A W,van Aalten D M.PRODRG:a tool for high-throughput crystallography of protein-ligand complexes.Acta Cryst D Biol Crystallogr,2004,60(8):1355-1363.
[14]Jung J H,Yoon D H,Kang P,et al.CAL-B catalyzed desymmetrization of 3-alkylglutarate:"olefin effect" and asymmetric synthesis of pregabalin.Org Biomol Chem,2013,11(22):3635-3641.
(责任编辑荀志金)
