HPLC-DLS法表征麻杏石甘汤中甘草酸成分
2015-12-29楚秋平高观祯柯李晶周建武饶平凡
沈 勇,楚秋平,高观祯,柯李晶,2,周建武,2,饶平凡,2
(1.福州大学生物工程研究所,福建福州 350002;2.中国科学院上海生命科学研究院-浙江工商大学食品营养科学联合研究中心,浙江杭州 310035)
0 引言
麻杏石甘汤源自汉代张仲景的《伤寒论》,是中国传统经典中药方剂之一,由麻黄、苦杏仁、石膏、甘草四味药组成,具有辛凉宣泄、清肺平喘的功效.甘草益气和中,与石膏合而生津,并能调和于寒温宣降之间,于麻杏石甘汤中为佐使之用.甘草酸作为甘草的主要活性成分之一,多以钾盐、钙盐的形式存在,其盐较易溶于水,具有抗炎、抗变态反应、抗病毒,清热解毒,抗氧化[1-2]调节机体免疫力,保肝[3]等广泛的生物活性[4].以往对甘草药材或汤剂中甘草酸检测都有研究报道,但麻杏石甘汤煎煮过程中甘草酸的质量浓度变化及其在汤剂中的具体存在形式尚未见有系统研究.
动态光散射技术(dynamic light scattering,DLS)是指通过测量散射光强的起伏变化来得出样品颗粒大小信息的一种技术,可用于分析溶液中颗粒粒径大小、分布和聚集状态等多种信息.通过高效液相色谱和动态光散射技术的联用对麻杏石甘汤煎煮过程中的甘草酸成分进行检测,其结果不仅反映了中药汤剂煎煮过程甘草酸质量浓度的变化规律,还体现了煎煮过程中甘草酸分子聚集成为胶体颗粒的过程.
1 材料
1.1 材料与试剂
生麻黄、杏仁、炙甘草、石膏(购于北京市双桥燕京中药饮片厂)经福建中医药大学张小如教授鉴定;甘草酸单铵对照品(购于福建省福州市药品检验所,批号110731-200615);甲醇(色谱纯);醋酸铵、冰醋酸(分析纯);纯净水.
1.2 仪器
Amicon Ultra 30 ku超滤离心管(美国 Millipore公司);L-2130高效液相色谱仪(日本 HITACHI公司);Daisogel-C18反相色谱柱(北京创新通恒科技有限公司);Nano ZS90 Zetasizer激光粒度分析仪(英国Malvern公司);CF15RX高速离心机(日本HITACHI公司).
2 方法
2.1 麻杏石甘汤样品制备
称取药材麻黄9 g,苦杏仁9 g,甘草6 g和石膏24 g,加200 mL水单煎麻黄20 min,然后加入预先浸泡于500 mL水中30 min的余药共煎60 min,经纱布过滤后,加一级水至400 mL得麻杏石甘汤样品.
2.2 高效液相色谱分析条件
参考中国药典[5]和其他常用甘草酸检测方法[6],色谱分析柱为 Daisogel- C18(250 mm×4.6 mm,5μm),流动相甲醇 -0.2 mol·L-1醋酸铵溶液 -冰醋酸体积比为67 ∶33 ∶1,流速 1.0 mL·min-1,检测波长250 nm,柱温25℃,进样量20μL.
2.3 标准曲线的制备
将甘草酸单铵置于105℃ 干燥箱中烘干3 h后,精密称量甘草酸单铵对照品7.5 mg,甲醇溶解定容至10 mL,摇匀得0.75 mg·mL-1对照品溶液.将其稀释成500、250、125、62.5、31.25、15.6、7.8 μg·mL-1对照液.0.45μm微孔滤膜过滤,依次进样20μL,得到甘草酸浓度(mg·mL-1)与峰面积 (A)的标准曲线.
2.4 精密度试验和重复性实验
取同一对照品溶液重复进样6次,每次20μL,进行色谱分析,考察此方法的精密度.取制备的麻杏石甘汤样品液重复测定6次,考察其重复性.
2.5 煎煮过程甘草酸质量浓度的变化
煎煮过程汤剂的制备方法同2.1,加入三味药材(苦杏仁,甘草,石膏)开始计时(该时刻取样标注为0 min),每隔10 min取样.样品处理:经5 000 r·min-1离心30 min,0.45μm 膜过滤,进样20μL,HPLC测定其甘草酸质量浓度变化.
2.6 汤剂中甘草酸的聚集状态
取2.5中样品,样品①:经5 000 r·min-1离心30 min,为超滤前样品,待用;样品②:经5 000 r·min-1离心30 min,过30 ku超滤膜超滤,为超滤后样品,待用.两组样品经0.45μm膜过滤,HPLC测定其甘草酸质量浓度,应用动态光散射(DLS)原理,联用Nano ZS90 Zetasizer粒度仪,分别测定其平均粒径变化.
3 结果分析
3.1 甘草酸标准曲线
甘草酸标准曲线回归方程 Y=35 869 224.65X+3 616.03(R2=0.999 3),表明甘草酸进样量在0.156~15μg与峰面积(A)的线性范围良好.
3.2 麻杏石甘汤中甘草酸质量浓度
甘草酸标准品色谱保留时间为7.95 min,据标准曲线方程可知,麻杏石甘汤样品中甘草酸质量浓度为86.0 μg·mL-1,即每克炙甘草含 5.73 mg 甘草酸.
3.3 精密度实验和重复性实验
甘草酸的峰面积RSD为2.25%(n=6),表明实验结果精密度良好;麻杏石甘汤中RSD为2.14%(n=6),表明实验结果重复性良好.

表1 甘草酸精密度实验结果和麻杏石甘汤原汤重复实验结果Tab.1 Precision of glycyrrhizic acid and repeated of Ma-Xing-Shi-Gan decoction
3.4 煎煮过程中甘草酸质量浓度的变化
测定不同煎煮时间,麻杏石甘汤中甘草酸质量浓度变化,结果如图1所示,0~20 min甘草酸质量浓度从0上升到80.1μg·mL-1;20~60 min甘草酸质量浓度基本不变,约82.4μg·mL-1.0~20 min 为麻杏石甘汤中甘草酸的溶出期,其浓度与煎煮时间成正相关.20 min后,麻杏石甘汤中甘草酸浓度基本达到饱和.
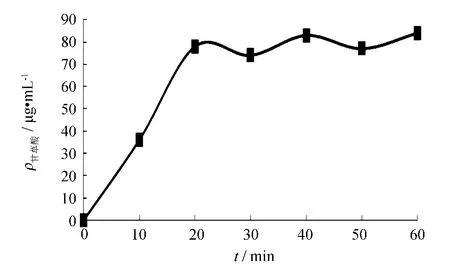
图1 麻杏石甘汤煎煮过程中甘草酸质量浓度变化Fig.1 The glycyrrhizic acid contents during the water boiling processing of Ma-Xing-Shi-Gan decoction
3.5 煎煮过程及超滤前后麻汤中甘草酸的聚集状态
图2所示,麻汤经超滤处理,甘草酸基本被30 ku超滤膜截留,在超滤液中质量浓度不超过4.01μg·mL-1.甘草酸单体(相对分子质量为822.9 u)相对分子质量远小于30 ku,理论上可完全透过30 ku超滤膜,徐浩坤等[7]研究表明甘草酸可透过30 ku超滤膜,透过率达90%以上.汤剂中甘草酸透过率仅为5.2%,推测甘草酸在水溶剂和麻杏石甘汤中的存在形式不同.
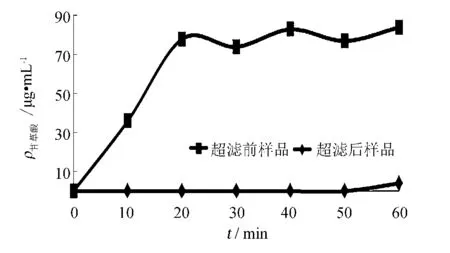
图2 煎煮过程中,超滤前后麻汤中甘草酸质量浓度的变化Fig.2 The glycyrrhizic acid contents during the water boiling processing of Ma-Xing-Shi-Gan decoction pre-/aft- ultrafiltration
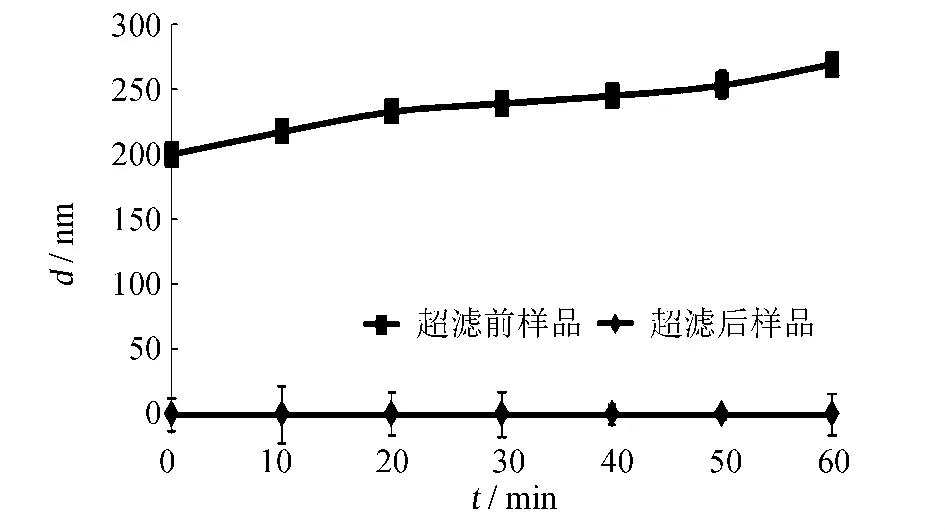
图3 煎煮过程中,超滤前后汤剂中颗粒平均粒径的变化Fig.3 Average particle size variation of the Ma-Xing-Shi-Gan decoction pre-/aft- ultrafiltration
如图3所示,麻黄单煎20 min和其他三味药(苦杏仁、甘草和石膏)混合形成粒径约为200.0 nm的纳米颗粒,随着煎煮时间延长,粒径逐渐增加到270.1 nm;超滤后样品由于截留作用,检测不到明显的颗粒.
研究表明,甘草酸具有和生物大分子发生超分子作用形成颗粒的能力[8],陈求浩等[9]研究表明麻黄碱和甘草酸能分别与生石膏中的 Ca2+、Fe2+、Zn2+和 Mn2+形成ML和 ML2型不同稳定程度的络合物.图3中汤剂里颗粒平均粒径逐渐增大,可能是由于溶出的甘草酸等与其他药效成分相互作用形成更大的纳米颗粒.
对比麻杏石甘汤超滤前后样品中甘草酸质量浓度变化(图2)和超滤前后颗粒平均粒径变化(图3),表明麻杏石甘汤煎煮过程中,甘草酸从药材释放到汤剂中,不是以单体形式存在的,而是通过超分子作用自聚或与其它化学成分形成相对分子质量大于30 ku的纳米颗粒,其粒径约为250.0 nm.
4 结论
通过HPLC检测煎煮过程中麻杏石甘汤中甘草酸质量浓度的变化,发现麻杏石甘汤中甘草酸的煎出率与煎煮时间相关,质量浓度为82.4μg·mL-1;对比超滤前后甘草酸质量浓度变化,推测甘草酸以自聚或复合胶束形式存在于汤剂中.联用Nano ZS90 Zetasizer粒度仪,从颗粒角度进一步探讨麻杏石甘汤中甘草酸以聚集状态存在,研究表明,甘草酸在汤剂中会自聚或与其他大分子物质结合形成平均粒径为250.0 nm的复合胶束.而它在汤剂中自聚方式、或与其他大分子物质的具体结合方式和数量比目前还有待进一步探究.
药物单体组分在体内与其它成分之间能发生非化学本质的相互作用,并可能进而改变药效.以麻黄的主要药效成分麻黄碱为例,它在有咖啡因存在的情况下其药物代谢和对激素分泌的刺激能力等指标均发生显著变化[10].胶体是药物成分之间通过各种次级键介导的超分子作用而形成的,在多种中药单复方煎剂中都广泛存在,并与煎剂的药效作用有直接联系[11].对麻杏石甘汤中甘草酸质量浓度及存在形式的研究表明,对于解释方药药效和多种成分之间的复杂联系,不仅要关注其质量浓度,其存在形式更为我们提供了新的阐述视角.
