低温下TiO2光催化降解三甲胺气体*
2015-12-25杨晓飞梅林王志耕薛秀恒
杨晓飞,梅林,王志耕,薛秀恒
(安徽农业大学茶与食品科技学院,安徽省农产品加工工程实验室,安徽合肥,230036)
三甲胺广泛分布于水产品、肉制品等食品中[1-3],并随着食品新鲜程度的下降,三甲胺的量会越来越多[4-5]。三甲胺具有腐败气味,人对三甲胺的嗅觉阈浓度为2 mg/m3[6]。当冰箱、冷藏室或冷藏车等密闭空间中长时间贮藏或运输水产品时,它们会散发出三甲胺气体,使密闭空间内产生异味,甚至污染其他食品。因此,三甲胺气体去除技术的研究,对提高密闭空间贮藏或运输水产品、肉制品的功能特性具有应用意义。
近年发展的光催化氧化技术因氧化能力极强,可以将有机物彻底氧化为无毒无害的小分子无机物而被广泛地应用于降解有机物。其中TiO2因其催化活性高、稳定性好而成为最受欢迎的催化剂之一。目前已经有不少研究利用TiO2光催化降解果蔬、土壤以及水体中的残留农药、有机物染料以及净化空气等[7-14],并都取得了良好的降解效果。但是关于TiO2光催化降解三甲胺气体的的研究鲜见报道。本文在冰箱冷藏室条件下,以紫外灯为光源,研究了TiO2光催化降解三甲胺气体的效果,并探讨了三甲胺初始浓度和紫外光强度对三甲胺光催化降解率和降解速率常数的影响,以期为低温下TiO2光催化降解三甲胺气体的应用提供技术支持,进而改善密闭空间贮藏或运输水产品、肉制品等食品的功能特性。
1 材料和方法
1.1 材料和仪器
TiO2和33%三甲胺水溶液,国药集团化学试剂有限公司;浓盐酸HCl(分析纯),西陇化工有限公司;NaOH(分析纯),无锡市亚盛化工有限公司。
Agilent7890B气相色谱仪,美国安捷伦科技有限公司;CP224C电子天平,奥豪斯仪有限公司;去离子水纯水机,克尔顿有限公司;BD/BC347KMN美的电冰箱,美的电冰箱有限公司;SHZ-D型循环水式真空泵,上海羌强实业发展有限公司;365 nm紫外灯,雪莱特光电科技股份有限公司。
1.2 实验方法
1.2.1 TiO2涂板的制备
称取10.0 g TiO2,用水分散后均匀涂布在面积为25 cm×40 cm的冰箱隔板上,然后置于40℃烘箱中烘干,制得TiO2涂层密度为10.0 mg/cm2的TiO2涂板。
1.2.2 实验装置
取容积为30 L的储藏箱,将紫外灯和TiO2涂板粘附于储藏箱内壁,将储藏箱密封后置于4℃冰箱中,模拟冰箱环境,然后在密封的储藏箱中进行三甲胺气体的降解。
1.2.3 三甲胺降解方法
向密封的储藏箱中送入三甲胺气体,再次密封,然后将储藏箱放入4℃冰箱,对储藏箱中的三甲胺进行降解处理一段时间,再采集和检测储藏箱中残留的三甲胺气体,计算三甲胺的残留浓度及降解率。
三甲胺的残留浓度[公式(1)]及降解率的计算[公式(2)]:

式中:C,储藏箱中三甲胺的残留浓度,mg/m3;c,三甲胺盐酸溶液的浓度,mg/L;V1,三甲胺盐酸溶液的体积,mL;V2,储藏箱体积,30 L;,采样回收率,%;C0,三甲胺初始浓度,mg/m3;y,三甲胺降解率,%。
1.2.4 标准三甲胺盐酸溶液的配制
取0.1 mL 33%的三甲胺水溶液溶于32.9 mL 1 mol/L的HCl溶液,混匀,制得1 g/L的三甲胺盐酸溶液。进一步稀释得到浓度为1,5,10,20和30 mg/L的标准三甲胺盐酸溶液。以三甲胺峰面积(pA)对标准三甲胺盐酸溶液的浓度(mg/L)作图,绘制标准曲线。
1.2.5 三甲胺气体的采集方法
根据中华人民共和国国家标准GB/T 4676—1993[15]并略作改进,用真空泵将密封储藏箱中的气体以0.3 L/min的速度经过装有10 mL 1 mol/L的HCl溶液的注射器全部抽出,使气体中的三甲胺溶于HCl溶液形成三甲胺盐酸溶液,然后进行检测分析。
1.2.6 三甲胺采样回收率试验
向密封储藏箱中送入GB 21551.4—2010[16]建议的最小初始浓度1 mg/m3和最大初始浓度12 mg/m3的三甲胺气体,然后进行采集和检测分析,确定平均采样回收率。
1.2.7 三甲胺气体的检测方法
根据中华人民共和国国家标准GB/T 4676—1993[15]并略作改进,取2 mL三甲胺盐酸溶液于10 mL的顶空瓶中,加入3 mL饱和的NaOH溶液,迅速密封,混匀,50℃水浴10 min使采集的三甲胺游离成气态并挥发,然后用微量进样器采集顶空瓶中液面上的气体进行气相色谱检测分析。以三甲胺的保留时间和色谱峰面积进行定性和定量分析。
色谱条件:色谱柱:DB-FFAP毛细管柱(15 m×250 mm ×0.25 μm);进样口温度:130 ℃;柱温:初始温度80℃,保持8 min,升温速率10℃/min,最终温度130℃,保持2 min;FID检测器温度160℃;进样量 100 μL,不分流进样;载气:氮气,40.0 mL/min;氢气流速40.0 mL/min;空气流速400.0 mL/min。
1.2.8 不同方法降解三甲胺效果的比较研究
向3组(每组7个)密封储藏箱中均送入初始浓度为12 mg/m3[16]的三甲胺气体,在4℃冰箱中按表1的处理方法对3组储藏箱中的三甲胺进行降解处理,然后分别于 0,10,20,30,40,50,60 min 后从各组中抽出1个储藏箱采集和检测其中残留的三甲胺气体,计算储藏箱中三甲胺的残留浓度和降解率,考察不同方法降解三甲胺的效果。
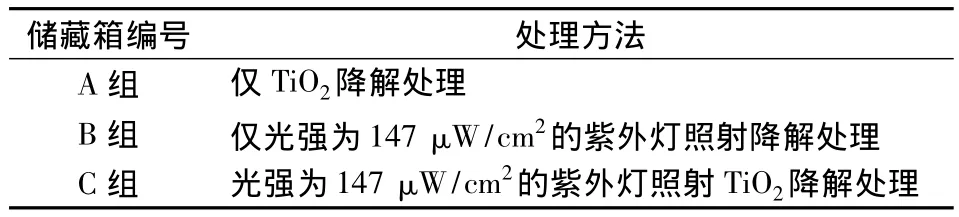
表1 不同的处理方法Table 1 The different treatments
1.2.9 三甲胺初始浓度对三甲胺光降解的影响
向4组(每组7个)密封储藏箱中分别送入初始浓度为3、6、9、12 mg/m3的三甲胺气体,在 4 ℃ 冰箱中对储藏箱中的三甲胺进行紫外灯(147 μW/cm2)激发 TiO2催化降解处理,然后分别于 0,10,20,30,40,50,60 min后从各组中抽出1个储藏箱采集和检测其中残留的三甲胺气体,分析初始浓度对三甲胺降解率的影响。
1.2.10 紫外光强度对三甲胺光降解的影响
向5组(每组7个)密封储藏箱中均送入初始浓度为12 mg/m3的三甲胺气体,在4℃冰箱中对5组储藏箱中的三甲胺进行光强为28,44,94,147和170 μW/cm2紫外灯激发TiO2催化降解处理,然后分别于0,10,20,30,40,50,60 min 从各组中抽出1 个储藏箱采集和检测其中残留的三甲胺气体,分析紫外光强度对三甲胺降解率的影响。
1.2.11 三甲胺光催化降解动力学研究
以TiO2为催化剂的光催化反应普遍符合Langmuir-Hinshelwood动力学方程,该方程表示为
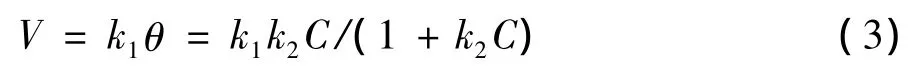
式(3)中V为反应速率,C为底物浓度,k1和k2分别为表观反应速率常数和吸附常数[17]。
在光催化降解过程中,当反应物浓度很低时,k2C≪1,则V≈k1k2C,积分后可得:
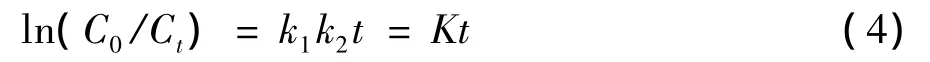
式(4)中C0和Ct分别为底物的初始浓度和降解t时间后的残留浓度,此反应表现为一级反应,ln(C0/Ct)与t呈直线关系,其中K=k1k2,为一级速率常数[18-19]。
本研究中三甲胺气体的浓度均不超过12 mg/m3,浓度较低,故对研究中得到的数据进行ln(C0/Ct)-t线性拟合,分析其降解的动力学过程。
1.2.12 数据统计分析
本研究所有试验均设3次重复,三甲胺的残留浓度和降解率取3次平行试验的平均值,将得到的实验结果利用Microsoft Excel进行处理分析。
2 结果和分析
2.1 标准曲线的绘制
以三甲胺色谱峰面积对三甲胺盐酸溶液的浓度作图绘制标准曲线,如图1所示。图1表明,当三甲胺盐酸溶液的浓度在1~30 mg/L时,三甲胺色谱峰面积和三甲胺盐酸溶液浓度之间呈良好线性关系,线性方程为y=21.372x-13.470,相关系数R2=0.994 7。
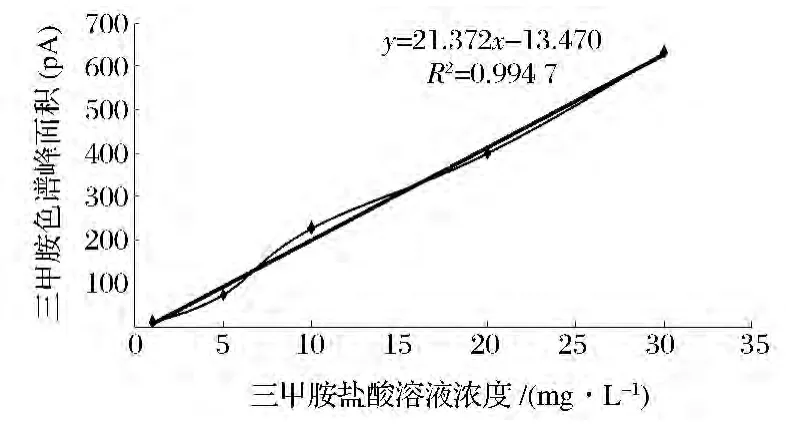
图1 标准曲线Fig.1 Calibration curve of standard solutions
2.2 采样回收率
三甲胺采样回收率试验结果如表2所示。由表2可知,当三甲胺初始浓度为1 mg/m3和12 mg/m3时,其平均回收率分别为83.48%和80.73%,RSD分别为6.99%和5.20%,采样回收率较高,且采样重复性较好。在本研究中,储藏箱中三甲胺气体的浓度在1~12 mg/m3之间,故在计算三甲胺残留浓度和降解率时统一使用三甲胺初始浓度为1 mg/m3和12 mg/m3时平均回收率的平均值=(83.48%+80.73%)/2=82.11%作为采样回收率。
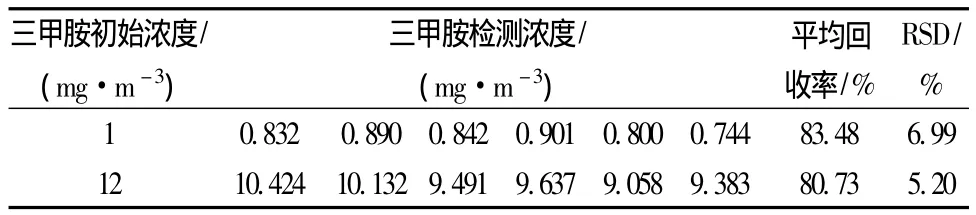
表2 三甲胺采样回收率Table 2 Recovery of sampling trimethylamines
2.3 不同方法降解三甲胺的效果
不同处理方法对三甲胺降解率的影响如图2所示。由图2可知,仅使用TiO2或仅使用紫外光处理时三甲胺的降解率均较低,降解效果较差,而TiO2光催化降解处理时降解率明显提高。当三甲胺初始浓度为 12 mg/m3、光强为 147 μW/cm2时,TiO2光催化降解处理60 min可使三甲胺的降解率达到75.86%,是单独使用紫外光处理60 min时三甲胺的降解率的3.29倍,表明TiO2光催化降解三甲胺气体具有较好的效果。光降解机理认为,TiO2受到λ<387.5 nm的光照射后,吸收与价带和导带带隙能相当的光能,使价带上的电子与空穴分离并迁移到导带上,从而产生具有很强活性的光生空穴(h+)和电子(e-),电子和空穴产生后向TiO2粒子表面迁移,捕获并氧化和还原吸附在TiO2表面的有机物,从而使有机物发生降解,并且降解产物从催化剂表面脱附下来后,空出来的活性位点可以持续吸附和降解有机物,从而促进有机物的降解[20-21]。三甲胺作为一种小分子有机物,同样可以吸附在TiO2表面并被具有强氧化性的空穴捕获,进而被氧化。另外,随着光照时间的延长,TiO2表面产生越来越多的电子-空穴对,因此随着光催化降解的时间增加,三甲胺的降解率也逐渐提高。
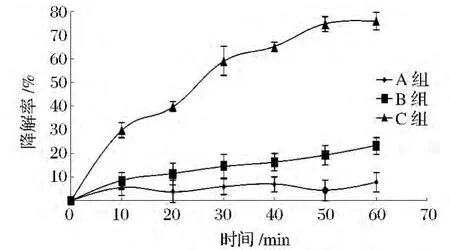
图2 不同处理方法对三甲胺降解率的影响Fig.2 Effect of different treatments on the degradation rate of trimethylamine
2.4 三甲胺初始浓度对三甲胺光降解效果的影响
三甲胺初始浓度对三甲胺光降解效果的影响参见图3。图3结果表明,在相同的降解条件下,三甲胺的降解率随初始浓度的增大而降低。在降解处理10 min时,三甲胺初始浓度为6,9和12 mg/m3时其降解率仅为初始浓度为3 mg/m3时的91.63%、67.96%和58.54%。由光降解机理可知,TiO2表面产生的光生电子和空穴可在小于10-9s的时间内完成复合,因此底物只有预先吸附在TiO2表面才能与具有高度活性的电子和空穴发生氧化或还原反应,进而被降解。但是对于固定的TiO2而言,其表面积是一定的,TiO2表面的光催化活性位点的数目也是一定的,当三甲胺浓度增加时增加的三甲胺不能立即被吸附到TiO2表面而无法及时参与氧化降解反应,所以在相同光降解条件下随着三甲胺初始浓度的增加,降解率逐渐下降[7,22]。
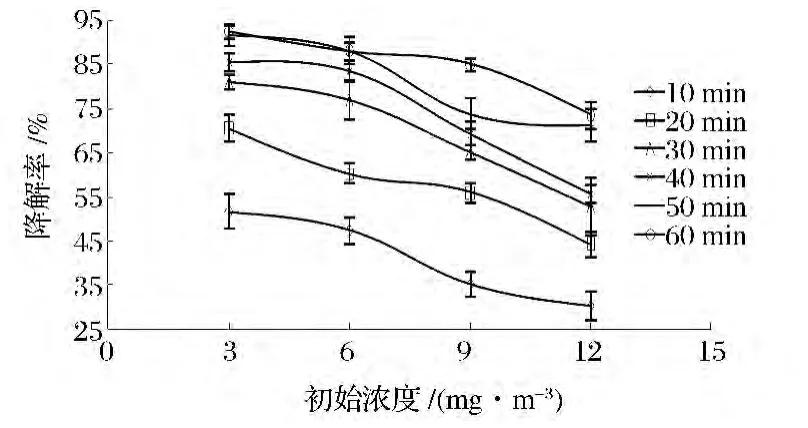
图3 三甲胺的降解率随初始浓度的变化曲线Fig.3 Curve of rate of degradation of trimethylamine with different initial concentration
对不同初始浓度下三甲胺的光催化降解数据进行ln(C0/Ct)-t线性拟合,其拟合曲线及相关参数如图4和表3所示。由图4和表3可以看出,在不同的初始浓度下,ln(C0/Ct)-t之间均呈良好的的线性关系,其拟合方程的R2均大于0.95,表明不同三甲胺初始浓度下TiO2光催化降解三甲胺的过程均基本符合一级反应动力学模型。
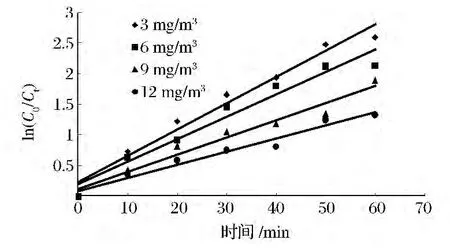
图4 不同初始浓度下三甲胺光催化降解一级反应动力学拟合曲线Fig.4 First-order reaction kinetics fitting curve of trimethylamine at different initial concentration

表3 不同初始浓度下三甲胺光降解一级动力学拟合方程及其相关参数Table 3 First-order reaction kinetics fitting equation of trimethylamine and the relative parameters of trimethylamine at different initial concentration
由表3还可以看出,光降解反应的一级反应速率常数K受三甲胺初始浓度的影响较大,随初始浓度的增大,K逐渐减小。将不同初始浓度下的一级反应速率常数K对三甲胺初始浓度C0作线性拟合,结果如图5所示,当三甲胺初始浓度在3~12 mg/m3时,可以得到如下关系:K=-0.002 4C0+0.050 2(R2=0.997 0),式中,K为一级反应速率常数(min-1),C0为三甲胺初始浓度(mg/m3)。
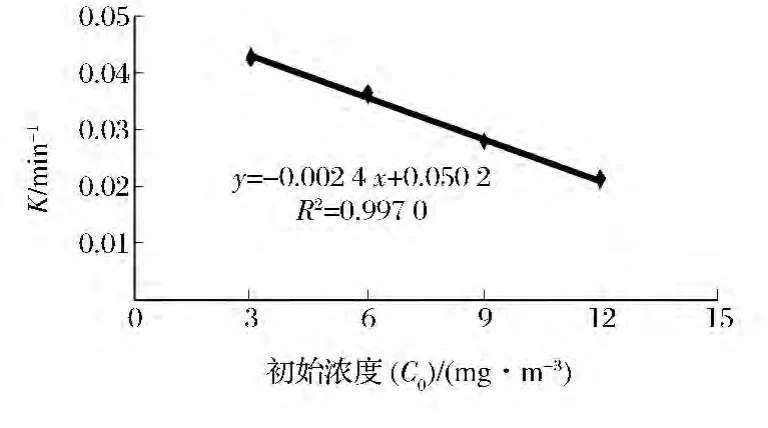
图5 K与C0的拟合曲线Fig.5 The fitting curve of K and C0
2.5 紫外光强度对三甲胺光催化降解的影响
紫外光强度对三甲胺的降解率的影响如图6所示。图6结果表明,在三甲胺初始浓度为12 mg/m3的条件下,三甲胺的降解率随光强的增大而增大。在降解处理10 min时,当紫外光强度从28 μW/cm2增大到 44,74,147,170 μW/cm2时,其降解率从12.25%逐渐增大到 21.17%,27.89%,30.27%,31.05%。这可能是因为光强时光催化的外在动力,当光强增加时,照射到TiO2表面的光量子数也增加,从而更多的TiO2价带上的电子受到激发而和空穴分离,产生更多的高能电子-空穴对,使TiO2表面的吸附的三甲胺被空穴捕获的几率增加,从而促进三甲胺的降解,提高其降解速度和降解率[23-24]。
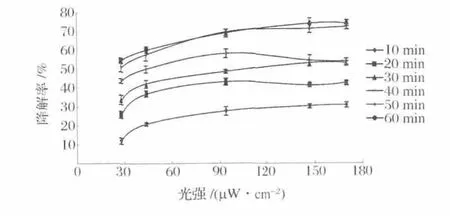
图6 三甲胺的降解率随光强的变化曲线Fig.6 Curve of degradation rate of trimethylamine with different UV light intensity
对不同光强下三甲胺的光降解数据进行ln(C0/Ct)-t线性拟合,其拟合曲线及相关参数如图7和表4所示。由图7和表4可知,当三甲胺初始浓度为12 mg/m3时在不同光强下,ln(C0/Ct)-t均呈良好的线性关系,其拟合方程的R2均大于0.96,表明不同紫外光强度下TiO2光催化降解三甲胺的过程基本上可由一级动力学方程描述。由表4还可以看出三甲胺光催化降解反应的反应速率常数K与光强I有关,随着光强I的增加,K值逐渐增大。将不同光强下的反应速率常数K对光强I进行线性拟合,可得到拟合曲线如图8所示。由图8可以看出,当紫外光强度在28~170 μW/cm2时,反应速率常数K(min-1)与辐照光强I(μW/cm2)具有良好的线性关系,其拟合方程为K=0.005 0ln(I)-0.003 3,相关系数R2=0.993 3。
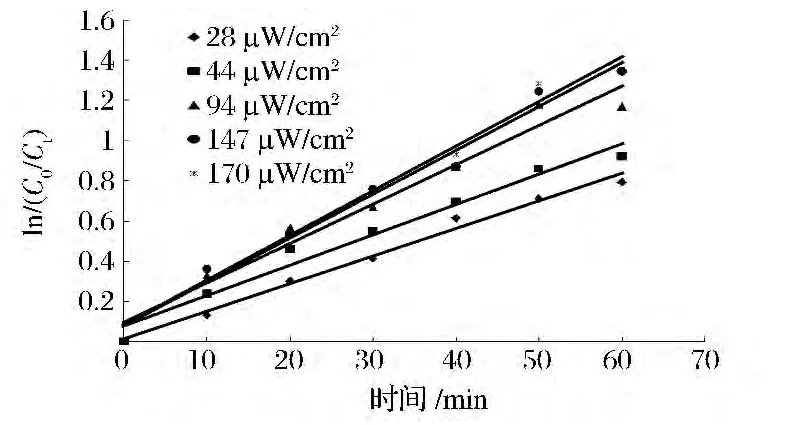
图7 不同光强下三甲胺光催化降解一级反应动力学拟合曲线Fig.7 First-order reaction kinetics fitting curve of trimethylamine at different UV light intensity

表4 不同光强下三甲胺光降解一级动力学拟合方程及其相关参数Table 4 First-order reaction kinetics fitting equation of trimethylamineand the relative parameters of trimethylamine at different UV light intensity
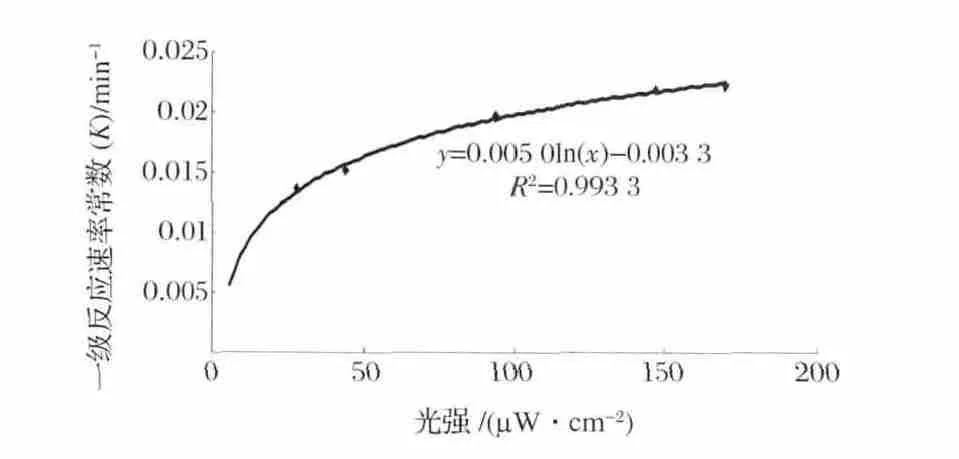
图8 K对光强I的拟合曲线Fig.8 The fitting curve of K and I
3 结论
(1)TiO2紫外光催化降解三甲胺效果显著,降解过程中ln(C0/Ct)-t呈良好的线性关系,三甲胺的光降解遵循一级反应动力学过程。
(2)在相同降解条件下,三甲胺的初始浓度从3 mg/m3升高至12 mg/m3时,其降解率和光催化降解速率常数均逐渐降低,三甲胺的初始浓度C0与其光催化降解速率常数K之间呈线性关系:K=-0.002 4C0+0.050 2(R2=0.997 0)。
(3)在三甲胺初始浓度和降解处理时间相同的条件下,当光强在28~170 μW/cm2时,随紫外光辐照强度I的增加,三甲胺的降解率和反应速率常数K均逐渐增大,K与I的线性关系为K=0.005 0ln(I)-0.003 3(R2=0.993 3)。在应用TiO2光催化净化冰箱内三甲胺气体时可适当增大紫外光强度,以提高其降解率及降解速率。
三甲胺气体去除技术研究,对净化密闭空间内空气,提高密闭空间贮藏或运输水产品、肉制品的功能特性具有应用意义,进而能够帮助促进水产品、肉制品工业的发展。
[1] 金良正,喻开瑞.肉品中三甲胺的提取及气相色谱测定[J].中国公共卫生,2000,16(6):548-549.
[2] Silvia A,Thierry Z,Victoria G,et al.Determination of trimethylamine in milk using an MS based electronic nose[J].Eur Food Res Technol,2002,214:163-167.
[3] 秦辉,夏文水.顶空气相色谱法测定河蟹中三甲胺的含量[J].食品工业科技,2008,29(5):280-282.
[4] 李丰.水产品中氧化三甲胺、三甲胺、二甲胺检测方法及鱿鱼丝中甲醛控制研究[D].保定:河北农业大学,2011:1-3.
[5] 胡彩虹,许梓荣.气相色谱法测定猪肉、鱼和虾中三甲胺的含量[J].食品科学,2001,22(5):62-64.
[6] 邓后勤,夏延斌,邓友光,等.三甲胺测定方法的研究进展[J].食品与发酵工业,2005,31(12):84-88.
[7] 刘威,张兵,廖宗文.TiO2-ZnO纳米复合材料光催化降解小白菜中4种残留有机磷农药[J].食品与发酵工业,2010,36(12):42-45.
[8] 孙媚华,陈迁,宋光泉,等.TiO2-ZnO纳米器件降解上海青中有机磷农药的研究[J].食品科技,2010,35(7):308-312.
[9] Sakkas A V,Albanis A T.Photocatalyzed degradation of the biocides chlorothalonil and dichlofluanid over aqueous TiO2suspensions[J].Applied Catalysis B:Environmental,2003(46):175-188.
[10] Satyen G,Sanjay P k,Sudhir B S,et al.Photocatalytic degradation of 3-nitrobermenesulfonic acid in aqueous TiO2suspensions[J].Journal of Chemical Technology and Biotechnology,2006,81(3):359-364.
[11] 汤心虎,谭淑英.TiO2光催化降解活性艳红X-3B的研究[J].工业水处理,2004,24(12):25-27.
[12] 曹长春,蒋展鹏,余刚,等.TiO2薄膜光电协同催化氧化降解活性艳红[J].环境科学,2002,23(6):108-110.
[13] 谭忆秋,李洛克,魏鹏,等.可降解汽车尾气材料在沥青路面中的应用性研究[J].中国公路学报,2010,23(6):21-27.
[14] 刘洋,杨海燕.TiO2光催化降解苯和甲苯的动力学研究[J].化学通报,2007(3):222-227.
[15] GB/T 14676—1993.中华人民共和国国家标准空气质量三甲胺的测定-气相色谱法[S].
[16] GB 21551.4—2010.中华人民共和国国家标家用和类似用途电器的抗菌、除菌、净化功能电冰箱的特殊要求[S].
[17] 夏启斌,李忠,奚红霞,等.气相苯在TiO2光催化剂上吸附常数和光催化反应常数测定[J].离子交换与吸附,2005,21(3):216-223.
[18] 张伟,李黎武,张茜,等.MWNTs/TiO2对典型氯苯类化合物的光催化降解研究[J].环境科学学报,2012,32(3):631-638.
[19] 阳海,曾健,黎源,等.氙灯/TiO2体系下敌草隆光催化降解动力学的研究[J].环境科学,2013,34(8):3137-3142.
[20] Fujishima A,Rao T N,Tryk D A.Titanium dioxide photocatalysis[J].Journal of Photochemistry and Photobiology C:Photochemistry Reviews,2000,1(1):1-21.
[21] 张金龙,徐华胜,安保正一.紫外光照射下丙炔光催化水解反应的研究[J].催化学报,2003,24(11):845-848.
[22] 李青松,高乃云,马晓雁,等.TiO2光催化降解水中内分泌干扰物17β-雌二醇[J].环境科学,2007,28(1):120-125.
[23] Lea J,Adesina A A.The photo-oxidative degradation of sodium dodecyl sulphate in aerated aqueous TiO2suspension[J].Journal of Photochemistry and Photobiology A:Chemistry,1998,118(2):111-122.
[24] 郑艳.苯系物气相光催化降解动力学及其机理研究[D].泰安:山东大学,2009:46-52.
