乌骨藤提取物对MKN-45大鼠人原位胃癌模型肿瘤生长、转移及环氧合酶-2表达的影响
2015-12-25陈轶,陈益耀,林诚
乌骨藤提取物对MKN-45大鼠人原位胃癌模型肿瘤生长、转移及环氧合酶-2表达的影响
陈轶陈益耀林诚
(海南省人民医院消化内科,海南海口570311)
摘要〔〕目的探讨乌骨藤提取物对MKN-45大鼠人原位胃癌模型肿瘤生长、转移及环氧合酶(COX)-2表达的影响。方法健康雄性裸大鼠,共24只,随机分为:乌骨藤组、西药组和对照组,收集体外培养生长处于对数期的MKN-45胃癌细胞,注射于裸大鼠近腋部皮下,当皮下移植瘤长至直径约1 cm左右时,取裸大鼠癌瘤组织,植入大鼠胃大弯的血管丰富处建立模型,于造模72 h后,对照组给予生理盐水灌胃,西药组和乌骨藤组分别给予塞来昔布和乌骨藤水提物灌胃,每次0.5 ml/10 g,1次/d。连续30 d。分别在给药第15天和第30天各处死半数裸鼠,检测癌瘤的生长,肝脏及肠系膜转移情况,Western印迹法检测胃黏膜组织COX-2蛋白表达。结果各组癌瘤重量和体积均随着时间的增加而不同程度的增长,与对照组相比,西药组和乌骨藤组的癌瘤重量和体积增长均显著减慢(P<0.05),与西药组相比,乌骨藤组对于癌瘤增长的控制作用更为显著(P<0.05),各药物组抑瘤率均显著高于对照组(P<0.05),与西药组相比,乌骨藤组的抑瘤率更高(P<0.05)。治疗15 d时,各组均未见肠系膜转移,仅对照组见肝脏转移。治疗30 d时,各组均见肝脏及肠系膜转移。各治疗组与对照组相比,肝脏及肠系膜转移数均显著减少,与西药组相比,乌骨藤组癌瘤的转移数减少的更为明显(P<0.05)。经药物治疗后,治疗后15 d,30 d各治疗组COX-2蛋白水平均显著降低,与对照组相比差异显著(P<0.05),与西药组相比,乌骨藤组的COX-2蛋白水平下降更为明显(P<0.05)。结论乌骨藤提取物抑制MKN-45大鼠人原位胃癌模型肿瘤生长、转移及COX-2表达具有明显的改善作用。
关键词〔〕乌骨藤提取物;胃癌;环氧合酶-2
中图分类号〔〕R285〔文献标识码〕A〔
第一作者:陈轶(1968-),女,副主任医师,主要从事消化道肿瘤基础与临床研究。
胃癌是消化道常见的恶性肿瘤之一,严重危害人类健康〔1,2〕。在原位癌的治疗中天然药物的地位日益重要。因此寻找中药抗肿瘤活性成分成为研究的重点。乌骨藤为番荔枝科植物白叶瓜馥木的根〔3〕。据《中药大辞典》记载:乌骨藤性辛,味温,入肝经,具有消炎,清热解毒,散结止痛等功效〔4〕。现代药理提示乌骨藤含有多种甾体酯苷、有机酸、多糖等化学成分,其中C21甾体苷和多糖成分具抗肿瘤活性〔5〕,对多种恶性肿瘤细胞有明显的抑制作用,曾用于治疗多种消化系统肿瘤,收获了较好的疗效。但对于乌骨藤提取物对于原位胃癌的治疗作用研究尚少。本文观察乌骨藤提取物对原位胃癌的生长、转移及环氧合酶(COX)-2表达的干预作用。
1资料与方法
1.1实验动物健康雄性裸大鼠,8~10周龄,体重200~230 g,共24只,由北京维通利华实验动物中心提供。裸大鼠及实验条件达到SPF。室温20℃~22℃,湿度50%~70%,自由进食、水。
1.2仪器及试剂人胃癌细胞株MKN-45(上海仁济医院);乌骨藤水提物;塞莱昔布胶囊(西乐葆,辉瑞制药有限公司);RPMI-1640 培养液(美国Gibco公司);25%胎牛血清(杭州四季青生物制品公司);水合氯醛;COX-2 抗体(Abcam公司)。
1.3实验方法
1.3.1模型的建立裸大鼠禁食12 h,经10% 水合氯醛麻醉,用75%酒精消毒裸大鼠腹部皮肤,收集体外培养生长处于对数期的MKN-45胃癌细胞,配制成单细胞悬液,1×107个/ml,用2 ml注射器抽取2 ml,于裸大鼠近腋部皮下进针,回抽无血,缓慢注射后迅速拔针,当皮下移植瘤长至直径约1 cm 左右时,取裸大鼠癌瘤组织,腹正中切口约1 cm,在胃大弯的血管丰富处,将备好的肿瘤组织块植入其中,进行缝合。见大鼠出现精神萎靡、嗜睡、反应迟钝、活动减少等现象,且胃部出现可触及的癌瘤,证明造模成功。
1.3.2分组及处理实验动物随机分为:乌骨藤组、西药组和对照组,每组8只裸鼠,于造模72 h后开始给药。对照组给予生理盐水灌胃,每次0.5 ml/10 g,西药组组和乌骨藤组分别给予塞来昔布和乌骨藤水提物灌胃,均为每次0.5 ml/10 g,1次/d。连续30 d。分别在给药第15天和第30天各处死半数裸鼠,检测相应指标。
1.4检测指标及观察方法
1.4.1癌瘤生长情况在给药第15天和第30天各处死半数裸鼠,剥取瘤块,用电子天平称量移植瘤体的质量,计算抑瘤率。测量肿瘤大小、计算肿瘤体积。
1.4.2癌瘤转移情况分别在第15天和第30天处死裸鼠,打开腹腔观察癌瘤转移情况,肉眼下计数肝脏及肠系膜表面的转移结节数,比较各组胃癌细胞发生转移结节个数。
1.4.3COX-2 的测定用Western印迹法,将匀浆提取的蛋白经变性处理。再行聚丙烯酰胺凝胶电泳,转膜,加入COX-2 的一抗(1∶500),孵育成功后,加入二抗后(1∶2 000),室温下孵育后,每张膜加1∶1的发光液1 ml,化学发光法显影,扫描条带后,上机分析。
1.5统计学方法采用SPSS19.0进行t检验及χ2检验。
2结果
2.1各组大鼠的癌瘤生长情况各组癌瘤重量和体积均随时间的增加而不同程度的增长,经药物干预后,癌瘤的重量和体积均得到了抑制,与对照组相比,西药组和乌骨藤组的癌瘤重量和体积增长均显著减慢(P<0.05),与西药组相比,乌骨藤组对于癌瘤增长的控制作用更为显著(P<0.05),各药物组抑瘤率均显著高于对照组(P<0.05),与西药组相比,乌骨藤组的抑瘤率更高(P<0.05)。见表1。
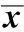
表1 各组大鼠癌瘤生长情况比较( ± s, n=4)
与对照组同时点比较:1)P<0.05;与西药组同时点比较:2)P<0.05,下表同
2.2各组大鼠的癌瘤转移情况两组裸大鼠在肝脏、肠系膜等部位也可见肿瘤结节,灰白色,大小不等。治疗15 d时,各组均未见肠系膜转移,仅对照组见肝脏转移。治疗30 d时,各组均见肝脏及肠系膜转移。各治疗组与对照组相比,肝脏及肠系膜转移数均显著减少,与西药组相比,乌骨藤组癌瘤的转移数减少的更为明显(P<0.05),见表2。
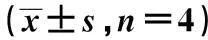
表2 各组大鼠转移病灶数
2.3各组大鼠胃黏膜组织COX-2蛋白水平比较经药物治疗后,治疗后15 d,30 d各治疗组COX-2蛋白水平均显著降低(P<0.05),与西药组相比,乌骨藤组的COX -2蛋白水平下降更为明显(P<0.05)。见表3,图1。
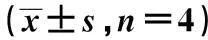
表3 各组大鼠COX-2蛋白水平比较

图1 各组大鼠胃黏膜组织COX-2蛋白表达
3讨论
随着人民生活水平的不断提高,胃肠道恶性肿瘤已成为严重威胁人类健康的主要疾病之一,我国胃癌发病人数占全世界发病总数的42%〔6〕,并有逐年上升的趋势,并且胃癌的发病年龄有年轻化的趋势,胃的原位癌是胃癌的前期表现,因此,原位癌的早期诊断和治疗对于胃癌的诊断和治疗个非常重要,直接影响到患者的长期生存率。COX是前列腺素合成过程中重要的限速酶〔7〕。正常胃黏膜COX-2表达很低甚至不能测出,在病理情况下,COX-2的高表达通过抑制细胞凋亡、促进新生血管的形成及帮助肿瘤细胞逃逸机体免疫监视等多种作用促进肿瘤的发生及发展〔8〕。近年来研究发现,COX-2 高表达与肿瘤发生发展密切相关。因此许多研究已把COX-2作为治疗胃癌的靶点。胃癌组织中COX-2的表达远高于正常胃黏膜〔9〕。它的表达延长了癌细胞的生存期,有利于癌细胞发生浸润与转移。大部分研究认为COX-2与浸润深度以及病理分期有关〔10〕。还有一些研究认为其与肿瘤大小有关〔11〕。因此,COX-2的过表达可能诱导胃癌的侵袭和转移。现代药理研究表明:乌骨藤中所含的C21 甾体苷、三萜和多糖是其抗肿瘤作用的主要活性物质。乌骨藤提取物对多种肿瘤细胞均有抑制作用〔12〕,但对于乌骨藤提取物对于原位胃癌的治疗作用研究尚少,为了减轻患者痛苦,改善其预后,笔者做了以上研究。
本研究表明药物治疗可以有效地抑制原位胃癌的增长,可以有效地抑制癌瘤组织的转移,且乌骨藤水提物的效果更好。表明药物能够降低COX -2水平,且乌骨藤水提物的效果更优,从而抑制肿瘤的增生和转移,与之前的研究结果相符。
总之,乌骨藤提取物抑制MKN-45大鼠人原位胃癌模型肿瘤生长、转移及COX-2表达具有明显的改善作用,对临床有指导意义,值得临床推广。
4参考文献
1Kemper K,Rodermond H,Colak S,etal.Targeting colorectal cancer stem cells with inducible caspase-9〔J〕.Apoptosis 2012;17(4):528-37.
2Zheng RS,Zhang SW,Wu LY,etal.Report of incidence and mortality from China cancer registries in 2008〔J〕.Clin Cancer,2012;21(1):1-12.
3Ferlay J,Shin HR,Bray F,etal.Estimates of worldwide burden of cancer in 2008 LGLOBOCAN 2008〔J〕.Int J Cancer,2010;127(11):2893-917.
4刑旺兴,陈斌.通光藤中两个新C21 甾体苷类成分〔J〕.药学学报,2004;39(4):272-5.
5娄红祥,李铣.C21 甾体甙的化学研究进展〔J〕.国外医药·植物药分册,1990;15(2):51-6.
6陈奇.中药药理实验方法学〔M〕.北京:人民卫生出版社,2001:113-5.
7Xue YW,Zhang QF,Zhu ZB,etal.Expression of cyclooxygenase-2 andclinicopathologic features in human gastric adenocarcinoma〔J〕.World J Gastroenterol,2003;9(2):250-3.
8Enders GA.Cyclooxygenase-2 overexpression abrogates the antiproliferative effects of TGF-beta〔J〕.Br J Cancer,2007;97(10):1388.
9吴平,陈念平,黄冰,等.环氧化酶-2基因和蛋白在人胃癌组织中的表达及临床意义〔J〕.中国肿瘤临床,2004;31(15):860-3.
10Farooq M,Haq I,Qureshi AS.Cardiovascular risks of COX inhibition:current perspectives〔J〕.Expert Opin Pharmacother,2008;9(8):1311.
11Han SL,Tang HJ,Hua YW,etal.Expression of COX-2 in stomach cancers and its relation to their biological features〔J〕.Dig Surg,2003;20(2):107-14.
12Na YR,Yoon YN,Son DI,etal.Cyclooxygenase-2 inhibition blocks M2 macrophage differentiation and suppresses metastasis in murine breast cancer model〔J〕.PLoS One,2013;8(5):e63451.
〔2013-12-17修回〕
(编辑安冉冉/曹梦园)
