胃肠道肿瘤患者术后责任制护理中营养风险筛查的应用
2015-12-23马纯雪兰亭林璋双
马纯雪 兰亭 林璋双
胃肠道肿瘤患者术后责任制护理中营养风险筛查的应用
马纯雪 兰亭 林璋双
营养风险筛查2002(NRS 2002)是欧洲肠外、肠内营养学会(ESPEN)于2002年推荐使用的筛查工具[1]。营养风险筛查是由医护人员实施的简便的筛查方法,用以决定是否需要制定或实施肠外、肠内营养支持计划[2]。有研究发现[3-4],对手术、肿瘤患者等进行营养风险筛查后的结果表明,营养等级较低患者的住院时间较长,生存率也更低,而对于这些较低的患者进行营养支持后,生存率和住院时间等均得到改善。但是营养风险筛查以及之后进行的营养支持需要很多的人力,如果安排不合理,不仅增加了护理人员和医师的工作,而且还会增加患者的医疗费用以及治疗的错漏[5]。因此,笔者将营养风险筛查工作应用于责任班次职责内,以便更好开展优质护理,给患者更优质、满意的护理服务,现将实施体会报道如下。
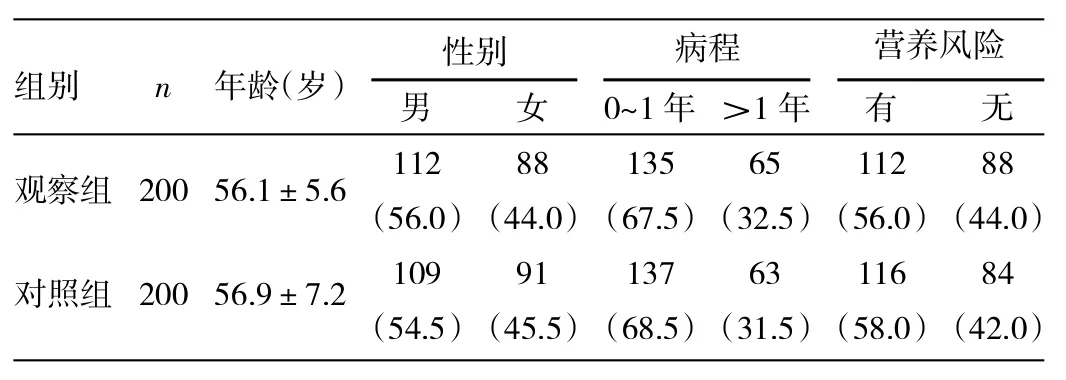
表1 两组患者一般资料的比较[例(%)]
1 资料和方法
1.1 一般资料 选择2010年10月至2012年3月我科新入院的胃肠道恶性肿瘤患者400例。纳入标准:年龄18~90岁,新入院,住院1d以上,将进行手术治疗,神志清者,研究前经知情同意愿意参与此研究,并签署知情同意书。男221例,女179例;年龄18~84岁,平均(56.2±11.4)岁;其中胃癌198例,胃癌伴糖尿病9例,胃癌伴高血压33例,肠癌63例,肠癌伴糖尿病16例,肠癌伴高血压10例。临床表现主要有消化不良、腹痛、腹水、中晚期有腹膜刺激征(腹部压痛、反跳痛和腹肌紧张)、腹部有难以忍受的剧烈疼痛、大汗淋漓、发热、全身虚弱无力、不语等症状等。严格按照随机化的原则,采用Excel随机数法将患者分为观察组和对照组,各200例。两组患者年龄、性别、病程等一般资料的比较差异均无统计学意义(均P>0.05),详见表1。
1.2 方法
1.2.1 营养风险评估 记录所有患者性别、年龄、病史、病情以及在入院后6h之内的诊断数据。第2天早上测量身高和体重,使用NRS2002评分系统进行评分,总分=病情评分+营养损伤情况评分+年龄评分,总分≥3分即为存在营养风险,应予营养支持。同时,分别使用Beckman DXC800全自动生化分析仪检测患者营养支持前后白蛋白和前白蛋白水平。
1.2.2 营养支持 所有患者在肿瘤切除术后均需进行营养支持。营养支持主要包括肠内营养和肠外营养,肠内营养包括口服营养素和通过胃液囊空肠导管给予营养物质,给予热量不低于10kJ/(kg·d)。肠外营养是指从静脉输入包括氨基酸、葡萄糖或脂肪在内的人工营养物质,其非蛋白热量不低于10kJ/(kg·d)。营养肠内营养或肠外营养在3d或3d以上者,即为给予营养支持。
1.2.3 术后并发症的发生率和住院时间 统计所有患者术后并发症的发生情况,并发症严重程度分级根据纠正并发症的治疗方法而定,常见的并发症有尿路感染、肺部感染、肠梗阻、切口感染、胃排空障碍、下肢静脉血栓、吻合口瘘和败血症等。统计所有患者的住院时间。1.3 护理方法 统计两组患者对于护理人员在专科护理、基础教育、健康教育、医疗满意度和患者满意度的评分(总分100分),并统计护理过失的发生率。
1.3.1 对照组患者的护理 患者入院后按照常规工作流程标准实施并处理医师下达的营养医嘱。
1.3.2 观察组患者的护理 观察组在对照组护理的基础上实施责任制护理,对其施行营养风险筛查工作,具体如下:(1)确定责任护士:选派高年资护士参加上海营养风险筛查培训班,组织全科护士学习营养风险筛查评分表所包含的各项内容及在筛查过程中要注意的事项;学习营养护理知识,健全落实营养筛查护理规章制度;组织护士学习营养护理中经常碰到患者询问的问题,掌握其发生的机制,以便迅速判断准确,确保护理工作质量;加强责任心,做好有效医护沟通;坚持每季度临床营养护理查房及会议,对营养护理操作、营养筛查技能进行培训考核,考核合格者方能担任此工作。对新入科的轮转护士进行培训并考核。将责任护师分成4个包干小组,每个小组包含1~2位高级责任护师、2~3位初级责任护师,每个小组负责一定数量的患者(一般为15例),每3个月轮换1次。(2)改革护师排班模式:实行早(A)、晚(P)、夜(N)三班制排班(A班时间:8:00~16:00;P班时间:16:00~22:30;N班时间:22:00~8:00),重点班次成立工作团队,由其中三、四级护师担任护理助长,一、二级护师进行分管床位。(3)工作流程:责任护师对当日新入院患者以及术后1周内患者使用欧洲营养学会推荐的NRS2002评分表进行首次营养风险筛查评分[1],NRS评分=疾病严重程度+营养状况受损评分+年龄评分(若年龄≥70岁,年龄评分+1分),并按规定把评分表放在病历首页供医师参考使用,同时进行编号登记。一般认为,营养风险筛查评分≥3分,提示患者存在营养不良风险;若营养风险筛查评分<3分,提示患者不存在营养不良风险,故当患者营养风险筛查评分≥3分时,由护师在评分表首页粘贴红色提示条码告知医师,条码内容为:“该患者营养风险筛查()分,需要营养支持吗?”,再由医师根据综合情况决定是否进行营养支持,营养支持内容通常为百普力肠内营养液,必要时利用肠外营养,快速纠正患者的低蛋白血症、负氮平衡,维持患者水、电解质平衡。接到出院医嘱时(指有营养风险筛查患者),由责任护师负责进行手术患者出院时营养风险筛查评分,并放入指定的营养筛查专柜。每月科室由专人负责完成营养筛查电脑输入工作。注意事项:每位护师认真掌握营养风险筛查评分工具;评分分值是每个子项目不累加计算,如1分分值中该患者有两项符合的也应记1分;在统计平均每天输液量是应是输液总量除以输注天数。(4)相关资料的保存:科室需腾出两个专柜分别放置营养筛查的空白表格和已完成的表格。制定营养筛查辅助工具如卡路里的换算及TNM分期的定义资料,放在固定的地方供护师查阅。
1.4 统计学处理 采用SPSS18.0统计软件,计量资料以表示,组间比较采用t检验;计数资料组间比较采用χ2检验。
2 结果
2.1 两组患者的营养状况 两组患者中均存在营养风险的患者,其中对照组中116例患者出现营养风险,占58%,观察组中112例患者出现营养风险,占56%,两组间差异无统计学意义(P>0.05)。所有出现营养风险的患者在肿瘤切除术后均进行了营养支持,根据患者本身的身体状况进行肠外营养支持和肠内营养支持,其中对照组患者进行肠内营养支持的为56例(48.3%),肠外营养支持为60例(51.7%);观察组患者进行肠内营养支持的为54例(48.2%),肠外营养支持为58例(51.8%),两组间比较差异无统计学意义(P>0.05)。两组患者在营养支持之前的白蛋白和前白蛋白水平基本一致,在营养支持之后,患者的上述指标均有所升高,营养支持前后的差异均有统计学意义(均P<0.05),但两组间的差异无统计学意义(P>0.05),详见表2。

表2 两组患者的白蛋白和前白蛋白水平的比较
2.2 两组患者住院时间和并发症发生率的比较 两组患者均有并发症如尿路感染、肺部感染、肠梗阻、切口感染、胃排空障碍、下肢静脉血栓、吻合口瘘和败血症等的发生,观察组的发生率略低于对照组,但是两组间比较差异无统计学意义(P>0.05),详见表3。观察组术后住院时间为(10.4±0.7)d,对照组为(11.2±1.4)d,观察组的住院时间略低于对照组,但两组间比较差异无统计学意义(P>0.05)。

表3 两组患者并发症发生率的比较[例(%)]
2.3 两组护理质量的比较 把营养筛查工作落实到责任班次职责内,每位护师对营养筛查相关技术操作及知识掌握有了一定程度的提高,病区护理质量有了显著提高,与对照组相比,差异有统计学意义(P<0.05),护理过失与对照组比较也明显减少,差异有统计学意义(P<0.05),详见表4。

表4 实施营养筛查工作前后护理质量比较(分)
3 讨论
本次研究的结果表明,结合责任制护理进行营养风险筛查后,尽管没有对并发症和住院时间产生有益的影响,但是增加了护理的满意度,得到了患者的好评,增加了护理工作的效率,同时也减少了护理过失的概率。
肿瘤患者由于疾病消耗或进食不足容易导致临床上的营养风险,此外,医师用药的不规范也会引起临床上营养制剂滥用现象[6-7]。因此,目前临床工作中迫切需解决的问题是如何提供合理营养支持使得患者获益。有报道表明[8],对于出现营养风险的胃肠道肿瘤患者进行营养支持可以降低并发症的发生率,减少住院时间,而对于无营养风险的患者进行营养支持后却出现相反的结果。因此,本研究仅对出现营养风险的患者进行了营养支持。此外,在营养支持的方式方面,给予肠内营养支持的效果要优于肠外营养支持,但是肠内营养支持本身会引起患者呕吐、腹胀、腹泻和腹痛等症状,所以笔者会根据患者的实际情况有选择地进行肠内或肠外营养支持[9-10]。
责任护师实施营养筛查工作明显激发了工作积极性,医护人员与患者接触更加频繁,病情了解更为细致,使护师认识到护理人员必须具备扎实的营养护理知识及敏锐的观察力、判断力才能更加细致观察动态病情[11]。同时提高了护师临床营养护理水平及技能,碰到困难疑惑与医师沟通解决,减轻临床医师在临床营养开展过程中的工作压力,使得医师有更充沛的精力投入到其他更重要的医疗工作中去;更加科学合理的对应关系处理模式下获得胃肠外营养支持更好的效果,更重要的是通过有效沟通教育,护理工作更加细致到位,提高患者满意度,增强患者对医疗环境的认同感、对医护人员依从性,从而使得病情恢复得更快[12]。
综上所述,把营养筛查工作落实到责任制护理后,病区的护理质量有了一定程度的提高;与此同时,护理过失与对照组比较也明显减少,值得在临床上进一步应用。
[1]Moeeni V,Walls T,Day A S.Nutritional status and nutrition risk screening in hospitalized children in New Zealand[J].Acta Paediatrica,2013,102(9):419-423.
[2]Holst M,Yifter‐Lindgren E,Surowiak M,et al.Nutritional screening and risk factors in elderly hospitalized patients:association to clinical outcome[J]?Scand J Car Sci,2013,27(4):953-961.
[3]Zhou W,Xu X,Yan J,et al.Nutritional risk is still a clinical predictor of postoperative outcomes in laparoscopic abdominal surgery[J].Surg Endosc,2013,27(7):2569-2574.
[4]Yu K,Zhou X,He S.A multicentre study to implement nutritional risk screening and evaluate clinical outcome and quality of life in patients with cancer[J].Eur J Clin Nutr,2013,67(7):732-737.
[5]Beck A M,Beermann T,Kja er S,et al.Ability of different screening tools to predict positive effect on nutritional intervention among the elderly in primary health care[J].Nutrition,2013,29(7):993-999.
[6]Schwegler I,Von Holzen A,Gutzwiller J P,et al.Nutritional risk is a clinical predictor of postoperative mortality and morbidity in surgery for colorectal cancer[J].Br J Surg,2010,97(1):92-97.
[7]Gavazzi C,Colatruglio S,Sironi A,et al.Importance of early nutritional screening in patients with gastric cancer[J].Br J Nutr,2011, 106(12):1773-7779.
[8]董峰,马君俊,冯波,等.两种营养支持方式在胃肠道肿瘤患者术后的疗效对比研究[J].现代生物医学进展,2013,21(2):4056-4059.
[9]陈巧女,谢浩芬,徐琴鸿,等.胃肠道肿瘤患者营养风险筛查与临床结局分析[J].中华现代护理杂志,2013,33(2):100-103.
[10]孙光,彭勃,徐超.胃肠道肿瘤患者术后两种早期营养支持的对比研究[J].中国普通外科杂志,2012,21(9):1119-1122.
[11]石英,杨辉,展淑敏,等.医护合作型责任制护理模式的实践及效果[J].中国护理管理,2013,(2):22-25.
[12]张爱华.责任制护理小组模式在肿瘤外科中的实践与效果[J].中国医药导报,2012,9(4):146-147.
(本文编辑:严玮雯)
角蛋白16和17在部分表皮肿瘤中的表达和意义
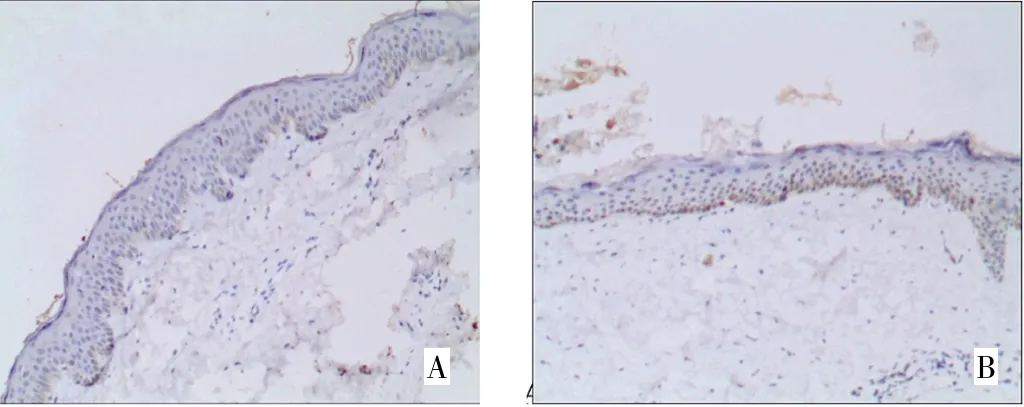
图1 正常皮肤中K16、K17的表达(A:K16;B:K17;DAB染色,×100)
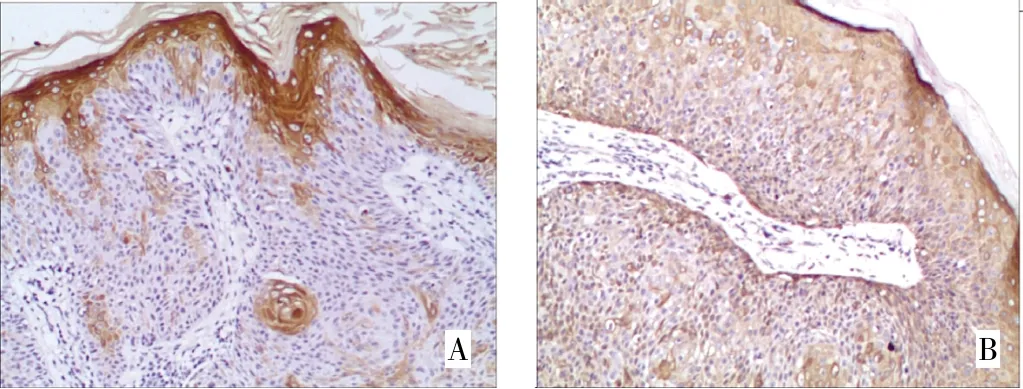
图2 脂溢性角化病皮损K16、K17的表达(A:K16;B:K17;DAB染色,×100)

图3 日光性角化病皮损K16、K17的表达(A:K16;B:K17;DAB染色,×100)

图4 皮角皮损K16、K17的表达(A:K16;B:K17;DAB染色,×100)
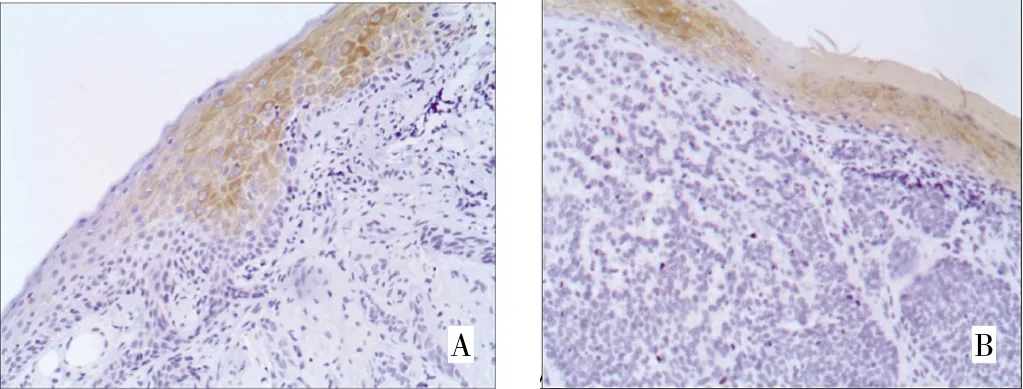
图5 基底细胞癌K16、K17的表达(A:K16;B:K17;DAB染色,×100)
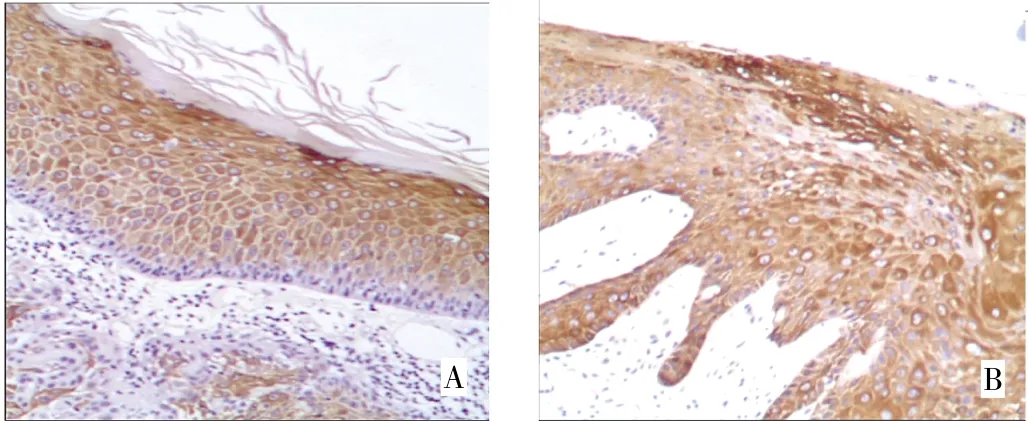
图6 鳞状细胞癌K16、K17的表达(A:K16;B:K17;DAB染色,×100)
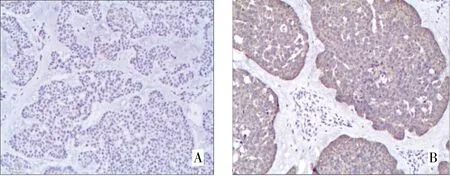
图7A 基底细胞癌K16、K17的表达(A:K16;B:K17;DAB染色,×100)

图8 鳞状细胞癌K16、K17的表达(A:K16;B:K17;DAB染色,×100)
2014-03-10)
325000 温州医科大学附属第一医院胃肠外科
马纯雪,E-mail:mcx207@163.com
