泽泻与格列齐特对原发性糖尿病大鼠治疗作用的评价
2015-12-21丁琛一谭擎英施宁川
丁琛一,谭擎英,施宁川
浙江大学 公共卫生学院,杭州310031
泽泻与格列齐特对原发性糖尿病大鼠治疗作用的评价
丁琛一,谭擎英,施宁川
浙江大学 公共卫生学院,杭州310031
目的 探讨单味中药泽泻与单味西药格列齐特对糖尿病的治疗作用,评价中西药物对糖尿病治疗的差异。方法 选择原发性糖尿病(GK)大鼠模型,将其分为空白组、泽泻组、格列齐特组,另选择Wistar大鼠作为正常组。给予2周药物治疗后,观察GK和Wistar大鼠体质量、进食量、空腹血糖、糖耐量等指标变化,综合评价中药、西药对糖尿病治疗的差异性。结果 体质量:正常组、空白组、格列齐特组给药2周后体质量增加 [(241.3±7.0)g比(263.5±11.1)g、(242.8±7.1)g比(267.9±16.8)g、(243.9±12.2)g比(277.9±9.8)g,P<0.05],泽泻组较其余3组给药后体质量下降 [(244.6±9.2)g比(227.9±13.7)g,P<0.05]。进食量:给药前后及给药2周后各组差异无统计学意义(P>0.05)。空腹血糖:给药1周后正常组较空白组、泽泻组、格列齐特组给药前空腹血糖显著降低 [(4.8±0.2)mmol/L比(8.2±1.4)mmol/L、(8.1±0.6)mmol/L、(8.1±0.9)mmol/L,P<0.05];空白组、泽泻组、格列齐特组给药前空腹血糖差异无统计学意义(P>0.05);给药2周后泽泻组、格列齐特组空腹血糖较给药后显著降低 [(6.9±0.7)mmol/L比(8.1±0.6)mmol/L,(5.8±0.5)mmol/L比(8.1±0.9)mmol/L,P<0.05];泽泻组、格列齐特组给药2周后较空白组空腹血糖显著降低,且两组间给药2周后差异也有统计学意义[(6.9±0.7)mmol/L比(8.8±0.6)mmol/L,(5.8±0.5)mmol/L比(8.8±0.6)mmol/L,(6.9±0.7)mmol/L比(5.8±0.5)mmol/L,P<0.05]。糖耐量:空白组、泽泻组、格列齐特组较正常组糖耐量异常,泽泻组在给予药物2周后糖耐量较给药前明显改善,且较空白组也显著改善(P<0.05);格列齐特组在给予药物2周后糖耐量与给药前及空白组相比,差异无统计学意义(P>0.05)。结论 单味中药泽泻、西药格列齐特有较好的降低空腹血糖的作用;然而西药作为单一靶点研发的药物,在降低空腹血糖作用上较中药泽泻强。中药泽泻较西药格列齐特在控制空腹血糖时,同样能控制体质量、改善糖耐量异常,体现出中药泽泻作为一个混合物对于综合性疾病能发挥多靶点干预的优势。
泽泻;格列齐特;原发性糖尿病大鼠
Acta Acad Med Sin,2015,37(4):451-455
随着中药现代化研究的深入,中药表现出不同于西药的多组分、多层次、多药效、多靶点等特点。西药是由单一或有限的几个化合物单体组成,在人体内主要作用于特异的靶点,具有相当高的选择性和专一性,被人体吸收后在特定的系统、组织、甚至器官中的含量分布相当高,并发挥特定的治疗作用。而中药也有特定的活性物质作用于特定的靶点,但更多的是不同的活性物质作用于多个不同的靶点而产生多个药理作用,很多甚至为协同、放大的优势作用。而且中医药以整体的观念治疗病症,由此可以把中药形象地比喻为“霰弹”[1]。西药多以恢复发生病理变化的脏器为目的,它是针对“病”引进“对抗”。而中药是以天然植物、动物、矿物等,按照一定原则组成的复方。它多是恢复人体与环境或人体各脏腑间的不平衡状况,它是将“证”引进调整。鉴于由中药的多成分与西药的组成相对单一这一特点引起的两大药物体系靶点差异性问题,本研究以糖尿病这一多遗传因素引起的疾病作为研究对象,选取中西药中各自具有代表性的降血糖药物泽泻与格列齐特,运用药效学方法从疾病治疗角度评价泽泻与格列齐特的差异性,希望因此映射出中药与西药对于某一疾病的治疗差异,为进一步深入研究中药作用特点和机制抛砖引玉。
材料和方法
实验动物 健康SPF级原发性糖尿病(Goto-Kakizaki,GK)大鼠36只,雄性,7周龄,体质量200~250 g,浙江中医药大学实验动物中心提供 [合格证号:SCXK(沪)2010-0006]。Wistar大鼠由浙江中医药大学实验动物中心提供。所有的大鼠均7周龄,雄性,体质量200~250 g。
材料 泽泻药材:批号:10032518,由浙江中医药大学中药饮片厂提供;格列齐特片:批号:2000032,施维雅制药有限公司生产;生理盐水:批号081212-3,浙江沙普爱思制药有限公司生产;葡萄糖:批号090610,烟台鼎峰生物科技有限公司生产;苦味酸:批号100325-5,石家庄凯德姆化工有限公司生产。大鼠灌胃器、电子天平:上海越平科学仪器有限公司生产;移液枪;旋转蒸发仪:上海申生科技有限公司,型号R204B3;涡旋混合器:美瑞泰克科技有限公司,型号MAXⅡ;血糖仪/试纸:强生医药器械有限公司,批号3004523。
方法
泽泻样品:取泽泻粉末150 g装入2 L的圆底烧瓶中用蒸馏水300 ml浸润1 h,加热回流提取循环操作3次。提取液趁热过滤。合并滤液,用旋转蒸发仪浓缩至500 ml(相当于含生药量为0.3 g/ml)。
格列齐特样品:取格列齐特缓释片60片去包衣(含1.8 g格列齐特),研磨成粉,精密称取格列齐特粉末800 mg,用32 ml生理盐水溶解,制备成25 mg/ml的格列齐特溶液。
葡萄糖水溶液配置:80 g葡萄糖用二级蒸馏水100 ml配成800 mg/ml。给药方式为灌胃法。
大鼠空腹血糖、糖耐量评价及分组 GK大鼠在无菌动物房适应性喂养3 d(自由进食,饮水;12 h光照)。次日晚8时起禁食不禁水,第2天早晨,称重、测前1日进食量(晚上食物重量减去早上食物重量)、苦味酸标记大鼠、测空腹血糖,之后给予每只大鼠采用灌胃法灌胃2 g/kg葡萄糖水溶液(0.0025 ml/g大鼠)测30、60 min糖耐量。将大鼠随机分成泽泻组、空白组、格列齐特组,保证3组空腹血糖差异无统计学意义。Wistar大鼠为正常组。
大鼠给药及给药后空腹血糖、糖耐量评价 将GK大鼠随机分成空白组(12只)、泽泻组(12只)、格列齐特组(12只)。Wistar大鼠组作为正常组(12只)。按照吴国亭和徐倍[2]方法给予格列齐特组剂量为0.06 mg格列齐特/g大鼠(0.002 ml/g)灌胃。泽泻组给与含生药量3 mg/g大鼠即0.002 ml/g(相当于临床成人用量的3倍)灌胃。空白组与正常组均给予给药组等体积的生理盐水灌胃。给药第1、2周时,当晚开始禁食,自由饮水。次日早晨按之前的方法测体质量、进食量、空腹血糖以及糖耐量。
统计学处理 应用SPSS 17.0统计软件,计数资料采用F检验,P<0.05为差异有统计学意义。
结果
GK大鼠体质量、进食量 正常组、空白组、泽泻组、格列齐特组给药前体质量差异无统计学意义(P>0.05),给药1、2周后,泽泻组体质量较给药前以及其他组体质量明显下降(P<0.05,P<0.01)。各组进食量给药前及给药1、2周后差异均无统计学意义(P>0.05)(表1)。
GK大鼠空腹血糖的变化 空白组、泽泻组、格列齐特组较正常组空腹血糖显著升高(P<0.05),且空白组给药1~2周后空腹血糖仍然无改善。格列齐特组较空白组相比,随着给药时间延长,空腹血糖得到显著改善(P<0.01),泽泻组在给药1周后空腹血糖与空白组比较,差异无统计学意义(P>0.05),与自身给药前比较,差异有统计学意义(P<0.05),当继续给药到2周后空腹血糖改善明显(P<0.01)。泽泻组与格列齐特组在改善空腹血糖方面,格列齐特组较泽泻组强且快(P<0.05)(表2)。
GK大鼠糖耐量的变化 正常组、空白组糖耐量随着给药时间无变化(P>0.05)。随着药物的治疗,泽泻组糖耐量随着时间的变化,有较明显的改善(P<0.05);格列齐特组糖耐量无变化(P>0.05)(表3)。
表1 泽泻与格列齐特对原发性糖尿病大鼠体质量、进食量的影响(n=12,±s,g)Table 1 Alisma and gliclazide’s influence on weight and intake in Goto-Kakizaki rats(n=12,±s,g)

表1 泽泻与格列齐特对原发性糖尿病大鼠体质量、进食量的影响(n=12,±s,g)Table 1 Alisma and gliclazide’s influence on weight and intake in Goto-Kakizaki rats(n=12,±s,g)
与正常组、空白组、格列齐特组比较,aP<0.05,bP<0.01;与给药前比较,cP<0.05,dP<0.01aP<0.05,bP<0.01 compared with the normal group,blank group,and gliclazide group;cP<0.05,dP<0.01 compared with before the administration
分组Group体质量Weight 进食量Intake给药前Before the administration给药后1周One week after administration给药后2周Two weeks after administration给药前Before the administration给药后1周One week after administration给药后2周Two weeks after administration正常组Normal group 241.3±7.0 252.3±10.8c 263.5±11.1d22.6±2.7 22.2±3.0 23.4±3.0空白组Blank group 242.8±7.1 255.6±21.2c 267.9±16.8d 23.0±3.2 23.1±2.5 23.0±2.5泽泻组Alisma group 244.6±9.2 233.5±16.6ac 227.9±13.7bd 23.7±2.9 23.2±2.2 23.2±2.6格列齐特组Gliclazide group 243.9±12.2 264.1±13.5c 277.9±9.8d23.9±2.1 22.3±2.1 20.7±2.7
表2 泽泻与格列齐特对原发性糖尿病大鼠空腹血糖的影响(n=12,±s,mmol/L)Table 2 Alisma and gliclazide’s influence on the treatment of Goto-Kakizaki rats’fasting glucose(n=12,±s,mmol/L)

表2 泽泻与格列齐特对原发性糖尿病大鼠空腹血糖的影响(n=12,±s,mmol/L)Table 2 Alisma and gliclazide’s influence on the treatment of Goto-Kakizaki rats’fasting glucose(n=12,±s,mmol/L)
与给药前比较,aP<0.05,bP<0.01;与正常组比较,cP<0.05,dP<0.01;与空白组比较,eP<0.05,fP<0.01aP<0.05,bP<0.01 compared with before the administration;cP<0.05,dP<0.01 compared with normal group;eP<0.05,fP<0.01 compared with blank group
分组Group空腹血糖Fasting glucose给药前Before the administration给药后1周One week after administration给药后2周Two weeks after administration正常组Normal group 4.8±0.2 4.8±0.2 5.1±1.0空白组Blank group 8.2±1.4d 8.9±0.5d 8.8±0.6d泽泻组Alisma group 8.1±0.6d 7.5±1.0ad 6.9±0.7bcf格列齐特组Gliclazide group 8.1±0.9d 6.5±0.6bce 5.8±0.5bf
表3 泽泻与格列齐特对原发性糖尿病大鼠糖耐量的影响(n=12,±s,mmol/L)Table 3 Alisma and gliclazide’s influence on the treatment of Goto-Kakizaki rats’tolerance(n=12,±s,mmol/L)
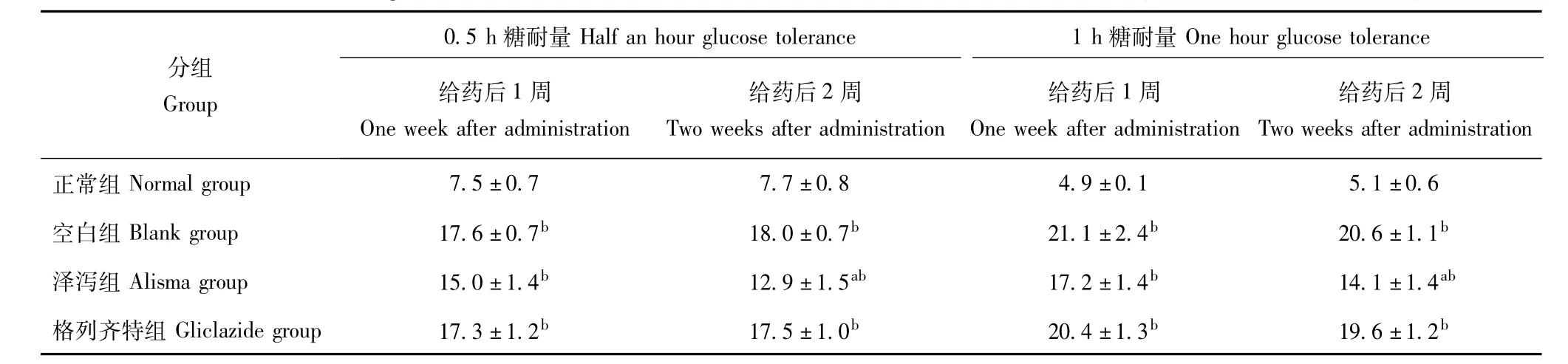
表3 泽泻与格列齐特对原发性糖尿病大鼠糖耐量的影响(n=12,±s,mmol/L)Table 3 Alisma and gliclazide’s influence on the treatment of Goto-Kakizaki rats’tolerance(n=12,±s,mmol/L)
与给药后1周比较,aP<0.05;与正常组比较,bP<0.01aP<0.05 compared with one week after administration;bP<0.01 compared with normal group
分组Group 0.5 h糖耐量Half an hour glucose tolerance 1 h糖耐量One hour glucose tolerance给药后1周One week after administration给药后2周Two weeks after administration给药后1周One week after administration给药后2周Two weeks after administration正常组Normal group 7.5±0.7 7.7±0.8 4.9±0.1 5.1±0.6空白组Blank group 17.6±0.7b 18.0±0.7b 21.1±2.4b 20.6±1.1b泽泻组Alisma group 15.0±1.4b 12.9±1.5ab 17.2±1.4b 14.1±1.4ab格列齐特组Gliclazide group 17.3±1.2b 17.5±1.0b 20.4±1.3b 19.6±1.2b
讨论
2型糖尿病作为综合性疾病主要由于遗传缺陷和后天多种环境因素共同导致的胰岛素分泌缺陷和胰岛素生物效应降低,继而引起以高血糖、胰岛素抵抗、β细胞损伤为主要特征,整个发病过程涉及到多个生理病理方面。不仅存在空腹血糖异常,还存在糖耐量、胰岛素分泌、胰岛素信号传导通路、体质量体脂方面的异常。因此,临床多考虑采用有互补作用机制的多种药物进行联合治疗。药物治疗有中药与西药治疗。目前主要以西药治疗为主,其原因可能如下:(1)成分明确,有统一质量标准可循;(2)作用靶点专一、疗效确切; (3)主要作用和不良反应机制明确。磺脲类药物作为经典的降血糖药物其主要是通过与β细胞表面特异受体的相互作用,刺激胰岛素分泌。当细胞外液中葡萄糖浓度上升时,β细胞内ATP/ ADP比值上升,细胞膜上K+通道关闭,细胞膜去极化,Ca2+通道开放,Ca2+内流并启动β细胞释放胰岛素。磺脲类药物和胰岛β细胞膜上磺脲类药物受体特异性结合,而磺脲类药物受体本身或其中一部分就是K+内流通道,从而使胰岛素(内源性)以“电脉冲”方式释放到细胞外,产生降血糖的药理效应[3]。中药降血糖药物筛选则为近几十年开始研究,学者们陆续发现,人参、黄芪、麦冬、葛根、泽泻、五味子、黄连、大黄等数十种中药[4-5]有较好的降血糖作用。而中药降血糖作用机制主要为以下几个方面:(1)促进胰岛素分泌,增加血清胰岛素含量;(2)促进胰岛β细胞的再生;(3)激活过氧化物酶体增殖物激活受体;(4)提高机体对胰岛素的敏感性;(5)促进外周组织对糖的利用;(6)延缓肠道对葡萄糖的吸收[6]。本研究所选的中药泽泻为泽泻科植物泽泻 Alisma orientale(Sam.)Juzep的干燥块根,其主要化学成分为萜类化合物,目前已经从泽泻中分离得到50多种三萜类、30多种倍半萜类、3种二萜类成分[7]。现代药理学表明这些萜类药物有着广泛的药理学活性。其中“降血脂、降血糖、降血压”及控制体质量作用尤其显著[8]。同时,泽泻的降空腹血糖作用与西药格列齐特一致,也是通过刺激胰岛素分泌这一机制[8]。这对于糖尿病这种“血糖和体质量(脂代谢)均出现异常的疾病而言,是较为代表的中药。并且近几十年对泽泻的研究证实了泽泻的物质基础:以萜类为主,含多种四环三萜、倍半萜、二萜化合物等;另外含甾醇、生物碱、苷类、黄酮、有机酸、氨基酸、多糖、挥发油等成分[9]。药理活性报道较多的有降血脂、利尿、降压、眩晕和抗脂肪肝等[9-10]。目前对泽泻药理活性报道最多的是降血脂作用。然而对其降血糖作用报道较少。仅有杨新波等[11-13]对其泽泻的降血糖作用做了较为系统研究,结果显示对于糖尿病小鼠模型,灌胃给予泽泻水提部分0.5 g/kg(浸膏重),给药10 d时,对糖尿病小鼠有显著的降血糖作用。此小鼠剂量折算成大鼠剂量为0.35 g/kg(浸膏重)。而本研究所用泽泻剂量为临床成人用量的最大剂量(30 g)换算成大鼠的剂量。在给药14 d后显示对糖尿病模型一定的降空腹血糖作用。但并未有文献报道的那么强。分析原因可能如下:(1)泽泻药材品质差异所导致的药效学差异;(2)不同动物种之间存在对药物敏感性差异;(3)原发性糖尿病模型本身与化学诱导的糖尿病模型之间无法等同,造成结果存在差异;(4)给药时间过长,动物对药物产生耐受;(5)长时间给予降血糖药物时,可能诱发激活旁生通路,使血糖上升。而在改善GK大鼠体质量、糖耐量方面,泽泻较格列齐特体现出优势,这可能与泽泻较格列齐特物质基础多样性有关。
综上,在对于糖尿病这样一种综合性疾病来讲,选择中西药治疗各有优势:(1)西药对于主要指标改善明显、起效快,但是往往难“全面兼顾”;(2)某些中药在治疗时较西药起效慢、作用弱,然而能兼顾到疾病的多个病理、生理环节,从整体角度改善疾病。本研究从药效学探讨了中药与西药的作用差异,为深入探讨中、西药作用差异做了前期工作。以后将高血糖、高血压、高血脂3种疾病作为一个统一的研究整体,选择基因芯片技术,希望筛选出这3种疾病都存在异常表达的基因,并将这些异常基因作为研究对象,从分子基因水平研究中药与西药的作用差异。
[1]薛燕,雷跻九.中药复方霰弹理论—论中药复方现代研究方法[M].北京:中国环境科学出版社,1996:4.
[2]吴国亭,徐倍.磺脲类药物对2型糖尿病大鼠心肌组织磺脲类药物手体表达的影响[J].上海医学杂志,2006,29(5):217-221.
[3]金锋,李雷,关瑜,等.磺脲类药物在治疗2型糖尿病过程中的安全性 [J].中国药物警戒,2010,7(5): 298-300.
[4]杨新波,黄正明,曹文斌,等.泽泻提取物对链脲佐菌素高血糖小鼠的治疗和保护作用[J].解放军药学学报,2002,6(6):336-350.
[5]梁静,白素芬.单味中药治疗糖尿病及其并发症的研究进展[J].中医与中西医结合,2010,13(5):778-780.
[6]邓晓迎.中药有效成分治疗糖尿病的研究进展[J].现代医药卫生,2010,26(16):2485-2486.
[7]肖飞艳,冯育林,杨世林,等.泽泻化学成分的研究进展[J].中药新药与临床药理,2009,20(5):491-495.
[8]郭钦惠,施发明,喻录容.中药泽泻研究近况[J].现代医药卫生,2010,26(9):1375-1376.
[9]张桥,吴启南.中药泽泻现代研究展望[J].基层中药杂志,2002,16(5):52.
[10]朱玉岚,彭国平.泽泻的萜类化学成分研究进展[J].天然产物研究与开发,2006,18(2):348.
[11]杨新波,黄正明,陈红艳,等.泽泻不同溶剂提取物对糖尿病小鼠血糖及血液生化指标的影响[J].解放军药学学报,2006,22(6):419-421.
[12]杨新波,黄正明.泽泻醇提取物对高血糖小鼠血液生化指标及胰岛素的影响[J].中国临床康复,2004,8(6): 1196-1197.
[13]杨新波,黄正明,曹文斌,等.泽泻提取物对正常及四氧嘧啶小鼠糖尿病模型的影响[J].中国实验方剂学杂志,2002,6(3):24-26.
Alisma versus Gliclazide in the Treatment of Primary Diabetes in Goto-Kakizaki Rats
DING Chen-yi,TAN Qing-ying,SHI Ning-chuan
Zhejiang University School of Public Health,Hangzhou 310031,China
Objective To compare the roles of alisma and gliclazide in the treatment of diabetes in Goto-Kakizaki(GK)rats.Methods GK rats were randomly divided into alisma group,gliclazide group,and blank group,and Wistar rats were used as the normal group.After two weeks of treatment,body weight,foodintake,fasting glucose,impaired glucose tolerance,and other indicators were measured.Results The body weight increased after the treatment in the normal group,blank group,and gliclazide group[(241.3±7.0)g vs.(263.5±11.1)g,(242.8±7.1)g vs.(267.9±16.8)g,(243.9±12.2)g vs.(277.9±9.8)g,P<0.05]but decreased in alisma group[(244.6±9.2)g vs.(227.9±13.7)g,P<0.05].The food intake showed no significant change before and after administration among different groups(P>0.05).Fasting glucose was significantly lower in normal group than in control group,alisma group,and gliclazide group[(4.8± 0.2)mmol/L vs.(8.2±1.4)mmol/L,(8.1±0.6)mmol/L,(8.1±0.9)mmol/L,P<0.05]one week after drug administration;it was not significantly different among blank group,alisma group,and gliclazide group before drug administration(P>0.05);however,it significantly decreased in alisma group and gliclazide group two weeks after administration[(6.9±0.7)mmol/L vs.(8.1±0.6)mmol/L; (5.8± 0.5)mmol/L vs.(8.1±0.9)mmol/L,P<0.05];compared with the blank group,the fasting glucose was significantly lower in the alisma group and gliclazide group,and it was also significantly different between these two groups[(6.9±0.7)mmol/L vs.(8.8±0.6)mmol/L,(5.8±0.5)mmol/L vs.(8.8±0.6)mmol/L,(6.9±0.7)mmol/L vs.(5.8±0.5)mmol/L,P<0.05].Compared with the normal group,glucose tolerance was abnormal in blank group,alisma group,and gliclazide group;after two weeks of treatment,glucose tolerance was significantly improved in alisma group(P<0.05);compared with the pretreatment level and that in the blank group,the glucose tolerance in gliclazide group showed no significant difference(P>0.05).Conclusions Both alisma and gliclazide monotherapy is effective in lowering fasting blood glucose.As a single-target drug,gliclazide has stronger effecacy in lowering fasting glucose.However,alisma,as a mixture,can also control weight and improve glucose intolerance.
alisma;gliclazide;Goto-Kakizaki rats
TAN Qing-ying Tel:0571-85273917,E-mail:tanqingying@126.com
R587.1
A
1000-503X(2015)04-0451-05
10.3881/j.issn.1000-503X.2015.04.015
2014-06-03)
谭擎英 电话:0571-85273917,电子邮件:tanqingying@126.com
