结直肠癌肝转移外科治疗策略
2015-12-21徐达邢宝才
徐达 邢宝才
·专家论坛·
结直肠癌肝转移外科治疗策略
徐达 邢宝才
邢宝才,教授,主任医师,博士研究生导师。现任北京大学肿瘤医院外科教研室主任,北京大学肿瘤医院肝胆胰外一科主任。从事肿瘤外科临床近30年,在肝胆胰腺外科领域积累了丰富的临床与实践经验。完成了1 000余例肝切除手术,能够完成包括全尾状叶在内的各个肝段肿瘤的切除,近5年无围手术期死亡与手术后肝功能衰竭的发生。在结直肠癌肝转移的治疗上经验丰富,积极倡导综合治疗的理念,开展结直肠癌肝转移的新辅助化疗与转化性治疗,在国内率先开展了结直肠癌肝转移的“liver first”手术、PVE联合二期切除的手术和复发后再切除的手术。兼任中国抗癌协会肝癌专业委员会常委、中华外科学会肝脏外科学组委员、中华肿瘤学会肝癌学组委员、中国抗癌协会大肠癌肝转移学组委员、中国抗癌协会胆道肿瘤委员会常委、中国抗癌协会胰腺癌专业委员会委员、卫生部肿瘤规范化治疗专家委员会委员、北京抗癌协会理事、北京抗癌协会肝胆胰肿瘤委员会主任委员、北京肿瘤学会委员、北京大学肝癌中心副主任、北方肝癌专家委员会副主任,担任多种杂志的编委和审稿专家。承担国家重大科学研究计划中国人类蛋白质草图项目的子课题,国家自然科学基金和北京市自然科学基金等多项科研课题。培养博士与硕士研究生10余名,发表文章50余篇。

目前手术切除是结直肠癌肝转移(CRLM)唯一具有治愈可能的治疗方式。近年来随着全身化疗及靶向药物的发展、肝动脉灌注化疗的应用,对于CRLM治疗的有效率明显升高,通过手术获益的患者逐渐增多;而如射频消融、二步切除等外科技术的进步,也为更多CRLM患者提供了治愈的机会。多学科诊疗模式(MDT)也为更多CRLM患者的个体化诊治创造了机会,使未来CRLM的治疗向更加精准的方向发展。
结直肠癌肝转移 外科手术 治疗
结直肠癌是我国常见的消化系统恶性肿瘤,发病率逐年增加,位居所有恶性肿瘤中第3位[1]。肝脏是结直肠癌转移最主要的靶器官,超过50%的结直肠癌患者会在其病程中出现肝脏转移,其中20%~25%是同时性的,2/3的结直肠癌患者因为肝脏转移而死亡[2]。目前肝切除是治疗结直肠癌肝转移(colorectal liver metastasis,CRLM)安全有效且唯一有治愈可能的方法,5年生存率大于50%,且有超过20%的患者存活超过10年;而单纯全身化疗中位生存期仅20个月左右[3]。因此,肝转移治疗的有效性直接决定结直肠癌患者生存。近15年来,随着全身化疗和靶向药物的发展,肝切除技术进步,肿瘤局部治疗(regional he⁃patic therapies,RHT)方法的应用,以及多学科综合团队(multidisciplinary team,MDT)模式的完善,越来越多的患者通过综合治疗获益。本文主要从以下几个方面对CRLM的外科治疗策略进行了探讨。
1 可切除肝转移的治疗
1.1 可切除的定义
既往可切除肝转移对于肿瘤大小数目分布、手术切缘、转移时间、甚至CEA水平都有严格的限定,在这种条件下只有不到10%的患者存在手术切除的机会。由于围手术期综合治疗的进步,目前对于CRLM可切除的定义,已经由转变为满足下面三个条件即可认为是可切除:1)完全切除肝转移灶;2)完全切除所有的肝外转移;3)残余肝体积大于30%,且残余的肝脏有很好的入肝与出肝血流和胆汁引流[4]。即便是这样,也只有大约20%的CRLM患者有手术切除的机会,并且依赖于外科医生的经验以及肝切除技术的差异。因此在目前的条件下,肝转移可切除的范畴能否扩大,使更多患者获益,是讨论的热点。2014年Mise等[5]的一项回顾性研究发现肝转移灶切除、肺转移未切除组预后明显优于肝肺转移均没有切除组。研究表明结直肠癌同时伴有肝转移及小的肺转移灶时,肝转移是影响患者生存的主要因素,因此单纯进行肝转移灶切除可行的[6],这对既往观点造成了极大的冲击。
对肝切缘认识的发展也在推动可切除概念的发展。早期认为肝转移切缘大于1 cm局部复发率最低[7]。但在某些情况下一味追求大于1 cm的切缘,须联合大血管切除,导致大范围的肝切除而使残余肝脏体积不足,故使一部分患者进入不可切除的范畴。近期一项多中心回顾性研究发现,切缘在1~4 mm、5~9 mm、以及大于1 cm 3组CRLM患者,无进展生存(diseasefree survival,DFS)和总生存(overall survival,OS)无显著性差异,认为只要保证切缘阴性即可(切缘≥1mm)[8]。Johns Hopkins医院的报道表明[9],对于R0、R1、R1→R0(术中初始切缘R1,然后补充切缘后为R0),3组不论是局部复发率还是远期生存情况,均无显著性差异(P=0.93)。Ayez等[10]亦发现在如今全身化疗的时代,R0和R1切除的差异越来越小。综上,可切除肝转移的范畴正在逐渐扩大,大量的中心进行了这方面的实践,但仍然需要更大规模的临床研究来进行证实。
1.2 新辅助化疗
术前新辅助治疗的优势在于消除微小转移灶,帮助判断肿瘤对治疗药物的敏感性并为术后药物治疗选择提供依据,但目前是否应该应用尚无定论。EPOC研究首先报道了对于可切除CRLM给予新辅助化疗(FOLFOX方案)可提高无疾病进展生存(pro⁃gression free survival,PFS),但对总生存(overall sur⁃vival,OS)虽有改善但无统计学意义;而增加了靶向药物的New EPOC研究显示西妥昔单抗联合化疗的新辅助治疗同样未使可切除肝转移的患者获益。目前并无前瞻性的研究结果支持对可切除的CRLM进行新辅助化疗,但新辅助化疗对于这部分患者一定无意义吗?实际上,肝转移切除术后的复发与患者手术前的临床危险因素评分[11](clinical risk score,CRS)有着密切的关系。一般来讲,CRS<3分为术后复发的低危险组,CRS≥3分的是高危险组。在EPOC研究中新辅助组及单纯手术组的中位生存时间分别达到了61.3个月和54.3个月,远远高于既往研究的生存结果,对EPOC研究入组患者进行分析后发现其中80%属于低危险复发组(CRS<3)。所以,认为新辅助化疗只是不能使低危复发组患者获益,而对于高危复发病患者的生存获益目前尚缺乏定论。最近的研究表明[12],对于切除难度大或者复发风险高可切除CRLM患者应该进行新辅助化疗。而来自荷兰的一项回顾性研究亦证实,对于高危复发人群进行新辅助化疗,患者有生存获益,并且已经有针对高危复发人群(CRS≥3)的患者实施新辅助治疗的Ⅲ期临床研究[13]。因此,对于可切除的患者行新辅助化疗需因人而异,应该在治疗前经过MDT查房分析后再做出决策(图1)。
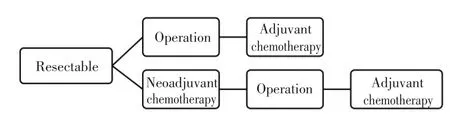
图1 可切除CRLM治疗流程Figure 1 Treatment process for resectable colorectal carcinoma liver me⁃tastasis
2 初始不可切除肝转移的治疗
2.1 转化治疗
对于初始不可切除的CRLM,非手术的治疗中位生存只有不到24个月,如果可以转化为可切除并进行手术,患者5年生存率可以达到33%[14]。因此如何能够获取更高的反应率,使更多患者获得手术机会,是提高初始不可切除CRLM患者治疗效果的关键。而在转化治疗方案选择上需要考虑以下四个因素:1)方案的有效性应该足够强;2)达到可切除的速度应足够快;3)化疗方案安全性应足够高,不良反应可耐受;4)方案能够带给患者的生存获益最大。早期在5-Fu时代,只有不到10%的初始不可切除患者可以通过化疗转化为可切除[15]。后期随着化疗药物(奥沙利铂和伊立替康)及靶向药物(西妥昔单抗和贝伐单抗)的临床应用,通过使用mFOLFOX6(奥沙利铂+氟尿嘧啶+亚叶酸钙)或FOLFIRI(伊立替康+氟尿嘧啶+亚叶酸钙)联合西妥昔单抗/贝伐单抗,可以将反应率提高到60%~70%[16-17]。近来FOLFOXIRI方案(奥沙利铂+伊立替康+氟尿嘧啶+亚叶酸钙)联合靶向药物进行转化治疗成为新的研究热点,通过强有力的化疗可以获得更高的反应率及转化率。2014年发表在新英格兰医学杂志(NEJM)的一项Ⅲ期的RCT临床研究证实,对比FOLFIRI联合贝伐,FOLFOXIRI联合贝伐组的ORR显著提高,PFS、OS显著延长[18]。另一项关于三药转化性治疗的研究于2015年将FOLFOXIRI联合贝伐与mFOLFOX6联合贝伐治疗不可切除的CRLM进行了对比[19],研究结果发现FOLFOXIRI联合贝伐组的ORR为81%,而mFOLFOX6联合贝伐组的ORR仅为62%。基于上述研究可以看出,三药(FOLFOXIRI)联合贝伐单抗与两药(FOLFOX/FOLFIRI)联合贝伐单抗相比,有效率、转化率明显提高。尽管三药组白细胞减少、腹泻、末梢神经炎等不良反应有所增加,但Ⅲ级以上不良事件发生率并无差异。因此,在身体状况允许的条件下,对于一些潜在可切除的患者,可以选择有效率更高的三药方案,并每4周期对肝转移进行评价。2012年结直肠癌肝转移外科治疗共识中指出,术前化疗后应根据肿瘤的不同反应情况分类处理:1)肿瘤部分缓解(PR)且可切除:及时手术;2)肿瘤部分缓解(PR)但仍然不可切除:继续原方案化疗;3)肿瘤维持稳定(SD):继续原方案化疗,4个月后如仍然维持SD,应考虑二线方案;4)肿瘤进展(PD):可考虑二线方案。
2.2 肝动脉灌注化疗
由于较高的肝内药物浓度以及相比于全身化疗更高的反应率[20],肝动脉灌注化疗(hepatic artery in⁃fusion,HAI)逐渐成为治疗初始不可切除CRLM的一项有效治疗手段。早期的Ⅰ期、Ⅱ期临床研究显示,HAI与全身化疗的联合应用治疗CRLM的有效率大约为52%~75%;转化率可达到47%[21]。近期来自斯隆凯瑟琳癌症纪念医院的一项Ⅱ期临床研究显示,入组患者中的65%属于二线或三线治疗,通过肝动脉灌注5-Fu及全身化疗联合或不联合贝伐单抗,总的反应率达到76%,约47%的初始不可切除的患者转化为可切除,中位生存期达到了38个月[22]。因此HAI应该作为不可切除CRLM的重要选择,尤其是对于肝转移负荷大且未无肝外转移,或者一线转化治疗失败的患者。未来仍需要大规模的RCT研究,来为HAI提供更加有力的证据。
2.3 肝切除联合射频消融治疗
射频消融技术已经在越来越多肝胆外科中心熟练开展。与手术切除相比,肝切除联合射频消融治疗(radiofrequency ablation,RFA)的优点有:微创、安全性高、患者痛苦小;但缺点亦显而易见,即没有病理结果证明肿瘤消除的完全性,而这会直接影响肿瘤的局部复发率。既往结果显示,RFA治疗CRLM的5年生存率为15%~48%,局部复发率已下降到5.2~8.8%[23-24]。2015年ASCO公布了CLOCC研究的长期随访结果,RFA联合手术与单纯全身化疗的中位OS分别为45.6、40.5个月(P=0.01);中位PFS分别为16.8、9.9个月(P=0.005);证实了RFA联合手术较单纯姑息化疗能够提高患者的生存[25],尽管如此,学者们对于其局部复发率仍存在争议。Tanis等[26]将CLOCC研究中进行RFA的患者与EPOC研究中进行手术的患者进行了比较,局部复发率分别为7.4%、14.5%;中位DFS分别为356天、412.5天,具有显著性差异。另外一项荟萃分析总结,尽管多项研究存在一定的偏倚,但在局部复发率方面手术切除显著优于RFA[27]。也就是说,RFA治疗在CRLM中应有一定的地位,但不应盲目选择,也无法取代手术的作用。对于不可单纯切除的患者,可以考虑通过切除联合射频达到根治效果。
2.4 分期肝切除方法
分期肝切除手术的出现和发展极大地推进了CRLM外科理念的进步。PVE/PVL的方法使许多没有手术机会的患者获得了根治的机会,5年和10年的总生存分别可以达到32.1%和24.1%,中位生存达43个月[28]。最近Schnitzbauer等人报道了一项新的二次肝切除的技术,即联合肝脏离断及门脉结扎的分次肝切除术(associating liver partition and portal vein ligation for staged hepatectomy,ALPPS),该技术的优点有几个:1)降低术后肝衰发生率;2)提供了与其他技术相比最大程度上的肝脏增生;3)可以最大程度上缩短二次肝切除间隔,降低了肿瘤进展的机会。国际上许多中心对这种方法进行了实践和研究,其中中位二次手术间隔为9~14天,左外叶体积增加74~87.2%,患者1、2年的生存率为73%、59%。但是,术后并发症发生率为53%~68%,死亡率为0~28%[29-30]。这种高并发症率及死亡率,引发了学者们对此技术临床安全性的思考。此外,一个来自国际ALPPS协作组的报告,对于CRLM进行ALPPS手术的患者,近80%患者首先接受了术前的化疗,如果经过术前的化疗仍然无进行常规切除的机会,才考虑行ALPPS。因此,对ALPPS的方法应该理性看待,除了是一种肿瘤切除的手段,还应充分考虑结直肠癌的特点及生物学行为,合理科学地应用这一技术。
综上所述,对于初始不可切除的肝转移,足够强、足够快、足够安全的转化治疗是首选,可以使大部分患者肿瘤降期获得R0切除机会。而对那些经过转化还是无法切除的患者,可以选择针对肝脏局部治疗效果更强的HAI继续转化,或者评估是否可以通过手术切除联合RFA以达到R0的效果。ALPPS为一些不可切除肝转移患者的长期生存提供了可能,但由于这一术式的高风险、高并发症以及长期生存效果的不确定性,可以作为一种补救方法慎重进行(见图2)。
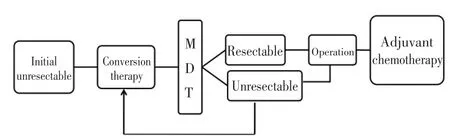
图2 初始不可切除CRLM治疗流程Table 2 Treatment process for initially non-resectable colorectal carci⁃noma liver metastasis
3 CRLM中的多学科查房
CRLM中的MDT查房模式在恶性肿瘤治疗过程中对临床决策的重要作用已经在世界范围内得到共识。而由于CRLM发病情况的复杂性,MDT的作用更加凸显。本科作为牵头科室组建了国内较早的CRLM团队,近年来取得了良好的效果。标准的MDT团队由肝胆外科、结直肠外科、肿瘤内科、影像科、放疗科、病理科、内镜科的医生共同参与,对于肝脏可切除状态的评估需要2名以上经验丰富的肝脏外科医师共同决定。研究表明,MDT查房可以为CRLM患者提供最佳的个体化治疗,进行MDT的中心对CRLM可切除性的评价更加准确,其治疗的远期预后也显著优于未进行MDT的中心[31]。
4 总结
总之,手术切除是CRLM的首选治疗,R0切除是CRLM治疗的目标。对于可切除CRLM是否进行新辅助治疗,需要进一步的研究以筛选出从中获益的人群;不可切除的CRLM应首选最高效的转化方案(三药联合/靶向),进行全身的系统性治疗以获取切除可能。RFA、HAI、PVE/ALPPS这些方法,可以为更多初始不可切除的CRLM患者创造R0的机会。而MDT是提高CRLM切除率,延长生存的关键因素,高水平的MDT团队能使患者生存获益最大化。
[1] He J,Zhao P,Chen WQ.Chinese cancer registries[M].Beijing: Military Medical Science Press,2012:1-2.[赫 捷,赵 平,陈万青.主编.中国肿瘤登记年报[M].北京:军事医学科学出版社,2012: 1-2.]
[2] Kopetz S,Chang GJ,Overman MJ,et al.Improved survival in metastatic colorectal cancer is associated with adoption of hepatic resection and improved chemotherapy[J].J Clin Oncol,2009,27 (22):3677-3683.
[3] Adam R,Hoti E,BredtL.Evolution of neoadjuvant therapy for extended hepatic metastases--have we reached our(non-resect⁃able)limit[J]?J Surg Oncol,2010,102(8):922-931.
[4] Adam R,Hoti E,FolprechtG&Benson,A.B.Accomplishments in 2008 in the management of curable metastatic colorectal cancer [J].Gastrointest Cancer Res,2009,3(Suppl 2):S15-S22.
[5] Mise Y,Kopetz S,Mehran R,et al.Is complete liver resection without resection of synchronous lung metastases justified[J]? Ann Surg Oncol,2015,22(5):1585-1592.
[6] Nordholm-Carstensen A,Krarup P,Jorgensen L,et al.Occur⁃rence and survival of synchronous pulmonary metastases in colorectal cancer:a nationwide cohort study[J].Eur J Cancer, 2014,50(2):447-456.
[7] Hughes K,Simon R,Songhorabodi S,et al.Resection of the liver for colorectal carcinoma metastases:a multi-institutional study of patterns of recurrence[J].Surgery,1986,100(2):278-284.
[8] Pawlik T,Scoggins C,Zorzi D,et al.Effect of surgical margin sta⁃tus on survival and site of recurrence after hepatic resection for colorectal metastases[J].Ann Surg,2005,241(5):715-722..
[9] Margonis G,SpolveratoG,KimY,et al.Intraoperative Surgical Margin Re-resection for Colorectal Liver Metastasis:Is It Worth the Effort[J]?J Gastrointest Surg,2015,19(4):699-707.
[10]Ayez N,Lalmahomed Z,Eggermont A,et al.Outcome of micro⁃scopic incomplete resection(R1)of colorectal liver metastases in the era of neoadjuvant chemotherapy[J].Ann Surg Oncol,2012, 19(5):1618-1627.
[11]Fong Y,Fortner J,Sun R,et al.Clinical score for predicting recur⁃rence after hepatic resection for metastatic colorectal cancer:analysis of 1001 consecutive cases[J].Ann Surg,1999,230(3):309-318.
[12]Jones R,Malik H,Fenwick S,et al.Perioperative chemotherapy for resectable colorectal liver metastases:where now[J]?Eur J Surg Oncol,2013,39(8):807-811.
[13]Ayez N,van der Stok E,de Wilt H,et al.Neo-adjuvant chemo⁃therapy followed by surgery versus surgery alone in high-risk pa⁃tients with resectable colorectal liver metastases:the CHARISMArandomized multicenter clinical trial[J].BMC cancer,2015,15:180.
[14]Adam R,Delvart V,Pascal G,et al.Rescue surgery for unresect⁃able colorectal liver metastases downstaged by chemotherapy:a model to predict long-term survival[J].Ann Surg,2004,240(4): 644-657.
[15]Bismuth H,Adam R,Levi F,et al.Resection of nonresectable liv⁃er metastases from colorectal cancer after neoadjuvant chemother⁃apy[J].Ann Surg,1996,224(4):509-520.
[16]Folprecht G,Gruenberger T,Bechstein W,et al.Tumour response and secondary resectability of colorectal liver metastases following neoadjuvant chemotherapy with cetuximab:the CELIM randomised phase 2 trial[J].Lancet Oncol,2010,11(1):38-47.
[17]Maughan T,Adams R,Smith C,et al.Addition of cetuximab to oxaliplatin-based first-line combination chemotherapy for treat⁃ment of advanced colorectal cancer:results of the randomised phase 3 MRC COIN trial[J].Lancet,2011,377(9783):2103-2114.
[18]Loupakis F,Cremolini C,Masi G,et al.Initial therapy with FOLFOXIRI and bevacizumab for metastatic colorectal cancer[J]. N Engl J Med,2014,371(17):1609-1618.
[19]Gruenberger T,Bridgewater J,Chau I,et al.Bevacizumab plus mFOLFOX-6 or FOLFOXIRI in patients with initially unresect⁃able liver metastases from colorectal cancer:the OLIVIA multina⁃tional randomised phaseⅡtrial[J].Ann Oncol,2015,26(4):702-708.
[20]Kemeny N,Niedzwiecki D,Hollis D,et al.Hepatic arterial infu⁃sion versus systemic therapy for hepatic metastases from colorec⁃tal cancer:a randomized trial of efficacy,quality of life,and mo⁃lecular markers(CALGB 9481)[J].J Clin Oncol,2006,24(9): 1395-1403.
[21]Kemeny N,Conti J,Cohen A,et al.PhaseⅡstudy of hepatic arte⁃rial floxuridine,leucovorin,and dexamethasone for unresectable liver metastases from colorectal carcinoma[J].J Clin Oncol,1994, 12(11):2288-2295.
[22]D'Angelica M,Correa-Gallego C,Paty P,et al.PhaseⅡtrial of hepatic artery infusional and systemic chemotherapy for patients with unresectable hepatic metastases from colorectal cancer:con⁃version to resection and long-term outcomes[J].Ann Surg,2015, 261(2):353-360.
[23]Gillams A,Lees W.Five-year survival in 309 patients with colorectal liver metastases treated with radiofrequency ablation[J]. Eur Radiol,2009,19(5):1206-1213.
[24]Abitabile P,Hartl U,Lange J,et al.Radiofrequency ablation per⁃ mits an effective treatment for colorectal liver metastasis[J].Eur J Surg Oncol,2007,33(1):67-71.
[25]Ruers T,Punt C,Van Coevorden F,et al.Radiofrequency abla⁃tion combined with systemic treatment versus systemic treatment alone in patients with non-resectable colorectal liver metastases: a randomized EORTC Intergroup phaseⅡ study(EORTC 40004)[J].Ann Oncol,2012,23(10):2619-2626.
[26]Tanis E,Nordlinger B,Mauer M,et al.Local recurrence rates af⁃ter radiofrequency ablation or resection of colorectal liver metasta⁃ses.Analysis of the European Organisation for Research and Treatment of Cancer#40004 and#40983[J].Eur J Cancer,2014, 50(5):912-919.
[27]Weng M,Zhang Y,Zhou D,et al.Radiofrequency ablation ver⁃sus resection for colorectal cancer liver metastases:a meta-analy⁃sis[J].PloS One,2012,7(9):e45493.
[28]Giuliante F,Ardito F,Ferrero A,et al.Tumor progression during preoperative chemotherapy predicts failure to complete 2-stage hepatectomy for colorectal liver metastases:results of an Italian multicenter analysis of 130 patients[J].J Am Coll Surg,2014,219 (2):285-294.
[29]Alvarez F,Ardiles V,Sanchez Claria R,et al.Associating liver partition and portal vein ligation for staged hepatectomy(ALPPS): tips and tricks[J].J Gastrointest Surg,2013,17(4):814-821.
[30]Schnitzbauer A,Lang S,Goessmann H,et al.Right portal vein li⁃gation combined with in situ splitting induces rapid left lateral liver lobe hypertrophy enabling 2-staged extended right hepatic resection in small-for-size settings[J].Ann Surg,2012,255(3):405-414.
[31]Lordan J,Karanjia N,Quiney N,et al.A 10-year study of out⁃come following hepatic resection for colorectal liver metastases-The effect of evaluation in a multidisciplinary team setting[J].Eur J Surg Oncol,2009,35(3):302-306.
(2015-07-15收稿)
(2015-08-05修回)
(编辑:周晓颖)
Surgical treatment of colorectal cancer liver metastasis
Da XU,Baocai XING
Key Laboratory of Carcinogenesis and Translational Research(Ministry of Education),Hepatobiliary Pancreatic Surgery Ward I, Peking University Cancer Hospital&Institute,Beijing 100142,China.
Surgical resection is currently the only cure treatment for colorectal carcinoma liver metastasis(CRLM).The efficiency of surgical resection has improved with the development of systemic chemotherapy and targeted drugs and the application of hepatic arterial infusion chemotherapy in recent years.The number of patients benefiting from surgery has gradually increased.The progression of surgical techniques such as radiofrequency ablation and staged hepatectomy provides chances of cure for patients with CRLM.Multidisciplinary team creates the opportunity of individual diagnosis and treatment for growing number of patients with CRLM,which,in turn,promotes the treatment of CRLM to a more precise future.
colorectal cancer liver metastasis,surgical resection,therapy

10.3969/j.issn.1000-8179.2015-17.773
北京大学肿瘤医院暨北京市肿瘤防治研究所肝胆胰外一科,恶性肿瘤发病机制及转化研究教育部重点实验室(北京市100142)
邢宝才 xingbaocai88@sina.com
徐达 专业方向为肝胆胰肿瘤的外科和基础研究。
E-mail:xuda1989212@126.com
