试剂槽贮存酶免试剂对检测结果的影响
2015-12-20齐文娟甄志军张志红
齐文娟,甄志军,张志红
试剂槽贮存酶免试剂对检测结果的影响
齐文娟,甄志军,张志红
目的:探讨尤瑞纳斯(Uranus)酶免分析仪试剂槽贮存不同时间的酶联免疫(enzyme linked immunosorbent assay,ELISA)试剂对丙型肝炎病毒(hepatitis C virus,HCV)抗体检测结果的影响。方法:将抗-HCV试剂采用Uranus试剂槽贮存,分别于0、7、14、21、28 d对HCV系列样本进行ELISA检测,并对样本吸光度(A)值进行统计学分析。结果:对于HCV抗体阴性样本,贮存7 d内的检测结果较0 d无明显变化(P>0.05),自14 d开始,A值逐渐升高(P<0.05),至21~28 d均显著高于0 d,差异有统计学意义(P<0.01);而对于HCV抗体弱阳性及阳性样本,自14 d开始,检测A值均显著低于0 d(P<0.01)。结论:抗-HCV试剂以试剂槽贮存至14 d对ELISA检测结果有明显影响,甚至导致弱阳性样本的漏检。应每7 d清洗试剂槽1次,并及时更换试剂。
贮存试剂;酶联免疫吸附测定;丙型肝炎病毒
0 引言
丙型肝炎病毒(hepatitis C virus,HCV)是国家规定的献血者筛查项目之一,间接酶联免疫吸附测定(enzyme linked immunosorbent assay,ELISA)是HCV抗体筛查的常用方法[1],尤瑞纳斯(Uranus)全自动酶免分析系统(以下简称“Uranus”)以高效率、循环进样、直观、易操作等优点用于ELISA检测,很大程度上提高了血液检测的质量[2],已普遍用于献血者筛查项目的ELISA检测。我站于2011年引进U-ranus AE280,厂家建议试验后将剩余酶免试剂以试剂槽4℃贮存,但对于有效贮存期限未给出明确的指导意见。以往研究报道[3-4],酶免试剂贮存不当会使试剂检测灵敏度下降,最终导致结果失控。为了探讨试剂槽贮存酶免试剂对检测结果的影响,我们将血站用于献血者HCV抗体检测的酶免试剂以Uranus试剂槽贮存,对不同确定结果的系列样本进行ELISA检测,现将结果报道如下。
1 资料与方法
1.1 实验样本
收集2012年11月至2013年11月无偿献血者血液样本,经2家HCV试剂盒检测,阴性样本20例,弱阳性样本(样本值/临界值(S/CO值)1~5)20例,阳性样本(S/CO值≥10)10例。其中,男39例,女11例。所有样本均无溶血、乳糜、黄疸,3 200 r/min离心15 min,分离血浆后,小心吸取上层血浆于新的Eppendorf管内,每管200 μL,每例样本共分装5管,置-20℃冰箱冷冻保存备用。
1.2 试剂
抗-HCV ELISA诊断试剂盒(国产某公司,批号:C20130508),经中国药品生物制品检定所批检合格;抗-HCV室内质控品,北京康彻思坦有限公司,批号为201303001,浓度为1 NCU/mL。所有试剂使用前经过确认,均在有效期内。
1.3 主要仪器
Uranus AE280全自动酶免分析系统(深圳爱康电子有限公司),台式普通高速离心机(德国TECAN公司)。
1.4 方法
1.4.1 试剂准备
将装有HCV抗体的ELISA试剂盒由4℃冰箱取出,平衡至室温(13~25℃),将HCV抗体试剂盒内样本稀释液、酶结合物、底物A、底物B、终止液分别倒入相应的Uranus试剂槽中,并放在相应的位置。
1.4.2 样本准备
取50例冻存的系列HCV样本,包括20例HCV阴性样本、20例HCV弱阳性样本、10例HCV阳性样本,将样本血浆于室温复融,并平衡至室温,实验前混匀。
1.4.3 实验
实验步骤严格按试剂说明书,设定空白对照、阴性对照、阳性对照、弱阳性室内质控孔,将系列HCV样本进行ELISA双孔检测,作为对照组(0 d)。在Uranus全自动酶免分析系统中进行稀释、加样、温育、洗板、读数,剩余试剂用Uranus试剂槽贮存置于4℃冰箱中,期间模拟日常实验时间将试剂槽取出于室温放置,并依次于7、14、21、28 d的同一时间分别取50例系列HCV样本进行ELISA双孔检测,实验均由同一操作人完成。
1.4.4 结果判断
取双孔的平均吸光度(A)值,S/CO值≥1.0判为阳性,<1.0判为阴性。
1.5 统计学处理
采用SPSS 16.0统计软件,计量资料均以“均数±标准差(±s)”表示,并进行正态分布及方差齐性检验,2组间的比较采用配对t检验,P<0.05为差异有统计学意义。
2 结果
不同贮存时间的试剂槽贮存试剂对HCV抗体检测A值的影响(±s)见表1。
表1 不同贮存时间的试剂槽贮存试剂对HCV抗体检测A值的影响(±s)
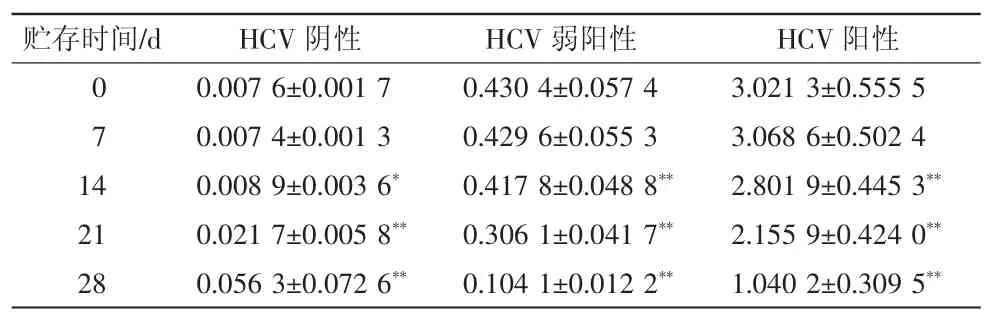
表1 不同贮存时间的试剂槽贮存试剂对HCV抗体检测A值的影响(±s)
注:*与0 d的比较,P<0.05,有显著差异;**与0 d的比较,P<0.01,有极显著差异
贮存时间/d HCV阴性 HCV弱阳性 HCV阳性00 0.007 6±0.001 7 0.430 4±0.057 4 3.021 3±0.555 5 07 0.007 4±0.001 3 0.429 6±0.055 3 3.068 6±0.502 4 14 0.008 9±0.003 6** 0.417 8±0.048 8** 2.801 9±0.445 3**21 0.021 7±0.005 8** 0.306 1±0.041 7** 2.155 9±0.424 0**28 0.056 3±0.072 6** 0.104 1±0.012 2** 1.040 2±0.309 5**
由表1可见,虽然所有HCV系列样本以7 d内的贮存试剂检测,结果较0 d无明显变化(P>0.05),但自14 d后试剂槽贮存试剂对HCV抗体样本的检测A值的影响显著:20例HCV抗体阴性样本,自14d开始,A值逐渐升高(P<0.05),及至21 d均显著高于0 d,差异有统计学意义(P<0.01);贮存试剂对弱阳性及阳性血液样本检测结果的影响更显著,20例HCV抗体弱阳性样本及10例阳性样本的检测结果显示:自14 d开始,检测样本的A值随试剂贮存时间的延长逐渐降低,均显著低于0 d,差异有统计学意义(P<0.01)。
3 讨论
丙型肝炎是世界各国及地区共同面临的严重传染病,特别是经济不发达地区。HCV是造成输血后肝炎的主要病因,经血传播是HCV传播的主要途径。全球已有1.17亿人受到感染,我国有感染者大约4 000万,有相当一部分慢性丙肝感染者会发展成肝硬化、肝癌,给家庭和社会造成沉重的经济负担[5-7]。因此,严把献血者丙肝病毒感染检测质量关,是切断输血传播丙型肝炎、保证临床用血安全的关键。
目前,ELISA法测抗-HCV是我国大多采供血机构用于献血员筛查丙肝病毒传染指标的最主要方法[8]。根据《血站质量规范》和《血站试验室质量管理规范》的规定,为了保证检测结果的可靠性,使酶免设备正常、高效地运行,要求对设备建立和实施维护、校准以及持续监控等管理制度,针对设备的性能,制定完善而有层次的维护保养方案,对设备定期实施不同层面的维护保养[9]。本研究旨在通过探究酶免试剂的试剂槽贮存时间对于献血者HCV抗体ELISA检测结果的影响,明确实验室对Uranus全自动酶免分析仪试剂槽的维护要求,为实验室优化设备维护程序提供数据支持。
研究显示,国产抗-HCV试剂可以用Uranus试剂槽贮存7 d而不影响阴性样本测定,自贮存14 d开始,血液样本的A值逐渐增高,直至28 d检测结果几乎接近“灰区”值(0.071~0.140),这表明试剂槽贮存试剂时间越长,其HCV检测的假阳性率将越高,一定程度上使假阳性样本增加,血液报废率提高,导致宝贵的血液资源浪费。阴性样本产生非特异性显色的原因可能与试剂槽贮存的样本稀释液有关。样本稀释液一般由磷酸盐缓冲液、牛血清白蛋白以及试剂稳定剂等组成,其可以保证血浆样本最合适的ELISA反应环境及微量血浆样本与聚乙烯包被孔接触面积大小的一致性。良好的样品稀释液可有效降低非特异性反应,提高ELISA检测方法的敏感性和特异性,保证ELISA检测结果的准确[10]。在HCV试剂说明书中,写明样本稀释液不宜长时间暴露于空气中,每次使用样本稀释液后应尽快盖好瓶盖,否则会影响实验结果。试剂槽贮存的样品稀释液长时间暴露于一般环境中,随着贮存时间的延长,试剂稳定剂中的氨基酸、糖类等有机物易受到空气的氧化,可能会导致稀释液pH的改变以及试剂中蛋白成分的变性,在ELISA检测中不能发挥应有的作用,产生非特异性反应。另外,底物B对光敏感,底物溶液用试剂槽贮存一定时间后易变蓝,使ELISA板底增高,影响测定结果。
特别值得关注的是,当以试剂槽贮存试剂检测HCV抗体弱阳性和阳性样本时,自贮存的14 d开始,样本的A值随着贮存时间的延长逐渐降低,特别是28 d后的弱阳性样本A值低于临界值(0.140),这样对处于临界值水平的HCV样本,增加结果判断难度,稍有不慎,使样本的检测结果发生质的改变,导致弱阳性样本的漏检。这也表明试剂槽贮存的酶免试剂对弱阳性、阳性样本的检测结果仍有较大影响。对于此结果,研究者认为可能由以下原因造成:一方面,在血站每个批次的样本检测中,从试剂平衡至室温到实验结束放回4℃冰箱,每次实验试剂槽内的试剂在室温中的暴露时间为4~5 h,而且实验后只在试剂槽上加盖一个自制的塑料盖便放入4℃冰箱贮存。酶结合物经反复使用,使贮存温度不恒定,极易使酶的催化活性和抗体的免疫活性降低。另一方面,底物A易挥发,试剂槽内的贮存试剂长时间暴露于空气中,可引起底物A的浓度变化及底物B的分解。底物A的浓度过低或过高都会抑制酶促反应[11],造成试剂盒的底物敏感度和稳定性降低,一定条件下可引起弱阳性和阳性样本A值降低,从而导致接近临界值样本出现假阴性,以致阳性样本的漏检,由此可能造成HCV通过输血途径传播的严重后果。
综上所述,用Uranus试剂槽贮存7 d内HCV抗体试剂对于ELISA检测结果并无影响。然而酶免试剂在经过试剂槽贮存过程中会受到各种因素(如空气、温度、振荡等)的影响,其试剂质量会发生不同程度的变化,试剂盒内任何一种组分不稳定都会导致酶免检测结果产生误差,特别是酶结合物、底物等。因此,对全自动酶免分析仪的试剂槽应进行周期性、多层次的维护保养[12]。一般进口酶免分析仪的试剂槽配置为消耗性器材,采用1周更换1次的方法对试剂槽进行维护[13-15],而Uranus全自动酶免分析仪的试剂槽为厂家固定配置器材,因此为了确保酶免试剂在献血员血液筛检中的高质量使用,首先建立试剂槽维护和持续监控等管理制度,并将维护保养方案写入实验室质量管理手册。其次,切实实施试剂槽周维护制度,每周对Uranus试剂槽进行1次一般维护,彻底清洗后,浸泡30 min后用纯水冲洗干净,将试剂槽倒扣于吸水纸上,实验前更换新试剂;每次维护时用棉签彻底清洁试剂槽内壁,特别是Uranus试剂槽为棕色壁,试剂变色不易察觉,如观察擦拭后的棉签上有蓝色或其他杂质,说明该试剂槽中的试剂组分已变质或已受污染,应用纯水浸泡过夜后彻底清洗干净,并用紫外线照射消毒;每天使用前应观察槽中的试剂是否变色、浑浊等,如试剂外观发生改变,立即按以上针对试剂槽污染程序的维护操作对其进行处理,实验换用备用的试剂槽。根据实验需要估计试剂用量,尽量减少试剂剩余量;使用后应及时加盖相应的试剂槽盖子并将试剂槽放人4℃冰箱贮存,并监测和记录冰箱温度,防止温度或其他因素对酶免试剂的质量造成影响[16],避免试剂槽贮存试剂带来的系统误差,保证检验结果的准确,确保临床用血安全。本实验为模拟实验,设计还不够完善,采用的血液样本数量及选取的时间点偏少,研究结果有待于进一步验证。
[1]李妙羡,王香玲,吴晓康,等.HCV抗原检测与HCV-RNA和HCV抗体检测的比较研究[J].现代检验医学杂志,2012,27(4):55-57.
[2]李鹏,聂心教.UranusAE200全自动酶免分析仪分析性能的确认[J].中国输血杂志,2011,24(11):982-984.
[3]桑列勇.酶结合物效价下降引起抗—HCV检测失控原因分析[J].临床输血与检验,2003,5(2):126-127.
[4]梁俊杰,肖玮,刘乐霞,等.运输温度对酶免试剂质量影响分析[J].河北医药,2012,41(16):2 526-2 527.
[5]Alter M J.Epidemiology of hepatitis C virus infection[J].World J Gastroenterol,2007,13(17):2 436-2 441.
[6]Lavanchy D.The global burden of hepatitis C[J].Liver Int,2009,29(Suppl 1):74-81.
[7]中华医学会肝病学分会和中华医学会传染病与寄生虫病学分会.丙型肝炎防治指南[J].实用肝脏病杂志,2004,25(5):369-375.
[8]邢培清,刘玉振.实用输血检验[M].郑州:郑州大学出版社,2001:78-83.
[9]张瑶婵,张泳.设备确认存在的问题及分析[J].中国输血杂志,2010,23(11):909-910.
[10]DU Gai-mei,LIU Mao-jun,GAN Yuan,et al.Study on screening of optimal blocking buffer and sample diluent for ELISA[J].Agricultural Science&Technology,2013,14(6):815-819,837.
[11]李红梅,陈佳,徐斐,等.ELISA测定中TMB显色体系的优化及其稳定性研究[J].生物技术通报,2010,26(2):126-130.
[12]高东英.采供血机构体外免疫诊断试剂评价系统的初步探讨[J].中国输血杂志,1999,12(1):56-57.
[13]武峰.Microlab FAME全自动酶免分析系统常见故障及排除方法[J].中国医学装备,2007,9(10):49-50.
[14]戴云,许雷,冯秋霞.全自动酶免分析仪FAME的保养及常见故障排除[J].医疗卫生装备,2012,33(3):140,142.
[15]郑允福,金莲花,赵仁玉,等.Microlab FAME全自动酶免分析仪的日常维护、保养及常见故障分析和处理[J].医学信息,2012,25(8):145-146.
[16]高均翠.抗-HCV ELISA检测试剂质量抽检分析[J].中国输血杂志,2011,24(6):512-514.
(收稿:2014-03-06 修回:2014-06-11)
Influence of reagents stored in tank on ELISA results
QI Wen-juan,ZHEN Zhi-jun,ZHANG Zhi-hong
(Blood Center of Xingtai,Xingtai 054000,Hebei Province,China)
ObjectiveTo discuss the influences of reagents storage time in Uranus tank on ELISA results for HCV detec tion.MethodsAnti-HCV reagents were stored in Uranus tank,and then underwent ELISA detection 0,7,14,21 and 28 d after,and the absorbance(A)values were analyzed statistically.ResultsThe negative reagents to HCV antibody had A values 7 d after with no significant difference with those of 0 d(P>0.05),and increased gradually 14 d after(P<0.05), and significantly higher than those of 0 d(P<0.01).The positive and weakly positive samples had A values significantly lower 14 d after than those of 0 d(P<0.01).Conclusion It′s proved that 14 d reagent storage in Uranus tank may obviously influence the ELISA results and may even result in missed detection of weakly positive samples.The tank has to be cleaned once a week,and the reagents have to be replaced timely.[Chinese Medical Equipment Journal,2015,36(1):87-89]
storage reagent;enzyme-linked immunosorbent assay;hepatitis C virus
R318.6;TH776
A
1003-8868(2015)01-0087-03
10.7687/J.ISSN1003-8868.2015.01.087
邢台市科技支撑项目(2012ZC170)
齐文娟(1976—),女,主管技师,主要从事输血检验方面的研究工作,E-mail:qiwenjuan2002@163.com。
054000河北邢台,邢台市中心血站(齐文娟,甄志军,张志红)
