黑龙江省生乳中β-内酰胺酶的监测与结果分析
2015-12-16杨光邢宇赵平陈丽丁松乔
杨光,邢宇,赵平,陈丽,丁松乔
(黑龙江省质量监督检测研究院,哈尔滨150028)
0 引言
随着人们生活水平的提高,乳制品的安全问题备受关注。由于利益驱动,一些不法商家,向生乳中添加“抗生素分解剂”来掩盖抗生素的存在。经证实,这种分解剂为“β-内酰胺酶”[1]。
β-内酰胺酶是细菌对抗生素产生耐药性的主要原因,因此,过多摄入会对人体产生不良后果[2]。卫生部于2009年3月相继发布了关于印发《全国打击违法添加非食用物质和滥用食品添加剂专项整治近期工作重点及要求》的通知(卫监督发[2009]21号)和关于印发《全国打击违法添加非食用物质和滥用食品添加剂专项整治抽检工作指导原则和方案》的通知(食品整治办[2009]29号),明确指出“添加β-内酰胺酶(等)非食品用物质属违法行为”[3,4]。
1 实验
1.1 样品来源
本研究共采集了400份生乳样品。样品采集地点分别为黑龙江省内的奶站、运输车、生产企业收奶间及奶仓等。根据生乳不易保存的特点,为确保监测准确性,必须在最短的时间内完成样品的检测工作;样品采集后立即放入0~4℃冷藏箱中保存,并于当天送至实验室进行检测。
1.2 方法
检测采用食品整治办[2009]29号指定检验方法4《乳及乳制品中舒巴坦敏感β-内酰胺酶类物质检验方法-杯碟法》进行[5]。
1.2.1 设备和材料
除微生物实验室常规灭菌及培养设备外,其他设备和材料如下:
抑菌圈测量仪;恒温培养箱(36℃±1℃);高压蒸汽灭菌器;无菌培养皿(内径90 mm,底部平整光滑的玻璃皿);无菌牛津杯(外径8.0 mm±0.1 mm,内径6.0 mm±0.1 mm,高度10.0 mm±0.1mm)。
标准比浊管;恒温水浴;无菌吸管:1 mL(0.01 mL刻度值),10 mL(0.1mL刻度值);加样器(5~20 μL,20~200 μL及配套吸头);全自动牛津杯放置器;陶瓦盖。
1.2.2 培养基和试剂
所用试剂均为分析纯,水为GB/T6682中规定的三级水。
实验菌种:藤黄微球菌(Micrococcus luteus)CMCC(B)28001,传代次数不得超过14次。
磷酸盐缓冲溶液(pH=6.0);生理盐水(8.5 g/L);青霉素钾盐(D.R)标准溶液;β-内酰胺酶(Sigema)标准溶液;舒巴坦(D.R)标准溶液;营养琼脂培养基;抗生素检测用培养基Ⅱ。
1.3 操作步骤
1.3.1 菌悬液的制备
将藤黄微球菌接种于营养琼脂斜面上,经(36±1)℃培养18~24 h,用生理盐水洗下菌苔即为菌悬液,测定菌悬液浓度,终浓度为1×1010mL-1,4℃保存,贮存期限2周。
1.3.2 样品的制备
将待检样品充分混匀,取1 mL待检样品于1.5 mL离心管中共4管,分别标为:A、B、C、D,每个样品做三个平行,共12管,同时每次检验应取纯水1 mL加入到1.5 mL离心管中作为对照。
1.3.3 检验用平板的制备
取90 mm灭菌玻璃培养皿,底层加10 mL灭菌的抗生素检测用培养基Ⅱ,凝固后上层加入5 mL含有浓度为1×108mL-1藤黄微球菌的抗生素检测用培养基Ⅱ,凝固后备用。
1.3.4 样品的测定
按照下列顺序分别将青霉素标准溶液、β-内酰胺酶标准溶液、舒巴坦标准溶液加入到样品及纯水中:
A :青霉素5 μL。
B :舒巴坦25 μL、青霉素5 μL。
C :β-内酰胺酶25 μL、青霉素G5 μL。
D :β-内酰胺酶25 μL、舒巴坦25 μL、青霉素5 μL。
混匀后,将上述A~D试样各200 μL加入放置于检验用平板上的4个无菌牛津杯中,(36±1)℃培养培养18~22 h,测量抑菌圈直径。每个样品,取三次平行试验平均值。
1.3.5 结果报告
纯水样品结果应为:(A)、(B)、(D)均应产生抑菌圈;(A)的抑菌圈与(B)的抑菌圈相比,差异在3 mm以内(含3 mm),且重复性良好;(C)的抑菌圈小于(D)的抑菌圈,差异在3 mm以上(含3 mm),且重复性良好。如为此结果,则系统成立,可对样品结果进行如下判定。
(1)如果样品结果中(B)和、(D)均产生抑菌圈,且(C)与(D)抑菌圈差异在3 mm以上(含3 mm)时,可按下述(2)(3)判定结果。
(2)(A)的抑菌圈小于(B)的抑菌圈差异在3 mm以上(含3 mm),且重复性良好,应判定该试样添加有β-内酰胺酶,报告β-内酰胺酶类药物检验结果阳性。
(3)(A)的抑菌圈同(B)的抑菌圈差异小于3 mm,且重复性良好,应判定该试样未添加有β-内酰胺酶,报告β-内酰胺酶类药物检验结果阴性。
(4)如果(A)和(B)均不产生抑菌圈,应将样品稀释后再进行检测。
2 结果与讨论
(1)本研究共监测生乳样品400批次,其中392批次检验结果为β-内酰胺酶阴性,8批次检验结果为β-内酰胺酶阳性,分布在5家企业。样品阳性率2%。8批次阳性样品分别在三次实验中出现,详细数据见表1。
(2)本研究采集的400批次样品,β-内酰胺酶阳性仅为8批次,阳性率为2%(见图1)。其原因主要是各级有关政府部门近年来加大了对使用非法添加物等行为的打击力度,并且企业也增加了对β-内酰胺酶的检测频次。即便如此,仍有8批次的生乳样品β-内酰胺酶检测结果呈阳性。这说明个别奶农仍因利益驱动,向含有抗生素的生乳中而非法加入β-内酰胺酶,以降解抗生素。
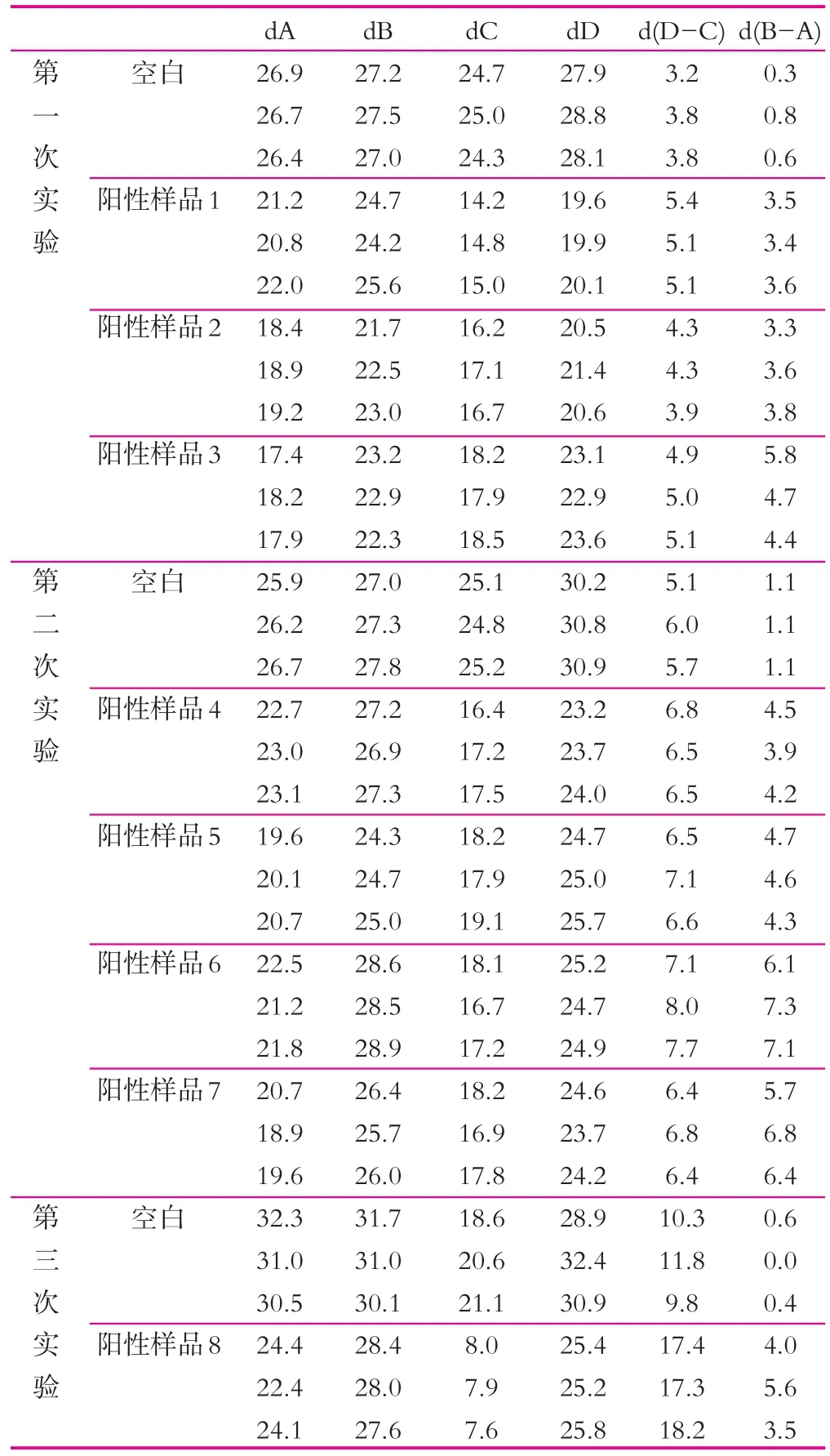
表1 β-内酰胺酶阳性样品实验数据 mm
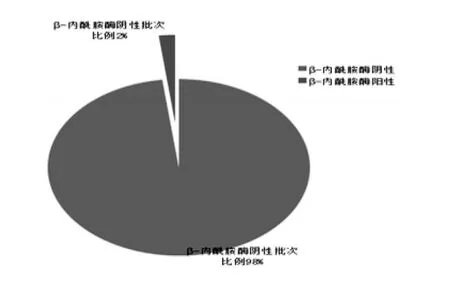
图1 生乳中β-内酰胺酶监测结果
本次乳及乳制品中β-内酰胺酶的样品采集涵盖了生产与流通两大领域。根据不同产品的特点,采样地点分别在奶站、运输车、生产企业收奶间及奶仓,表2体现了不同采样环节的样品情况。
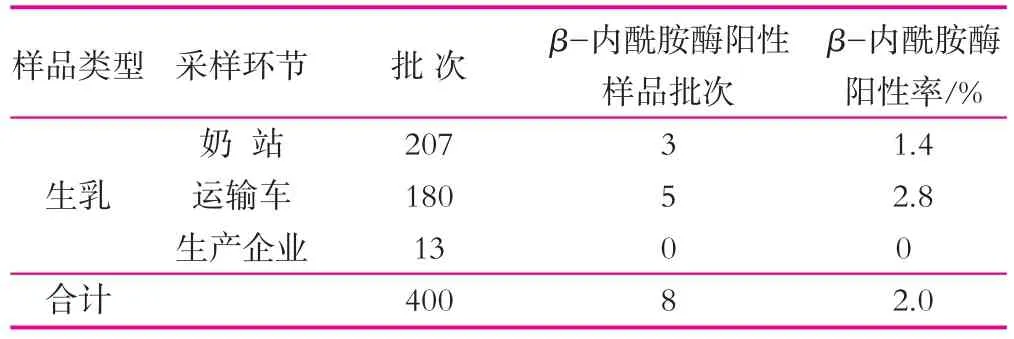
表2 不同采样环节乳及乳制品β-内酰胺酶检测结果统计结果
监测结果表明:在奶站采集的207批次产品,3批次呈阳性,阳性率1.4%;运输车抽检180批次,5批次呈阳性,阳性率2.8%。说明最易出现问题的两个环节为奶站与运输车,不排除在这两个环节非法添加β-内酰胺酶的可能性。
2.3 原因分析
近十几年来,我国奶牛养殖业快速发展,养殖模式向着集约化、现代化大型牧场发展。特别是2014年起国家要求婴幼儿配方乳粉生产企业须建自有牧场更加速了这一进程。但根据我国国情,目前仍以分散养殖为主。由于分散养殖饲养条件差、技术落后等因素致使奶牛乳房炎等疾病发病率仍居高不下,导致奶农盲目大量使用抗生素。特别是β-内酰胺类抗生素由于价格低、效果好、容易获得等原因而普遍使用。这对于泌乳期的奶牛而言,所生产的牛奶中就会含有一定量的抗生素残留。个别奶农为减小损失仍将含有抗生素残留的牛奶送交企业,就需在奶中加入β-内酰胺酶以降解抗生素。自2009年3月原卫生部将其列为非法添加物以来,随着相关部门监管力度加大与企业在收购时的检测,非法添加β-内酰胺酶现象逐年下降,由原来的普遍添加到目前极个别奶农的非法添加。即便如此,仍时有发生,不能从根本上加以拒绝。根据对不同环节β-内酰胺酶检测结果看,不合格样品全部来自于奶站与运输车,所以在这两个环节添加β-内酰胺酶可能性极大。由于此种非法添加只有在奶牛使用抗生素后才使用,就黑龙江而言,8~10月份属于奶牛疾病低发阶段,这也是检出β-内酰胺酶较低的原因之一。为确保安全,必须加强对整个乳业产业链的监管。
3 结束语
基于本次乳及乳制品中β-内酰胺酶专项监测结果,虽然生乳中非法添加β-内酰胺酶为个别现象,但仍然存在个别奶农的违规现象。由于黑龙江省奶牛养殖模式仍以分散养殖为主,乳腺炎等疾病发病率高,抗生素使用不规范等特点,短期内牛奶中抗生素残留的问题仍会普遍存在。而奶农为减小损失会设法将含有抗生素的牛乳通过加入β-内酰胺酶等方式以掩盖抗生素残留送交到乳品企业。所以其危害性仍不容忽视,为此建议相关部门:
一是加大监测频次,特别是在最可能非法添加β-内酰胺酶的奶牛疾病高发期进行监测;
二是加大监管力度,使专项监测形成常态化,建议在全国范围内开展乳和乳制品β-内酰胺酶风险监测工作,据此可及时发现非法添加β-内酰胺酶发生的重点地区与时间,为政府监管提供可靠的依据,同时也可震慑不法分子的非法添加等行为。
[1]崔生辉,李景云,马越.“生鲜牛乳抗生素分解剂”的鉴定与检测[J].中国卫生食品杂志,2007,19(2)113-116.
[2]沈浥,刘洋,李兆阶.乳与乳制品中β-内酰胺酶的研究进展和标准化现状[J].中国乳品工业,2014,288,(11):35-38.
[3]卫生部.关于印发《全国打击违法添加非食用物质和滥用食品添加剂专项整治近期工作重点及要求》的通知(卫监督发[2009]21号).
[4]卫生部.关于印发《全国打击违法添加非食用物质和滥用食品添加剂专项整治抽检工作指导原则和方案》的通知(食品整治办[2009]29号).
[5]食品整治办[2009]29号指定检验方法4.乳及乳制品中舒巴坦敏感β-内酰胺酶类药物检验方法(杯碟法).
