磷酸盐及钙离子对浓缩乳清蛋白热稳定性的影响
2015-12-16李妍李海梅杨与争王红张列兵
李妍 ,李海梅,杨与争,王红,张列兵,4
(1.北京工商大学北京市食品添加剂工程技术研究中心,北京100048;2.中国粮油控股有限公司研发部,北京100020;3.中国农业大学食品科学与营养工程学院,北京100083;4.东北农业大学食品安全与营养协同创新中心,哈尔滨150030)
0 引言
浓缩乳清蛋白(WPC)是干酪加工副产物乳清经膜过滤后浓缩干燥得到的蛋白质质量分数在34%~80%的乳基配料。其富含各种必需氨基酸,尤其是支链氨基酸,并且具有良好乳化、凝胶、持水性和发泡性,广泛应用于食品工业[1-2]。然而乳清蛋白应用中面临的最大挑战是其在热处理过程中的稳定性。热处理是多数食品加工必不可少的工序,乳清蛋白在热处理过程中容易发生变性,产生絮凝、分层沉淀,使其应用受到一定的限制[3]。
乳清蛋白的热稳定性受离子环境、pH值、热处理温度等影响[3]。磷酸盐可以改善牛乳蛋白的热稳定性[4-5],研究认为磷酸盐对牛乳环境钙离子及酪蛋白结构的影响而增强其热稳定性[6]。对于磷酸盐对乳清蛋白热稳定性的影响研究很少。本研究探讨了各种磷酸盐和钙离子浓度对WPC80热稳定性的影响,并分析磷酸盐改善WPC热稳定的能力与钙离子浓度的关系。
1 实验
1.1 WPC溶液制备
按溶液蛋白质质量分数3.5%将WPC80溶于40℃去离子水中,搅拌器转速为500 r/min,搅拌30 min后备用。
1.2 热稳定性测定
向WPC水溶液中分别添加不同浓度的三聚磷酸钠、磷酸氢二钠、磷酸二氢钠、焦磷酸钠以及乙二胺四乙酸二钠,充分溶解后,用HCl或NaOH调节溶液pH值至所需值,140℃油浴中测定各溶液的热絮凝时间(HCT)。
1.3 钙离子浓度
钙离子浓度采用钙离子选择电极测定
1.4 数据处理分析
采用SPASS进行多重比较分析,采用Excel软件进行作图和标准差分析。
2 结果分析
2.1 磷酸盐对WPC80热稳定性的影响
图1为不同磷酸盐不同质量浓度下WPC80的HCT变化。由图1可以看出,磷酸盐种类和浓度的变化对WPC热稳定性的影响不同。磷酸氢二钠和三聚磷酸钠盐对WPC热稳定性影响趋势相近,随着盐浓度增加,HCT值呈先上升后下降的趋势,添加量质量浓度为1 g/L时WPC溶液的热稳定性最高。磷酸氢二钠和焦磷酸钠改善WPC溶液热稳定性的效果也是随着磷酸盐质量浓度的增加而逐渐增加,添加1.5 g/L的HCT值最高。磷酸氢二钠和焦磷酸钠对HCT的影响低于磷酸氢二钠和三聚磷酸钠。
在pH值为6.8~7.2范围内,添加相同磷酸盐相同质量浓度条件下,WPC80的热稳定性都会随pH的增大而增强。说明pH值变化对WPC80热稳定性有重要影响,前面的研究也证实这一点[7]。
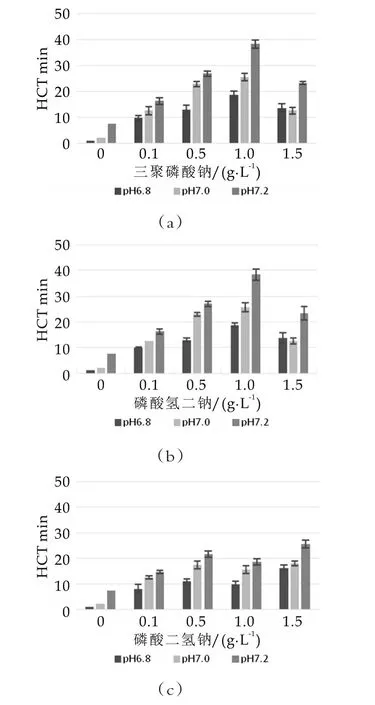
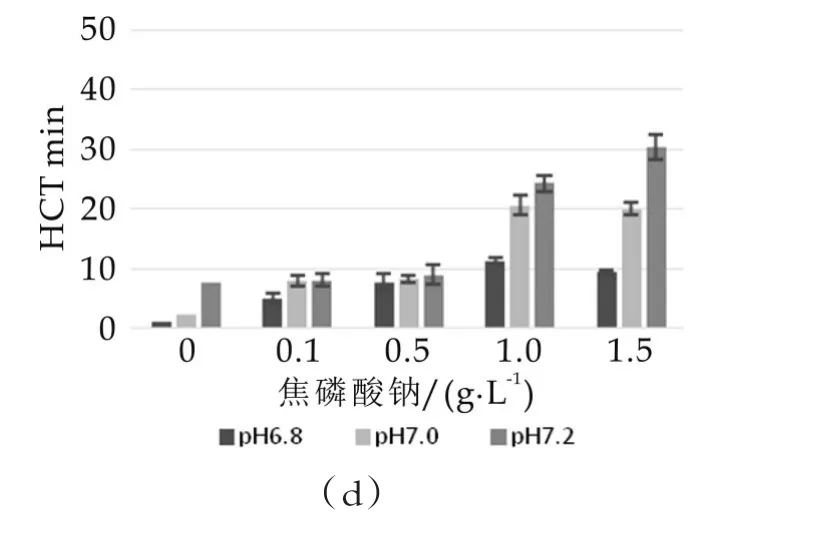
图1 不同磷酸盐不同质量浓度下WPC80的HCT变化
2.2 钙离子对WPC热稳定性的影响
通过向WPC溶液中添加不同浓度乙二胺四乙酸二钠(EDTA)螯合钙离子,改变溶液的钙离子浓度,分析钙离子变化对WPC热稳定性的影响,结果如图2所示。由图2可以看出,WPC溶液钙离子浓度变化对其热稳定性影响很大,随钙离子浓度降低HCT增大,WPC热稳定性增强,两者呈显著负相关(P<0.05)。并且,在pH值为6~7.5范围内,相同钙离子浓度下,随着pH值增大,HCT有增大的趋势,pH越高、钙离子浓度越低,这种趋势越明显。

图2 钙离子浓度与WPC热稳定性关系
2.3 磷酸盐对WPC溶液钙离子浓度的影响
不同磷酸盐对WPC溶液游离钙离子的影响差异明显(见图3)。三聚磷酸钠与焦磷酸钠对钙离子的影响变化趋势相近,随着盐浓度增加,钙离子浓度显著降低(P<0.05);相同盐浓度下,三聚磷酸钠比焦磷酸钠对WPC溶液游离钙离子的螯合作用更大,钙离子浓度更低(P<0.05)。磷酸氢二钠和磷酸二氢钠对钙离子的降低效果随浓度的增加变化趋势不明显,仅磷酸氢二钠添加量质量浓度1.5g/L(pH=7.0和pH=7.2)时,WPC溶液游离钙离子浓度有较明显降低(P<0.05)。
图3为添加不同磷酸盐对WPC80溶液钙离子浓度影响。由图3可以看出,在所研究的pH值范围内,随着pH值升高,WPC溶液钙离子浓度呈明显降低趋势。
2.4 WPC热稳定性与游离钙离子浓度间的相关性分析
添加不同浓度的磷酸盐后,WPC溶液的游离钙离子浓度和热稳定性都发生变化,分析钙离子浓度和HCT之间的相关性(spearman检验),具有相关性的结果如表1所示。由表1可以看出,只有pH值为7.2条件下,添加不同质量浓度的磷酸氢二钠和焦磷酸钠的WPC溶液中钙离子浓度与HCT值变化呈显著负相关,其他各组样品中两参数之间均不具有统计相关性。
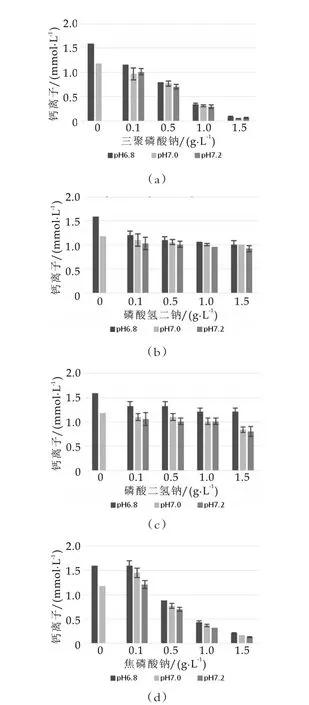
图3 不同磷酸盐对WPC80溶液钙离子影响

表1 不同pH值钙离子浓度与HCT之间的相关性检验
3 讨论
磷酸盐可以提高牛乳的热稳定性。研究认为磷酸盐能改善乳制品热稳定性的主要原因是其可减少钙离子与酪蛋白的结合,保持酪蛋白原有的负电荷,从而保持分子间的静电排斥作用;同时磷酸盐同钙离子的结合减弱酪蛋白的疏水互相作用,避免酪蛋白间的聚集或沉淀[8]。但是磷酸盐对乳清蛋白热稳定性的影响报道不多。Dewit等对脱盐和非脱盐乳清的热稳定性研究发现,在pH值为6.2~7.4范围内,相同钙离子浓度的脱盐乳清受热时会发生大量蛋白质凝集,而正常乳清并未发生这种现象[9]。分析两者的区别,主要在于磷酸盐和柠檬酸盐存在形式不同,脱盐乳清中磷酸根离子少可能与其热不稳定性有关。本研究发现添加磷酸盐可以改善WPC溶液中清蛋白的热稳定性,三聚磷酸钠和磷酸氢二钠的改善效果最好。并且这种改善作用在pH值为6.8~7.2范围内随pH值增大作用增强。pH是影响WPC热稳定的重要因素,前期研究也表明在pH值为6-8范围内,随pH升高,WPC热稳定性增强[7,10]。本研究在磷酸盐存在的情况下,两者存在一定的协同作用。
钙离子也是影响WPC热稳定性的重要因素,在乳清蛋白等电点的碱性范围内随着钙离子浓度增加,乳清蛋白热凝聚增强[11]。乳清蛋白变性后展开的蛋白质分子在远离蛋白质等电点的pH值和较低离子浓度时,由于静电斥力而保持分离状态,不会互相接近而凝聚,而较高的钙离子浓度会屏蔽这些静电斥力,使变性的蛋白质分子互相接近、聚集,形成凝胶[12]。本研究也表明在pH值为6~7.5范围内钙离子浓度与WPC溶液热稳定性呈负相关。
已有研究证实钙离子螯合剂可以改变乳蛋白溶液的离子环境,尤其是钙离子浓度,从而增强乳清的溶解性[13-15]。磷酸盐改善清蛋白的热稳定性也与其钙离子螯合作用有关。本研究分析了添加不同种类和不同浓度磷酸盐的WPC溶液游离钙离子含量的变化。添加磷酸盐一定程度上可以降低WPC溶液的游离钙离子浓度,但大部分情况下钙离子浓度降低程度与乳清蛋白热稳定性改善效果并不具有相关性。这说明除螯合钙离子之外,磷酸盐与乳清蛋白之间还存在其他有助于增强后者热稳定性的作用机制,有待进一步研究。
4 结论
添加磷酸盐能够改善WPC溶液的热稳定性,改善效果因磷酸盐种类、浓度以及溶液pH值的不同而不同。在pH值为6.8~7.2范围内,三聚磷酸盐和磷酸氢二钠的效果较好。WPC溶液钙离子浓度的变化与其热稳定性呈负相关。磷酸盐对钙离子的螯合作用并非磷酸盐改善WPC热稳定性的唯一原因,磷酸盐改善乳清蛋白热稳定性的作用机制有待进一步研究。本研究结果为生产企业应用磷酸盐改善WPC热稳定性提供参考。
[1]张佳程,张和平,张列兵.现代乳品工业手册[M].第二版.中国轻工业出版社,2012.
[2]孙宝国,曹雁平,李健,等.食品科学研究前沿动态[J].食品科学技术学报,2014(02):1-11.
[3]WIJAYARTI H B,BANSAL N,DEETH H C.Stability of Whey Proteins during Thermal Processing:A Review[J].Comprehensive Reviews in Food Science and Food Safety,2014,13(6):1235-1251.
[4]SIKAND V,TONG P,WALKER J.Effect of adding salt during the diafiltration step of milk protein concentrate powder manufacture on mineral and soluble protein composition[J].Dairy Science&Technology,2013,93(4-5):401-413.
[5]SINDHU J S.Influence of sodium phosphate on the heat stability of buffalo milk and its concentrate[J].Journal of Food Processing and Preservation,1985,9(2):57-64.
[6]SIKAND V,TONG P S,WALKER J.Heat stability of reconstituted,protein-standardized skim milk powders[J].Journal of dairy science-Journal of dairy science,2010,93(12):5561-5571.
[7]杨与争,李妍,李海梅,等.pH值对浓缩乳清蛋白热稳定性的影响[J].中国乳品工业,2013(09):14-17.
[8]UDABAGE P,MCKINNON I R,Augustin M A.Effects of Mineral Salts and Calcium Chelating Agents on the Gelation of Renneted Skim Milk[J].Journal of Dairy Science,2001,84(7):1569-1575.
[9]DEWIT J N,KLARENBEEK G.Effects of Various Heat Treatments on Structure and Solubility of Whey Proteins[J].Journal of Dairy Science,1984,67(11):2701-2710.
[10]DE LA FUENTE M A,SINGH H,HEMAR Y.Recent advances in the characterisation of heat-induced aggregates and intermediates of whey proteins[J].Trends in Food Science&Technology,2002,13(8):262-274.
[11]RYAN K N,VARDHANABHUTI B,JARAMILLO D P,et al.Stability and mechanism of whey protein soluble aggregates thermally treated with salts[J].Food Hydrocolloids,2012,27(2):411-420.
[12]XIONG Y L.Influence of pH and ionic environment on thermal aggregation of whey proteins[J].Journal of Agricultural and Food Chemistry,1992,40(3):380-384.
[13]HAVEA P,SINGH H,Creamer L K.Heat-Induced Aggregation of Whey Proteins:?Comparison of Cheese WPC with Acid WPC and Relevance of Mineral Composition[J].Journal of Agricultural and Food Chemistry,2002,50(16):4674-4681.
[14]DE WIT J N,KESSEL T V.Effects of ionic strength on the solubility of whey protein products.A colloid chemical approach[J].Food Hydrocolloids,1996,10(2):143-149.
[15]BERNAL V,JELEN P.Effect of Calcium Binding on Thermal Denaturation of Bovine α-Lactalbumin[J].Journal of Dairy Science,1984,67(10):2452-2454.
