纯硅酸溶液的聚合行为
2015-12-14何龙超李辽沙
何龙超,李辽沙
(安徽工业大学a.安徽省冶金工程与资源综合利用重点实验室;b.冶金减排与资源综合利用教育部重点实验室,安徽马鞍山243002)
纯硅酸溶液的聚合行为
何龙超a,b,李辽沙a,b
(安徽工业大学a.安徽省冶金工程与资源综合利用重点实验室;b.冶金减排与资源综合利用教育部重点实验室,安徽马鞍山243002)
以纯硅酸溶液为研究体系,采用紫外/分光光度仪、傅立叶红外光谱仪(FT-IR)分别表征溶液吸光度与凝胶基团,探究纯硅酸溶液的聚合行为,探讨实验条件对纯硅酸胶凝时间的影响。结果表明:在没有金属离子的干扰下,纯硅酸溶液胶凝曲线最高点出现在pH=1.10附近,pH升高,导致硅酸溶胶的形成速率减小,引起溶液吸光度增加;pH<2.27时,随着pH升高,纯硅酸聚合的氧联作用所占比例增加,聚合活化能升高,pH>2.27时,聚合以氧联作用为主,活化能保持在最大值;随着pH升高,纯硅酸凝胶中Si-O-Si反对称收缩振动吸收峰发生红移,是由胶体结构单元[SiO4]4+聚合度的降低导致。
纯硅酸溶液;活化能;胶体;凝胶;聚合
国内外学者针对硅酸溶液的聚合研究已近百年,最为著名的是硅酸聚合理论[1-3],系统阐明了含碱金属离子硅酸溶液的2种聚合机制。Dobrzyński[4],Spadini等[5]研究了Al3+与硅酸之间的配位络合作用;Oncsik等[6]、许韵华等[7]研究了不同多价金属离子对硅酸聚合机制的影响,认为在较低pH下金属离子对硅酸聚合的影响以静电作用为主,而在较高pH下以化学作用为主;Novikovadeng等[8]、Shabanova等[9]研究了碱金属离子对硅酸溶液聚合的影响。上述研究中主要采用SiO2·nNa2O酸化法获得硅酸溶液,此法获得的硅酸溶液属含金属离子的非纯体系,其研究结论存疑。原因在于硅酸分子的聚合度随硅酸钠模数不同而变化[10],并且溶液中Na+对硅酸溶液聚合行为的影响是无法排除的。而国内外对纯硅酸溶液聚合行为的研究报道较少,因此探索纯硅酸溶液聚合行为对丰富“硅酸聚合理论”具有重要意义。
文中依托《一种不含金属离子的高纯硅溶胶的制备方法》发明专利[11],采用酸化硅酸钙的方法制备纯硅酸溶液,研究pH对纯硅酸溶液的胶凝时间、吸光度、聚合活化能、凝胶基团的影响,探讨pH等对纯硅酸聚合的活化能及其与纯硅酸溶液聚合规律的内在关系,以期丰富硅酸溶液的聚合理论。
1 实 验
1.1 试剂、仪器
试剂:浓硫酸、浓氨水、钼酸铵、浓盐酸、二次蒸馏水,以上试剂均为分析纯;自制的不含碱金属离子的纯硅酸溶液[11]。
仪器:PHS-2C精密pH计(上海般特仪器有限公司,每次使用前均使用标准溶液校正);DZF-6210真空干燥箱(上海恒科技有限公司);HJ-3A恒温磁力搅拌器(上海梅颖浦仪器制造有限公司),HH-2恒温水浴锅(常州国华电器厂);Nicolet6700傅立叶红外光谱仪(美国Nicolet公司),SPECORD200紫外/分光光度仪(德国耶拿公司)。
1.2 实验方法
1)根据文献[11],采用硫酸酸化水淬硅酸钙的方法制备纯硅酸溶液。
2)量取200 mL步骤1)中制备的纯硅酸溶液,用氨水溶液(1.5 mol/L)调节硅酸溶液pH,并均分为5份,放在带胶塞的试管中,分别置于30,35,40,45,50℃恒温水浴锅中。
3)重复步骤2),制备不同pH的纯硅酸溶液,pH范围是0.65~3.55。记录硅酸溶液从开始到胶凝的时间(参照文献[12]的方法)。上述样品同时制备2组,一组用于测定胶凝时间,另一组用于胶凝过程取样,采用“硅钼黄比色法”[1]测定纯硅酸溶液吸光度。
4)胶凝结束后,反复“抽滤-水洗”清洗凝胶,直至滤液为中性为止。
5)将凝胶放至真空干燥箱中,在120℃下保温12 h,采用Nicolet6700傅立叶红外光谱仪分析不同条件下纯硅酸凝胶基团变化。
2 实验结果及分析
2.1 pH对纯硅酸溶液胶凝时间的影响
以硅酸溶液胶凝时间t的对数logt为纵坐标,pH为横坐标绘制纯硅酸溶液的胶凝曲线。50℃下纯硅酸溶液的胶凝曲线如图1。从图1可以得出,pH在0.65~3.55范围内,纯硅酸溶液胶凝曲线最高点,即纯硅酸溶液稳定性最佳出现在pH=1.10附近,这与Mal’kova[13]认为强酸溶液中胶凝曲线的最高点出现在pH为2~3之间有较大不同。纯硅酸溶液胶凝曲线最高点对应pH显著减小,因为实验中采用的硅酸溶液为自制的不含碱金属离子的纯硅酸溶液,排除了采用酸化硅酸钠的办法制得的硅酸溶液中大量钠离子的干扰。
在硅酸溶液体系中,随着溶液pH降低,H+浓度的增加,硅酸分子应存在质子化过程,如反应式(1)[14]。用酸化硅酸钠的办法制得的硅酸溶液中存在大量钠离子,其与硅酸胶体羟基存在反应,如反应式(2)[15]。
其中SiOS-OH代表硅酸溶液中硅胶分子。根据文献[3],硅酸溶液胶凝曲线的最高点出现在浓度等于浓度的pH下,即与的等电点。由酸化硅酸钠获得的硅酸溶液中,由于反应式(2)的存在,提高了溶液中H+浓度,促进硅酸溶液中硅酸分子的质子化过程,即反应式(1),利于溶液中的生成以及抑制的生成。导致酸化硅酸钠获得的硅酸溶液中与的等电点对应pH增加,相应硅酸溶液胶凝曲线的最高点对应的pH增大,体现在纯硅酸溶液胶凝曲线上,即纯硅酸溶液胶凝曲线的最高点对应的pH小于酸化硅酸钠获得的硅酸溶液胶凝曲线最高点对应的pH。这就是纯硅酸溶液与含碱金属离子硅酸溶液聚合规律不同的本质原因,由此也证明,硅酸溶液中的金属离子对其聚合行为有明显影响,这也与传统的认知不一致。
2.2 pH、反应时间对纯硅酸溶液吸光度的影响
图2是pH=1.00,2.00时,采用“硅钼黄比色法”测定的不同反应时间下纯硅酸溶液吸光度。由图2可知,随着时间的增加,溶液的吸光度不断减小,且pH=2.00时的吸光度大于pH=1.00时的吸光度。
纯硅酸溶液的吸光度正比于硅酸溶液中单硅酸分子的浓度[1],通过比较吸光度的变化能够判定单硅酸分子浓度的变化。因此从图2可以得出,随着时间的增加,纯硅酸溶液中单硅酸分子的浓度不断减小,而反应过程中,pH=2.00的样品中单硅酸分子浓度大于pH=1.00样品中单硅酸分子的浓度,由此表明,硅酸分子聚合形成溶胶的速率随pH升高而降低,形成溶胶时间因此增加。硅酸溶液形成硅酸凝胶的过程包含硅酸分子聚合形成溶胶及溶胶形成凝胶的两个阶段,故此硅酸溶液的胶凝时间包含硅酸分子聚合形成溶胶的时间和溶胶形成凝胶的时间。结合图1,纯硅酸溶液的胶凝时间在pH=1.00时大于pH=2.00时。因此,纯硅酸溶胶形成凝胶的时间随pH的升高而缩短。综合上述分析,认为:pH升高,降低单硅酸分子聚合长大形成硅酸溶胶的速率,而增大溶胶形成凝胶的速率。
2.3 pH对纯硅酸聚合活化能的影响
图3为纯硅酸溶液在不同温度下的胶凝曲线。从图3可得出,随着温度的升高,纯硅酸溶液的胶凝时间显著减小,胶凝曲线最高点对应的pH变化不大。
表1是根据不同pH下硅酸溶液聚合活化能(Ea)计算公式,式(3)[2],计算得出的不同pH下纯硅酸聚合的活化能。
式中:K是胶凝时间的对数logt与热力学温度(T)的倒数组成的直线的斜率;R为气体常数。
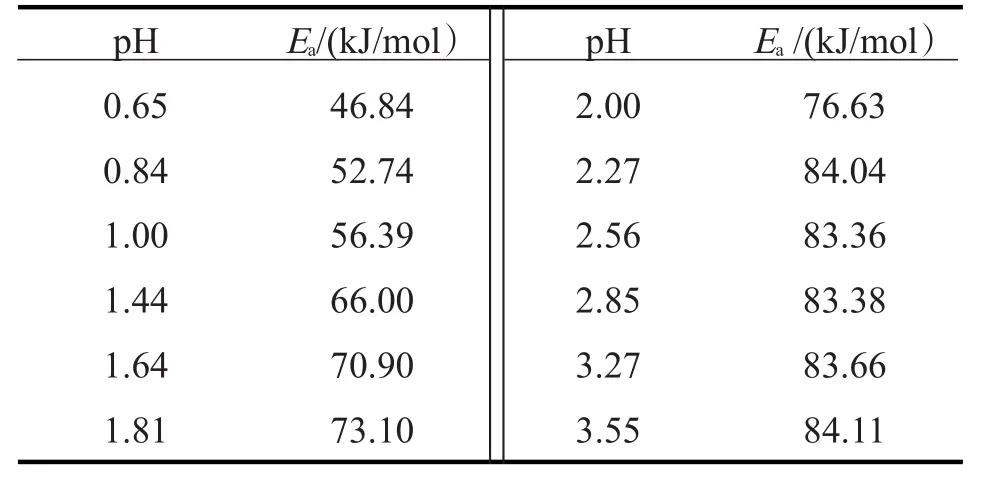
表1 不同pH值下纯硅酸聚合的活化能Tab.1 Polymerization activation energy of pure silicic acid solution at different pH values
由表1得出:pH在0.65~2.27范围内,纯硅酸聚合的活化能随着体系pH升高而增加,硅酸分子聚合跨越的能垒增加导致硅酸分子聚合长大形成硅酸溶胶的速率降低,这与本文2.2中得出结论相符;纯硅酸溶液聚合的活化能在pH为2.27~3.55时保持在最大值,活化能对形成溶胶的速率影响可以忽略,而胶凝时间随着pH的升高而减小,进一步说明溶胶形成凝胶的时间随pH的升高而缩短。
纯硅酸聚合活化能随pH的变化而改变,可以采用有盐体系中硅酸溶液聚合的机理解释[2]。硅酸分子聚合过程中存在氧联作用和羟联作用,羟联作用本质是硅酸分子配位数的增加,反应易进行。而氧联作用涉及羟基的断裂,对应活化能较大,而随着pH升高,纯硅酸聚合过程中氧联作用占的比例升高,相应纯硅酸聚合的活化能升高,当pH>2.27时,聚合以氧联作用为主,纯硅酸聚合的活化能保持在最大值。
结合图2可知,pH<1.10时,纯硅酸溶液的胶凝时间由形成硅酸溶胶的过程决定,随着pH的升高胶凝时间增加;pH>1.10时,胶凝时间由溶胶形成凝胶的过程决定,随着pH的升高硅酸溶胶形成凝胶的速率增加,胶凝时间减小;pH=1.10时,形成硅酸溶胶与溶胶形成凝胶两个阶段对胶凝时间影响相互抵消,胶凝时间最长。
2.4 pH对纯硅酸凝胶基团的影响
图4是不同pH下纯硅酸体系凝胶红外谱图。图中波数965 cm-1对应Si-OH的弯曲振动,799 cm-1对应Si-O键的对称收缩振动,1 080 cm-1对应的是Si-O-Si反对称收缩振动,3 474 cm-1对应凝胶内的毛细孔水、结构水中O-H键的反对称收缩振动[16-18]。
随着pH的升高,Si-O-Si反对称收缩振动吸收峰由1 084 cm-1变为1 073 cm-1。pH升高抑制形成纯硅酸溶胶过程,导致溶胶聚沉中胶体颗粒减小,胶体结构单元中[SiO4]4+聚合度降低,引起Si-O-Si反对称收缩振动吸收峰向低波数方向移动[19]。这也从另一方面说明pH升高,抑制单硅酸分子聚合长大形成硅酸溶胶的过程,促进溶胶形成凝胶的过程。
3 结 论
研究pH对纯硅酸胶凝时间、吸光度、聚合活化能、凝胶产物基团的影响,发现:由于没有钠离子的干扰,纯硅酸溶液胶凝曲线最高点出现在pH=1.10附近;pH升高,导致硅酸溶胶的形成速率减小,引起溶液吸光度增加;pH<2.27时,随着pH升高,纯硅酸聚合的氧联作用所占比例增加,聚合活化能升高,pH>2.27时,聚合以氧联作用为主,活化能保持在最大值;纯硅酸凝胶中Si-O-Si反对称收缩振动吸收峰发生红移,是由胶体结构单元[SiO4]4+聚合度的降低导致。
[1]朱屯,钱保华,陈荣三,等.硅酸及其盐的研究Ⅹ-单硅酸聚合反应动力学[J].化学学报,1981,39(1):1-11.
[2]陈荣三,张雪琴,王伯康,等.硅酸及其盐的研究Ⅺ-单硅酸胶凝作用的温度效应和活化能[J].高等学校化学学报,1980, 1(2):31-38.
[3]戴安邦,陈荣三,柳海澄,等.硅酸及其盐的研究Ⅷ-单硅酸胶凝作用中的离解常数[J].化学学报,1982,40(8):767-769.
[4]Dobrzyński D.Chemistry of neutral and alkaline waters with low Al3+activity against hydroxyaluminosilicate HASB solubility.The evidence from ground and surface waters of the Sudetes Mts(SW Poland)[J].Aquatic Geochemistry,2007,13(3):197-210.
[5]Spadini L,Schindler P W,Sjöberg S.On the stability of the AlOSi(OH)32+complex in aqueous solution[J].Aquatic Geochemistry, 2005,11(1):21-31.
[6]Oncsik T,Trefalt G,Csendes Z,et al.Aggregation of negatively charged colloidal particles in the presence of multivalent cations [J].Langmuir,2014,30(3):733-741.
[7]许韵华,尹承龙,朱红,等.金属离子对硅酸聚合胶凝影响的研究[J].北方交通大学学报,2003(6):97-100.
[8]Novikova N A,Golikova E V,Chernoberezhskii Y M,et al.The effect of pH on aggregation kinetics of monodisperse silica sol in NaCl solutions[J].Colloid Journal,2014,76(1):66-75.
[9]Shabanova N A,Sergeeva M N.Regularities of the change in colloid-chemical properties of silica hydrosols in the presence of alkali metal hydroxides[J].Russian Journal ofApplied Chemistry,2009,82(5):832-835.
[10]曹德光,苏达根,宋国胜.低模数硅酸钠溶液的结构及其键合反应特性[J].硅酸盐学报,2004,32(8):1036-1039.
[11]申星梅,李辽沙,罗涛,等.一种不含金属离子的高纯硅溶胶的制备方法:CN102838124A[P].2012-12-26.
[12]Li L S,Lu T T.Condensation mechanism and influencing factor of stability of complicated silicic acid system[J].AIChE Journal,2011,57(5):1339-1343.
[13]Mal’kova M Y.Synthesis of a nanodispersed silica sol and its aggregative stabilit[J].Russian Metallurgy(Metally),2013(12): 913-915.
[14]TaiAP.Atheory of polymerization of silicic acid[J].Journal of Nanjing University(Natural Sciences),1963,10(9):1311-1320.
[15]陈荣三,王金晞,柳海澄,等.硅酸及其盐的研究ⅩⅣ-Ca2+、Na+和K+与硅胶表面硅羟基的反应[J].南京大学学报(自然科学版),1983,40(1):73-84.
[16]尹万云,裴立宅,金仁才,等.从柠檬酸前驱体合成超细氧化铝及莫来石粉末[J].安徽工业大学学报(自然科学版),2011, 28(1):34-38.
[17]陆婷婷,李辽沙.高炉渣制备聚硫酸铝硅絮凝剂[J].安徽工业大学学报(自然科学版),2010,27(3):225-228.
[18]裘小宁.SO42-/TiO2-SiO2固体超强酸的制备及应用[J].安徽工业大学学报(自然科学版),2005,22(3):246-252.
[19]徐迅.纳米SiO2和硅灰的火山灰活性差异的研究[J].中国水泥,2007(3):64-66.
责任编辑:何莉
Polymerization Behavior of Pure SilicicAcid Solution
HE Longchaoa,b,LI Liaoshaa,b
(a.Anhui Provincial Key Laboratory of Metallurgical Engineering&Resources Recycling;b.Key Laboratory of Metallurgical Emission Reduction&Resources Recycling of Ministry of Education,Anhui University of Technology,Ma'anshan 243002,China)
Taking the pure silicic acid solution as research system,the absorbance of pure silicic acid solution and the functional groups of the silica gel were separately characterized by spectrophotometer and IR spectra.The polymerization behavior of pure silicic acid solution was studied,and the effect of experimental conditions on its gel time was investigated.It shows that the maximum gel time of pure silicic acid occurs at pH=1.10.The formation rate of silicic acid sol decreases with the increasing of pH value.The polymerization activation energy of pure silicic acid increases with the pH value rising as pH<2.27 and keeps to a maximum as pH>2.27.The structural unit of pure silicic acid sol particles is[SiO4]4+and the polymerization degree of[SiO4]4+decreases with the increasing of pH value.The antisymmetric vibration absorption peak of Si-O-Si moves to lower wavenumbers for the polymerization degree decrease.
pure acid solution;activation energy;colloid;gel;polymerization
TQ219
A
10.3969/j.issn.1671-7872.2015.04.009
2015-03-05
安徽省科技厅项目(1506c085003);2014年马鞍山市科技计划
何龙超(1987-),男,河北定州人,硕士生,研究方向为冶金二次资源综合利用。
李辽沙(1957-),男,安徽霍丘人,博士,教授,研究方向为冶金二次资源高效利用。
1671-7872(2015)-04-0343-05
