一种色氨酸修饰的苯并呋咱类碱性荧光探针的合成与性能研究
2015-12-13李煦田梁凤娇马立军
唐 健,李煦田,梁凤娇,张 敏,马立军
(华南师范大学化学与环境学院,广州510006)
人体细胞内的pH 值对一系列生理活动有着极其重要的影响[1],例如细胞的增殖与凋亡[2]、离子运输[3]、神经信号传递[4]、肌肉收缩[5]等. 正常情况下人体血液的pH 值为7.4 ±0.5,过酸或者过碱都会影响正常的生理功能并导致疾病的发生,例如癌症[6]和阿尔茨海默综合症[7]. 因此研究和监测细胞内pH 值的变化对生理活动的影响有着重要的意义[8].
与传统的检测pH 值方法如指示剂法、电极法相比[9],荧光光谱法是以光信号为基础的检测方法,它具有实时、原位、高灵敏度、高选择性、快速响应、对样品无破坏等优点[10],因此能应用于细胞等生物体系的pH 值检测. 近年来,许多新型的pH 荧光探针被报道. Song 等[11]合成了一种具有聚集诱导发光增强的比率型pH 荧光探针,由于C—N 键分子内自由内旋转及非平面构型的限制,在聚集/固态中显示聚集诱导发光增强,并且该探针能在活细胞中对pH 5.0~7.0 有检测响应. Liu 等[12]合成了一种香豆素-吲哚基的近红外比率型pH 荧光探针,得益于较大的Stokes 位移,该探针具有快速响应和高灵敏度特性,在pH 2.0~7.0 有响应,并且能应用于细胞内酸性环境的检测. 1968年,Ghosh 和Whitehose[13]第一次提出以4-氯-7-硝基苯并呋咱作为一种氨基化合物的衍生试剂,并与其它亲核试剂反应产生荧光. 此类探针含有推电子氨基和强拉电子的硝基,可增强分子内的电荷转移,又有羟基和氮氢阴离子的结合点,对阴离子的识别有很强的能力.本文将水溶性良好的色氨酸与苯并呋咱结合,合成了一种水溶性好的7-硝基苯并呋咱色氨酸(简称FSS),研究发现该探针能够在水溶液中对OH-表现出高选择性的荧光识别效应,表现为一种碱性荧光探针.
1 实验部分
1.1 实验仪器与试剂
仪器:荧光分光光度计(HITACHI F-2500 FL Spectrophotometer),溶液样品所采用的激发波长均为470 nm;紫外-可见分光光谱仪(SHIMAZU UV-1700 UV-vis spectrometer);核磁共振波谱仪(Varian NMR Systems 400 MHz spectrometer);质谱仪(LCQ Deca XP MAX)液相色谱-质谱联用仪;pH 计(上海精密雷磁PHS-3B 酸度计).
试剂:三乙胺、无水甲醇、4-氯-7-硝基苯并呋咱(简称物质A)、色氨酸、无水硫酸镁、二氯甲烷、乙酸乙酯、氢氧化钠、盐酸、去离子水.
1.2 探针的合成与表征
7-硝基-苯并呋咱-色氨酸(FSS)的合成路线如图1 所示,首先将色氨酸进行酯化生成色氨酸甲酯盐酸盐,然后将其与4-氯-7-硝基苯并呋咱化合获得7-硝基-苯并呋咱-色氨酸甲酯(简称FSZ),最后FSZ 水解生成探针FSS.
1.2.1 色氨酸甲酯盐酸盐的合成 色氨酸甲酯盐酸盐的合成参照文献[14],合成后应立即进行下一步的反应.
1.2.2 FSZ 的合成 将色氨酸甲酯盐酸盐溶于30.0 mL 甲醇中,冰盐浴下冷却5.0 min 后,向其中缓慢滴加0.1 mL 的三乙胺,继续冷却搅拌30.0 min. 用恒压漏斗将溶于甲醇的4-氯-7-硝基苯并呋咱缓慢滴加到上述冷却液中,溶液变为棕色. 放于室温下搅拌反应20.0 h 后,抽滤并蒸干溶剂得到深棕色的粗产物. 然后用二氯甲烷溶解粗产物,并用去离子水洗至水层呈中性,以除去三乙胺. 有机层用无水硫酸镁干燥、抽滤,将滤液蒸干,将此粗产物用乙酸乙酯作展开剂进行硅胶柱层析分离. 过柱分离后得到棕色的固体产物FSZ.
1.2.3 FSS 的合成 将FSZ 溶于60.0 mL 的0.1 mol/L NaOH 水溶液中,室温下搅拌30.0 min 后,FSZ 全部溶解. 用乙酸乙酯萃取5 次以除去未反应的FSZ 和一些可能的副产物. 水相(棕色)中加入0.5 mol/L 盐酸至弱酸性(pH≈5.5),萃取液经无水硫酸镁干燥后抽滤,蒸干溶剂. 用乙酸乙酯作展开剂进行硅胶柱层析分离,过柱分离后得到深棕色固体产物FSS.
化合物FSS 的1H-NMR 谱(500 MHz,CDCl3)中化学位移和对应的质子类型归属为:8.18~6.860(m,6H,indole(H)),6.932、5.173(s,2H,benzoxadiazole(H)),5.866(s,1H,—NH—),4.595(s,1H,—CH),3.508~3.247(m,2H,—CH2—). 理论计算的相对分子质量(C17H13N5O5)为367.32,实际测试中质荷比为366.10 为FSS 去质子化所形成的质谱峰.
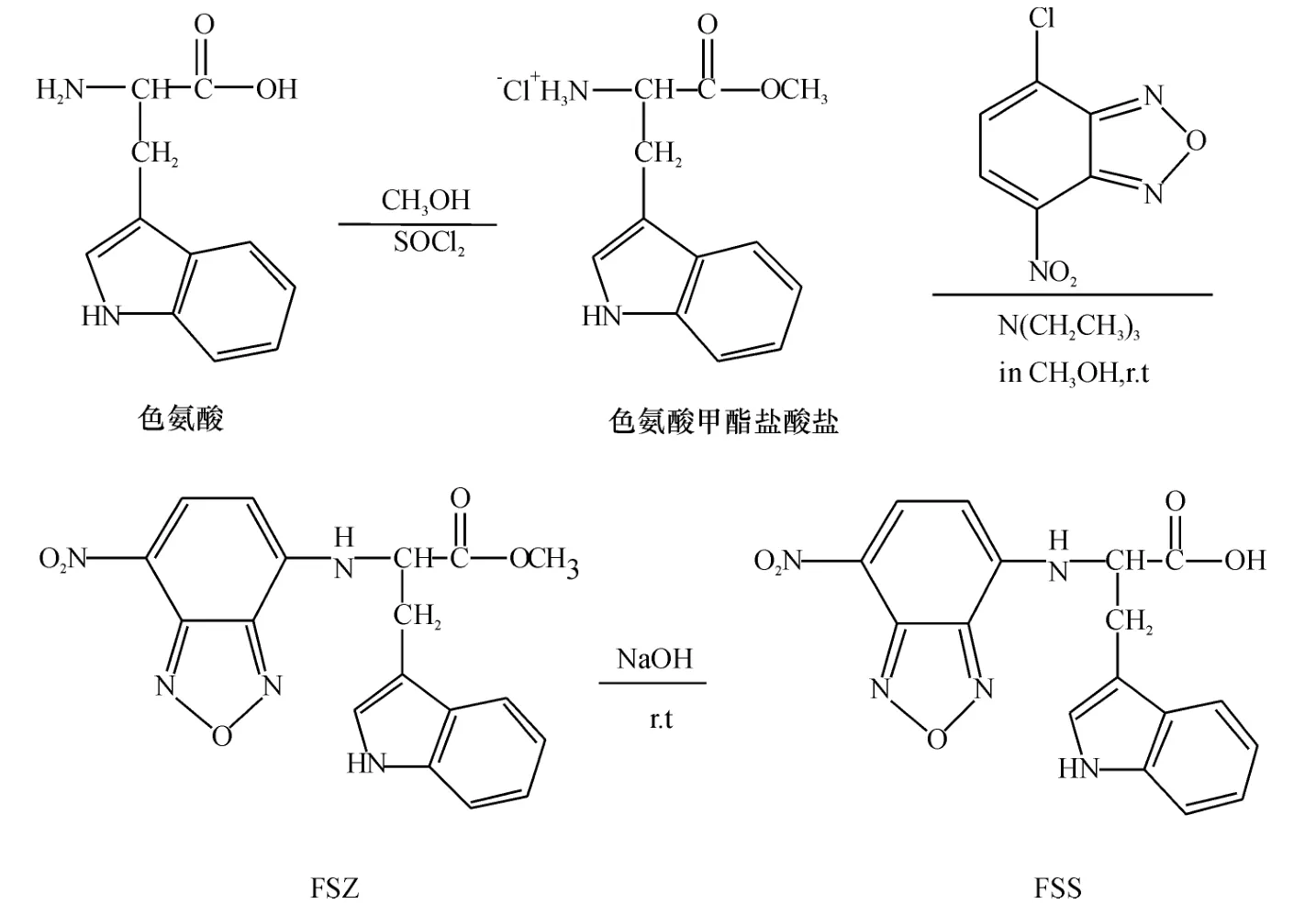
图1 FSS 的合成路线Figure 1 Synthetic route of FSS
1.3 测试溶液的配制
将FSS 溶于DMSO 中,配制成浓度为2.0 mmol的母液,用固体NaOH 和去离子水配制成0.1 mol/L的碱性水溶液. 取30.0 μL 的FSS 母液加入到3.0 mL 的离心管中,配制成浓度为20.0 μmol 的含5%DMSO(体积分数)的水溶液. 用上述0.1 mol/L 的NaOH 溶液调节体系的pH 值,再进行相应的光谱测试.
2 结果与讨论
2.1 探针FSS 对OH-响应的紫外-可见光谱
如图2 所示,FSS 的紫外-可见光谱在pH 为7.94 时出现2个吸收峰(480 和350 nm 处),它们为苯并呋咱的特征吸收峰. pH 从7.94 到12.24 过程中,480 nm 处的吸收峰强度下降,并出现蓝移,与此同时350 nm 处的吸收峰强度不断增大,伴随着红移现象,当pH 最终达到11.39 后,此探针仅在390 nm处存在一个新的吸收峰. 整个pH 变化过程中,在440 nm 处出现一个等吸收点. 同时,溶液的颜色从pH 为7.94 时的橙红色变成pH 为12.24 时的黄色,pH 为10.18 是橙红色到黄色的转折点,并且随着pH 的增大,黄色不断加深(图2 插图). 产生这种变化的原因可能是随着溶液碱性的增强,FSS 分子上的亚氨基发生去质子化作用,使得苯并呋咱芳香环的电子云密度发生改变,从而导致光吸收性质发生明显的改变,同时在溶液的颜色上发生变化.
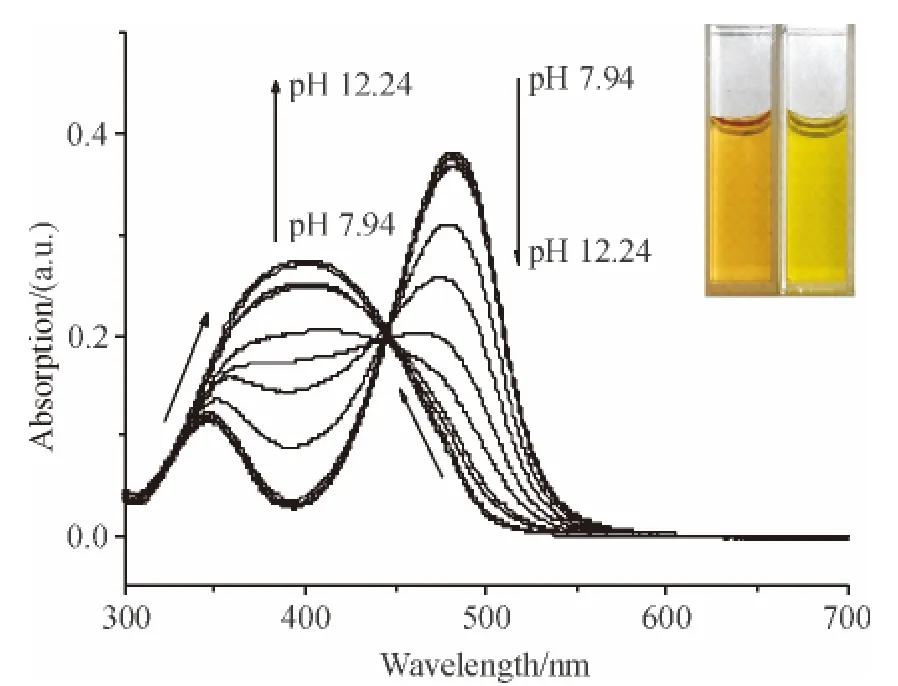
图2 不同pH 下FSS 的紫外-可见光谱和颜色变化Figure 2 UV-vis spectra and color transformation of FSS at different pHs
从FSS 的紫外-可见吸收光谱(图2)可明显看出,随着pH 的增加,480 nm 处的吸收峰逐渐下降,同时390 nm 处的峰不断增加,导致FSS 对碱性pH表现出比率型变化规律(图3),在390 和480 nm 处吸收峰强度的比值Ⅰ390/Ⅰ480,能够对溶液的酸碱度表现出不同的比值响应. 在pH <9.57 时,Ⅰ390/Ⅰ480基本不变;当pH >9.57 时,其比值不断增大,Ⅰ390/Ⅰ480能够作为碱性条件下pH 的响应信号.
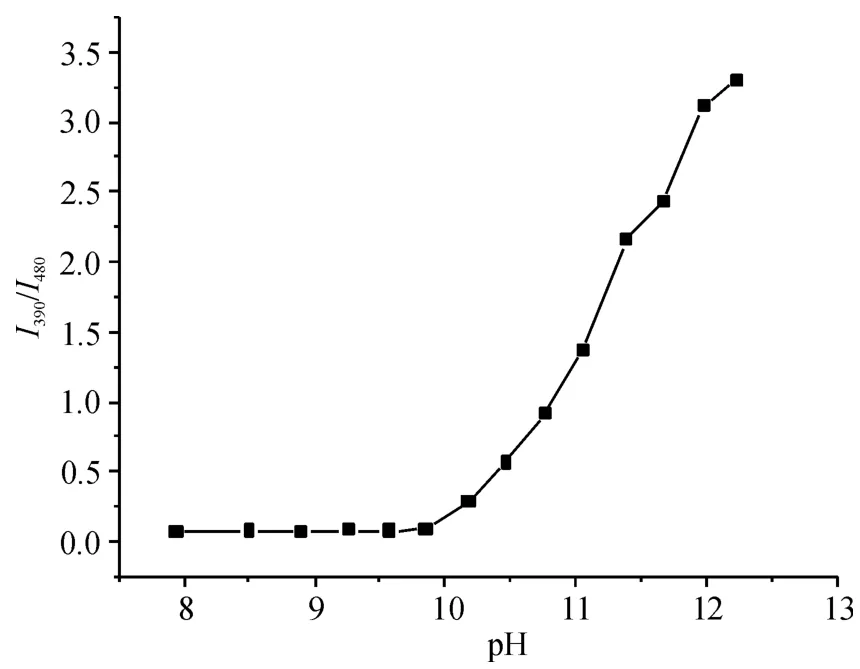
图3 不同pH 下Ⅰ390/Ⅰ480的变化趋势Figure 3 Change tendency of Ⅰ390/Ⅰ480 at different pHs
2.2 探针FSS 对OH-的荧光识别
在470 nm 波长光的激发下,FSS 的水溶液在546 nm 处有较强的荧光发射峰(图4),随着pH 值的不断增大,FSS 的荧光强度发生明显变化,在pH为7.94~9.26 时FSS 的荧光强度基本不变,当pH为9.57~12.24 时,荧光强度呈现明显规律性的猝灭变化. 当pH 达到12.24 时,FSS 的荧光峰的强度下降了70.8%,表现出荧光猝灭响应信号. 产生这种变化的原因可能是在碱性条件下,FSS 分子中苯并呋咱芳香环上的亚氨基发生了去质子化作用,由于苯并呋咱环上存在吸电子的硝基产生电子推拉效应,使得苯并呋咱环上的电子云密度发生较大改变,从而导致荧光强度减弱[15]. 因此,碱性条件下FSS 对pH具有荧光猝灭响应识别作用,荧光峰强度发生变化.
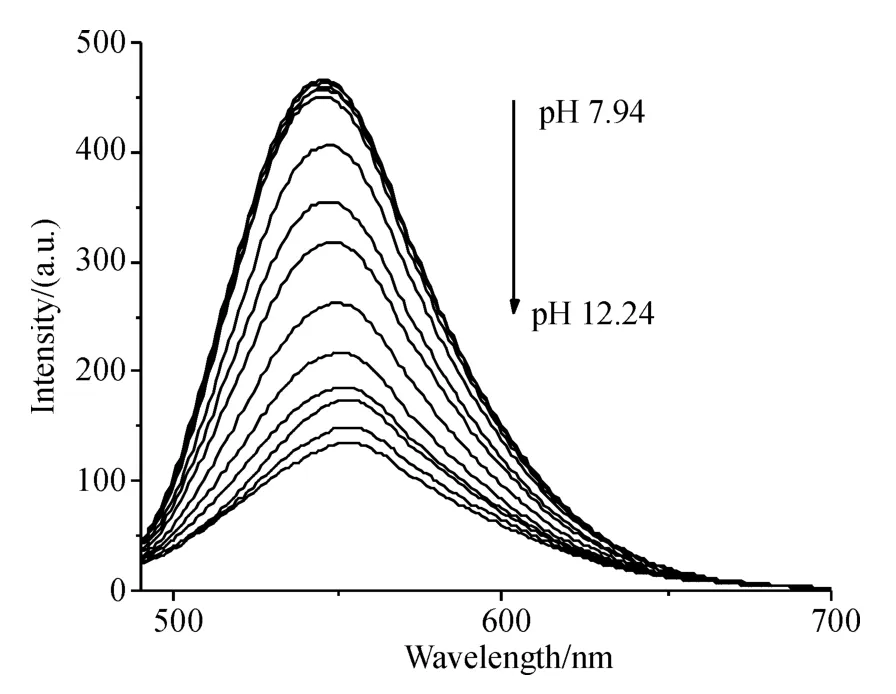
图4 不同pH 下FSS 的荧光光谱Figure 4 Fluorescence emission spectra of FSS at different pHs
根据pKa=pH +lg[(Fmax-F)/(F-Fmin)][16]计算出FSS 的pKa(图5),FSS 的pKa为10.64. 结果说明,FSS 在碱性pH 范围内能很好地检测溶液的pH 值,FSS 可作为一种对OH-有识别作用的灵敏的“荧光猝灭型”pH 探针.
2.3 FSS 荧光响应的可逆性
荧光探针的可逆性也被检测,在上述强碱性FSS 溶液中滴加盐酸调整pH 值使之逐渐变小,同时测试FSS 的荧光发射光谱. 随着pH 从强碱性到弱碱性的逐渐变化,荧光强度逐渐增强,在pH 为9.57时其荧光强度基本与初始测试状态的荧光强度保持一致,并且溶液的颜色也从黄色变回橙红色. 这样的结果说明FSS 对pH 的响应具有可逆性.

图5 FSS 的最大荧光发射峰的强度与pH 值的关系以及pKaFigure 5 Intensity of the strongest fluorescence emission peak of FSS at different pHs and pKa
3 结论
采用色氨酸与4-氯-7-硝基苯并呋咱合成了一种水溶性良好的荧光探针——7-硝基苯并呋咱色氨酸(FSS),并表征了它的结构. 通过测试紫外-可见光谱和荧光发射光谱,发现FSS 在碱性条件下对水溶液的pH 值表现出紫外光谱的比率型变化和荧光猝灭型双重识别响应,并且颜色有明显的从橙红到黄的转变.计算得到pKa为10.64,说明它能应用于碱性pH 的检测,同时它也能够用于pH 值的重复测量,是一种碱性pH 值探针.
[1]Roos A,Boron W F. Intracellular pH[J]. Physiological Reviews,1981,61(2):296-434.
[2]Casciari J J,Sotirchos S V,Sutherland R M. Variations in tumor cell growth rates and metabolism with oxygen concentration,glucose concentration,and extracellular pH[J]. Journal of Cellular Physiology,1992,151(2):386-394.
[3]Mobasheri A,Mobasheri R,Francis M J O,et al. Ion transport in chondrocytes:Membrane transporters involved in intracellular ion homeostasis and the regulation of cell volume,free[Ca2+]and pH[J]. Histology and Histopathology,1998,13(3):893-910.
[4]Kaplan D R,Miller F D. Neurotrophin signal transduction in the nervous system[J]. Current Opinion in Neurobiology,2000,10(3):381-391.
[5]Waddell W J,Butler T C. Calculation of intracellular pH from the distribution of 5,5-dimethyl-2,4-oxazolidinedione (DMO). Application to skeletal muscle of the dog[J]. Journal of Clinical Investigation,1959,38(5):720-729.
[6]Webb B A,Chimenti M,Jacobson M P,et al. Dysregulated pH:A perfect storm for cancer progression[J]. Nature Reviews Cancer,2011,11(9):671-677.
[7]Davies T A,Fine R E,Johnson R J,et al. Non-age related differences in thrombin responses by platelets from male patients with advanced Alzheimer's Disease[J]. Biochemical and Biophysical Research Communications,1993,194(1):537-543.
[8]Plette A C C,van Riemsdijk W H,Benedetti M F,et al.pH dependent charging behavior of isolated cell walls of a gram-positive soil bacterium[J]. Journal of Colloid and Interface Science,1995,173(2):354-363.
[9]苏美红,聂丽华,马会民. pH 荧光探针的研究进展[J]. 分析科学学报,2005,21(2):210-214.Su M H,Nie L H,Ma H M. Progress of pH fluorescence probes[J]. Journal of Analytical Science,2005,21(2):210-214.
[10]马立军.基于氨基酸的重金属离子荧光探针的设计、合成、及识别机理[D]. 长春:吉林大学,2008.
[11]Song P,Chen X,Xiang Y,et al. A ratiometric fluorescent pH probe based on aggregation-induced emission enhancement and its application in live-cell imaging[J].Journal of Materials Chemistry,2011,21(35):13470-13475.
[12]Liu X D,Xu Y,Sun R,et al. A coumarin-indole-based near-infrared ratiometric pH probe for intracellular fluorescence imaging[J]. Analyst,2013,138(21):6542-6550.
[13]Ghosh P B,Whitehouse M W. Potential antileukemic and immunosuppressive drugs. Preparation and in vitro pharmacological activity of some 2,1,3-benzoxadiazoles(benzofurazans)and their N-oxides (benzofuroxans)[J].Journal of Medicinal Chemistry,1968,11(2):305-311.
[14]李洪伟.基于磺酰胺基团的汞离子荧光探针的设计、合成及识别机理研究[D].长春:吉林大学,2009.
[15]Jiang W,Fu Q,Fan H,et al. A highly selective fluorescent probe for thiophenols[J]. Angewandte Chemie,2007,119(44):8597-8600.
[16]Bissell R A,de Silva A P,Gunaratne H Q N,et al. pKawas calculated by the equation:pKa=pH +lg[(Fmax-F)/(F-Fmin)][J]. Chemical Society Reviews,1992,21:187-195.
