T4期鼻咽癌适形调强放疗联合化疗的疗效及预后分析
2015-12-02罗杨坤杨桄权郎锦义
罗杨坤,高 扬,杨桄权,郎锦义△
(1.四川省肿瘤医院放疗中心,成都 610041;2.四川省自贡市第四人民医院放疗科,四川自贡 643000)
鼻咽癌(nasopharyngeal carcinoma,NPC)是中国南方常见的头颈部恶性肿瘤[1]。放疗是NPC治疗的主要手段。早期NPC单纯放疗的5年总生存率约90%[2]。但是大多数患者就诊时已经表现为局部晚期。根据AJCC 2010版分期[3],T4期定义为肿瘤侵犯颅内,和或颅神经侵犯;侵犯下咽;眼眶,或侵犯颞下窝/咀嚼肌间隙。由于邻近危及器官如脊髓,脑干,T4期NPC的放疗常受到剂量限制,传统二维放疗的局部区域控制率较差。适形调强放疗(intensity-modulated radiotherapy,IMRT)由于剂量学优势逐渐取代了二维放疗,其联合化疗取得了较高的局部控制率[4-6]。但是提高的局部控制率并未平行相应的提高总生存率。放化疗不同组合方案的研究结果[7-11]均得出了较高的局部控制率,但是总生存率尤其是远处转移仍然不理想。目前,分析T4期NPC的适形调强放疗的研究较少;而再程调强放疗(IMRT replanning)是近年来研究较多的IMRT治疗模式,但几乎没有长期研究随访结果说明其是否临床获益。本研究回顾性总结我院110例T4患者IMRT的远期疗效,并分析其预后因素。
1 材料与方法
1.1 一般资料
纳入2005年3月至2010年3月在我院初治的,无远处转移的110例T4期NPC患者110例。治疗前辅助检查包括:血常规,生化,内窥镜,头颈部MRI,胸部CT或胸片,腹盆B超,骨扫描。所有患者诊断均经病理学证实。T分期根据AJCC2010版确定。患者临床特点总结见表1。
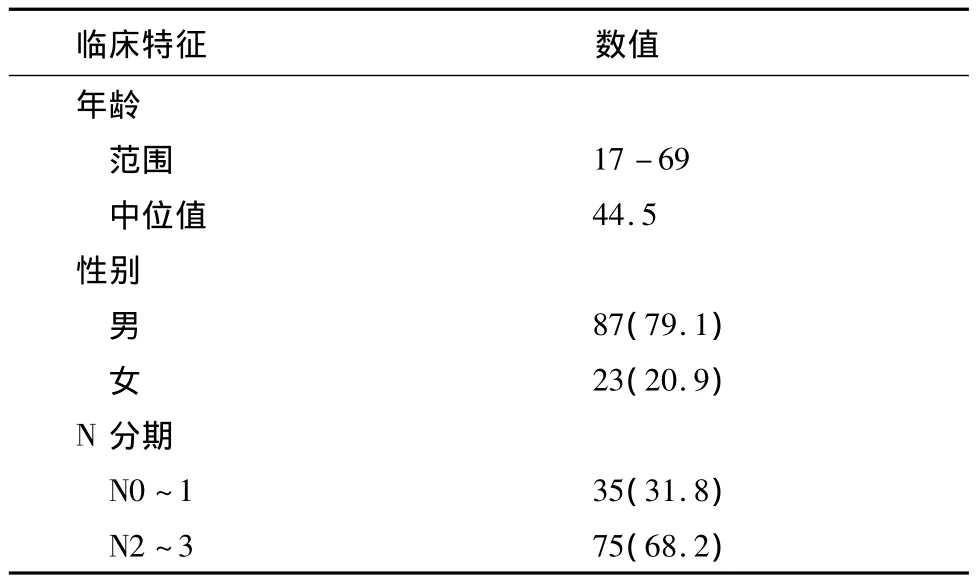
表1 110例T4期鼻咽癌的临床特点

临床特征 数值GTVnx volume范围 22.37-246.10中位值 77.27 GTVln volume范围 0-180.15中位值 14.1化疗同步化疗 75(68.2)诱导+同步化疗 35(31.8)IMRT replanning否63(57.3)是47(42.7)靶向治疗否83(75.5)是27(24.5)咽后淋巴结转移否13(11.8)是97(88.2)淋巴结坏死否68(61.8)是42(38.2)
1.2 治疗方案
1.2.1 适形调强放疗 所有患者均接受适形调强放疗。放射治疗靶区规定参照ICRU50号及62号标准。放疗计划的设计和优化采用CORVUS 3.4-4.2逆向计划系统。GTVnx(原发灶)及GTVln(阳性淋巴结)勾画以CT和或MRI为基础。高危亚临床靶区(CTV1)包括GTVnx外扩5~10mm范围以及高危区域。低危亚临床靶区包括可能侵犯的区域,一般包括整个鼻咽腔,上颌窦,翼腭窝,后组筛窦,咽旁间隙,颅底,斜坡前1/3,蝶窦底部,海绵窦等。CTVln包括淋巴结引流区域(双侧咽后淋巴结,II区,III区和 Va区)。剂量:GTVnx:66~76 Gy;GTVln:60~70 Gy;CTV1:60~66Gy;CTV2:54~60Gy;CTVln:50~54Gy,照射30~33次,使用同步加量的方法。危及器官限制标准参考RTOG0225试验。下颈淋巴结引流区采用60Co或者6 MV X线照射,剂量46~50 Gy,阳性淋巴结采用电子线加量照射至60~70 Gy。适形调强放疗采用每天1次,每周5次的照射方法。
1.2.2 再程调强放疗 47例(42.7%)患者接受中位值为3次的再程放疗计划。是否进行再程计划由医师决定,并参考以下因素:体重丢失,营养状态,可触及或可见的肿块变化,颈肩膜固定情况以及急性放疗反应。当肿瘤邻近重要危及器官,如脑干,脊髓或者其他重要器官的时候,再程放疗常需早期介入并且可能需要多程的再计划。当肿瘤需要加量放疗时候,常规进行一次再程计划。所有再程计划均需重新进行CT扫描并保持相同体位,使用新扫描的CT制作新计划并执行相应的放疗次数。为保证靶区勾画的相对一致性,使用刚性配准并以感兴趣区手动调整进行新CT与初始CT融合。在新CT上勾画GTVnx,GTVln和正常器官。CTV应保持一致性但需根据肿瘤解剖结构的变化进行调整。从新CT扫描到执行新的再程计划的时间为1~3天。本研究中第一次再程计划的中位剂量为44Gy(8.8~57.2Gy)。
1.2.3 化疗 包括诱导+同步化疗或同步化疗。所有患者均接受顺铂为基础的化疗方案,均未接受辅助化疗。诱导化疗方案包括1~2周期的TP方案(多西他赛 60 mg/m2·d-1,d1,顺铂30mg/m2·d-1,d1~3)或 PF 方案(顺铂 30mg/m2·d-1,d1~3+5-Fu 750mg/m2·d-1,d1~5)。同步化疗行2~3周期化疗,方案包括单铂方案(顺铂80mg/m2,d1,3周1疗程)。TP及PF方案同诱导化疗方案。27(24.5%)例患者接受 Cetuximab或 Nimotuzumab靶向治疗。
1.3 随访及统计学方法
所有患者治疗中每周进行评估。治疗后按以下进行随访:放疗后1月,放疗后2年内每3个月,放疗后3~5年每6个月,之后每年随访1次。随访内容包括鼻咽纤维镜,腹部B超,胸片,血常规及生化;头颈部CT或MRI。采用SPSS 16.0进行统计分析。生存指标均从治疗日期第一天开始计算。Kaplan-Meier法计算 LRFS、RRFS、DMFS、PFS 和 OS。单因素分析采用log-rank test。多因素分析采用Cox回归模型。P <0.05认为差异具有统计学意义。
2 结果
2.1 生存情况
中位随访58个月(12~120个月)。全组患者5 年 LRFS,RRFS,DMFS,PFS 和 OS 分别为90.1%,97.0%,67.5%,63.9% 和 64.5%(图1)。是否IMRT replanning的患者 5年 LRFS分别为 97.7%和83.8%(P=0.023)(图 2A,表 2)。咽后淋巴结未转移和转移患者5年OS分别为91.7% 和61.0%(P=0.034)(图 2B,表 2)。GTVln≤14.1cc 和GTVln>14.1cc患者5年 DMFS,PFS和 OS分别为79.0%和 56.1%(P=0.007);73.1% 和 55.0%(P=0.021),75.6% 和53.0%(P=0.028)(图 3,4,5)。

图1 110例T4期鼻咽癌患者的5年LRFS,RRFS,DMFS,PFS 和 OS
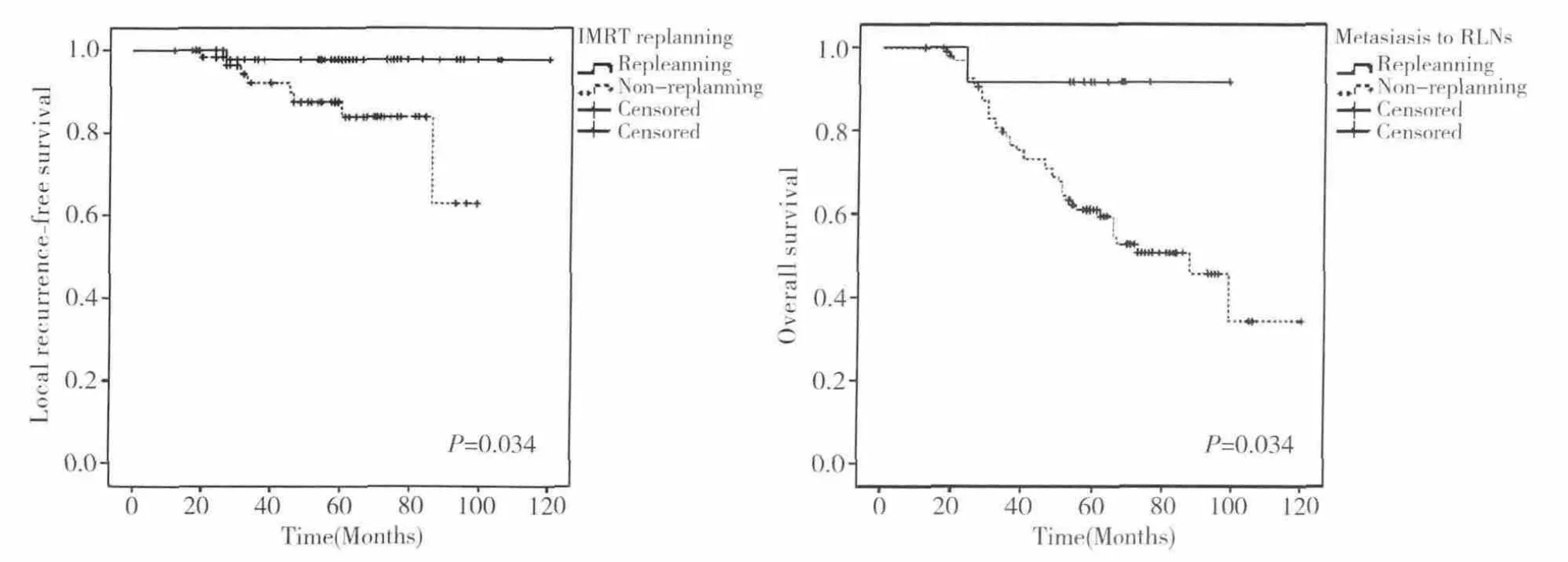
图2 A:接受IMRT replanning与non replanning患者LRFS曲线,B:咽后淋巴结转移与未转移患者OS曲线
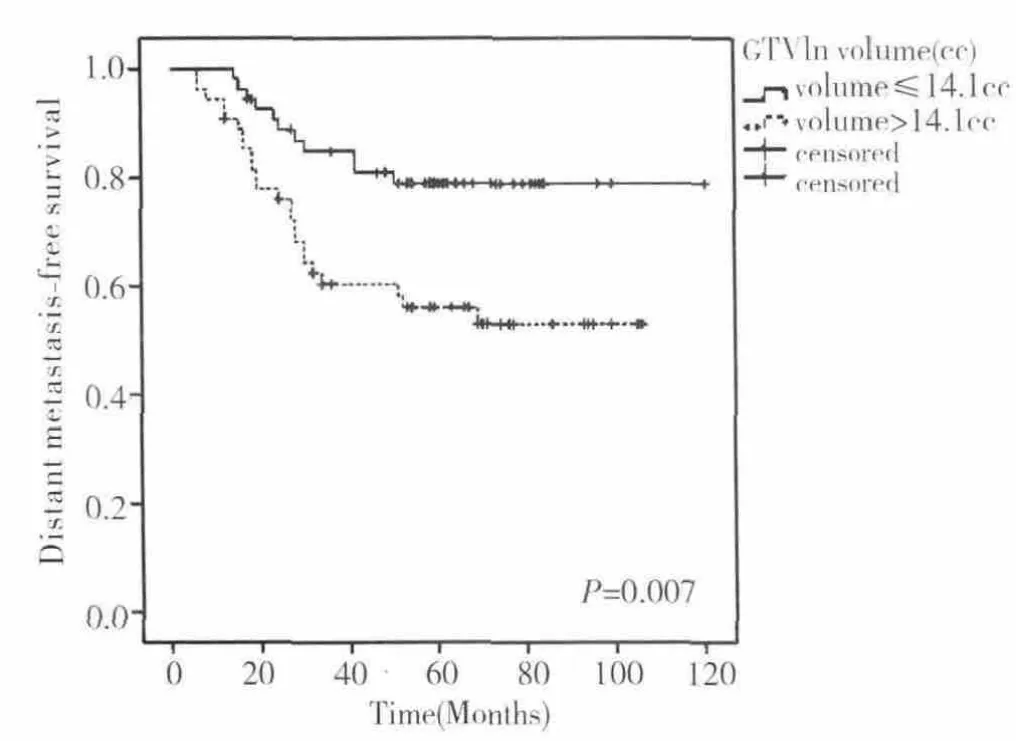
图3 GTVln volume≤14.1 cc 与GTVln volume>14.1 cc患者 DMFS曲线

图4 GTVln volume≤14.1 cc 与GTVln volume>14.1 cc患者 PFS曲线
共有45例患者死亡,其中5例死于鼻咽部大出血,1例死于鼻咽部大出血伴局部区域复发,5例患者死于不明原因内科疾病,5例死于局部区域复发,3例死于局部区域复发和远处转移,26例患者死于远处转移。共有41例(37.3%)治疗失败,包括30例远处转移,5例局部复发,2例区域复发,3例局部复发伴远处转移,1例区域复发伴远处转移。
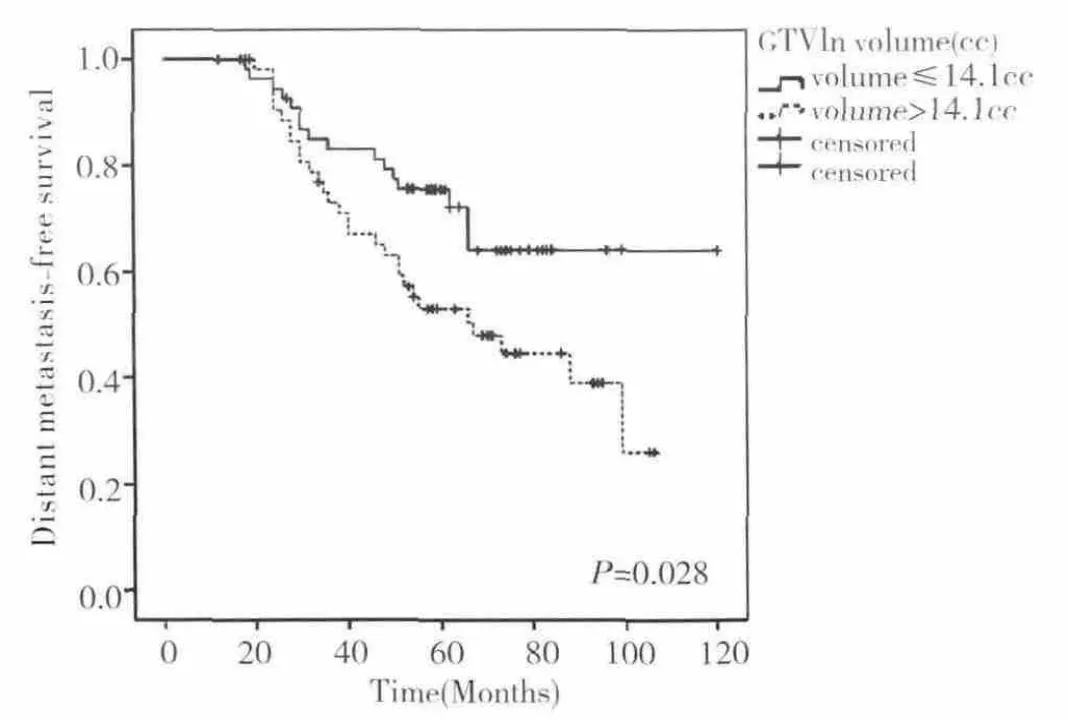
图5 GTVln volume≤14.1 cc与GTVln volume>14.1 cc患者 OS曲线
2.2 预后因素
将年龄、性别、N 分期、GTVnx volume、GTVln volume、化疗方案、IMRT replanning、靶向治疗、咽后淋巴结转移、淋巴结坏死等纳入单因素分析显示GTVln volume与 DMFS,PFS和 OS相关,IMRT replanning与LRFS相关,咽后淋巴结与OS相关(表2)。多因素分析显示GTVln volume是DMFS,PFS独立预后因素(HR=2.718,95%CI 1.324~5.577,P=0.006;HR=2.159,95%CI 1.141~4.088,P=0.018)。而 GTVln volume具有影响 OS的趋势(HR=1.875,95%CI 1.001~3.512,P=0.050)。

表2 110例T4期鼻咽癌PFS和OS的单因素分析
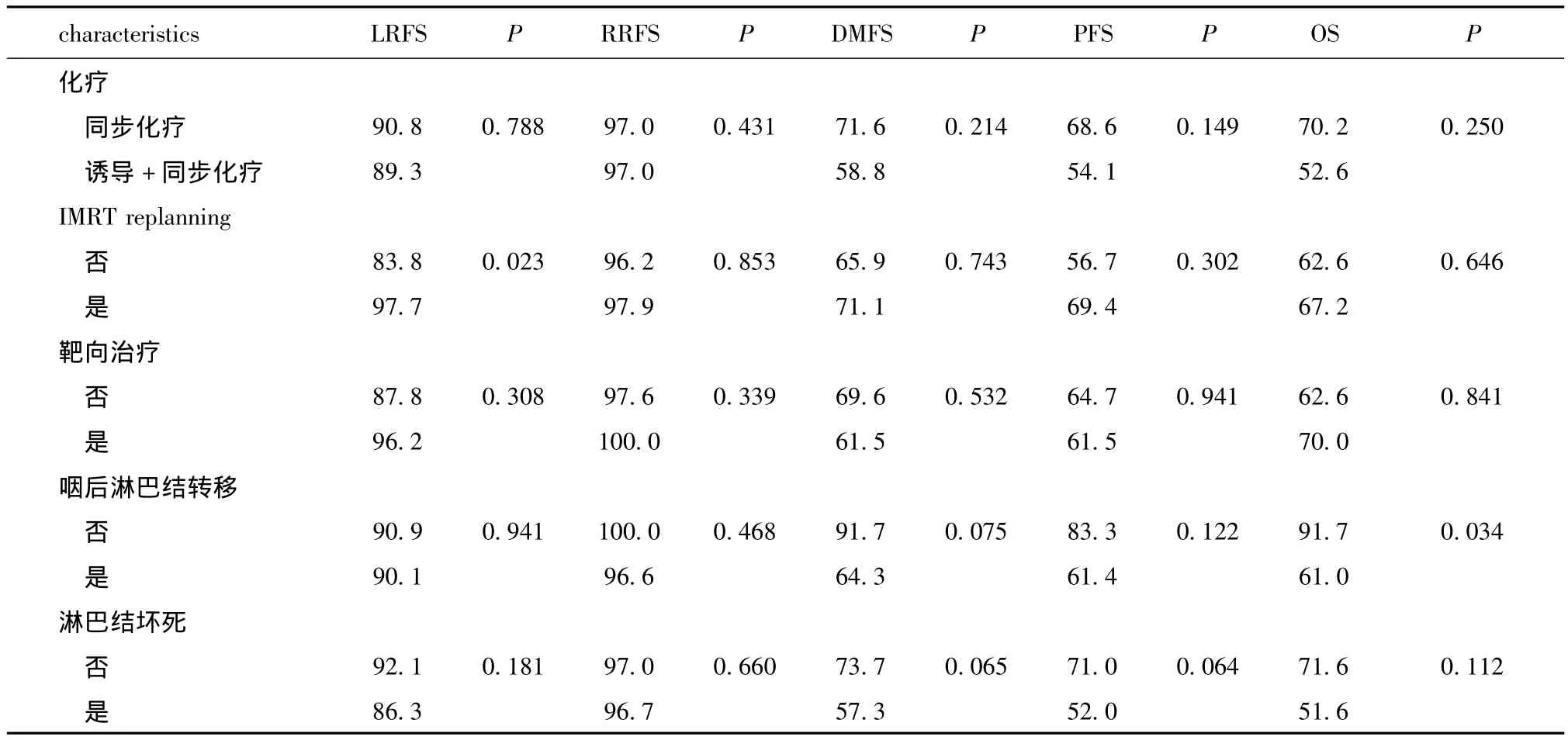
characteristics LRFS P RRFS P DMFS P PFS P OS P化疗同步化疗 90.8 0.788 97.0 0.431 71.6 0.214 68.6 0.149 70.2 0.250诱导 + 同步化疗 89.3 97.0 58.8 54.1 52.6 IMRT replanning否83.8 0.023 96.2 0.853 65.9 0.743 56.7 0.302 62.6 0.646是97.7 97.9 71.1 69.4 67.2靶向治疗否87.8 0.308 97.6 0.339 69.6 0.532 64.7 0.941 62.6 0.841是96.2 100.0 61.5 61.5 70.0咽后淋巴结转移否90.9 0.941 100.0 0.468 91.7 0.075 83.3 0.122 91.7 0.034是90.1 96.6 64.3 61.4 61.0淋巴结坏死否92.1 0.181 97.0 0.660 73.7 0.065 71.0 0.064 71.6 0.112是86.3 96.7 57.3 52.0 51.6
3 讨论
IMRT由于具有给予肿瘤高剂量以及保护危及器官的优势已经取代二维常规放疗,提高了疗效尤其是局部区域控制率。Chen等[12]报道了140例T4期NPC经IMRT的结果,5年OS、无局部失败生存率(local relapse-free survival,LRFS)和 DMFS 分别为 69.3%、84.9% 和 73.6%。另一研究[13]包括了335例T4期NPC的5年局部无失败生存率(local failure-free survival,LFFS)、区域无失败生存率(regional failure free-survival,RFFS)、无远处转移生存率(distant failure-free survival,DFFS)和 OS 分别为84.1%、92.2%、74.1% 和 63.0%。Sun 等[6]报道 5年疾病特异性生存率(disease specific survival,DSS)、DMFS、LRFS、PFS 分别为 70.7%、71.7%、83.3%和 59.8%。本研究显示全组 5年 LRFS、RRFS、DMFS、PFS 和 OS 分 别 90.1%、97.0%、67.5%、63.9%和 64.5%。与前述研究结果相似。本研究结果显示远处转移是治疗失败的主要原因和导致死亡的主要原因,而局部区域复发率很低,与其他调强放疗的研究结果类似[5,6,14-16]。所以,尽管IMRT能达到较好的局部控制,但是这种优势并不是平行地转化为生存优势。既往研究[17]显示淋巴结状态是远处转移和总生存的预测指标。当前淋巴结状态的研究常包括淋巴结大小及引流水平,淋巴结包膜外侵犯(extranodal neoplastic spread,ENS),淋巴结坏死,咽后淋巴结转移等[6,17-20]。本研究结果的单因素分析显示咽后淋巴结转移与OS相关(P=0.034)。而淋巴结坏死具有影响DMFS和PFS的趋势(P=0.065;P=0.064)。N分期具有影响OS的趋势 (P=0.087)。多因素分析显示GTVln volume是DMFS和PFS的独立预后因素(P=0.006;P=0.018),并具有影响 OS的趋势 (P=0.050)。众所周知,鼻咽癌具有较高的微转移的可能性。咽后淋巴结转移和较大的GTVln体积意味着转移几率高。而淋巴结坏死也与较高的N分期相关[19]。所以肿瘤负荷可能比单纯的N分期更为重要。因为IMRT能达到较好的局部控制而不能消除在治疗前已经存在的微转移灶,所以导致了高局控率和高转移率。因此,对于T4期NPC,将GTVln volume整合到现有的N分期中,可能具有更高的预测价值,但是需要扩大样本做进一步研究。
与传统二维放疗相比,IMRT的生存获益主要来自于局控率的提高[21]。自适应放疗(adaptive radiotherapy,ART)是近年来研究较多的IMRT治疗模式,其目的是确保肿瘤靶区的覆盖,通过降低正常组织剂量提高治疗后生存质量[22-26]。为纠正肿瘤和正常组织的在分次放疗中的变化,常需要在相应的时间点获得在线或离线影像修改放疗计划。我院较早开展自适应再程调强放疗技术(adaptive IMRT replanning)。根据疗程中热塑颈肩膜固定状态,临床医师每周查体,以及肿瘤侵犯的范围等因素,采用离线影像引导进行多程再计划。第一程再程调强放疗计划的中位剂量为44Gy。完成再程计划的次数的中位值为3次。尽管没有标准的规范确定是否进行再程调强放疗以及其介入时间,但本研究结果显示,与未接受再程调强放疗相比,接受再程调强放疗的患者能获得更好的局部控制率(97.7% VS.83.8%,P=0.023),但 DMFS,PFS 和 OS 均无统计学意义,与既往研究相似[22-23,26]。限制于本研究较小的样本含量,再程调强放疗对局部控制的获益能否转化为总生存获益尚需扩大样本,开展前瞻性随机对照试验进一步研究。
根据NCCN指南,局部晚期NPC的治疗方案包括同步放化疗伴或不伴随辅助化疗;诱导化疗+同步放化疗。诱导化疗能杀灭更多的局部病灶和可能的远处微转移灶,并通过降低肿瘤负荷减轻放疗副作用。然而,本研究显示与同步化疗相比,诱导化疗在 LRFS、RRFS、DMFS、PFS 和 OS 中差异均无统计学意义。但是最近一项Meta分析[27]显示局部晚期NPC中诱导化疗可以显著减少疾病进展和远处转移。另外一个选择是加入辅助化疗,一项基于Bayesian network的 Meta分析[28]显示辅助化疗不能提高生存,而MAC-NPC的Meta分析[29]却显示同步化疗后加入辅助化疗的模式在所有模式中的对肿瘤相关的疗效作用最大。因此在当今研究中,诱导或辅助化疗的结论多样且相互矛盾。本研究结果还显示使用靶向治疗并无获益。这也可能与本研究样本量较小有关。不管怎样,对于T4期NPC,最佳治疗模式还需要进一步研究。
本研究具有以下缺点,包括回顾性研究的本质以及较小的样本量。医疗数据以及影像资料的问题导致一些具有潜在可能的预后因素如颅神经侵犯,颅底颅内侵犯范围等未被纳入研究。这些因素可能会影响本研究的结果。另外,本研究并未对IMRT再程计划做剂量学研究以及未做患者治疗毒性和生活质量的分析。但是,本研究所有患者均接受铂类为基础的化疗,并采用当前流行的治疗模式(同步放化疗或诱导+同步放化疗),以及较长的随访年限并得出了再程调强放疗对T4期鼻咽癌的临床局部控制获益。所以本研究具有一定的价值。
综上,适形调强放疗联合化疗治疗T4期鼻咽癌的局部区域控制可。IMRT再程调强放疗的获益与局控率提高相关。GTVln volume是影响生存的独立预后因素。远处转移是治疗失败的主要模式,降低远处转移率和增加生存率的治疗方案应该进一步探索。
[1] Chan AT,Teo PM,Johnson PJ.Nasopharyngeal carcinoma[J].Ann Oncol,2002,13(7):1007-1015.
[2] Chan AT,Leung SF,Ngan RK,et al.Overall survival after concurrent cisplatin-radiotherapy compared with radiotherapy alone in locoregionally advanced nasopharyngeal carcinoma[J].J Natl Cancer Inst,2005,97(7):536-539.
[3] Edge SB,Compton CC.The American Joint Committee on Cancer:the 7th edition of the AJCC cancer staging manual and the future of TNM[J].Ann Surg Oncol,2010,17(6):1471-1474.
[4] Kam MK,Teo PM,Chau RM,et al.Treatment of nasopharyngeal carcinoma with intensity-modulated radiotherapy:the Hong Kong experience[J].Int J Radiat Oncol Biol Phys,2004,60(5):1440-1450.
[5] Lee N,Harris J,Garden AS,et al,Intensity-modulated radiation therapy with or without chemotherapy for nasopharyngeal carcinoma:radiation therapy oncology group phase II trial 0225[J].J Clin Oncol,2009,27(22):3684-3690.
[6] Sun X,Su S,Chen C,et al.Long-term outcomes of intensitymodulated radiotherapy for 868 patients with nasopharyngeal carcinoma:an analysis of survival and treatment toxicities[J].Radiother Oncol,2014,110(3):398-403.
[7] Bae W,Hwang J,Shim H,et al.Phase II study of docetaxel,cisplatin,and 5-FU induction chemotherapy followed by chemoradiotherapy in locoregionally advanced nasopharyngeal cancer[J].Cancer Chemother Pharmacol,2010,65(3):589-595.
[8] Chen L,Hu CS,Chen XZ,et al.Concurrent chemoradiotherapy plus adjuvant chemotherapy versus concurrent chemoradiotherapy alone in patients with locoregionally advanced nasopharyngeal carcinoma:a phase 3 multicenter randomised controlled trial[J].Lancet Oncol,2012,13(2):163-171.
[9] Fountzilas G,Ciuleanu E,Bobos M,et al.Induction chemotherapy followed by concomitant radiotherapy and weekly cisplatin versus the same concomitant chemoradiotherapy in patients with nasopharyngeal carcinoma:a randomized phase II study conducted by the Hellenic Cooperative Oncology Group(HeCOG)with biomarker evaluation[J].Ann Oncol,2012,23(2):427-435.
[10] Hui EP,Ma BB,Leung SF,et al.Randomized phase II trial of concurrent cisplatin-radiotherapy with or without neoadjuvant docetaxel and cisplatin in advanced nasopharyngeal carcinoma[J].J Clin Oncol,2009,27(2):242-249.
[11] Lee AW,Tung SY,Chua DT,et al.Randomized trial of radiotherapy plus concurrent-adjuvant chemotherapy vs radiotherapy alone for regionally advanced nasopharyngeal carcinoma[J].J Natl Cancer Inst,2010,102(15):1188-1198.
[12] Chen L,Liu LZ,Chen M,et al.Prognostic value of subclassification using MRI in the t4 classification nasopharyngeal carcinoma intensity-modulated radiotherapy treatment[J].Int J Radiat Oncol Biol Phys,2012,84(1):196-202.
[13] Cao CN,Luo JW,Gao L,et al.Update report of T4 classification nasopharyngeal carcinoma after intensity-modulated radiotherapy:an analysis of survival and treatment toxicities[J].Oral Oncology,2015,51(2):190-194.
[14] Lee N,Xia P,Quivey JM,et al.Intensity-modulated radiotherapy in the treatment of nasopharyngeal carcinoma:an update of the UCSF experience[J].Int J Radiat Oncol Biol Phys,2002,53(1):12-22.
[15] Lin S,Lu JJ,Han L,et al.Sequential chemotherapy and intensity modulated radiation therapy in the management of locoregionally advanced nasopharyngeal carcinoma:experience of 370 consecutive cases[J].BMC Cancer,2010,10:39.doi:10.1186/1471-2407-10-39.
[16] Wong FC,Ng AW,Lee VH,et al.Whole-field simultaneous integrated-boost intensity-modulated radiotherapy for patients with nasopharyngeal carcinoma[J].Int J Radiat Oncol Biol Phys,2010,76(1):138-145.
[17] Mao YP,Liang SB,Liu LZ,et al.The N staging system in nasopharyngeal carcinoma with radiation therapy oncology group guidelines for lymph node levels based on magnetic resonance imaging[J].Clin Cancer Res,2008,14(22):7497-7503.
[18] Lee AW,Ng WT,Chan LL,et al.Evolution of treatment for nasopharyngeal cancer-success and setback in the intensity-modulated radiotherapy era[J].Radiother Oncol,2014,110(3):377-384.
[19] Lan M,Huang Y,Chen CY,et al.Prognostic value of cervical nodal necrosis in Nasopharyngeal carcinoma:analysis of 1 800 patients with positive cervical nodal metastasis at MR imaging[J].Radiology,2015,276(2):619.
[20] Tang LL,Guo R,Zhou G,et al.Prognostic value and staging classification of retropharyngeal lymph node metastasis in nasopharyngeal carcinoma patients treated with intensity-modulated radiotherapy[J].PLoS One,2014,10,9(10):e108375.
[21] Lai SZ,Li WF,Chen L,et al.How does intensity-modulated radiotherapy versus conventional two-dimensional radiotherapy influence the treatment results in nasopharyngeal carcinoma patients[J].Int J Radiat Oncol Biol Phys,2011,80(3):661-668.
[22]Chen AM,Daly ME,Cui J,et al.Clinical outcomes among patients with head and neck cancer treated by intensity-modulated radiotherapy with and without adaptive replanning[J].Head Neck,2014,36(11):1541-1546.
[23] Yang H,Hu W,Wang W,et al.Replanning during intensity modulated radiation therapy improved quality of life in patients with nasopharyngeal carcinoma[J].Int J Radiation Oncol Biol Phys,2013,85(1):e47-54.
[24]Wang W,Yang H,Hu W,et al.Clinical study of the necessity of replanning before the 25th fraction during the course of intensitymodulated radiotherapy for patients with nasophryngeal carcinoma[J].Int J Radiation Oncol Biol Phys,2010,77(2):617-621.
[25] Nishi T,Nishimura Y,Shibata T,et al.Volume and dosimetric changes and initial clinical experience of a two-step adaptive intensity modulated radiation therapy(IMRT)scheme for head and neck cancer[J].Radiother Oncol,2013,106(1):85-89.
[26] Zhao L,Wan Q,Zhou Y,et al.The role of replanning in fractionated intensity modulated radiotherapy for nasopharyngeal carcinoma[J].Radiother Oncol,2011,98(1):23-27.
[27] Song Y,Wang W,Tao G,et al.Survival benefit of induction chemotherapy in treatment for locally advanced nasopharyngeal carcinoma-a time-to-event meta-analysis[J].Oral Oncology,2015,51(8):764-769.
[28] Yan M,Kumachev A,Siu LL,et al.Chemoradiotherapy regimens for locoregionally advanced nasopharyngeal carcinoma:a Bayesian network meta-analysis[J].European Journal of Cancer,2015,51(12):1570-1579.
[29] Blanchard P,Lee A,Marguet S,et al.Chemotherapy and radiotherapy in nasopharyngeal carcinoma:an update of the MAC-NPC meta-analysis[J].Lancet Oncol,2015,16(6):645-655.
