Cu(Ⅱ)助剂与石墨烯协同增强AgBr可见光光催化性能
2015-12-01王明芳徐顺秋李小争
王明芳 王 苹 徐顺秋 李小争
(武汉理工大学化学化工与生命科学学院化学系,武汉430070)
Cu(Ⅱ)助剂与石墨烯协同增强AgBr可见光光催化性能
王明芳 王 苹*徐顺秋 李小争
(武汉理工大学化学化工与生命科学学院化学系,武汉430070)
采用简单、低温的溶液浸渍法制备了Cu(Ⅱ)助剂和石墨烯共修饰的高效AgBr可见光光催化剂。降解甲基橙的实验结果表明:经Cu(Ⅱ)助剂与石墨烯协同修饰后的AgBr表现出很好的降解性能,其中Cu(Ⅱ)(0.5 mol·L-1)/AgBr-rGO(0.5wt%)具有最高性能(rGO代表还原石墨烯),速率常数是0.027 31 min-1,是AgBr(0.008 07 min-1)的3.38倍、AgBr-rGO(0.5%)(0.015 98 min-1)的1.7倍、Cu(Ⅱ)(0.5 mol·L-1))/AgBr(0.015 19 min-1)的1.8倍。Cu(Ⅱ)助剂与石墨烯复合协同作用增强光催化性能的原因是:Cu(Ⅱ)易于捕获光生电子,石墨烯比表面积大,可为Cu(Ⅱ)提供更多的还原位点,加快了AgBr上的光生电子-空穴对的有效分离。本研究可以为制备高性能AgBr光催化剂提供新的思路。
AgBr;Cu(Ⅱ)助剂;石墨烯;协同作用;可见光光催化性能
光催化技术因高效降解有机污染物、清洁无污染的优点,已广泛应用于环境治理领域[1]。在半导体光催化材料中,传统的TiO2由于化学性质稳定、无二次污染而受到关注[2]。但是,它的带隙较宽,只能利用约占太阳光能量5%的紫外光,无法利用太阳光中可见光[3-4]。因此,寻找能利用可见光的光催化剂成为研究的重点[5-7]。最近,很多研究证明银类化合物是一类新型高效的可见光光催化材料,在光催化降解水中有机污染物的过程中,往往表现出比传统TiO2更高的光催化活性[8-10]。为了进一步提高银类光催化剂的性能,发展各种改性方法是非常重要的研究课题。
一方面,离子助剂修饰光催化剂是提高光催化性能的有效方法之一[11-13]。作者所在课题组之前的工作采用低温离子注入法以Cu(Ⅱ)和Fe(Ⅱ)修饰银类化合物以提高其催化性能[12-13]。降解甲基橙的实验表明,经Fe(Ⅱ)修饰的AgBr最高性能是AgBr的2.35倍[12],经Cu(Ⅱ)修饰的AgCl最高性能是AgCl的2.1倍[13]。其基本原理是:当银类化合物表面经过渡金属离子改性后,催化剂表面的光生电子易于被催化剂表面的过渡金属离子捕获,再与空气中的氧气反应,使银类化合物上的光生电子-空穴对得到有效分离,因而Cu(Ⅱ)/银类化合物复合可见光光催化剂具有更高的光催化活性。另一方面,很多研究证明石墨烯复合是提高光催化性能的一种有效方法[14-16]。我们之前的工作采用Ag离子与石墨烯复合再经FeCl3氧化,制备得到的Ag/AgCl-rGO性能是Ag/AgCl的2.0~2.4倍[14]。另有研究发现用油水微乳液法制备的Ag/AgBr-GO(GO指氧化石墨烯)对甲基橙的降解百分率最高达94%,远大于Ag/AgBr的62%[16]。石墨烯复合能提高光催化剂降解性能的主要原因是:石墨烯的比表面积大,可提供更多的活性位点,有很高的电子迁移率,能有效的转移光生电子并促进与空穴的分离。由上可知,离子助剂修饰和石墨烯复合都是提高光催化性能的有效方法,但目前还没有过渡金属离子和石墨烯协同作用来提高银类光催化剂可见光光催化性能的报道。
本研究为进一步提高AgBr的可见光光催化性能,利用简单、低温的溶液法制备了Cu(Ⅱ)助剂和石墨烯复合协同作用的高效Cu(Ⅱ)/AgBr-rGO复合可见光光催化剂。采用了XRD、XPS、FESEM、紫外光谱和拉曼光谱等测试手段对合成的复合催化剂进行表征,并测试了在可见光下降解甲基橙的光催化性能。最后,分析了Cu(Ⅱ)助剂和石墨烯复合协同作用下的光催化机理。
1 实验部分
1.1 主要试剂
Cu(NO3)2·3H2O、NaBr、AgNO3和抗坏血酸均为分析纯,购于上海化学试剂公司。所用水均为去离子水。氧化石墨稀(GO)溶液为本课题组制备,方法见文献[17]。
1.2 样品制备
1.2.1 AgBr
取1 mL 0.6 mol·L-1AgNO3溶液滴加到1 mL 0.6 mol·L-1NaBr溶液中,反应生成AgBr固体后,用去离子水洗涤3次,自然晾干后即得到0.1 g淡黄色AgBr粉末。
1.2.2 AgBr-rGO
将一定量石墨烯溶液滴加到1 mL 0.6 mol·L-1AgNO3溶液中,磁力搅拌45 min,使石墨烯充分吸附Ag+,形成Ag+-GO。再把1 mL 0.6 mol·L-1NaBr溶液滴加到上述溶液,静置得到沉淀即为原位生成的AgBr-GO固体。用去离子水洗涤3次,自然晾干后得到AgBr-GO样品。再加入0.1 g抗坏血酸,继续搅拌30 min,将产物用去离子水洗涤3~4次,室温晾干后,得到以抗坏血酸作为还原剂还原后的AgBrrGO复合光催化剂0.1 g。样品编号为AgBr-rGO (Xwt%),其中X为石墨烯的质量百分比。
1.2.3 Cu(Ⅱ)/AgBr-rGO
取0.05 g制备好的AgBr-rGO(0.5wt%)复合光催化剂,加入到不同浓度的Cu(NO3)2溶液中,磁力搅拌45 min,静置,用去离子水洗涤3次,室温晾干,得到产物。样品编号为Cu(Ⅱ)(Y)/AgBr-rGO,Y为Cu(NO3)2溶液的浓度。为了与Cu(Ⅱ)直接修饰AgBr的样品进行对比,用相同方法将0.05 g AgBr固体加入到0.5 mol·L-1Cu(NO3)2溶液中,所制备的样品编号为Cu(Ⅱ)(0.5 mol·L-1)/AgBr。
1.3 光催化性能测试
光催化性能测试参考文献[18]的方法进行。具体步骤如下:在室温下,称取0.05 g光催化剂置于干燥清洁的培养皿中(其直径为5 cm),加入10 mL浓度为20 mg·L-1甲基橙溶液。在黑暗中放置约1 h,使之达到吸附平衡。然后放置在可见光源为装有滤光片(滤去波长小于400 nm的紫外光)的氙灯下照射,平均光强为40 mW·cm-2。每照射3 min后,取上清液在波长553 nm用可见分光光度计(722N型,上海精密科学仪器有限公司)测定吸光度。由于甲基橙水溶液在较低浓度下的光催化降解反应属于准一级反应,反应物浓度(c)和反应时间(t)之间满足对数关系ln(c0/ct)=kt(其中c0和ct分别是初始浓度和反应到t时刻的浓度,k为速率常数),因此,可用降解甲基橙的速率常数k来评价光催化性能。
1.4 样品表征
采用日本Rigaku公司生产的D/Max-RB型X射线粉末衍射仪测定样品的晶相。利用USA-FEI公司的Quanta x50型场发射扫描电镜观察样品的形貌。利用日本Shimadzu公司生产的型号为UV-2450的紫外-可见分光光度计测定紫外-可见漫反射光谱,测试标样为BaSO4。采用英国Renishaw公司的INVIA拉曼光谱仪测定样品的拉曼光谱。采用英国Kratos Ltd公司生产的型号为VG Multilab 2000的XPS仪器测定X射线光电子能谱。
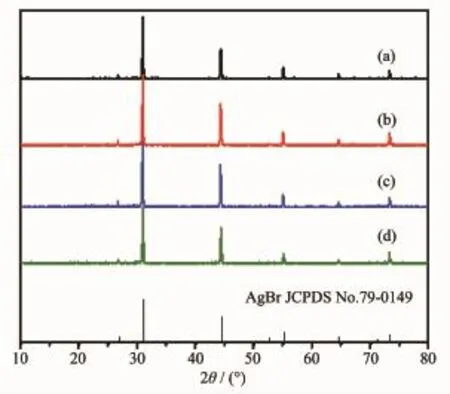
图1 不同样品的XRD图Fig.1XRD patterns of different samples

图2 不同样品的场发射扫描电镜图Fig.2FESEM images of different samples
2 结果与讨论
2.1 样品的结构和形貌分析
图1a是AgBr的XRD图,所有衍射峰都符合标准AgBr图谱(PDF文件卡号79-0149),可以确定合成的产物为AgBr。图1b和图1c分别是石墨烯复合和Cu(Ⅱ)修饰后AgBr的图谱,与图1a具有相同的衍射峰,说明低温下石墨烯复合和Cu(Ⅱ)助剂修饰都不影响AgBr的晶型。图1d是石墨烯和Cu(Ⅱ)协同作用后的AgBr图谱,由图谱可以看出AgBr的晶型没有发生变化。以上结果表明,石墨烯复合、Cu(Ⅱ)助剂修饰及两者协同修饰后的AgBr,具有与纯AgBr相同的XRD特征峰,说明石墨烯复合、Cu(Ⅱ)修饰以及两者协同修饰过程都不影响AgBr的晶型和晶化程度。
图2是不同样品的场发射扫描电镜图。从图2a可以看出AgBr是颗粒状的,颗粒大小范围在0.5~2 μm。从图2b可以发现,AgBr与石墨烯复合后颗粒大小变化不大,石墨烯薄纱状表面附着了大量的AgBr颗粒,表明AgBr与石墨烯成功复合。图2c是经Cu(Ⅱ)修饰后的AgBr颗粒,大小与AgBr相差不大,而且由插图中的EDS图也可以看出颗粒表面有微量的Cu元素存在。图2d是石墨烯和Cu(Ⅱ)共修饰后的AgBr,可以看到其颗粒大小与AgBr相近,AgBr颗粒分布在石墨烯表面,由插图中的EDS图同样也可以看出AgBr-rGO表面有微量的Cu元素存在。所以,扫描电镜图片为本研究成功制备了Cu(Ⅱ)助剂和石墨烯共修饰的Cu(Ⅱ)/AgBr-rGO光催化剂提供了有力的证据。
图3为不同样品的UV-Vis谱图。从图3a中可以看出,AgBr样品呈淡黄色,吸收边在480 nm左右。根据AgBr样品的紫外漫反射的曲线,可以计算出AgBr的禁带为2.54 eV,与文献报道的2.5 eV非常接近[19]。图3b是经石墨烯复合后的灰黑色AgBrrGO样品,吸收边蓝移,这可能是量子限域引起的[20]。图3c是样品Cu(Ⅱ)/AgBr,颜色和纯AgBr样品接近,两者的吸收边完全一样,说明用Cu(Ⅱ)修饰AgBr后并不影响AgBr对光谱的吸收。图3d是石墨烯和Cu(Ⅱ)协同作用后的AgBr,颜色也是灰黑色,其吸收边和AgBr-rGO基本一样。从图3b、d中可以看出,样品在480~630 nm之间有少量吸收。因此,由谱图可以看出,石墨烯复合后的AgBr在可见光区的吸收均有所增强,Cu(Ⅱ)(0.5 mol·L-1)/AgBr-rGO (0.5wt%)吸收最强。
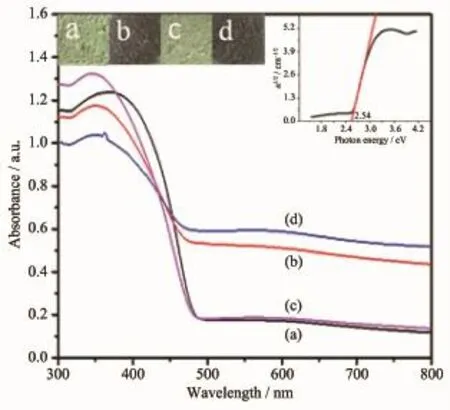
图3 不同样品的紫外漫反射光谱Fig.3UV-Vis diffuse reflectance spectra of different samples
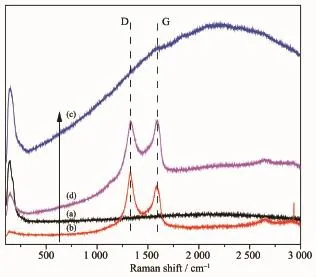
图4 不同样品的拉曼光谱Fig.4Raman spectra of different samples
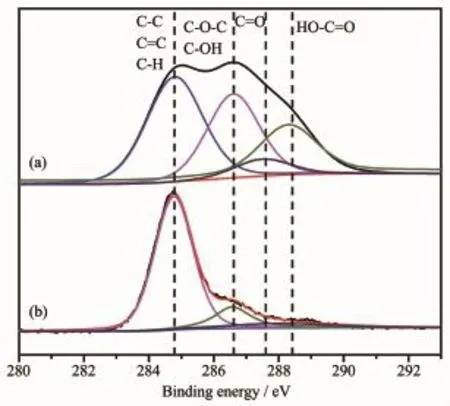
图5 不同样品的X射线光电子能谱Fig.5XPS spectra of different samples
图4的拉曼光谱可以提供石墨烯的结构信息。由文献[21]可知,石墨烯的拉曼光谱有D峰与G峰两个特征峰。图4a和图4c AgBr的拉曼曲线上没有D峰与G峰的存在。而从图4b及图4d可以分别看出AgBr-rGO和Cu(Ⅱ)/AgBr-rGO复合材料在1 327 cm-1和1 587 cm-1处有明显的D峰和G峰。因此,拉曼光谱中D峰与G峰的存在为石墨烯与AgBr成功复合提供了明确的证据,与之前扫描电镜结果相符。
图5是氧化石墨烯(GO)和Cu(Ⅱ)(0.5 mol·L-1)/ AgBr-rGO的XPS图谱。从图5a中可以看出氧化石墨烯含氧官能团的主要分布。在波数284.8 cm-1处的是C-C、C=C和C-H,而C-OH和C-O-C对应在286.6 cm-1波数处,C=O和HO-C=O分别分布在波数287.6和288.4 cm-1处[18]。图5b是用抗坏血酸还原后的Cu(Ⅱ)/AgBr-rGO复合光催化剂,与氧化石墨烯对比可明显发现,含氧官能团C-OH、C-O-C、C=O和HO-C=O强度很明显的下降,说明含氧基团明显减少,氧化石墨烯被还原为还原石墨烯(rGO)。由此可以证明,实验所制备Cu(Ⅱ)/AgBr-rGO复合光催化剂中的石墨烯是还原石墨烯。
2.2 光催化性能及光催化机理分析
图6是样品在可见光下对甲基橙的降解速率常数柱形图。图6a表示纯AgBr的速率常数,数值为0.008 07 min-1。从图6b和图6c柱形可以得出,经过石墨烯复合或Cu(Ⅱ)修饰过的AgBr的光催化性能与纯AgBr(图6a)相比,都有了明显的提高。由图6d、e、f、g可明显发现:在石墨烯含量相同的情况下(0.5wt%),Cu(Ⅱ)浓度从0.05 mol·L-1增加到0.5 mol ·L-1,光催化性能逐渐提升,其中,Cu(Ⅱ)(0.5 mol·L-1)/ AgBr-rGO(图6f)的速率常数达到最高值0.027 31 min-1,是图6b速率常数(0.015 98 min-1)的1.7倍左右,是Cu(Ⅱ)(0.5 mol·L-1)/AgBr(图6c)速率常数(0.015 19 min-1)的1.8倍左右。当Cu(Ⅱ)浓度增加到1 mol·L-1时,性能比0.5 mol·L-1时略有下降,但仍然比石墨烯和Cu(Ⅱ)单独修饰的样品性能要高。综上可知,石墨烯和Cu(Ⅱ)协同作用的AgBr光催化性能分别比纯AgBr、经石墨烯复合、经Cu(Ⅱ)助剂修饰的光催化性能都高。

图6 不同光催化剂降解甲基橙的速率常数(样品石墨烯含量皆为0.5wt%)Fig.6Rate constant(k)of the MO decomposition by various photocatalysts
为了验证光催化剂的性能稳定性,测定了AgBr、AgBr-rGO(0.5wt%)和Cu(Ⅱ)(0.5 mol·L-1)/AgBrrGO(0.5wt%)样品的4次循环性能图(图7)。由图可以发现:样品Cu(Ⅱ)(0.5 mol·L-1)/AgBr-rGO(0.5wt%)的光催化性能远远高于AgBr-rGO(0.5wt%),而样品AgBr-rGO(0.5wt%)的光催化性能始终高于AgBr。随着循环次数的增加,样品的性能略有下降,性能降低可能的原因是多次循环、多次洗涤和离心造成光催化剂的量(原始的光催化剂质量只有0.05 g)有部分损失。但总体来说,石墨烯与Cu(Ⅱ)协同修饰的样品性能都要高于石墨烯复合AgBr和纯AgBr。因此,Cu(Ⅱ)(0.5 mol·L-1)/AgBr-rGO(0.5wt%)的性能是比较稳定的。
图8是Cu(Ⅱ)助剂与石墨烯协同增强AgBr可见光光催化性能的机理图。由电子排布可知,Cu(Ⅱ)的外层电子结构为3d94s0,在捕获一个电子后,形成比较稳定的3d104s0的Cu(Ⅱ)。在可见光的照射下,AgBr价带上的电子发生跃迁,被激发到导带,并留下空穴,而生成的电子-空穴对则转移到AgBr的表面,极易被光催化剂表面的Cu(Ⅱ)捕获,形成的Cu(Ⅱ)再与空气中的氧气反应,又被氧化成Cu(Ⅱ)附着在AgBr表面[13]。当AgBr复合石墨烯后,由于石墨烯具有很高的电子迁移率,能有效地转移电子,防止电子-空穴的再次复合;另外,石墨烯具有很大的比表面积,可为Cu(Ⅱ)提供更多的活性位点。因此,在Cu(Ⅱ)和石墨烯两者共修饰AgBr后,光生电子转移的速度得到明显地加快,Cu(Ⅱ)捕获电子的效率提高,可以大幅度的提高光生电子-空穴对的分离,极大的提高了Cu(Ⅱ)/AgBr-rGO可见光光催化活性。
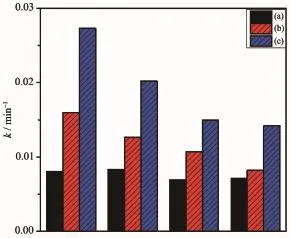
图7 不同样品的循环性能图Fig.7Cycling runs of different samples
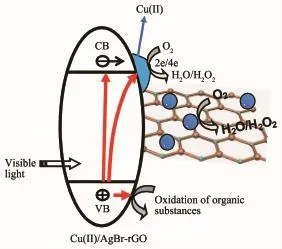
图8 Cu(Ⅱ)/AgBr-rGO光催化机理示意图Fig.8Schematic diagram showing the possible photocatalytic mechanism Cu(Ⅱ)/AgBr-rGO
3 结论
本研究采用低温的溶液法成功制备了Cu(Ⅱ)助剂和石墨烯共修饰的高效AgBr光催化剂。以扫描电镜加元素分析以及拉曼光谱证明了成功制备Cu(Ⅱ)/AgBr-rGO复合光催化剂,以X射线光电子能谱证明了复合光催化剂中的石墨烯为还原石墨烯。经石墨烯和Cu(Ⅱ)协同共修饰的AgBr光催化剂表现出很高的可见光光催化性能,其中Cu(Ⅱ)(0.5 mol· L-1)/AgBr-rGO(0.5wt%)具有最高性能,远高于AgBr、AgBr-rGO(0.5%)和Cu(Ⅱ)(0.5 mol·L-1)/AgBr,而且该光催化剂经多次循环实验证明性能比较稳定。Cu(Ⅱ)助剂与石墨烯复合协同作用增强光催化性能的原因是:Cu(Ⅱ)易于捕获光生电子,而石墨烯比表面积大,可提供更多的还原位点,两者协同作用使银类化合物上的光生电子-空穴对得到有效分离,有效地提高可见光光催化性能。
[1]Wang G M,Wang H Y,Ling Y C,et al.Nano Lett.,2011,11 (7):3026-3033
[2]Ohko Y,Ando I,Niwa C,et al.Environ.Sci.Technol.,2001, 35(11):2365-2368
[3]WEN Yan-Yuan(温艳媛),DING Chan-Ming(丁旵明).Chin. J.Catal.(催化学报),2011,32(1):36-45
[4]YU Yang-Yang(于洋洋),YU Mei-Yan(于美燕),ZHANG Yue(张玥),et al.Chinese J.Inorg.Chem.(无机化学学报), 2013,29(08):1657-1662
[5]Bi Y P,Ye J H.Chem.Commun.,2009,43:6551-6553
[6]Wang X J,Chang L L,Wang J R,et al.Appl.Surf.Sci., 2013,270:685-689
[7]Wei H M,Gong H B,Chen L,et al.J.Phys.Chem.C,2012, 116(19):10510-10515
[8]Wang P,Huang B B,Zhang X Y,et al.Chem.Eur.J.,2009, 15(8):1821-1824
[9]Wang X F,Li S F,Yu H G,et al.Chem.Eur.J.,2011,17 (28):7777-7780
[10]Yu H G,Liu L,Wang X F,et al.Dalton Trans.,2012,41 (34):10405-10411
[11]Zhu M S,Chen P L,Liu M H.J.Am.Chem.Soc.,2011,5 (6):4529-4536
[12]Yu H G,Xu L L,Wang P,et al.Appl.Catal.,B:Environ., 2014,144:75-82
[13]Wang P,Xia Y,Wu P P,et al.J.Phys.Chem.C,2014,118 (17):8891-8898
[14]Luo G Q,Jiang X J,Li M J,et al.ACS Appl.Mater.Interfaces, 2013,5(6):2161-2168
[15]Bhunia S K,Jana N R.ACS Appl.Mater.Interfaces,2014,6 (22):20085-20092
[16]Zhu M S,Chen P L,Liu M H.Langmuir,2012,28(7):3385-3390
[17]Wang P,Wang J,Wang X F,et al.Appl.Catal.,B:Environ., 2013,132-133:452-459
[18]Wang P,Ming T S,Wang G H,et al.J.Mol.Catal.A:Chem., 2014,381:114-119
[19]Lin H L,Cao J,Luo B D,et al.Catal.Commun.,2012,21: 91-95
[20]ZHOU Tian(周田),CHEN Bing-Di(陈炳地),YAO Ai-Hua (姚爱华),et al.Chinese J.Inorg.Chem.(无机化学学报), 2013,29(02):231-236
[21]YANG Yong-Hui(杨勇辉),SUN Hong-Juan(孙红娟),PENG Tong-Jiang(彭同江).Chinese J.Inorg.Chem.(无机化学学报),2010,26(11):2083-2090
Cooperation Effect of Cu(Ⅱ)Cocatalyst and Graphene for Enhanced AgBr Visible-light Photocatalytic Performance
WANG Ming-FangWANG Ping*XU Shun-QiuLI Xiao-Zheng
(Department of Chemistry,School of Chemistry,Chemical Engineering and Life Science, Wuhan University of Technology,Wuhan 430070,China)
In this study,a simple low-temperature solution-impregnation method was developed for the fabrication of highly efficient AgBr photocatalyst with cooperation effect of Cu(Ⅱ)cocatalyst and graphene.Photocatalytic experimental results for the depolarization of methyl orange(MO)aqueous solution indicated that the AgBr with cooperation effect of Cu(Ⅱ)cocatalyst and graphene displayed very good photocatalytic activity.Especially,Cu(Ⅱ)(0.5 mol·L-1)/AgBr-rGO(0.5wt%)(rGO,reduced graphene oxide)showed the highest photocatalytic activity with a rate constant 0.027 31 min-1,while this value is higher than that of the pure AgBr(0.008 07 min-1),AgBr-rGO(0.5%) (0.015 98 min-1)and Cu(Ⅱ)(0.5 mol·L-1)/AgBr(0.015 19 min-1)by a factor of 3.38,1.7 and 1.8,respectively.The reason for enhanced photocatalytic performance is that Cu(Ⅱ)can quickly catch the photogenerated electrons from AgBr and graphene has large specific surface which may provide a lot reduction active sites for Cu(Ⅱ),resulting in a rapid separation of photogenerated electrons and holes.This work may provide the new insights for the preparation of high performance AgBr photocatalyst.
AgBr;Cu(Ⅱ)cocatalyst;graphene;cooperation effect;visible-light photocatalytic activity
O643.36
A
1001-4861(2015)10-1981-06
10.11862/CJIC.2015.235
2015-03-02。收修改稿日期:2015-07-04。
国家级大学生创新创业训练计划项目(No.20141049714006)和国家自然科学基金(No.21477094)资助项目。
*通讯联系人。E-mail:wangping0904@whut.edu.cn
