一步合成铁氮掺杂碳纳米粒子及其可见光催化
2015-12-01李洪仁刘诗琪
李洪仁 张 岩 刘诗琪 李 锋
(沈阳大学师范学院化学系,沈阳110044)
一步合成铁氮掺杂碳纳米粒子及其可见光催化
李洪仁 张 岩 刘诗琪 李 锋*
(沈阳大学师范学院化学系,沈阳110044)
使用柠檬酸、草酸铵作为碳源物质,三氯化铁为铁源,直接热分解法一步合成铁氮掺杂碳纳米粒子。所得的铁氮掺杂碳纳米粒子溶液在365 nm的紫外辐射下发射蓝色荧光。对铁氮掺杂碳纳米粒子进行了XRD、TEM、FTIR、FL、XPS表征。合成的铁氮掺杂碳纳米粒子分散均匀,直径大约3~5 nm。荧光光谱表明:粒子荧光性能优良,发射光谱依赖激发波长变化,具有多色性。此外,合成的掺杂碳纳米粒子溶液在长波长的可见光和红外光激发下有较好的荧光辐射,具有上转换功能。将其应用于可见光光降解亚甲基蓝MB,在MB起始浓度为20 mg·L-1,不使用氧化剂时,15 h可以使褪色率达到90%;使用过氧化氢为氧化剂,15 min可以达到97%,其光催化性能优良。对其氧化还原反应机理进行了电化学评估,评估结果与理论吻合。
铁氮掺杂;碳纳米粒子;荧光;热分解合成;光催化
0 引言
自从2006年Sun等对碳点进行系统研究以来[1],碳纳米材料已经经历了数十年的发展。碳点以其优异的光学、电学性质在生物成像、活体标记、太阳能、催化剂[2-6]等方面取得了广泛应用。随着碳纳米材料应用的扩展,其合成方法也不断更新,许多新工艺、新方法不断被报道。早期的碳纳米材料的合成方法是采用激光等手段对大块碳材料进行分割,使之产生微小碳颗粒,再将其用表面活性剂处理,使之表面产生活性基团。碳纳米粒子表面形成活性基团这一过程称为钝化,钝化后的碳点有荧光。钝化碳点还可以采用强氧化性的酸处理碳微粒使表面产生活性基团,如-COOH、-OH等。上述制备方法粒子由大到小,称为自上向下法。
由于有机化合物热分解也可以产生碳,所以热分解有机物并使之聚合也是合成碳纳米材料的一种方法。控制聚合过程可以控制碳纳米粒子大小,所以这种方法更方便采用。由于碳纳米粒子的形成是由小到大,又称为自下向上法。不是所有的有机物热分解都可以获得碳纳米粒子,前驱体一般为富含羟基、羧基、氨基的有机物,如糖类、多羟基羧基有机酸(柠檬酸、酒石酸、维生素C、氨基酸等)。
本方法成本比自上向下法更低。由于聚合前前驱体含有活性基团,碳化聚合后仍然保留部分活性成分,通常不需要钝化就有良好的荧光性[7-8]。近年来,采用天然材料制备碳点的报道也有很多,采用蛋黄、果汁、玫瑰花[9-11]等天然原料制备碳点都获得了成功。天然材料富含糖类、氨基酸、维生素C等,它们容易热分解形成碳点。其原理与有机物热分解的过程相似。
因为碳点是纳米级粒子,有半导体性质,表面具有电子空穴,是电子的受体和供体,具有光催化作用。碳点作为催化剂的研究已经有报道[12],大多数是利用碳点催化降解染料污水,效率有限。为了提高效率,丰富催化剂的品种,人们将碳点和金属复合,形成金属掺杂碳点以提高效率。但就目前的研究来看,催化效果较好的是贵金属与碳点的复合物,如碳点与Pt、Au、Pd等[13-14]。因此,寻找一种廉价、无毒的金属与碳点复合是今后研究工作的主要方向。本文进行了这方面的研究,将碳点与铁元素复合,合成了铁掺杂碳纳米粒子,并将其应用于光降解染料,取得了一些进展。
1 实验部分
1.1 试剂和仪器
柠檬酸,草酸铵,三氯化铁、过氧化氢、亚甲基蓝均为分析纯试剂,均购自国药集团化学试剂有限公司,实验用水为蒸馏水,透析袋MWCO:1000
透射电子显微镜(TEM):日本日立公司,H-7650,工作电压100 kV,取少量试样超声溶解于水中,将液体样品滴在铜网上,自然风干后进行电镜扫描;XPS多功能表面分析系统:美国Thermo VG公司,ESCALAB250;荧光分光光度计:日本日立公司,F7000荧光分光光度计;紫外可见分光光度计:北京瑞利分析仪器公司,UV-2601;X射线衍射仪;荷兰PANalytical公司PANalytical XPert PRO X射线衍射仪电压40 kV,电流40 mA,扫描角度10°~80°,扫描速度0.06°·min-1;红外分光光度计:PE Spectrum one红外光谱仪,美国PerkinElmer公司,溴化钾压片法。LK9805电化学综合测试系统,天津兰立科高科技有限公司;光源为500 W碘钨灯,辐照度测定采用TES1333R太阳能功率表:台湾泰任电子工业有限公司。
1.2 Fe/NCNPs的合成
称取0.50 g柠檬酸,0.50 g草酸铵,0.10 g三氯化铁,置于200 mL烧杯中,加入少量蒸馏水搅拌溶解,然后转入干燥箱中恒温200℃,保温2 h,取出,自然冷却至室温。得棕色固体粉末。将粉末溶解于水中得棕黄色溶液。此溶液为荧光掺杂碳纳米材料溶液。将所得溶液在4500 r·min-1的低速离心机上离心分离大颗粒杂质.再将溶液用MWCO:1000透析袋透析72 h,真空干燥得棕黄色残留物,此残留物粉末为碳纳米粒子,将所制备的碳纳米粒子进行FTIR、XRD、TEM、XPS表征。
1.3 Fe/NCNPs催化光降解亚甲基蓝
以亚甲基蓝(MB)为模拟污染物降解模板,以碘钨灯为光源模拟太阳光,对催化剂光催化性能进行评估。取1.0 mL 1.0 mg·mL-1MB溶液,置于100 mL烧杯中加入20 mg碳点,加入0.050 mL 30%过氧化氢,稀释至50 mL,放入搅拌子。置于磁力搅拌器上搅拌光照。每隔一段时间取样在紫外-可见分光光度计上分析,工作波长为667 nm,吸光度法检验MB的剩余浓度,降解率的计算采用下列公式:×100%,且假定,光降解实验光的辐照度0.085 W·cm-2。c0、A0为MB溶液起始浓度、吸光度,c、A为不同t时刻MB溶液浓度、吸光度值。
1.4 电化学反应机理评估
氧化还原机理电化学评估采用0.10 mol·L-1的磷酸二氢钠溶液作为底液,用氢氧化钠调节pH= 7.0,采用三电极系统,玻碳电极为工作电极,直径0.5 mm。铂电极为对电极,Ag/AgCl作为参比电极,玻碳电极采用1.0和0.3 μm的氧化铝抛光,用无水乙醇超声清洗,再用蒸馏水反复超声清洗数十分钟。循环伏安法测定循环伏安曲线,扫描速度25 mV· s-1,扫描范围-0.8~0.7 V。
2 结果与讨论
以柠檬酸、草酸铵、三氯化铁为原料合成铁掺杂碳纳米粒子反应原理如下:

柠檬酸、草酸铵可以和铁离子生成配位化合物,配位化合物与柠檬酸混合热分解脱水形成碳粒子,而碳粒子中夹杂着铁离子和氮。氮掺杂会使纳米粒子荧光性能加强;铁的存在会使光催化活性提高。因为铁离子和过氧化氢有Fenton反应,纳米粒子有纳米效应,两者结合使反应活性更高。
2.1 Fe/NCNPs溶液的照片
图1为Fe/NCNPs水溶液在日光和365 nm紫外灯下的照片,照片显示呈在日光下棕黄色,在365 nm紫外灯下溶液呈亮蓝色,且荧光强,亮度高,肉眼可以在暗处观察到荧光,容易用照相机拍摄照片。说明铁掺杂不降低碳纳米材料的发光性能,该材料荧光性能优良。

图1 Fe/NCNPs水溶液在日光和365 nm紫外灯下的照片Fig.1Images of the solution of Fe/NCNPs under daylight and 365 nm UV light
2.2 XRD表征
图2给出了样品的XRD图,图上显示在大约2θ=27°左右有一个宽大的吸收峰。这个吸收峰表明所获得的样品含有石墨相碳[15]。XRD图显示所合成的纳米粒子含有石墨相结构。
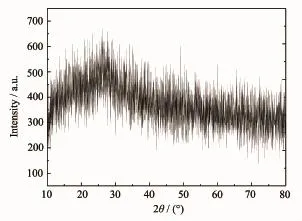
图2 Fe/NCNPs的XRD图Fig.2XRD pattern of as-prepared Fe/NCNDs

图3 样品的TEM图像Fig.3TEM image of as-prepared Fe/NCNPs
2.3 TEM表征
Fe/NCNPs的透射电镜照片如图3所示,照片显示该法合成的Fe/NCNPs形状不是很规则,呈现的不规则圆形,边界基本可见,粒子的粒径大小约为3~5 nm,说明柠檬酸、草酸铵和三氯化铁热分解可以制备出掺杂碳纳米粒子。
2.4 FTIR表征
为了确定样品的表面性质,对其进行了FTIR表征。样品的FTIR谱图见图4,在3 422 cm-1处有一宽而强的吸收峰,这一吸收归属于-OH、-NH的伸缩振动,在1 634 cm-1吸收代表C=O伸缩振动,1 406 cm-1吸收代表C-N酰胺伸缩振动。
C-N在所用原料中不存在,而产物的FTIR光谱明确反映出存在信息,说明原料共热发生了化学反应。合成的Fe/NCNPs表面富含-OH、-NH、C=O等亲水性基团。
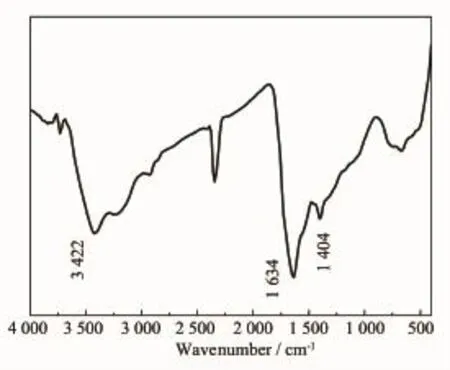
图4 样品的红外吸收光谱Fig.4FTIR spectra of as-prepared Fe/NCNPs
2.5 XPS表征
为了进一步确定样品的表面性质,对样品进行了XPS分析。XPS结果表明:样品表面含有C、N、O、Fe 4种元素,其含量分别为(wt%):60.26、9.96、26.06、1.49,证实纳米粒子主要成分为碳,掺杂有Fe/ N。以碳峰为内标物(285 eV)对XPS结果进行校正,校正后见图5a,Cl2p、C1s、N1s、O1s、Fe2p元素的电子结合能分别为199.27、285、400.07、531.75、710.96 eV[16]。图b为Fe2p谱,由图b可见,Fe2p在710.96 eV附近并伴有卫星峰,与Fe(Ⅲ)特征吻合[17],说明样品中的Fe以Fe(Ⅲ)价态存在。
使用分峰软件对C1s峰进行了分峰处理,分峰结果图6。C1s峰被分出4个峰,峰值为288.5、285.9、285.1、284.4 eV,分别代表样品中含有COO、C-O、C-N、C-C基团特征[18]。这一点,与FTIR分析结果完全一致,进一步证实纳米粒子表面富含活性基团。

图5 (a)Fe/NCNPs的XPS谱(b)Fe/NCNPs的Fe2p XPS谱Fig.5(a)XPS survey spectrum of pristine as-prepared Fe/NCNPs.(b)XPS Fe2p spectra of as-prepared Fe/NCNPs
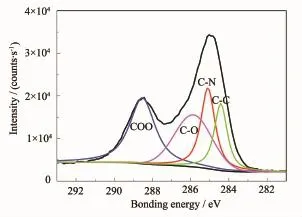
图6 Fe/NCNPs的C1s XPS分峰谱Fig.6XPS C1s spectra of as-prepared Fe/NCNPs
2.6 Fe/NCNPs的UV和FL光谱
图7a是制备样品溶液的UV吸收光谱,UV光谱显示样品在200~400 nm紫外区有明显的强吸收,在大约345 nm处有一吸收峰,这个吸收峰位置与荧光激发峰相近,这一点与大多数碳纳米粒子UV吸收光谱吻合[19]。说明纳米粒子将吸收的紫外光能量转化为发射荧光。在可见光区,400~600 nm有吸收,没有峰,正是这个吸收使纳米粒子在可见光区有光催化作用,600~800 nm没有明显吸收。
图7 b、c是制备样品的荧光激发和发射光谱。b为激发光谱,c为发射光谱,b的峰值为367 nm,峰型基本对称,激发范围为300~450 nm;c在452 nm处有一强发射峰,发射范围400~600 nm。从激发-发射图谱看,该纳米粒子的荧光性能良好,有较宽的激发、发射范围。因为发射范围较宽,所以在365 nm紫外灯下,样品溶液呈现亮蓝色,与光谱数据吻合。
图8是样品溶液在不同的激发波长下的荧光发射图谱。图谱显示在激发波长由300~460 nm范围内均有荧光发射,发射范围350~600 nm。随着激发波长的增加发射波长红移,强度逐渐下降,在激发波长360~370 nm时发射峰最大,暗示最佳激发波长大约360 nm左右,与图7的测定吻合。此后发射荧光强度逐步下降,这一点与大多数碳纳米粒子相似,发射波长随激发波长增加而增加。有文献报道,发射荧光波长不仅取决于激发波长而且取决于纳米粒子的大小[20]。

图7 Fe/NCNPs的UV吸收光谱(a)和样品的FL激发(b)与发射(c)谱Fig.7UV absorption spectrum of the solution of as-pre pared Fe/NCNPs(a)and Fluorescence excitation (b)and emission spectra(c)

图8 样品溶液在不同的激发波长下的FL图谱Fig.8Emission spectra of tthe solution of as-preparedFe/NCNPs at different excitation wavelengths
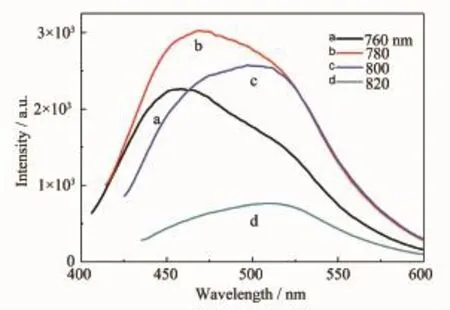
图9 样品溶液的FL上转换图谱Fig.9Up-conversion emission spectra of the solution of as-prepared Fe/NCNPs at different excitation wavelengths

图10 无过氧化氢时Fe/NCNPs催化MB溶液降解的c0/c-t曲线Fig.10Relationship between MB concentration c0/c and reaction time for different catalysts
经测试样品具有上转换性质,如图9所示,当激发光波长为760~820 nm时样品溶液发射出短波长的发射,显示样品具有上转换功能。上转换荧光光谱与下转化激发荧光光谱类似,随激发波长增加,发射光谱强度逐渐增强,发射光谱最大发射峰红移。当在激发波长为780 nm时,发射强度达到最大,发射波长为465 nm,再增加激发波长时,发射光谱强度逐步下降。上转换的发射峰较宽,在400~600 nm范围。因为样品具有上转换功能,其可见光催化可能更好,其在上转换成像、催化等领域有潜在的应用。
2.7 Fe/NCNPs的光催化活性及机理评估
2.7.1 Fe/NCNPs的光催化活性
图10是MB溶液在无过氧化氢时Fe/NCNPs催化的脱色曲线,图中线a为没有催化剂时,单纯MB溶液曲线。由曲线可以看出当没有Fe/NCNPs催化时MB溶液几乎没有脱色,c/c0对时间t变化为水平直线,几乎不分解。图中线b为催化剂对MB的吸附作用的影响曲线,由曲线可见,没有光照时,也有轻微褪色作用,15 h MB脱色率大约10%。图中线c是当有催化剂光照下MB溶液曲线,c/c0随时间t逐步降低,反应时间达到15 h时,脱色率可以达到90%以上,扣除吸附作用的影响,脱色率大于80%。没有过氧化氢氧化剂时也可以使染料脱色,暗示催化剂的催化能力较强。
图11是MB溶液在有过氧化氢时Fe/NCNPs催化的脱色曲线。在没有Fe/NCNPs的情况下,MB溶液的c/c0对时间t变化几乎为水平直线。图中线a为单纯MB溶液的曲线;线b为加入过氧化氢后的降解曲线,没有加入Fe/NCNPs的降解曲线。而Fe/ NCNPs和过氧化氢同时存在时线c显示,反应异常迅速,15 min脱色率达到97%,实验表明有过氧化氢时催化剂的催化能力较强。15 min内吸附不明显,吸附对褪色影响可以忽略。
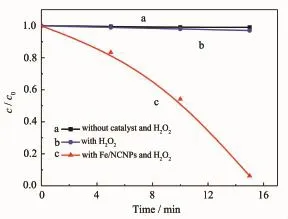
图11 有过氧化氢时FeNCNPs催化MB溶液降解的c0/c-t曲线Fig.11Relationship between MB concentration c0/c and reaction time for different catalysts in the present of H2O2
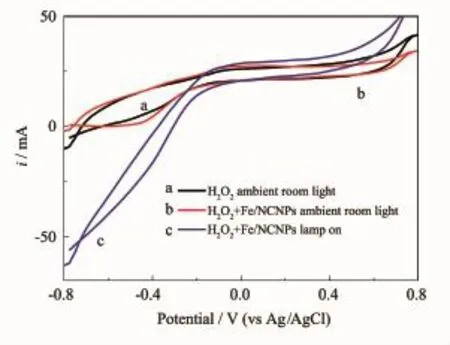
图1 210mmol·L-1H2O2,10 mmol·L-1H2O2和10 mg· L-1Fe/NCNPs在玻碳电极上的循环伏安曲线Fig.12Cyclic voltammograms of glassy carbon electrode in the presence of 10 mmol·L-1H2O2and in the presence of 10 mmol·L-1H2O2and 10 mg· L-1Fe/NCNPs
2.7.2 Fe/NCNPs的光催化机理
对有过氧化氢存在的催化机理的研究采用电化学方法。过氧化氢在本实验中作为氧化剂,其氧化还原态均在溶液中,需要依靠惰性电极将其产生的电子导出,选用玻碳电极作为惰性电极导出电子,评估其氧化还原行为。底液选择为0.1 mol·L-1pH=7.0的磷酸盐,Fe/NCNPs浓度为10 mg·L-1。见图12。图12曲线a是单纯过氧化氢循环伏安曲线(室内光),曲线显示过氧化氢在设定的条件下没有明显的氧化还原峰,表明过氧化氢的氧化还原反应较弱;曲线b是加入Fe/NCNPs的过氧化氢循环伏安曲线(室内光),曲线与单纯过氧化氢伏安扫描没有大的变化;说明在弱光下氧化剂过氧化氢的氧化还原活性没有因为催化剂加入显著增强。曲线c是加入Fe/NCNPs的过氧化氢在灯光辐照下循环伏安曲线,曲线与前者对比有了显著变化,表明光辐照对过氧化氢的氧化还原有显著影响。通过对比发现,过氧化氢在没有催化剂和光辐照时反应起始电势为-0.7 V,而加催化剂和辐照后起始氧化电势-0.34 V,过氧化氢反应起始电势正移说明其氧化能力提高,这一现象与文献的报道吻合[21]。其原因是Fe/NCNPs在400~600 nm范围的可见光区有吸收,能够吸收可见光光能,吸收光能传递给过氧化氢使其能量提高,反应活性提高;在400~820 nm的可见光及其红外区,Fe/NCNPs具有上转换功能,能够将低能量的光转化为可以被过氧化氢利用的能量,催化结果与电化学结果一致。
光辐照也能够影响亚甲基蓝的氧化还原性能,为此配制含有亚甲基蓝10 mg·L-1,选择同样的底液和电化学条件进行扫描,曲线见图13。
图13中的曲线a为亚甲基蓝在室内光下的循环伏安曲线,有氧化还原峰,还原峰在-0.3 V左右。b为亚甲基蓝加光辐照后的循环伏安曲线,由曲线清楚的看出:其氧化反应部分变化较小,而其还原反应部分变化显著,还原峰负移至-0.35 V,峰电流绝对值显著增加。以上数据表明,辐照后亚甲基蓝溶液更容易发生还原反应,还原性能显著增强,还原活性增加。
综上所述,在可见光辐照的条件下由于催化剂光吸收和上转换效应,过氧化氢氧化能力得到提高;同时,亚甲基蓝的还原能力得到提高,二者协同效应更加提升了氧化还原反应活性。
光化学反应归根到底是对光的吸收或转化,过氧化氢本身对可见光没有吸收因而不能转化,不可能直接利用可见光进行光化学反应。而Fe/NCNPs能够吸收可见光光能,并有上转换的功能,吸收或转化光能后传递给过氧化氢,加速过氧化氢分解,使其氧化能力加强。而染料直接能够吸收可见光能量,也能将能量传递给过氧化氢,更加敏化这种反应。除此之外纳米材料的纳米效应也对反应有促进作用,纳米材料有电子空穴,在光的作用下,产生光生电子,光生电子使过氧化氢产生氧化性更强的羟基游离基,游离基直接降解染料。此外纳米材料表面积都比较大,易于吸附反应物,使其在表面发生反应,起到浓集的作用。Fe/NCNPs更有其特殊性,其表面有Fe3+,发生Fenton效应,是纳米粒子与Fenton效应的结合粒子。一般Fenton反应在紫外光下完成,因为碳纳米粒子对可见光的吸收和上转换功能,此反应可见光下即可进行,二者结合,扩大了Fenton反应的适用光的范围,其碳纳米粒子效应起较大作用。
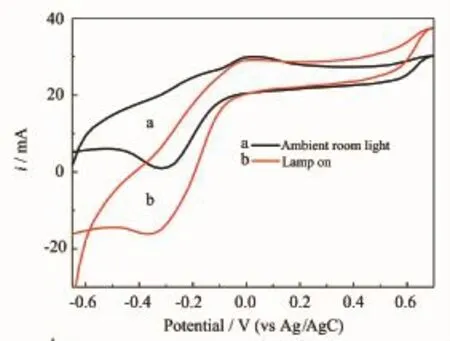
图1 310mg·L-1MB在玻碳电极上的循环伏安曲线Fig.13Cyclic voltammograms of glassy carbon electrode in the presence of 10 mg·L-1MB

图14 光降解原理示意图Fig.14Photodegradation principle diagram
3 结论
本文采用由草酸铵、柠檬酸和三氯化铁直接热分解法合成铁氮掺杂碳纳米粒子,其方法简单,成本低廉,该方法无毒、原料易得,所合成的碳纳米粒子荧光性能优良,荧光强度高。此外所合成的碳纳米粒子具有上转换性能,实验证明所合成的碳纳米粒子具有良好的可见光光催化性能,可被应用于光降解污水。以亚甲基蓝为模板,起始浓度20 mg·L-1,在不使用过氧化氢为氧化剂时,15 h可以使褪色率达到90%;使用过氧化氢为氧化剂,15 min褪色率可以达到97%。所合成的碳纳米粒子有可能应用于光化学反应催化等领域,应用前景广阔。本方法合成掺杂碳纳米粒子工艺简单,适合于大规模生产。
[1]Sun Y,Zhou B,Lin Y,et al.J.Am.Chem.Soc.,2006,128 (40):7756-7757
[2]Li N,Liang X,Wang L,et al.J.Nanopart Res.,2012,14: 1177-1186
[3]Goh E,Kim K,Kim Y,et al.J.Am.Chem.Soc.,2012,13: 2554-2561
[4]Yu X,Liu R,Zhang G,et al.Nanotechnology,2013,24:335401 -335407
[5]Hu S,Tian R,Wu L,et al.Chem.Asian J.,2013,08(05): 1035-1041
[6]Zhang Y,Ma D,Zhang Y,et al.Nano Energy,2013,2:545 -552
[7]Qu S,Wang X,Lu Q,et al.Angew.Chem.Int.Ed.,2012, 51:12215-12218
[8]Li H,Li F,Wang G,et al.J.Lumin.,2014,156:36-41
[9]Wang J,Wang C,Chen S.Angew.Chem.Int.Ed.,2012,51: 9297-9301
[10]Lu W,Qin X,Liu S,et al.Anal.Chem.,2012,84:5351-5357
[11]Feng Y,Zhong D,Miao H,et al.Talanta,2015,140:128-133
[12]Li F,Wang G,Li H,et al.Mater.Lett.,2014,122:352-354
[13]Luo P,Li C,Shi G.Chem.Phys.,2012,14:7360-7366
[14]Li J,Zhang B,Wang F,et al.New J.Chem.,2011,35:554 -557
[15]Mewada A,Pandey S,Shinde S,et al.Mater.Sci.Eng.C, 2013,33:2914-2917
[16]Wang L,Ruan F,Lü T,et al.J.Lumin.,2015,158:1-5
[17]Wilson D,Langell M A.Appl.Surf.Sci.,2014,303:6-13
[18]Gong X,Lu W,Chin M,et al.Anal.Chim.Acta,2015,861: 74-84
[19]Zhang B,Liu C,Liu Y,et al.Eur.J.Inorg.Chem.,2010,28: 4411-4414
[20]Cao L,Wang Meziani X M,et al.Am.Chem.Soc.,2007, 129(37):11318-11319
[21]Liu R,Huang H,Li H,et al.ACS Catal.,2014,4:328-335
One Step Synthesis of Fe/N Co-Doped Carbon Nanoparticles for Photocatalysis
LI Hong-RenZHANG YanLIU Shi-QiLI Feng*
(Normal College,Shenyang University,Shenyang 110044,China)
A one step method of synthesis of iron-nitrogen doped carbon nanoparticles(Fe/NCNPs)is developed by pyrolysis using citric acid and ammonium oxalate as carbon source and FeCl3as iron source.The solution of as-prepared Fe/NCNPs emits blue fluorescent under 365 nm UV.As-prepared Fe/NCNPs are investigated by XRD,TEM,FTIR,FL and XPS.The result indicates that as-prepared Fe/NCNPs are well-dispersed with an average diameter of about 3~5 nm.Its fluorescence spectra show that the particles have excellent fluorescence performance,and with increasing excitation wavelength,the fluorescence spectra shift to longer wavelengths, which is multicolor.In addition,the solution of as-prepared Fe/NCNPs has good short wavelength optical emission with long wavelength visible and infrared light excitation,which is the up-converting function.When as-prepared Fe/NCNPs are applied to photocatalytic degradation of methylene blue(20 mg·L-1)irradiated by visible light, when the H2O2is absent,the decolorization rate is over 90%in 15 hours;when H2O2is present as oxidant,the decolorization rate is over 97%in 15 min,revealing excellent photocatalytic activity.The redox reaction mechanism of the photocatalytic degradation is evaluated by electrochemical method,and the result is consistent with the theory.
Fe/N co-doped;carbon nanoparticles;fluorescence;pyrolysis synthesis;photocatalysis
O613.7
A
1001-4861(2015)10-1938-08
10.11862/CJIC.2015.270
2015-03-31。收修改稿日期:2015-08-27。
沈阳大学博士启动基金支持项目(No.11202127012)资助项目。
*通讯联系人。E-mail:syufengli@126.com;Tel:+86-24-62721002
