纳米三氧化钨的制备、表征及对六硝基六氮杂异伍兹烷热分解的影响
2015-12-01赵宁宁贺翠翠赵凤起胡荣祖马海霞
赵宁宁 贺翠翠 王 通 安 亭 赵凤起 胡荣祖 马海霞*,
(1西北大学化工学院,西安710069)
(2西安近代化学研究所燃烧与爆炸技术重点实验室,西安710065)
纳米三氧化钨的制备、表征及对六硝基六氮杂异伍兹烷热分解的影响
赵宁宁1贺翠翠1王 通1安 亭2赵凤起2胡荣祖2马海霞*,1
(1西北大学化工学院,西安710069)
(2西安近代化学研究所燃烧与爆炸技术重点实验室,西安710065)
采用水热法通过控制前躯体钨酸钠的加入量和反应时间制备了长方体形纳米WO3,利用X射线粉末衍射(XRD)、透射电镜(TEM)、扫描电镜及能量散射光谱仪(SEM-EDS)对样品进行表征。并运用差示扫描量热法(DSC)研究纳米WO3对六硝基六氮杂异伍兹烷(CL-20)热分解特性的影响。结果表明:与单组分CL-20相比,纳米WO3的加入使复合物WO3/CL-20的热分解峰温降低2.95℃,活化能减小7.74 kJ·mol-1,因此纳米WO3能够加速CL-20的热分解。
纳米三氧化钨;六硝基六氮杂异伍兹烷;水热法;热分解
纳米WO3作为一种重要的过渡金属氧化物,具有光、电、气质变色等性质,在半导体、气敏材料和催化等[1-6]领域有重要的潜在应用。近年来,随着纳米技术的发展,国内外研究者在纳米WO3的制备及应用方面做了大量工作。已有文献报道合成不同形貌和尺寸的纳米WO3,如纳米线[7]、纳米片[8-9]、纳米颗粒[10]、纳米棒[11-12]、纳米多孔网状结构[13]。但是纳米WO3的研究整体上仍处于初步发展阶段[14],探索合成不同尺寸和形貌的纳米WO3对于其工业化发展有着重要而深远的意义。
六硝基六氮杂异伍兹烷(CL-20)因其高能量密度而被用于炸药、固体推进剂和发射药中。以CL-20为主要含能组分的固体推进的燃烧性能与CL-20的热分解特性密切相关,因此研究CL-20的热分解性能对预估相应固体推进剂的燃烧效果有重要意义。纳米催化剂能够影响CL-20的热分解特性,目前研究者已探讨了纳米碳管对CL-20热分解过程的影响[15],但纳米WO3对CL-20热分解的影响研究却未见报道。
本文以钨酸钠和浓盐酸为原料,加入十八胺辅助合成WO3长方体形纳米粉末,并探讨钨酸钠的加入量和反应时间对产物形貌和尺寸的影响。采用超声复合法制备出WO3/CL-20复合物,运用差示扫描量热法(DSC)法研究了纳米WO3对CL-20热分解性能的影响,计算获得CL-20与混合体系WO3/CL-20的热分解动力学方程及热力学参数。
1 实验部分
1.1 原料
钨酸钠(Na2WO4·2H2O,分析纯,天津市博迪化工有限公司);浓盐酸(HCl,分析纯,西陇化工有限公司);无水乙醇(C2H6O,分析纯)和十八胺(C18H39N,分析纯)购于天津市福晨化学试剂厂。所有试剂未经进一步纯化,实验用水均为去离子水。
1.2 纳米WO3的制备
将1 mmol钨酸钠溶解于20 mL的蒸馏水,并将该钨酸钠水溶液加入到0.5 g熔融的十八胺中,形成白色絮状沉淀,随后加入6 mL浓HCl,形成乳白色前驱物,将上述前驱物移至高压反应釜的聚四氟乙烯内衬中,控制反应温度为150℃,反应时间为12 h。反应结束后将反应釜自然冷却到室温,所得浅黄色沉淀用乙醇离心洗涤数次,在干燥箱中干燥,得纳米WO3。
1.3 复合物WO3/CL-20的制备
称取少量CL-20在一定量的无水乙醇中超声分散均匀,按照质量比2∶1加入适量纳米WO3继续超声分散均匀,静置,干燥,得到复合物WO3/CL-20。
1.4 样品表征
采用美国FEI公司Quanta400场发射环境扫描电子显微镜分析样品形貌(电压20 kV,电流4 A)。用英国牛津公司INCAIE350能谱仪对样品进行元素分析。透射电镜测试由日本日立公司HITACHI H-7650B型透射电子显微镜完成,操作电压为80 kV,分辨率为0.2 nm(晶格像)。X射线粉末衍射测试采用日本理学D/MAX-3C型粉晶衍射仪,X射线源采用Cu Kα,波长为0.154 06 nm,测角仪精度±0.02°,重现性±0.03°(2θ),强度综合稳定度±0.5%。
1.5 纳米WO3对CL-20热分解的影响
采用差示扫描量热仪(Q2000-DSC型,美国TA公司)进行热分解实验,在动态高纯氮气气氛保护下,分别测试CL-20与复合物WO3/CL-20的热分解特性,动态流速为50 mL·min-1,温度范围50~300℃,升温速率为2.5、5.0、7.5、10.0℃·min-1,参比物为α-Al2O3,试样量约为0.22 mg,样品池为铝质坩埚。
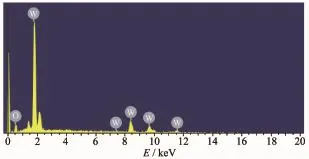
图1 纳米WO3的EDS图Fig.1EDS image of WO3nanoparticles
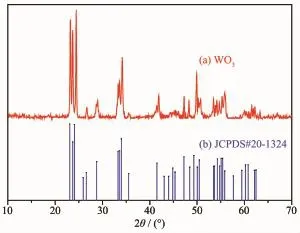
图2 纳米WO3(a)和JCPDS卡片20-1324(b)的XRD图Fig.2XRD pattern of nano-WO3(a)and JCPDS card 20-1324(b)
2 结果与讨论
2.1 组成分析
采用能谱分析仪对水热法制备的样品进行元素组成分析,结果如图1所示。图1显示被测样品中仅包含W、O两种元素,没有其他元素,说明制得的样品是钨氧化物。结合样品颜色为黄色,初步判定合成的样品为黄色氧化钨。
将制得的黄色产物通过XRD进行物相组成分析,结果如图2所示。图2中,2θ角为23.31°、23.62°、24.41°、26.44°、26.75°、28.94°、33.31°、33.62°、34.25°、35.50°、41.90°、43.16°、44.40°、45.34°、46.12°、47.36°、48.46°等处的衍射峰,分别对应于斜方晶系结构WO3的(001)、(020)、(200)、(120)、(111)、(021)、(201)、(220)、(121)、(221)、(031)、(320)、(131)、(311)、(002)、(040)等晶面(JCPDS No.20-1324),晶胞参数a= 0.738 4 nm,b=0.751 2 nm,c=0.384 6 nm,无其他杂峰存在,证明样品是纯WO3。与标准卡片对应的衍射峰相比,图2a中衍射峰出现宽化现象,这是由于合成的WO3为纳米级,粒径较小,产生小尺寸效应,影响其自身的XRD衍射峰。
3.2 形貌分析
图3(a)、(b)分别为纳米WO3的SEM和TEM图,从图3(a)中可以看出,产物为长方体形,颗粒较小,其尺寸大约在150~300 nm之间,没有明显的团聚现象。其透射电镜图(图3(b))进一步证明纳米WO3具有规则的长方体形形貌,分散性良好。

图3 纳米WO3的SEM图(a)和TEM图(b)Fig.3SEM(a)and TEM(b)images of WO3nanoparticles
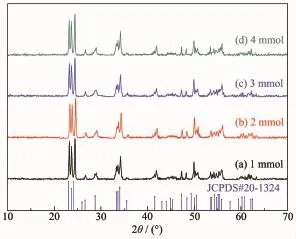
图4 不同钨酸钠加入量得到的纳米WO3的XRD图Fig.4XRD patterns of WO3nanoparticles obtained with different amount of sodium tungstate

图5 不同钨酸钠加入量得到的纳米WO3的SEM图Fig.5SEM images of nano-WO3obtained under different amount of sodium tungstate
3.3 纳米WO3形貌和组成的影响因素
3.3.1 钨酸钠的加入量
保持其它实验条件不变,改变钨酸钠的加入量,研究钨酸钠的量对WO3形貌的影响。图4是钨酸钠的加入量为1~4 mmol时得到的纳米WO3的XRD图。图中曲线衍射峰都与WO3的XRD标准卡片JCPDS 20-1324基本一致,没有其它杂质峰,说明制备的样品是纳米WO3。随着钨酸钠加入量的增加,相应产物的衍射峰强度未发生明显变化,且均较尖锐,说明产物纳米WO3均具有良好的结晶性。
图5是不同钨酸钠加入量得到的纳米WO3的SEM图。由图可见,随着钨酸钠量的增加,纳米WO3的形貌由规则的长方体形逐渐变为不规则的块状,同时出现了严重的团聚现象。这是由于钨酸钠加入量过多,与浓HCl反应后剩余的钨酸根离子吸附在水合氧化钨离子表面上,形成较稳定的带负电荷的胶体[16],致使合成的WO3颗粒相互粘结,影响了产物的分散性。结合图4可知,钨酸钠加入量为1 mmol时得到的样品具有良好的结晶性,形貌规则,且分散性较好。
3.3.2 反应时间
图6为不同反应时间获得的WO3的SEM图。当反应时间为3 h时,无纳米WO3颗粒形成,当反应时间为6 h时,最先形成微小的纳米粒子,不规则的纳米颗粒由无数个纳米小颗粒团聚构成。在水热条件下,由于受表面能的影响,纳米颗粒趋向逐渐团聚形成大颗粒以减少其表面能。因此,随着反应时间的延长,反应时间为10 h时,不规则颗粒的尺寸逐渐变大,出现比较均匀的WO3颗粒,但颗粒大小不一,团聚现象很严重。时间延长至12 h时,出现分布均匀的纳米WO3长方体。
图7为不同反应时间得到的纳米WO3的XRD图。对比WO3的XRD标准卡片JCPDS 20-1324可知,图中曲线衍射峰出现宽化现象,导致出峰密集区域某些峰叠加,但衍射峰位置与标准卡片基本一致,没有其它杂质峰,说明制备的样品是纳米WO3。

图6 不同反应时间得到的纳米WO3的SEM图Fig.6SEM images of WO3nanoparticles obtained with different reaction times
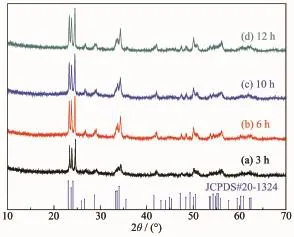
图7 不同反应时间得到的纳米WO3的XRD图Fig.7XRD patterns of WO3nanoparticles obtained with different reaction times
通过对不同水热时间下颗粒形貌的分析,得到纳米WO3可能的生长机理(如图8所示:成核—外延生长—重结晶。钨酸钠先与浓HCl反应使足够的钨酸完全沉淀后,在十八胺的辅助下形成凝聚体,随反应时间延长,小颗粒逐渐从凝聚体上剥离形成纳米晶核,纳米晶核按一定取向进一步生长,当反应时间延长至12 h时,得到形貌规则且分散性良好的长方体形纳米WO3。
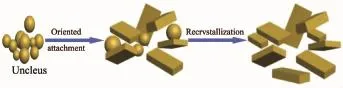
图8 纳米WO3晶体的形成机理示意图Fig.8Schematic illustration of the formation mechanism of nano-WO3crystal
3.4 纳米WO3对CL-20热分解的影响
用DSC法分别研究了CL-20和复合物WO3/ CL-20的热分解行为,结果如图9所示。随加热温度的升高,CL-20和复合物WO3/CL-20均发生分解反应,在50~300℃温度范围内仅出现一个放热峰,峰温分别为248.83℃和246.03℃。加入纳米WO3后使CL-20的分解峰温降低了2.95℃。运用量热法评估纳米WO3与CL-20的相容性[17-19],评价等级为B (轻微敏感),表明两种物质混合可短期内使用。
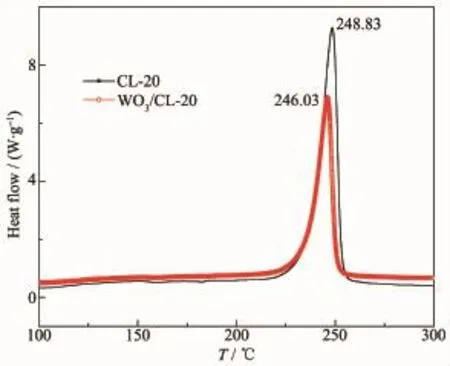
图9 CL-20和复合物在10℃·min-1升温速率下的DSC曲线Fig.9DSC curves of CL-20 and composite at 10℃·min-1
以上相容性分析可知,与CL-20热分解相比,纳米WO3的加入可降低混合体系分解峰峰温,为进一步研究纳米WO3对CL-20热分解性能的影响,确定其遵循的最概然机理函数f(α),对CL-20及混合体系WO3/CL-20在差示扫描量热仪上进行不同升温速率的非等温热分解动力学分析。利用Kissinger方程[20]和Flynn-Wall-Ozawa[21]方程计算得到CL-20和复合物WO3/CL-20的热分解动力学参数(表观活化能(Ea)和表观指前因子(A))。
表1为在不同升温速率(β)下计算得到的CL-20和复合物WO3/CL-20热分解的动力学参数。由表1可知,CL-20的活化能为180.83 kJ·mol-1,复合物WO3/CL-20的活化能为173.09 kJ·mol-1,加入纳米WO3后,复合物的活化能较单组分CL-20降低7.74 kJ·mol-1,说明纳米WO3能够加速CL-20的热分解反应。
从不同升温速率(β)下CL-20、复合物WO3/CL-20热分解的DSC曲线中获得Ti,并由Ozawa方程计算出反应分数α对应的表观活化能Eα,取α及Eα绘制Eα~α曲线,结果如图10所示。从中发现在α为0.400~0.800之间时,活化能变化很小,意味着在这个过程中分解机理没有本质的改变。
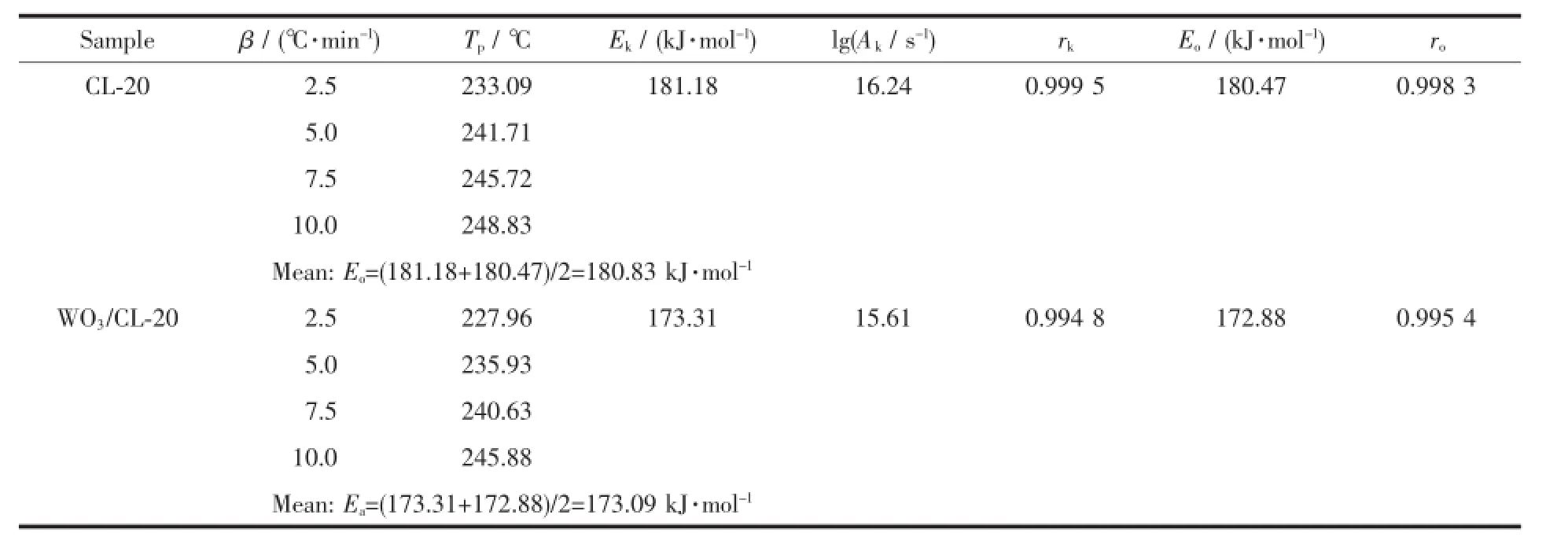
表1 不同加热速率(β)下CL-20和WO3/CL-20的动力学参数的计算值Table 1Calculated values of kinetic parameters of CL-20 and WO3/CL-20 at the different heating rates(β)

表2 CL-20和WO3/CL-20动力学参数的计算值Table 2 Calculated values of kinetic parameters of CL-20 and WO3/CL-20
将α(0.400~0.800),升温速率(β)为2.5、5.0、7.5、10.0℃·min-1对应的Ti(任意点α对应的温度)数据和41种动力学机理函数[22]中的每一个G(α)和f(α)代入MacCallum-Tanner、šatava-šesták、Agrawal和General integral方程[23],用线性回归处理和逻辑选择法确定的CL-20和WO3/CL-20放热分解反应的动力学参数,列于表2。计算得到的活化能E和指前因子A与表1相应数值基本一致,由此确定CL-20和WO3/CL-20放热分解遵循Avrami-Erofeev方程,其动力学机理函数分别为f(α)=5(1-α)[-ln(1-α)]3/5/2和f(α)=3(1-α)[-ln(1-α)]2/3。分别将表2中CL-20和WO3/CL-20的活化能E、指前因子A和f(α)代入方程可得CL-20和WO3/CL-20热分解放热过程的动力学机理方程分别为:
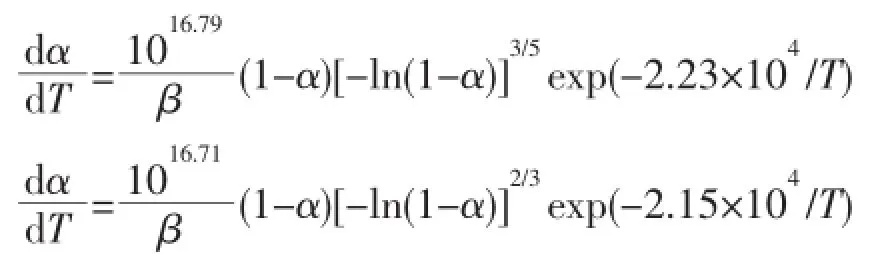
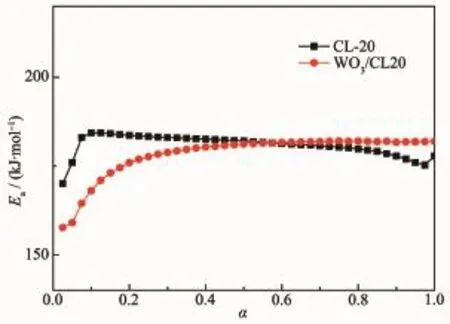
图10 由Ozawa法得到的CL-20和WO3/CL-20的Ea~α曲线Fig.10Ea~α curves of decomposition of CL-20 and WO3/CL-20 by Ozawa method
CL-20分解以N-NO2键断裂为初始控制步骤,反应在较多的“活性中心”开始“成核”,并进行“核生长”,随着NO2的释放还有H2O、NO、CO2、N2O、NH3等气体产物生成。同时生成高稳定性的环状连氮化合物会在固体表面上吸附,使活性中心失活,反应速度减慢[18],并且该环状连氮化合物对燃速也有抑制作用[24-25]。当加入纳米WO3后,由于其颗粒尺寸小,表面能高,可吸附CL-20反应生成的气体,促进NNO2键断裂,减缓生成环状连氮化合物的速度,从而降低其分解温度和活化能。
4 结论
采用水热法合成纳米WO3,研究获得形貌均一、结晶性和分散性良好的长方体形纳米WO3的最佳反应条件为:反应物钨酸钠的加入量为1 mmol,150℃下反应12 h,其形成机理为成核—外延生长—重结晶。将该样品与CL-20复合进行热分解动力学研究,发现加入纳米WO3后,较单组分CL-20,混合体系的分解峰温降低2.95℃,活化能降低7.74 kJ·mol-1,纳米WO3能够加速CL-20的热分解过程,CL-20和复合体系的热分解遵循Avrami-Erofeev方程。
[1]Li X L,Lou T J,Sun X M,et al.Inorg.Chem.,2004,43(17): 5442-5449
[2]WANG Chao(王超),XU You(许友),ZHANG Bing(张兵). Chinese J.Inorg.Chem.(无机化学学报),2014,30(7):1575-1581
[3]Gondal M A,Dastageer M A,Khalil A.Catal.Commun., 2009,11(3):214-219
[4]Baek Y,Yong K.J.Phys.Chem.C,2007,111(3):1213-1218
[5]Wang Z,Sun P,Yang T,et al.Sensor Lett.,2013,11(2):423-427
[6]Zhang G,Guan W,Shen H,et al.Ind.Eng.Chem.Res., 2014,53(13):5443-5450
[7]Mwakikunga B W,Sideras-Haddad E,Forbes A,et al.Phys. Status Solidi A,2008,205(1):150-154
[8]Mwakikunga B W,Forbes A,Sideras-Haddad E,et al. Nanoscale Res.Lett.,2010,5(2):389-397
[9]Yagi M,Maruyama S,Sone K,et al.J.Solid State Chem., 2008,181(1):175-182
[10]Lee S H,Deshpande R,Parilla P A,et al.Adv.Mater.,2006, 18(6):763-766
[11]Wang J,Khoo E,Lee P S,et al.J.Phys.Chem.C,2008, 112(37):14306-14312
[12]Wang J,Khoo E,Lee P S,et al.J.Phys.Chem.C,2009, 113(22):9655-9658
[13]Ou J Z,Balendhran S,Field M R,et al.Nanoscale,2012,4 (19):5980-5988
[14]WEI Xiao-Lan(魏小兰),SHEN Pei-Kang(沈培康).Sci. China Ser.B(中国科学:B辑),2005,35(4):291-295
[15]YU Xian-Feng(于宪峰).Chin.J.Expls.Propell.(火炸药学报),2004,27(3):78-80
[16]LIU Xin-Jin(刘新锦),LUO Chao-Jun(罗朝军),HUANG Tie-Gang(黄铁钢).J.Xiamen Univ.(厦门大学学报),1996,35 (5):750-754
[17]AN Ting(安亭),ZHAO Feng-Qi(赵凤起),GAO Hong-Xu(高红旭).Chin.J.Mater.Eng.(材料工程),2011,11:23-28,34
[18]LIU Zi-Ru(刘子如).Thermal Analyses for Energetic Materials (含能材料热分析).Beijing:National Defense Industry Press, 2008:21-22
[19]YAN Qi-Long(严启龙),LI Xiao-Jiang(李笑江),LIAO Lin-Quan(廖林泉),et al.Chin.Energ.Mater.(含能材料),2008, 16(3):309-314
[20]Kissinger H E.Anal.Chem.,1957,29(11):1702-1706
[21]Ozawa T B.Chem.Soc.Jpn.,1965,38(11):1881-1886
[22]HU Rong-Zu(胡荣祖),SHI Qi-Zhen(史启祯).Thermal Analysis Kinetics(热分析动力学).Beijing:Science Press, 2001:127-131
[23]Hu R Z,Yang Z Q,Liang Y J.Thermochim Acta,1988,123: 135
[24]Volk F.Propell.Explos.Pyrot.,1985,10:139-146
[25]Williams G K,Palopoli S F,Brill T B.Combust.Flame, 1994,98:197-204
Nano-WO3:Preparation,Characterization and Effect on Thermal Decomposition of Hexanitrohexaazaisowurtzitane
ZHAO Ning-Ning1HE Cui-Cui1WANG Tong1
AN Ting2ZHAO Feng-Qi2HU Rong-Zu2MA Hai-Xia*,1
(1School of Chemical Engineering,Northwest University,Xi′an 710069)
(2Science and Technology on Combustion and Explosion Laboratory,Xi′an Modern Chemistry Research Institute,Xi′an 710065)
The cuboid-shaped WO3nanoparticles were prepared by the hydrothermal method with controlling the amount of reactant and reaction time,then the as-prepared particles were characterized by X-ray powder diffraction(XRD),transmission electron microscope(TEM),and scanning electron microscope-energy dispersive spectrometry(SEM-EDS).The Effects of WO3powders on the thermal decomposition of hexanitrohexaazaisowurtzitane(CL-20)were investigated by differential scanning calorimetry(DSC).The results show that the peak temperature of the decomposition and the activation energy of WO3/CL-20 have 2.95℃and 7.74 kJ·mol-1lower than that of CL-20,indicating that nano-WO3could accelerate the thermal decomposition of CL-20.
nanosized tungsten trioxide;hexanitrohexaazaisowurtzitane;hydrothermal method;thermal decomposition
O643
A
1001-4861(2015)10-1959-07
10.11862/CJIC.2015.263
2015-01-13。收修改稿日期:2015-07-16。
国家自然科学基金(No.21073141,21373161);教育部新世纪优秀人才支持计划基金(No.12-1047);高等学校博士学科点专项科研基金(No.20126101110009);燃烧与爆炸技术重点实验室基金(No.9140C3501041001)资助项目。
*通讯联系人。E-mail:mahx@nwu.edu.cn;会员登记号:S06N4591S1504(赵宁宁)和S06N4041M1101(马海霞)。
