聚乙烯基三苯乙炔基硅烷的制备及热性能分析
2015-11-30谭德新王艳丽邢宏龙史铁钧
谭德新,王艳丽,邢宏龙,唐 玲,史铁钧
(1.安徽理工大学化工学院,安徽 淮南 232001;2.安徽理工大学材料科学与工程学院,安徽 淮南 232001;3.合肥工业大学化工学院,合肥 230009)
近年来,含有芳炔基团的有机硅聚合物以其优良的光敏、导电、耐高温等特性,引起了人们的广泛关注[1].该类树脂含碳量达90%以上,热解残炭率极高[2].目前,该类单体的合成方法主要有偶合脱氢反应法、亚铜化物法、有机锂法、格氏试剂法等,但由于操作工艺和原料价格的影响,使得该类材料的研究与应用受到限制[3-4].在这4种合成方法中,格氏试剂法可以简化合成工艺,降低合成成本,虽然产率不是很高,但反应条件比较温和,没有严格的无水无氧限制,便于实验室研究与工业应用[5-6].
对于本文合成的乙烯基三苯乙炔硅烷,目前只检索到德国学者采用络合催化剂法合成相应的结构并通过氢谱来证实产物的部分结构,而对于其物理性能和化学性能没有作进一步的研究[7].目前人们主要关注含硅芳炔单体及其聚合物的合成及其结构与性能之间的关系,对其热分解相关性能关注较少[8-9].
本文以氯硅烷、苯乙炔为原料,镁带为催化剂,采用格式反应,合成了乙烯基三苯乙炔基硅烷(VTPES),运用红外、核磁对合成产物进行了结构分析,并通过热重分析法研究了该聚合物的热分解行为.
1 实验
1.1 实验原料及仪器
苯乙炔,CR,山东淄博汉王公司;镁条,AR,上海化学试剂有限公司;乙烯基三氯硅烷,CR,安徽凤台淮河化工厂;四氢呋喃、盐酸,AR,上海中试化工总公司;溴乙烷、无水氯化钙,AR,天津市大茂化工试剂厂;二甲基甲酰胺,AR,国药集团化学试剂有限公司;真空管式炉,GSL 1600X,合肥科晶材料技术有限公司;傅里叶变换红外光谱仪,Spectrum 100,美国PerkinElmer;热重分析仪,TG209F3,德国 Netzsch;傅立叶核磁共振谱仪,Avance AV-400,瑞士布鲁克.
1.2 实验单体及聚合物的制备
单体的合成实验室自制[10],反应式如图1所示.
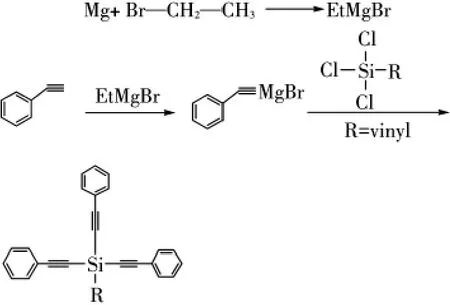
图1 格氏反应示意图
单体VTPES的固化反应程序温度控制如下,其中温度取值根据DSC曲线获得[10]:
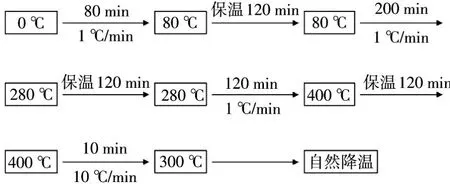
1.3 结构及性能测试
单体PTPES红外测试采用KBr压片法;核磁测试用氘代氯仿为溶剂,TMS为内标;热重分析是将聚合物PPTPES固体进行充分研磨后过200目筛子,每次称量取相同质量,约6.0 mg,升温速率分别取 5、10、20、40 ℃ /min,氮气流量为40 mL/min,升温范围为室温~800℃.
2 结果与讨论
2.1 单体VTPES结构分析
单体VTPES的红外谱图见图2,其中,主要特征峰对应的波数如下:2 919、2 945、3 057、1 600、1 491 cm-1,1 220 和1 026 cm-1为苯环的吸收振 动 峰,2 160 cm-1为的吸收峰,756 cm-1为的吸收峰.由图2可知:红外谱图中的3 340~3 250 cm-1处没有吸收峰,说明苯乙炔已经反应完全;506 cm-1处没有出现尖锐的强峰,表明键也已反应完全.
单体的氢谱见图3,其中,化学位移6.33是CH=CH2上氢的位移,而化学位移为7.35~7.59的峰是苯环上氢的化学位移.另外,乙烯基上氢(m,3H,CH=C H2)、炔基相连苯环上邻位的氢以及与炔基相连苯环上非邻位上的氢(m,9H,PhH)对应的峰的面积比为3∶6∶9,与结构式上3种氢的个数相对应,与文献分析相一致[11-13].
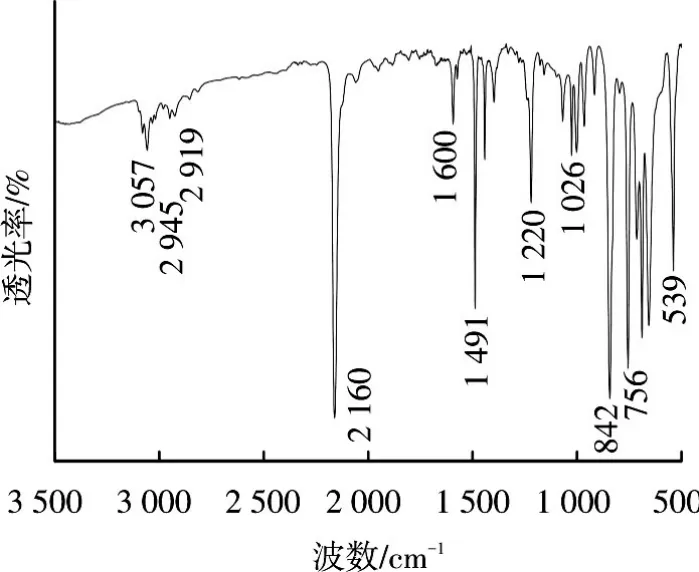
图2 单体VTPES的FTIR
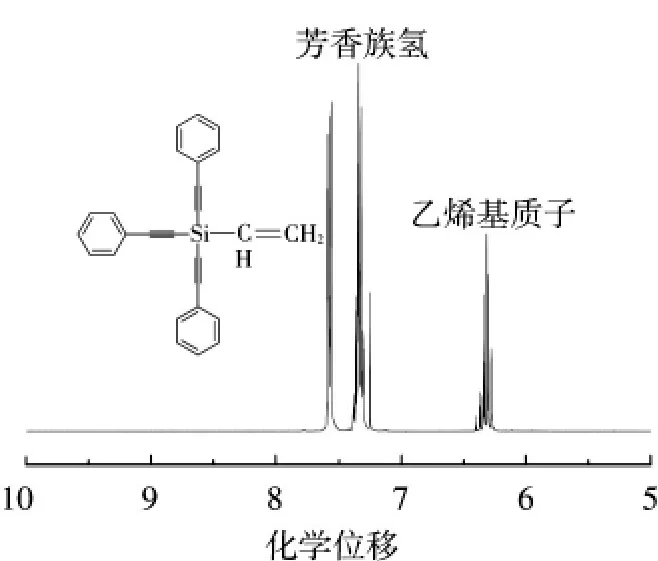
图3 单体FVTPES的1H-NMR
单体的碳谱如图4所示,其中,化学位移86.9、107.88 对应硅炔上的碳,107.9 对应苯炔上的炔碳,131.90、137.38 对应硅烯上的碳,而苯环上碳的化学位移为122.62、128.72、129.87 和132.79.图5为单体的29Si-NMR 谱图,图中显示硅的化学位移为-71.34,单体中硅原子所处的化学环境相同.
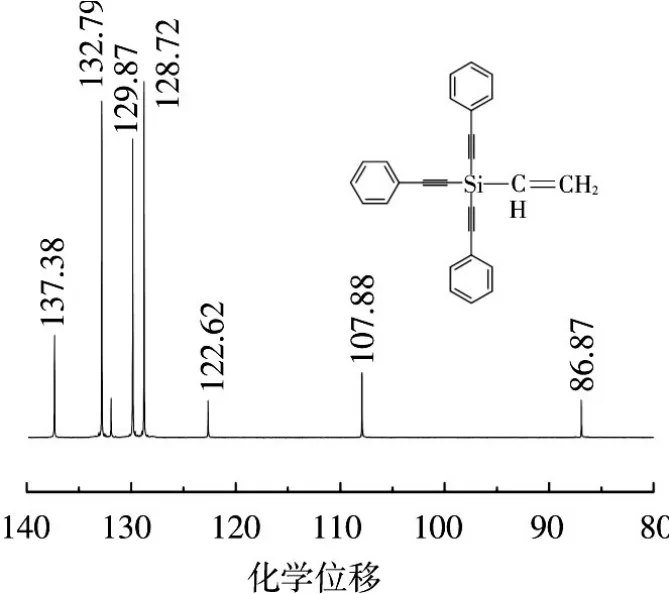
图4 单体VTPES的13C-NMR
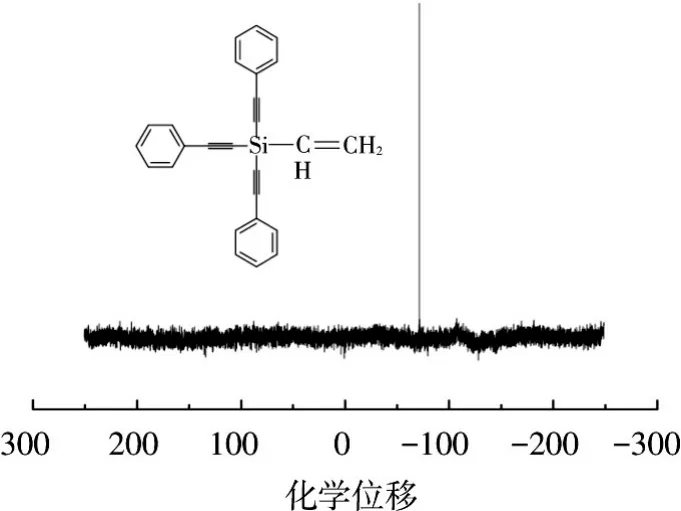
图5 单体VTPES的29Si-NMR谱图
2.2 聚合物的热分解动力学分析
图6分别是不同升温速率下聚合物PVTPES的TG和DTG曲线.结合图6(a)与图6(b)可知,PVTPES的TG曲线只有一个热分解阶段,Td5为550℃左右,而且当温度增加到800℃左右时,聚合物的残炭率仍在80%左右,表明聚合物具有较高的耐热性和残炭率.
研究热分解过程的动力学分析方法有很多,较常用的有Kissinger最大热失重率法、Owaza等转化率法、Freeman-carroll差减微分法、Reich拐点最大速率法[14].其中,Kissinger法是利用 DTG曲线的峰值对应的温度和升温速率的关系进行动力学参数的计算,其计算过程简便,取点容易,适用于任何反应级数;而对于多数碳聚合物,Ozawa法同样适用,而且结果更为可靠.这两种方法因不涉及机理,所以一直被广泛用来分析聚合物的热分解行为.
本文采用Kissinger最大热失重率法和Ozawa等失重百分率法计算出聚乙烯基三苯乙炔基硅烷树脂的热分解动力学参数(活化能以及指前因子),并通过Crane方程求得分解反应的反应级数.
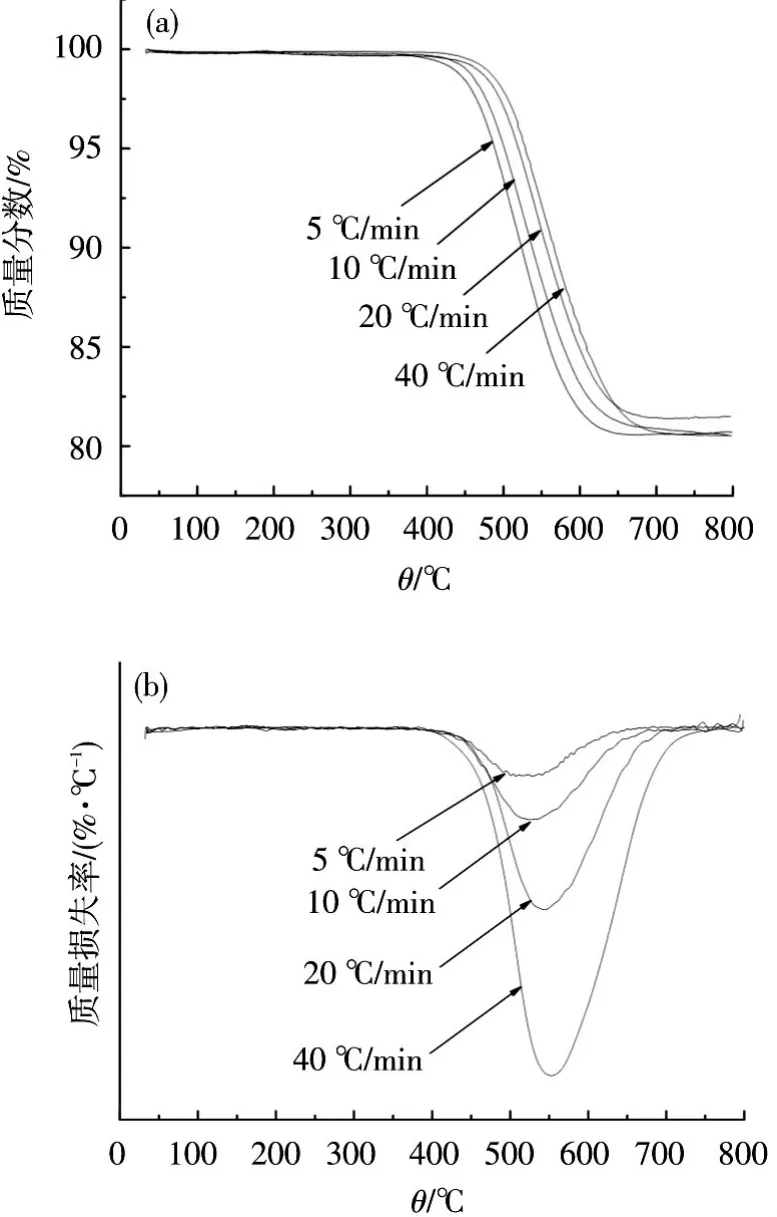
图6 不同升温速率下PVTPES树脂的热重曲线(a)和微分热重曲线(b)
2.2.1 Kissinger最大失重率法
Kissinger最大失重率法理论见文献[15],根据文献,以ln(β/Tp2)对1/TP作图得图7曲线.由图7可得:相关系数 R=0.997 5,斜率为-32.06,则分解活化能为E=266.55 kJ/mol;截距为29.06,则 A=1.33×1014s-1.同时根据 Crane 方程[16],以ln β对 1/Tmax作图得拟合曲线斜率为-34.37(R=0.997 1),根据曲线斜率即可求出 n=0.93.
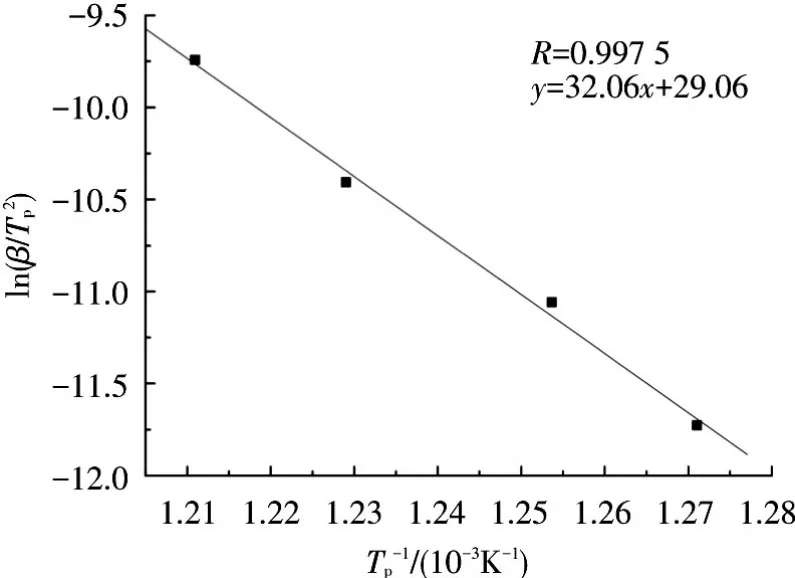
图7 PVTPES的ln(β/TP2)-1/Tp
2.2.2 Ozawa等失重百分法
Oawza理论见参考文献[14],根据文献在不同转化率下以lg β对1/T作图,得图8,拟合曲线的线性相关性及热分解活化能见表1.
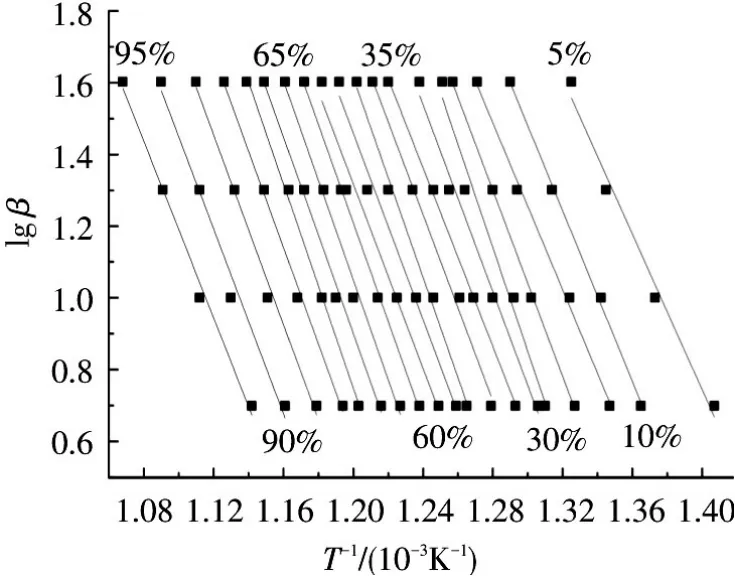
图8 PVTPES 的lg β -T-1
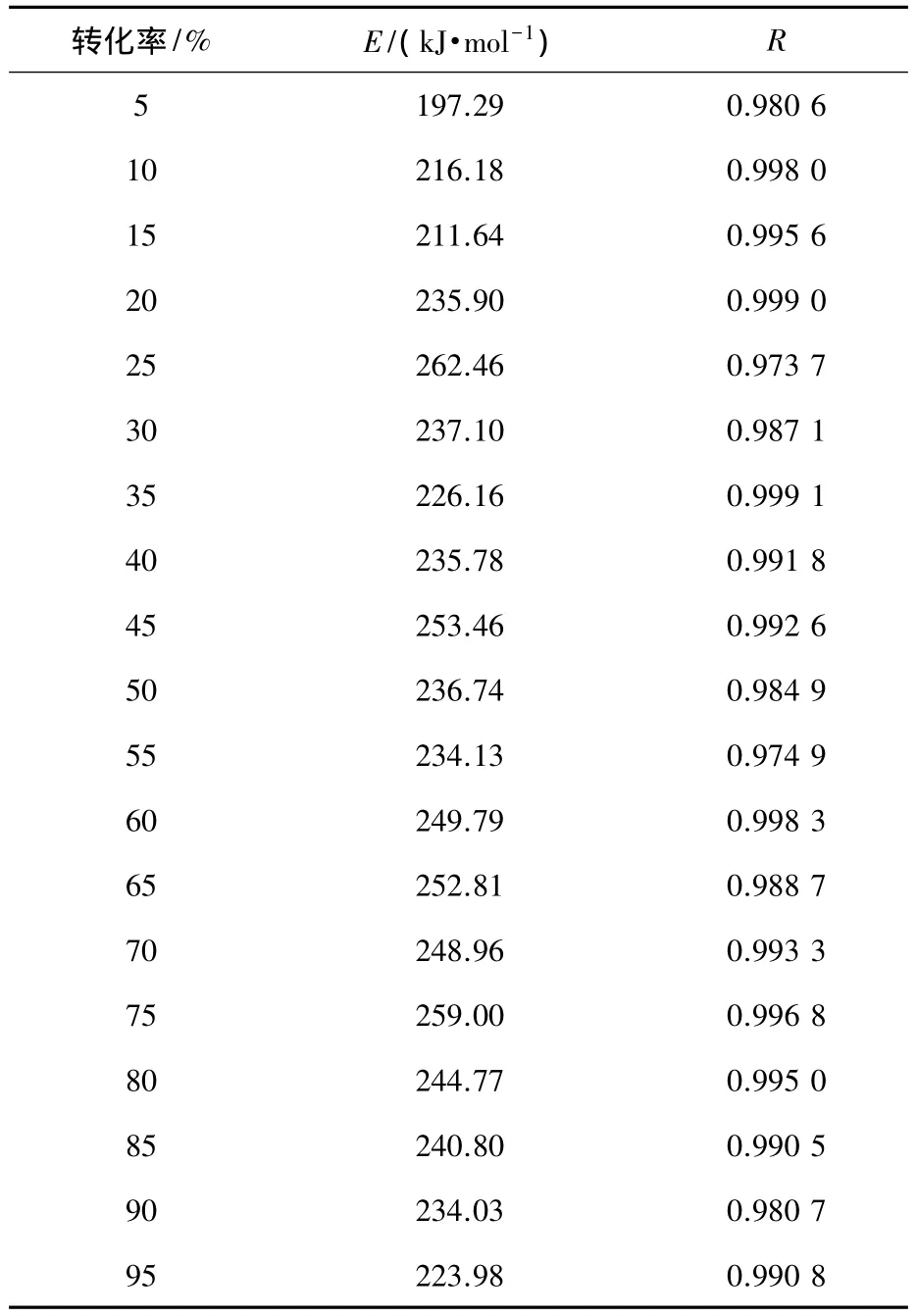
表1 Ozawa法计算得到的聚合物PVTPES特征参数
结合图8和表1可以知道,对于转化率在5%到95%之间变化,反应体系的活化能从197.29 kJ/mol增加到 262.46 kJ/mol,变化区间并不大,另外相关系数的值都比较接近1,相关性很好,所以数据有一定的可靠性,可进一步求得E的平均值为236.89 kJ/mol.
通过两种分析方法得到的PVTPES聚合物的热分解活化能分别为266.55 和236.89 kJ/mol,两种分析方法所计算得到的活化能基本一致,其偏差是由于不同的假设而引起的,表明聚合物PVTPES的分解反应活化能在250 kJ/mol左右,另外Crane方程求出的反应级数为0.93,接近1,说明反应为一级反应.
3 结 论
1)以苯乙炔和乙烯基三氯硅烷为原料,利用格氏反应成功制备了乙烯基三苯乙炔基硅烷单体,利用热聚合法通过程序控温制备了聚乙烯基三苯乙炔基硅烷树脂,热重分析显示树脂Td5在550℃左右,800℃时树脂的残炭率在80%左右,显示很好的热稳定性.
2)Kissinger法和Ozawa法计算得到的树脂分解活化能分别为266.55 和236.89 kJ/mol,两种分析方法计算得到的活化能基本一致.用Kissinger法计算得到的指前因子为1.33×1014s-1.
3)Crane方程计算出的结果表明,聚合物PVTPES热分解反应近似为一级反应.
[1] LIU J Z,LAM J W Y,TANG B Z.Acetylenic polymers:syntheses,structures,and functions[J].Chem Rev,2009,109:5799-5867.
[2] 黄发荣.先进树脂基复合材料[M].北京:化学工业出版社,2008:80.
[3] JIANG Z X,MENG L H,HUANG Y D,et al.Influence of coupling agent chain lengths on interfacial performances of polyarylacetylene resin and silica glass composites[J].Appl Surf Sci,2007,253:4338 -4343.
[4] ISHIKAWA J,INOUE K,ITOH M.Dehydrogenative Cross-coupling reactions between phenylsilane and ethynylbenzene in the presence of metal hybrides[J].J Organomet Chem,1998,552(1/2):303-311.
[5] 陈麒,倪礼忠,李杨,等.苯乙炔基硅烷及其制备方法:中国,1421446A[P].2003-06-04.
[6] CHEN Q,LI Y,DAI Z L,et al.Synthesis and characterization of methyl-di(phenylethynyl)silane and its network polymer[J].Acta Chim Sin,2005,63(3):254-258.
[7] LANG H R,BLAU S,RHEINWALD G,et al.Synthese,koordinationsverhalten und thermolyse alkinylfunkionalisierter übergangsmetall-komplexe;kristallstruktu r(Mo2(η5—C5H5)2(CO)4((μ4—η2:2:2:2—Me3SiC ≡ C—C ≡ C SiMe3)—Co2(CO)6))[J].J Organomet Chem,1995,494(1/2):65-73.
[8] ZHOU Q,NIL Z.Thermalcharacteristicsand pyrolysis of methyl-di(phenylethynyl)silane resin[J].J Appl Polym Sci,2007,103:605-610.
[9] 徐美玲,石松,王禹慧,等.含硅芳炔树脂热裂解行为及动力学[J].玻璃钢/复合材料,2010(6):35-39.XU Meiling,SHI Song,WANG Yuhui,et al.Thermal pyrolytic behaviors and kinetics of silicon-containing arylacetylene resin[J].Fiber Reinforced Plastics/Composites,2010(6):35-39.
[10] TAN D,SHI T,LI Z.Synthesis,characterization and non-isothermal curing kinetics of two silicon-containing arylacetylenic monomers[J].Res Chem Intermed,2011,37(8):831-845.
[11] MELISSARIS A P,LITT M H.New high-Tg,heatresistant,cross-linked polymers:synthesis and characterization of di-p-ethynyl-substituted benzyl phenyl ether monomers[J].Macromolecules,1994,27(4):883-887.
[12] ITOH M,INOUE K,IWATA K,et al.New highly heat-resistant polymers containing silicon:poly(silyleneethynylenephenyleneethynylene)s[J].Macromolecules,1997,30(4):694-701.
[13] OHSHITA J,IIDA T,IDEDA M,et al.Synthesis of poly{[bis(diethynylphenyl)-silylene]phenylene}s with highly heat-resistant properties and an application to conducting materials[J].J Organomet Chem,2004,689:1540-1545.
[14] 胡荣祖,高胜利,赵凤起,等.热分析动力学[M](2版).北京:科学出版社,2008:79-117.
[15] 卢林刚,张晴,徐晓楠,等.一种无卤阻燃聚丙烯的热分解动力学[J].高分子材料科学与工程,2010,26(11):39-43.LU Lingang,ZHAN Qing,XU Xiaonan,et al.The kinetics of thermal deregradation of a halogen-free flame-retarded polypropylene[J].Polymer Materials Science and Engineering,2010,26(11):39-43.
[16] 李爱玲,熊金平,左禹,等.聚氨酯胶黏剂的热分解动力学研究[J].物理化学学报,2007,23(10):1622-1626.LI Ailing,XIONG Jinping,ZUO Yu,et al.Thermal decomposition kinetics of polyurethane adhesive[J].Acta Phys Chim Sin,2007,23(10):1622-1626.
