电渗析技术清洁分离纯化肌氨酸
2015-11-26汪耀明李为徐铜文
汪耀明,李为,徐铜文
电渗析技术清洁分离纯化肌氨酸
汪耀明1,李为2,徐铜文1
(1中国科学技术大学化学与材料科学学院,安徽合肥230026;2合肥科佳高分子材料科技有限公司,安徽合肥 230601)
肌氨酸作为一种高附加值的精细化工产品具有广泛的应用前景。目前肌氨酸的生产过程中存在肌氨酸产品与无机盐的分离过程。传统的分离方法为分步结晶法,存在能耗高、消耗的化学试剂多、污染大等缺点。为实现肌氨酸的清洁生产,本文采用自制电渗析装置对肌氨酸进行分离纯化,考察了操作电流以及溶液起始pH对整个分离效果的影响。结果表明,当操作电流为2 A,起始pH为6.5时,电渗析过程中无机盐的去除率大于99%,其产品得率为71.5%,电渗析工艺生产肌氨酸的能耗为26.4 kW·h·t-1,总成本仅为311元·t-1,大大优于传统的生产工艺。由此可见,电渗析工艺可实现肌氨酸产品的节能、环保生产。
离子交换膜;电渗析;肌氨酸;清洁生产
引 言
肌氨酸,又名-甲基甘氨酸,是合成肌酸的中间体,传统上是作为工业用品染料稳定剂和日用化学品氨基酸型表面活性剂[1]。同时,肌氨酸还有一些独特的生理功能,如提高人的智力、增加肌肉无氧力量和爆发力、防治大脑损伤、改善运动表现等诸多生理功能,在医药、保健品中得到越来越广泛的使用[2-3]。特别是近年来的研究发现肌氨酸可作为前列腺癌非损伤性诊断的高灵敏性和特异性检测试剂,具有广泛的应用前景[4-7]。
肌氨酸的制备方法为化学合成法[8-11],主要分为两种,一种是从羟基乙腈出发,与甲胺进行反应生成甲氨基乙腈,甲氨基乙腈在碱性下水解得到肌氨酸钠,肌氨酸钠再通过酸化得到肌氨酸;另一种是从氯乙酸钠出发,与甲胺在80~85℃下反应得到甲氨基乙腈,再在碱性下水解得到肌氨酸钠,肌氨酸钠再通过酸化得到肌氨酸。无论是哪种方法都会得到中间产物肌氨酸钠,肌氨酸钠通过强的无机酸(通常是盐酸)进行酸化,得到掺杂无机盐(氯化钠)的目标产物。为了得到高纯的肌氨酸,需要一个脱盐纯化的工艺,目前最常用的是分步结晶法,主要利用肌氨酸与氯化钠在不同温度下的溶解度差异性,氯化钠随温度变化的溶解度差异较大而首先分离出整个体系。但是,这种传统分离方法存在很多局限性。首先,整个分离过程很难精确控制。由于分离过程是根据结晶先后次序不同而进行的,无法定量地判断分离终点,导致不同批次间的分离效果差异性较大。其次,这种传统分离过程很难制备出高纯度的产品。再次,整个分离过程的产品得率较低,分离过程中的肌氨酸的损失较大。最后,这种分步分离过程的能耗较大,环境污染严重。因此,如何选择一种更加环境友好、能耗低、分离效率高的分离方法,是制备高纯度肌氨酸产品的关键。
基于离子交换膜的电渗析作为一种环境友好、方便快捷的新型分离技术得到了人们越来越普遍的关注[12-14],它的原理是利用离子的定向迁移和离子交换膜的选择透过性,可以实现电解质溶液的浓缩或淡化[15-17]。利用电渗析的原理,进行常规氨基酸的分离纯化常见报道,如胱氨酸、谷氨酸、酪氨酸、乳酸、甘氨酸等[18-21],但是这类氨基酸都是属于生命蛋白的基本氨基酸,而利用基于电渗析的电膜技术用于精细化工产品的新型氨基酸如肌氨酸的分离转化却鲜见报道。由于肌氨酸是弱酸,在其等电点处呈电中性,而氯化钠是强电解质,利用这个特点,将掺杂无机盐的肌氨酸母液的pH调节至肌氨酸的等电点,利用电渗析的原理,便可以实现对肌氨酸和氯化钠的分离。本文主要探讨利用电渗析技术生产肌氨酸的可行性,并对整个分离过程的经济性进行评价。由于肌氨酸作为众多化学合成氨基酸产品中的一种,其制备方法与其他氨基酸产品(如蛋氨酸、,-二甲基甘氨酸、苯甘氨酸、维生素B12、缬氨酸)比较类似,这类氨基酸化学合成法制备过程中均存在一个脱盐的工艺,因此,本文提供的电渗析分离法可为这类氨基酸的清洁生产提供参照。
1 实验材料和方法
1.1 材料
含氯化钠的肌氨酸初品由某公司提供,以溶液形式存在,称为肌氨酸母液,其盐质量分数为2.1%。均相阴、阳离子交换膜(CJ-MA-2、CJ-MC-2)由合肥科佳高分子材料科技有限公司提供,其主要性能指标列于表1。
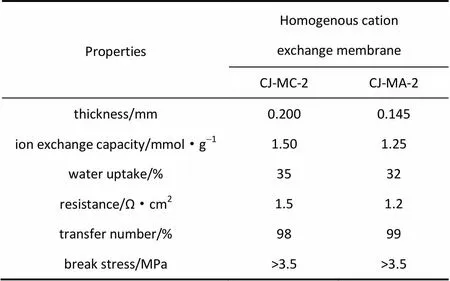
表1 膜的主要技术指标
1.2 实验装置
CJ-ED-1实验室普通电渗析脱盐系统,是由合肥科佳高分子材料科技有限公司自主设计产品,含有1对电极和7对均相离子交换膜(其中阴离子交换膜为CJMA-2,阳离子交换膜为CJMC-2),有效面积为300 cm2,整个电渗析过程的原理如图1所示。DDS-307A型电导率测定仪(上海盛磁仪器有限公司)、SC-3610型离心机(安徽中科中佳科学仪器有公司)、IC-3000型离子色谱仪(戴安公司)。
1.3 电渗析实验过程
本实验所用的CJ-ED-1实验室普通电渗析脱盐系统,由合肥科佳高分子材料科技有限公司自主设计,整个电渗析系统主要由4部分构成:
①直流电源(WYL-605×2S,杭州余杭四岭有限公司)。
②烧杯,用于储存料液,分别为极室、浓缩室和淡化室(料液室)。
③潜水泵(HJ-311,浙江森森有限公司),用于循环料液,最大流速300 L·h-1,3台泵分别与3个料液室通过硅胶管相连,形成3个独立的闭合 回路。

图1 电渗析法分离氨基酸母液的原理示意图
Note: The dotted box means the repeating number of anion and cation exchange membrane is five
④电渗析膜堆。
膜堆包括:
①阳极和阴极,材质为钌铱电极。
②带格网的有机复合垫片,厚度为0.08 cm,用于分隔相邻的离子交换膜同时提供液体流动的通道。
③7张CJMC-2阳离子交换膜和7张CJMA-2阴离子交换膜,单张膜有效面积为110 mm×270 mm。
④支撑电解质:极室为400 ml,0.3 mol·L-1的硫酸钠溶液作为极室的支撑电解质;在淡化室注入400 ml肌氨酸母液,浓缩室注入同样体积的自来水。
在接入直流电源之前,膜堆先行循环30 min,使料液得到充分的循环和稳定。实验过程中,连续测量电导率,按照设定的时间记录数据;当电导率降至1000 μS·cm-1时停止电渗析实验,同时取样进行肌氨酸含量的检测。整个实验在室温下进行。
1.4 计算公式
脱盐率(r)的计算公式如下
式中,为电渗析实验结束时肌氨酸液相色谱峰的峰面积;0为实验开始时,母液中肌氨酸液相色谱峰的峰面积。
电渗析过程中的能耗(,kW·h·L-1)计算公式如下
式中,为膜堆的电压降,V;为施加的电流,A;为料液室的体积,L;为时间。
1.5 测定方法
电导率通过电导率仪直接测定。
pH由pH计测定。
肌氨酸含量通过液相色谱仪(Agilent 1260 Infinity)进行测定。流动相为甲醇与水的混合溶液,比例为1:9,流速为1 ml·min-1;进料量为20 µl;检测波长为210 nm。
2 实验结果与讨论
2.1 不同电流分离效果
图2所示为电渗析不同操作电流对膜堆电压降及溶液电导率的影响情况。从图2 (a)中可以看出,随着电流的增加,处理同等体积的料液所需的时间是逐步减少的,这主要是由于电流越大,电渗析过程中离子迁移的推动力越大,处理能力越快。同时,膜堆的电压降随着时间的进行有一个先降低后上升的趋势,这是由本电渗析实验中料液体系决定的。由于本电渗析实验中浓缩室中的起始料液为自来水,在电场的作用下,肌氨酸母液中的盐离子会迁移出淡化室,并不断在浓缩室中累积;随着离子的不断迁移,整个浓缩室的电阻是不断下降的,这也使得整个膜堆的电阻呈现出下降的趋势。但是,随着电渗析实验的不断进行,淡化室中可导电的无机离子逐渐减少,随着淡化室中氯化钠的耗尽,淡化室中的溶液电阻急剧上升,这也使得膜堆的电压降急剧上升。当电流在1.0和1.5 A时,由于离子迁移的推动力相对较小,膜堆电压降上升的速率较慢;而在高电流下,电压上升的趋势较快,并在直流电源最大电压量程处保持恒定。从图2 (b)中也可以看出,整个料液体系的电导率随时间是逐步减少的,这也说明整个体系中的盐含量是逐步减少的,肌氨酸母液中的盐离子在电场的作用下,逐步迁移出整个体系。淡化室的电导率下降速率与施加的电流也直接相关,电流越大,电导率下降速率越快,这是由于电流越大,脱盐驱动力越大,这与图2 (a)中膜堆电压降变化趋势的原因是一致。
图3显示肌氨酸母液脱盐率和产品得率随不同操作电流的变化情况。从图中可以看出,肌氨酸母液的脱盐率在不同电流下均实现了99%以上的去除率,这也说明,通过电渗析过程可成功实现肌氨酸产品中氯化钠的高效去除。从产品的得率来看,在电渗析过程中,肌氨酸的得率在不同电流下基本上都维持在70%左右的水平,这个值高于传统的分步结晶法60%左右的得率。在电渗析过程中,肌氨酸产品有一定的损失,这主要是由两方面原因导致:其一,由于肌氨酸既带有碱性的氨基基团,又带有酸性的羧基基团,这种两性物质会发生部分解离,在电场的作用下,从淡化室迁移至浓缩室中,可称之为电渗漏[22-23]。其二,由于肌氨酸为弱酸,由于淡化室中其含量较高,而浓缩室中含量较低,在浓度差的作用下,肌氨酸分子也会从淡化室中扩散至浓缩室,可称之为分子扩散[24]。另外,从图中也可以看出,肌氨酸的得率随操作电流的增加有一个微幅下降的趋势,电流越大,其产品的得率越小,这是由于电流越大,其电渗漏效应越明显。从产品的得率考虑,整个电渗析过程在较低的电流下进行操作较为适宜。但是,电流越小,电渗析过程对肌氨酸母液的脱盐速率越小,处理同等质量的肌氨酸产品所需的膜面积也就越大,其设备投资成本也就越大。折中产品得率和处理速率,操作电流选择为2 A较为合适。

图2 不同电流下的膜堆电压降及溶液电导率变化
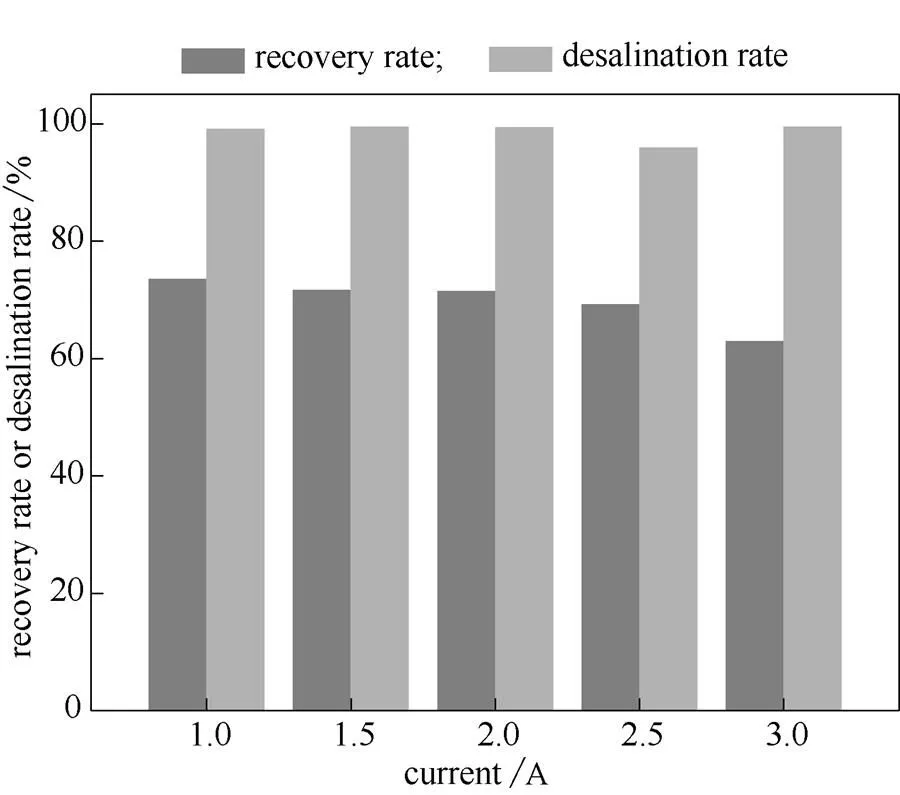
图3 不同电流下的肌氨酸母液脱盐率及产品得率
2.2 不同pH分离效果
图4所示为在电渗析操作电流为2 A时,不同pH的肌氨酸母液对膜堆电压降及溶液电导率的影响情况。从图4 (a)中可以看出,不同pH的肌氨酸母液对电压降的影响不是特别显著。处理同等体积的肌氨酸母液在pH为4和9时所需的时间比pH为6.5时略有增多,这主要是由肌氨酸这种两性物质的特性导致的。根据文献所示,肌氨酸的等电点为6.73[25];在pH为4和5时,肌氨酸分子失去质子,主要以带负电的羧酸根离子形式存在;在pH为8和9时,肌氨酸分子得到质子,主要以带正电的铵根离子形式存在(如图5所示)。因此,肌氨酸母液的起始pH在偏酸性和碱性时,其肌氨酸分子会发生部分解离,当肌氨酸母液中的无机离子迁移出淡化室时,这部分解离出弱电解离子可充当电解质,使得实验所需时间略有增加。从图4 (b)中可以看出,电渗析过程中淡化室的溶液电导率随时间逐步下降,不同pH之间的下降速率基本一致。

图4 溶液不同起始pH下的膜堆电压降及溶液电导率变化

图5 肌氨酸分子电荷变化图
图6显示肌氨酸母液脱盐率和产品得率随不同起始pH的变化情况。从图中可以看出,肌氨酸母液的脱盐率在不同起始pH下均实现了99%以上的去除率。同时,当pH为6.5时,肌氨酸产品的得率最高,达到了71.5%。而pH为酸性和碱性时,由于其离子解离比例比较大,在电渗析过程中随电场发生迁移的比例也会越大,导致最终产品的收率会略有下降。

图6 不同pH下的肌氨酸母液脱盐率及产品得率
2.3 过程能耗
通过对电渗析过程的能耗及成本进行评估[26-27],可为企业对项目立项的判断提供依据。根据电渗析成本评估公式,对电流为2 A,初始pH为6.5时,电渗析处理肌氨酸母液的成本和能耗进行了评价,结果见表2。整个电渗析过程的成本包括能耗成本和投资成本。固定投资成本包括设备投资、利息以及设备维护费用;设备投资主要包含膜堆成本以及外辅成本;膜堆成本一般为膜成本的1.5倍,而外辅成本为膜堆成本的1.5倍;利息和维修费用按总投资的8%和1%进行计算。从表中可以看出,利用电渗析处理肌氨酸料液的能耗仅为26.4 kW·h·t-1,远远低于传统的蒸发结晶过程,电渗析过程处理氨基丁酸料液的总成本仅为311元·t-1。

表2 电渗析处理肌氨酸料液能耗及成本分析
3 结 论
(1)电渗析过程实现了肌氨酸产品的清洁化生产,整个过程不添加额外化学试剂,过程优化,操作方便快捷。
(2)电渗析过程对肌氨酸母液中氯化钠的去除率大于99%,产品得率为71.5%,无论是去除率还是得率均高于传统的分步结晶过程。
(3)电渗析工艺生产肌氨酸的能耗为26.4 kW·h·t-1,电渗析技术生产肌氨酸的总成本为311元·(t母液)-1,通过规模化生产,其处理费用有望进一步降低。
[1] Wang Meng (王萌). The clinical use of sarcosine [D]. Beijing: Peking Union Medical College, 2012.
[2] Allen R H, Stabler S P, Lindenbaum J,. Serum betaine,,-dimethylglycine and-methylglycine levels in patients with cobalamin and folate deficiency and related inborn errors of metabolism [J].:, 1993, 42 (11): 1448-1460.
[3] Tsai G, Lane H, Yang P,. Glycine transporter Ⅰ inhibitor,-methylglycine (sarcosine), added to antipsychotics for the treatment of schizophrenia [J].., 2004, 55 (5): 452-456.
[4] Sreekumar A, Poisson L M, Rajeniran T M,. Metabolomic profile delineate potential role for sarcosine in prostate cancer progression [J]., 2009, 457 (7231): 910-914.
[5] Cernei N, Zitka O, Ryvolova M,. Spectrometric and electrochemical analysis of sarcosine as a potential prostate carcinoma marker [J]....., 2012, 7: 4286-4301.
[6] Schalken J A. Is urinary sarcosine useful to identify patients with significant prostate cancer? The trials and tribulations of biomarker development [J]..., 2010, 58 (1): 19-20.
[7] Botchorishvili G, Matikainen M P, Lilja H. Early prostate-specific antigen changes and the diagnosis and prognosis of prostate cancer [J]., 2009, 19 (3): 221-226.
[8] Caverly W R, Point C. Manufacturer of sarcosine [P]: US, 2720540. 1955-10-11.
[9] Leake P H, Breakbill E K, Va H,. Process for the production of sarcosine and related alkylamino-acetic acids [P]: US, 3009954. 1961-11-12.
[10] Yao Fang (姚方), Xu Tianyou (徐天有). Study on the synthesis of sodium-methylglycinate [J]., 2003, 17 (3): 34-36.
[11] Zhang Guoji (张国基). Preparation of sarcosine [P]: CN, 102584612. 2012-07-18.
[12] Xu T W, Huang C H. Electrodialysis-based separation technologies: a critical review [J].., 2008, 54: 3147-3159.
[13] Strathmann H, Grabowski A, Eigenberger G. Ion-exchange membranes in the chemical process industry [J].....,2013, 52:10364-10379.
[14] Zhang Y, Pinoy L, Meesschaert B,. Separation of small organic ions from salts by ion-exchange membrane in electrodialysis [J].., 2011, 57:2070-2078.
[15] Readi O M K, Rolevink E, Nijmeijer K. Mixed matrix membranes for process intensification in electrodialysis of amino acids [J].....,2014, 89: 425-430.
[16] Xu T W. Ion exchange membranes: state of their development and perspective [J]...., 2005, 263: 1-29.
[17] Strathmann H. Membrane separation process: current relevance and future opportunities [J].., 2001, 47: 1077-1087.
[18] Grib H, Belhocine D. Desalting of phenylalanine solutions by electrodialysis with ion-exchange membranes [J]...., 2000, 30: 259-262.
[19] Liu L F, Yang L L, Jin K Y,. Recovery of L-tryptophan from crystallization wastewater by combined membrane process [J]...., 2009, 66: 443-449.
[20] Kumar M, Tripathi B P, Shahi V K. Electro-membrane reactor for separation andsubstitution of glutamic acid from its sodium salt [J]., 2009, 54: 4880-4887.
[21] Chen Y, Zhang Y P, Yue M Z,. Production of L-lysine from L-lysine monohydrochloride by electrodialysis [J]., 2011, 25: 291-296.
[22] Gineste J L, Pourcelly G, Lorrain Y,. Analysis of factors limiting the use of bipolar membranes: a simplified model to determine trends [J]....,1996, 112: 199-208.
[23] Wilhelm F G, Punt I, van der Vegt N F A,. Optimisation strategies for the preparation of bipolar membranes with reduced salt ion leakage in acid-base electrodialysis [J]...., 2001, 182: 13-28
[24] Jaime-Ferrer J S, Couallier E, Viers P,. Three-compartment bipolar membrane electrodialysis for splitting of sodium formate into formic acid and sodium hydroxide: role of diffusion of molecular acid [J]...., 2008, 325: 528-536.
[25] ExPASy bioinformatics resource portal [EB/OL]. [2015-04-01]. http://web.expasy.org/cgi-bin/compute_pi/ pi_tool
[26] Wang Y, Wang A, Zhang X,. Simulation of electrodialysis with bipolar membranes: estimation of process performance and energy consumption [J]....., 2011, 50 (24): 13911-13921.
[27] Strathmann H, Koops G H. Process economics of electrodialytic water dissociation for the production of acid and base//Kemperman A J B. Handbook on Bipolar Membrane Technology [M]. Enschede: Twente University Press, 2000: 191-220.
Electrodialysis for cleaner separation and purification of sarcosine
WANG Yaoming1, LI Wei2, XU Tongwen1
School of Chemistry and Material ScienceUniversity of Science and Technology of ChinaHefeiAnhuiChinaHefei ChemJoy Polymer Materials CoLtdHefeiAnhuiChina
Sarcosine is a high-value fine chemical which has many significant applications. Now there is a separation process to remove the inorganic salts from the target product during the production of sarcosine. Multistage fractional crystallization is the conventional separation technology for sarcosine production which has many drawbacks such as high energy consumption, large consumption of chemicals and environmental pollution. To achieve cleaner production of sarcosine, a self-made electrodialysis stack was used in the separation and purification of the target product. The influences of current density and initial pH value in the feed solution on the production of sarcosine were investigated. Results indicated that salt removal rates higher than 99% and a product recovery ratio of 71.5% can be obtained at a current of 2 A and initial feed solution of pH 6.5. The total energy consumption for sarcosine production was 26.4 kW·h·t-1and the total process cost was estimated at 311 ¥·t-1, which is much less than the conventional separation technologies. It can be seen that electrodialysis is not only energy-saving but also environment- friendly for the industrial production of sarcosine.
ion exchange membrane; electrodialysis; sarcosine; cleaner production
2015-05-25.
Prof.XU Tongwen, twxu@ustc.edu.cn
10.11949/j.issn.0438-1157.20150701
TQ 028.8
A
0438—1157(2015)08—3137—07
徐铜文。
汪耀明(1984—),男,博士,副研究员。
国家自然科学基金项目(21276247,21476220)。
2015-05-25收到初稿,2015-06-08收到修改稿。
supported by the National Natural Science Foundation of China (21276247, 21476220).
