碳青霉烯酶耐药基因blaIMP-4的基因环境分析
2015-11-24袁敏李娟
袁敏,李娟
·调查与研究·
碳青霉烯酶耐药基因blaIMP-4的基因环境分析
袁敏,李娟
可转移金属酶即B组碳青霉烯酶已成为近年来耐药领域关注的热点[1]。中国学者有限的研究报道显示B组碳青霉烯酶中IMP家族如IMP-4、IMP-9亚型,VIM家族中VIM-2亚型在中国地区分离的金属酶阳性的菌株中占一定的比例,这些耐药基因在临床分离的菌株间传播甚至偶尔造成医院感染爆发的事实是确定的[2-4]。这些基因的传播机制是我们亟需解释的问题——是由携带耐药基因的广宿主质粒在菌与菌之间穿梭,还是由含有耐药基因的DNA片段通过转座、整合或同源重组的方式在不同菌属中播散。
这些耐药基因传播的确切机制尚未阐明,但我们所掌握的信息在不断增加。blaIMP-4基因首次检出于我国香港分离的一株不动菌属中[5],之后又在澳大利亚悉尼分离的肠杆菌中检出[6],几乎同年(2003年)又在澳大利亚墨尔本的肠杆菌中检出并引起了院内感染爆发[7]。这些菌中blaIMP-4基因都定位于含相同基因盒blaIMP-4-qacG2-aacA4-catB3的整合子上,并位于大小不同的质粒上,其中澳大利亚悉尼分离菌中携带的blaIMP-4质粒被证明是广宿主质粒。blaIMP-4基因环境的相似之处及定位于不同的质粒提示blaIMP-4基因及其侧翼序列能够移动。
越来越多的证据显示耐药基因的传播更大程度上取决于耐药基因的侧翼序列,而不是耐药基因本身[8],因此我们对目前NCBI(http://www.ncbi.nlm.nih.gov/)上提供的有关不同种属中blaIMP-4基因的基因环境做系统分析比对,以期能找到一些规律,为后续阐明blaIMP-4基因如何传播提供依据。
1 方法
登录β内酰胺酶分类网站(http://www.lahey.org/studies)检索blaIMP-4基因参考序列GenBank号AF244145,在NCBI网站Nucleotide入口检索AF244145,下载blaIMP-4基因全长741 bp的序列,在NCBI网站Blast入口提交检索与参考序列100%相同的序列。筛选含blaIMP-4基因及其侧翼环境的基因序列进行分析。下载描绘基因排列图,比较分析序列异同,检出的种属、国家等信息。
2 结果
2.1 GenBank中部分携带blaIMP-4基因菌株相关信息汇总
GenBank中已有的blaIMP-4基因及其侧翼环境的菌株及序列相关信息见表1。
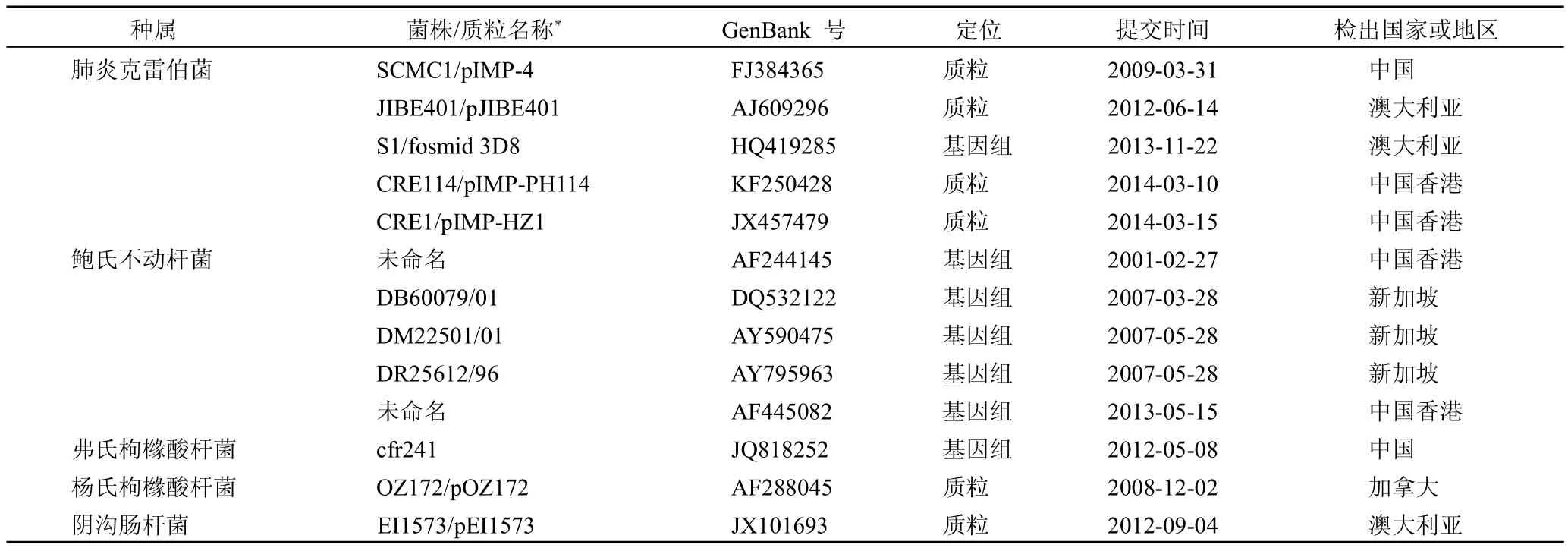
表1 不同国家和地区分离的携带blaIMP-4基因的菌株信息
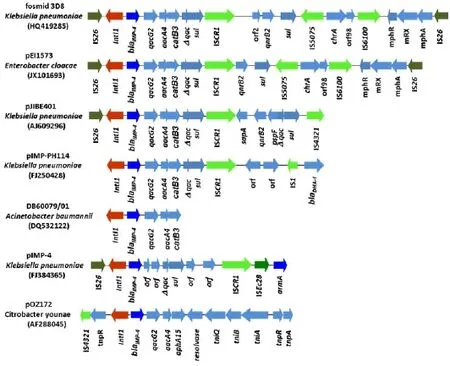
图1 NCBI GenBank中提交的部分有代表性的含blaIMP-4基因的质粒序列中blaIMP-4基因环境绘图分析
由表1中的信息我们可知,blaIMP-4基因的检出国家主要分布在中国(6/13),其次为新加坡(3/13)和澳大利亚(3/13)。序列提交时间分布在2001-2014年,检出种属主要分布在肠杆菌科的肺炎克雷伯菌(5/13)、枸橼酸杆菌(2/13)、阴沟肠杆菌(1/13)和非发酵的鲍氏不动杆菌(5/13)。虽然序列提交的多少不能确切地反映当地真实的耐药基因流行病学数据,但是在没有更多流调文献可参考的情况下,仍然可以一定程度上反映出不同地域检出的blaIMP-4基因的频率及种属分布差异。
2.2 典型blaIMP-4基因环境绘图及比对
blaIMP-4基因环境绘图,见图1。
3 讨论
如图1所示,blaIMP-4基因的基因环境在不同的种属中有很大的相似性,澳大利亚分离到的肺炎克雷伯菌S1的黏粒3D8和阴沟肠杆菌质粒pEI1573携带的blaIMP-4基因的基因环境仅有非常细微的差别,表现为后者在ISCR1下游有部分序列的缺失。澳大利亚分离的另一株肺炎克雷伯菌质粒pJIBE401携带的blaIMP-4基因与上述两株菌的区别主要在ISCR1下游序列不一致,但是介导喹诺酮类药物耐药基因qnrB2基因与介导碳青霉烯类药物耐药基因blaIMP-4共存于一个复合型I型整合子是这三株菌的共同特点。中国香港分离的肺炎克雷伯菌CRE114质粒pIMP-PH114和新加坡分离的鲍氏不动杆菌DB60079/01携带的blaIMP-4与上述菌株相比都有相同的blaIMP-4-qacG2-aacA4-catB3基因盒序列,提示基因的传播有共同的来源。中国分离肺炎克雷伯菌SCMC1质粒pIMP-4上有blaIMP-4基因,其位于I型整合酶的下游但其基因环境与之前提到的不同,提示blaIMP-4作为基因盒被新的I型整合子捕获。
从现有的信息仍不能得出确切的介导blaIMP-4移动的机制,基因盒可以以环状形式脱落,环状形式的基因盒也可以被新的I型整合子捕获[9],但我们观察到的是含有blaIMP-4-qacG2-aacA4-catB3基因盒序列以一个整体在转移,提示有其他的机制参与整合子的转移。从已知的结构分析有三种可能:①两个拷贝的IS26介导的包括blaIMP-4基因在内的长片段DNA的转座。②ISCR1介导的其上下游基因片段的转移。因7条已知序列中有5条在blaIMP-4下游出现了ISCR1。而ISCR1已被证明与很多耐药基因的转移相关[10]。③上述两种机制可能共同参与到blaIMP-4基因的转移中。
综上所述,blaIMP-4基因主要报道在肠杆菌科细菌和非发酵鲍氏不动杆菌中检出。世界各地报道的blaIMP-4基因的侧翼结构具有相似性,blaIMP-4基因以基因盒的形式存在于I型整合子中,两个拷贝的IS26形成的转座子的转座和(或)ISCR1介导的上下游序列的转移两种机制可能参与blaIMP-4基因的广泛转移。
[1]Nordmann P,Naas T,Poirel L.Global spread of carbapenemaseproducing Enterobacteriaceae.Emerg Infect Dis,2011,17(10):1791-1798.
[2]Lo WU,Cheung YY,Lai E,et al.Complete sequence of an IncN plasmid,pIMP-HZ1,carrying blaIMP-4 in a Klebsiella pneumoniaestrain associated with medical travel to China.Antimicrob Agents Chemother,2013,57(3):1561-1562.
[3]Xiong J,Hynes MF,Ye H,et al.Bla(IMP-9)and its association with large plasmids carried by Pseudomonas aeruginosa isolates from the People's Republic of China.Antimicrob Agents Chemother,2006,50(1):355-358.
[4]Yu YS,Qu TT,Zhou JY,et al.Integrons containing the VIM-2 metallo-beta-lactamase gene among imipenem-resistant Pseudomonas aeruginosa strains from different Chinese hospitals.J Clin Microbiol,2006,44(11):4242-4245.
[5]Chu YW,Afzal-Shah M,Houang ET,et al.IMP-4,a novel metallo-beta-lactamase from nosocomial Acinetobacter spp.collected in Hong Kong between 1994 and 1998.Antimicrob Agents Chemother,2001,45(3):710-714.
[6]Peleg AY,Franklin C,Bell JM,et al.Emergence of IMP-4 metallo-beta-lactamase in clinical isolate from Australia.J Antimicrob Chemother,2004,54(3):699-700.
[7]Peleg AY,Franklin C,Bell JM,et al.Dissemination of the metallo-beta-lactamasegeneblaIMP-4amonggram-negative pathogens in clinical setting in Australia.Clin Infect Dis,2005,41(11):1549-1556.
[8]Walsh TR.Combinatorial genetic evolution of multiresistance.Curr Opin Microbio,2006,9(5):476-482.
[9]Fluit AC,Schmitz FJ.Class 1 integrons,gene cassettes,mobility and epidemiology.Eur J Clin Microbiol Infect Dis,1999,18(11):761-770.
[10]TolemanMA,BennettPM,Walsh TR.ISCRelement:novel gene-capturing systems of the 21st century?Microbiol Mol Biol Rev,2006,70(2):296-316.
10.3969/cmba.j.issn.1673-713X.2015.01.017
传染病预防控制国家重点实验室面上项目(2012SKLID205);国家“十二五”艾滋病和病毒性肝炎等重大传染病防治专项(2013ZX 10004-217)
102206北京,中国疾病预防控制中心传染病预防控制所细菌耐药室传染病预防控制国家重点实验室
李娟,Email:lijuan@icdc.cn
2014-05-09
