疏水离子液体中生物不对称还原制备手性醇
2015-11-11穆晓清
宋 洁,穆晓清,王 栋,徐 岩
(江南大学 生物工程学院 教育部工业生物技术重点实验室,江苏 无锡 214122)
疏水离子液体中生物不对称还原制备手性醇
宋 洁,穆晓清,王 栋,徐 岩
(江南大学 生物工程学院 教育部工业生物技术重点实验室,江苏 无锡 214122)
针对近平滑假丝酵母全细胞不对称还原2-羟基苯乙酮制备光学纯(R)-苯基乙二醇反应中底物的质量浓度、产量及质量平衡低的问题,运用多相萃取生物转化的原理,比较不同非水介质对不对称还原反应效率的影响,构建具有良好生物相容性和高质量平衡的水/疏水离子液体1-丁基-3-乙基咪唑六氟磷酸盐([BEIM]PF6)双相反应体系。考察该体系下辅助底物种类、辅助底物用量、底物质量浓度、催化剂用量、离子液体比例、pH和反应温度对生物催化反应的影响,通过正交试验设计和响应面法优化不对称还原2-羟基苯乙酮的反应条件,在最优反应条件下,产物质量浓度、产率和质量平衡得率分别达到15.35g/L、76.8%和84.3%,产物的对映消旋值(e.e.值)大于99.9%。
不对称还原;全细胞;(R)-苯基乙二醇;离子液体;质量平衡
(R)-苯基乙二醇((R)-PED)作为一种重要的手性砌块,是制备多种生物活性化合物的重要中间体[1-2],同时也是液晶中不可缺少的手性添加剂。利用传统化学方法合成手性醇,存在合成步骤复杂、反应条件苛刻、反应选择性低、产物分离困难和环境污染等缺点[3-4]。而生物合成手性醇方法则有反应条件温和[5]、反应立体选择性高、区域选择性高和化学选择性高[6-7]、环境友好等优点,符合原子经济、绿色化学的发展方向。
手性生物合成法催化剂主要以游离酶或全细胞参与反应。全细胞催化剂具有使用便捷、易于回收、能够重复利用等优点,其作为氧化还原反应催化剂时,可以通过添加廉价的辅助底物,利用细胞内辅酶体系为还原反应提供还原型辅酶,同时酶存在于天然的细胞环境中不易失活、稳定性好。
但生物合成法存在底物难溶、产物浓度低等缺点,运用多相萃取技术向反应体系中加入非水介质,能够增加底物溶解度、降低底物对催化剂的毒害作用,实现产物浓度的提高。离子液体(ILs)作为一种环境友好型的绿色反应介质,对多数疏水性化合物溶解性良好[8],具有稳定性好、不易挥发、生物相容性好等优点[9-10],可以有效提高反应速率和产物的光学纯度[11-12]。
本研究中,笔者使用所在实验室保藏的1株近平滑假丝酵母Candida parapsilosis JNYX全细胞作为生物催化剂,以不对称还原2-羟基苯乙酮(2-HAP)制备(R)-PED为模式反应,经比较不对称还原反应在不同体系下的催化效果选择绿色溶剂离子液体(ILs)作为反应介质,并筛选到疏水性离子液体1-丁基-3-乙基咪唑六氟磷酸盐([BEIM]PF6)构建水/[BEIM]PF6双相反应体系,以考察该体系下反应条件并进行优化,以提高反应的底物浓度、产率和反应质量平衡以及催化剂在双相反应体系中的稳定性,为生物合成手性醇提供基础数据。
1 材料与方法
1.1 材料
1.1.1 菌种
近平滑假丝酵母Candida parapsilosis JNYX为笔者所在实验室保藏菌种。
1.1.2 培养基
酵母培养基:葡萄糖40g/L,酵母浸膏5g/L,无机盐溶液10%(体积分数)。pH 7.0。
无机盐溶液(g/L):(NH4)2HPO413,KH2PO47,MgSO4·H2O 0.8,NaCl 0.1。
1.1.3 主要试剂及仪器
2-羟基苯乙酮(2-HAP),日本TCI公司;离子液体[BEIM]PF6,中国科学院兰州物理化学研究所;其他离子液体由浙江大学吴起老师提供。
高效液相色谱P680(紫外检测器),美国Dionex公司;Chiralcel OB-H色谱柱(4.6mm×250mm),日本Daicel公司。
1.2 菌体培养
种子培养 从斜面接两环菌种,接种到装液量为20%(体积分数)的250mL三角瓶中,置于150r/min的摇床中30℃恒温振荡培养24 h。
菌种培养 以2%的接种量将种子液接种至装液量为 20%的 500mL三角瓶中,于 30℃、150r/min摇床上培养 48 h。发酵结束后,于 4℃、12 000r/min离心,并用生理盐水洗涤2次后收集细胞,4℃下保存待用。
1.3 不对称还原反应
2mL反应体系,加入0.5g湿菌体、20g/L 2-HAP、0.4g葡萄糖,30℃、200r/min反应24 h。反应结束后,反应液离心(12 000r/min),上清液用乙酸乙酯萃取,乙酸乙酯相用于HPLC检测。
1.4 水/[BEIM]PF6双相体系反应条件的优化
通过正交试验设计对辅助底物种类、辅助底物用量、底物质量浓度、催化剂用量、ILs比例、pH和反应温度7个因素进行优化,试验设计为L18(37),30℃、200r/min反应24 h,HPLC检测反应结果。
对正交试验设计中影响较为显著的因素使用响应面法进一步优化,使用响应面分析软件Design Expert设计实验方案,HPLC检测反应结果。
1.5 水/[BEIM]PF6双相体系中催化剂稳定性研究
在优化反应条件下进行重复批次实验,反应24 h离心收集菌体(4℃、12 000r/min,10min),用生理盐水洗涤2次,相同条件下进行下一批次反应。
1.6 分析方法
乙酸乙酯萃取样品,采用HPLC分析,色谱柱为Chiralcel OB-H柱(4.6mm×25mm;Daicel),流动相为正己烷/异丙醇(体积比 9∶1),流速 0.4mL/min,柱温38℃,紫外检测器,检测波长215 nm。(S)-PED和(R)-PED的出峰时间分别为19.5min和23.5min,2-HAP出峰时间为27.5min。
(R)-PED光学纯度计算见式(1)。

(R)-PED得率计算见式(2)。

反应质量平衡收率计算见式(3)。

式中:cS、cR分别为反应结束后(S)-PED和(R)-PED的浓度,c0为2-HAP的浓度,cH为反应结束后剩余2-HAP浓度。
2 结果与讨论
2.1 反应体系对不对称还原反应效率的影响
近平滑假丝酵母通常不对称还原2-HAP生成(S)-PED,本研究室从保藏的近平滑假丝酵母中筛选获得 1株具有高度立体选择性的 Candida parapsilosis JNYX,其不对称还原2-HAP能够制备(R)-PED,e.e.值大于99.9%。水相反应体系研究表明,该方法存在2个主要缺陷。首先,非天然底物2-HAP溶解度仅为11g/L,限制了反应底物浓度的提高;其次,在水相反应体系中,催化剂对底/产物存在代谢作用,导致反应质量平衡显著降低。非水多相萃取反应体系是解决上述问题的一种简单、有效的方法[13-14],本研究考察水/有机溶剂、水/助溶剂、水/树脂(NKA-Ⅱ)、水/离子液体反应体系对产物浓度和反应质量平衡的影响,结果见表1。
由表1可知:异丙醇助溶剂体系和水/树脂(NKA-Ⅱ)双相反应体系中反应产率和质量平衡收率没有明显变化;水/邻苯二甲酸二丁酯双相反应体系中,产物质量浓度下降0.97g/L,质量平衡收率提高29.1%;水/[BMIM]PF6双相反应体系产物质量浓度下降2.49g/L,质量平衡收率增加42.8%。由于有机溶剂具有对催化剂有毒、易燃、易挥发[15]等缺点,ILs作为一种绿色溶剂,比有机溶剂稳定并具有良好生物相容性[16-17],因此选择ILs([BMIM]PF6)作为反应介质进行下一步研究。

表1 反应体系对不对称还原2-HAP反应效率的影响Table 1 Effects of reaction systems on asymmetric reduction efficiency of 2-HAP
2.2 离子液体类型对不对称还原反应效率的影响
ILs对生物催化剂的催化特性具有重要影响[3,18],在水/离子液体双相反应体系中,ILs离解形成具有极性区域和非极性区域的微小结构,可以通过改变酶分子电荷分布、影响底物和产物的溶剂化状态、改变反应介质的特性而影响酶促反应催化效率。
考察不同ILs对细胞不对称还原2-HAP反应效率的影响,结果见表2。由表2可知,ILs的水溶性对催化反应具有明显影响。亲水性离子液体介质中均没有检测到产物;疏水性离子液体反应体系中检测到产物,且反应质量平衡收率大于85%。这可能是因为疏水性离子液体作为反应介质的催化效果与离子液体黏度有关,黏度随阳离子组分咪唑基碳链长度增加而增大[15,19-20]。高黏度反应体系降低酶和底物之间的传质速率,是导致转化效率下降的主要原因。传质速率的降低同样降低了细胞对底/产物的代谢速率,而反应质量平衡收率随离子液体黏度增加而增加。综合考虑反应产率和质量平衡收率,选择离子液体[BEIM]PF6作为2-HAP不对称还原制备(R)-PED的反应介质。
2.3 反应条件对水/[BEIM]PF6双相体系中催化效率的影响
2.3.1 辅助底物对不对称还原反应效率的影响
不对称还原反应需要等量辅酶(NADH或NADPH)作为氢供体,酵母细胞内辅酶量较少,需要向体系内添加辅助底物以维持反应正常进行。考察不同辅助底物对细胞不对称还原2-HAP反应效率的影响,结果见图1。

表2 不同ILs对不对称还原2-HAP反应效率的影响Table 2 Effects of various ILs on asymmetric reduction efficiency of 2-HAP
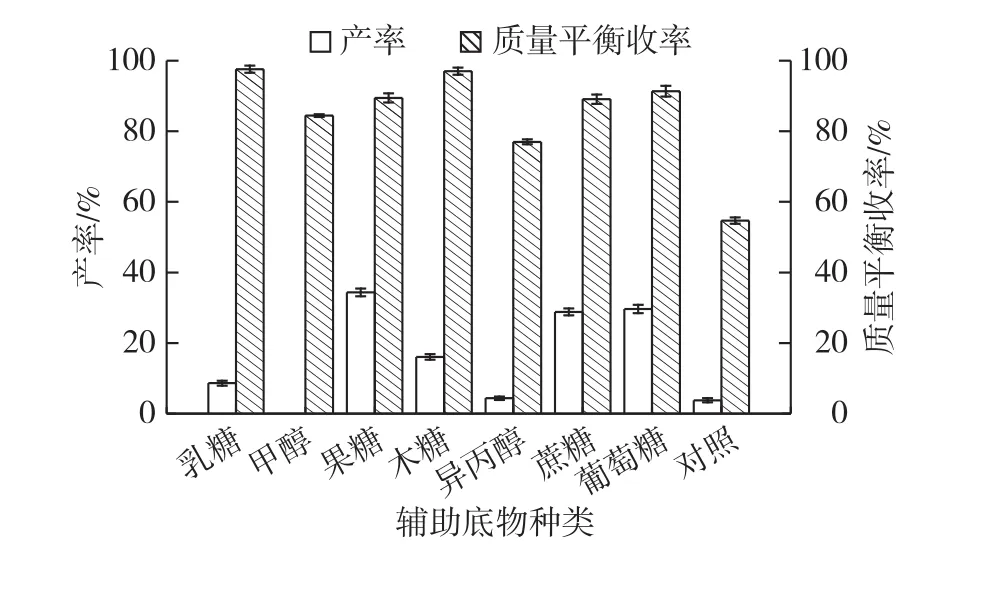
图1 辅助底物对不对称还原2-HAP反应效率的影响Fig.1 Effects of co-substrates on asymmetric reduction efficiency of 2-HAP
由图1可知:醇类辅底物不能提高反应产率,糖类辅底物则可以有效提高产率,当果糖、蔗糖和葡萄糖作为辅助底物时,反应产率较高。实际生产应用中,果糖成本过高,与果糖相比,蔗糖和葡萄糖作为辅助底物时的产率仅分别降低了3.5%和5.9%。因此,选择相对廉价的葡萄糖作为不对称还原制备(R)-PED的辅助底物。
2.3.2 葡萄糖用量对不对称还原反应效率的影响
葡萄糖作为辅助底物时,其用量对催化反应的影响结果见图2。由图2可知:葡萄糖用量对反应产率具有显著影响,用量小于0.08g时,产率随葡萄糖用量增加而增加;葡萄糖用量大于0.08g时,产率随葡萄糖用量增加大幅度下降,说明过多的葡萄糖不仅不能提高产率,反而会对细胞代谢活性产生抑制作用,因此葡萄糖用量应选择在0.08~0.12g。由此可见,合理控制辅底物用量,对于提高反应产率具有重要影响,同时辅底物用量与催化剂用量、底物浓度密切相关,是反应条件中影响反应效率的关键因素。
2.3.3 底物质量浓度对不对称还原反应效率的影响
考察水/[BEIM]PF6双相体系中底物质量浓度对不对称还原反应效率的影响,结果见图3。由图3可知:底物质量浓度变化对质量平衡收率无明显影响,但随着底物质量浓度增加,产物质量浓度不断增加,而产率持续下降。因此,在高底物浓度条件下,要将底物完全转化需要大幅度延长反应时间,然而反应时间的延长和产物的不断积累使催化剂受到的产物毒害及抑制作用增强,严重降低整个批次反应的时空转化率。因此,底物质量浓度应选在20g/L左右。

图2 葡萄糖用量对不对称还原2-HAP反应效率的影响Fig.2 Effects of glucose concentration on asymmetric reduction efficiency of 2-HAP

图3 底物质量浓度对不对称还原2-HAP反应效率的影响Fig.3 Effects of substrate concentration on asymmetric reduction efficiency of 2-HAP
2.3.4 催化剂用量对不对称还原反应效率的影响
考察催化剂(细胞)用量对不对称还原反应效率的影响,结果见图4。由图4可知:不对称还原反应产率随催化剂用量增加而增加,由于催化剂对底/产物具有代谢作用,反应质量平衡收率随催化剂用量增加而下降。同时,催化剂用量过多也会增加反应体系黏度,影响反应的传质。综合考虑产率和反应质量平衡收率,催化剂用量应控制在0.8g以内。
2.3.5 离子液体对不对称还原反应效率的影响
两相反应体系中,细胞只有在水相中可催化不对称还原反应,两相体积比不仅决定了底/产物在两相中的分配比,同时两相体积比会影响相界面面积大小,从而影响生物转化的效率[13]。因此,考察离子液体比例对反应产率和质量平衡收率的影响,结果见图5。由图5可知:离子液体的比例对反应产率和质量平衡收率都具有显著影响。产率在离子液体比例为20%(体积比)时达到最大,而质量平衡收率随离子液体比例的增大持续增加,这是由于随着离子液体比例增大,整个反应体系黏度增加,高黏度反应体系阻碍酶和底物之间的传质[21],降低了细胞对底/产物的代谢速率。综合考虑反应产率和质量平衡收率,离子液体比例选择为20%。
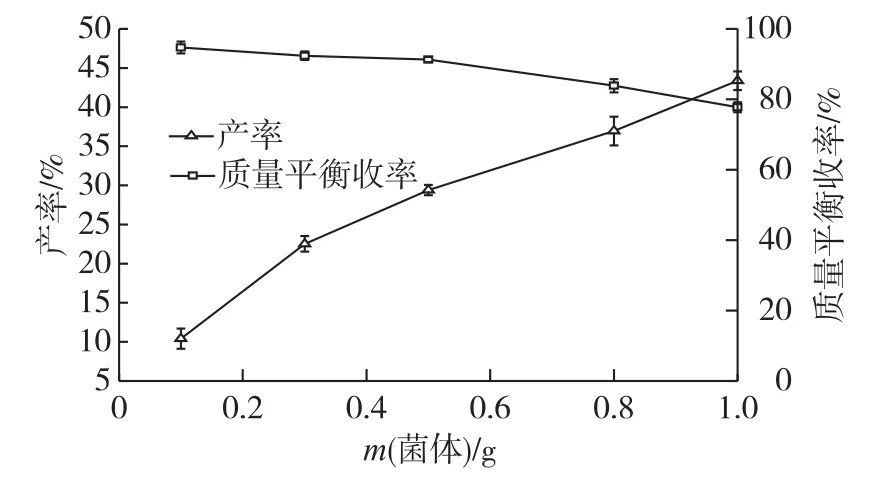
图4 细胞量对不对称还原2-HAP反应效率的影响Fig.4 Effects of cell mass on asymmetric reduction efficiency of 2-HAP

图5 离子液体用量对不对称还原2-HAP反应效率的影响Fig.5 Effects of ILs volume ratio on asymmetric reduction efficiency of 2-HAP
2.3.6 缓冲液pH对不对称还原反应效率的影响
反应体系的pH不仅会影响羰基还原酶的活性,还会影响到细胞内辅酶再生。考察反应体系pH对不对称还原2-HAP反应效率的影响,结果见图6。由图6可知:pH变化对反应质量平衡收率无明显影响,对产率则存在影响,当pH为2.0~4.0时,反应产率维持在较高水平,随着pH的进一步升高,产率明显下降,当pH范围在6.0~9.0时,产率保持在较低水平无明显变化。因此,该反应适宜控制在酸性环境下进行,pH选择在4.0。

图6 pH对不对称还原2-HAP反应效率的影响Fig.6 Effects of pH value on asymmetric reduction efficiency of 2-HAP
2.3.7 反应温度对不对称还原反应效率的影响
对于水/[BEIM]PF6双相反应体系,反应温度不仅影响细胞和羰基还原酶的活性,同时通过影响ILs黏度改变整个反应的传质速率。图7所示为反应温度(20~40℃)对反应效率的影响。由图7可知:产率在反应温度为25℃时达到最大。反应质量平衡收率在反应温度为40℃明显降低,这是由于较高温度下离子液体黏度降低有利于体系内传质,增大了细胞对底/产物的代谢速率。因此,反应温度在25℃时有利于反应效率的提高。

图7 反应温度对不对称还原2-HAP反应效率的影响Fig.7 Effects of temperature on asymmetric reduction efficiency of 2-HAP
2.4 水/[BEIM]PF6双相体系中不对称还原反应条件的优化
在单因素实验基础上,设计L18(37)正交试验优化不对称还原反应的反应条件。单因素实验结果表明,辅助底物用量对不对称还原反应效率具有较大影响,同时辅底物用量与催化剂用量、底物浓度存在直接关系。因此在正交试验设计中,催化剂用量采用m(催化剂)/m(辅底物)的方式表示,即以参与单位辅底物代谢所需细胞量表征催化剂用量;同样,因辅底物用量直接决定整个辅酶循环过程中还原型辅酶的总量,还原型辅酶和底物转化存在等摩尔量关系,因此底物质量浓度以ρ(底物)/m(辅底物)表示。正交试验设计各因素水平取值及结果见表3。
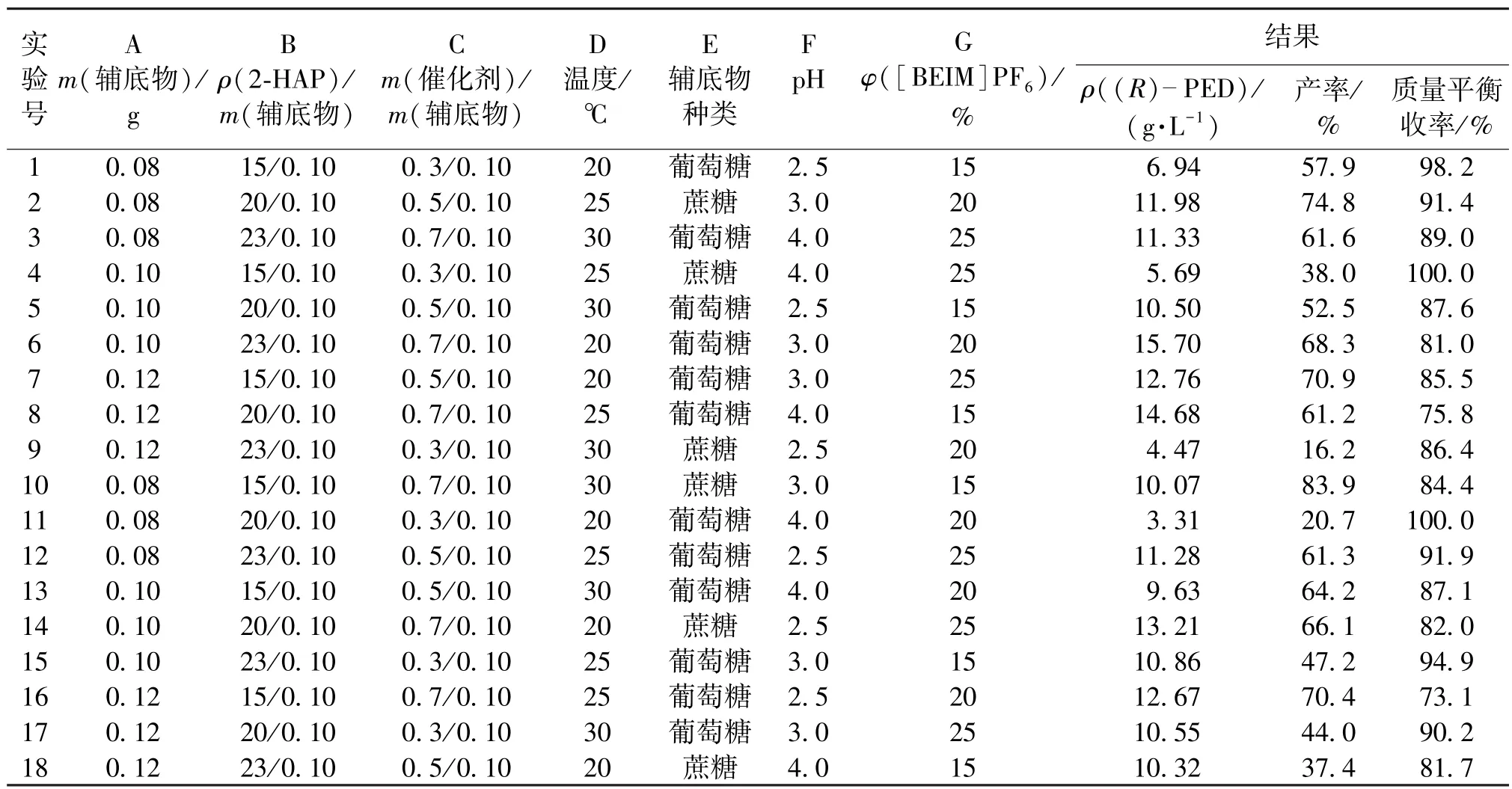
表3 正交试验设计及结果Table 3 Orthogonal experimental design and results
对表3实验结果进行均值计算,分别得到当产量、产率、质量平衡收率最大时的反应优化条件,对三组优化条件进行验证实验(数据未列出)发现,以产量为参考值时得到的优化条件(0.1g葡萄糖,20g/L 2-HAP,0.7g菌体,[BEIM]PF625%,pH 3.0,反应温度25℃)下反应效率最好,产物质量浓度15.22g/L,产率76.1%,质量平衡收率81.9%。
进一步对正交试验结果进行极差分析和方差分析,结果见表4。由表4可知:因素A、C、F的水平变化对于产量、产率和质量平衡收率都具有较大影响。同时,为了将因素水平变化引起的实验结果间的差异与误差波动引起的差异区分开来,对表3数据进行了方差分析,结果表明因素C对产量、产率和质量平衡收率的影响具有显著性,因素A、G对质量平衡收率的影响具有显著性。

表4 正交试验设计极差分析和方差分析Table 4 Range analysis and variance analysis of orthogonal experimental design
由表4还可知:对3个主要影响因素A、C、F使用响应面法进一步优化(数据未列出),最终确定不对称还原2-HAP制备(R)-PED的反应条件为0.08g葡萄糖,20g/L 2-HAP,0.55g菌体,反应温度25℃,pH 3.5,离子液体比例25%。该优化条件下底物质量浓度20g/L,反应24 h后产物质量浓度15.35g/L,产率76.8%,质量平衡收率84.3%。本研究结果的底物浓度比已有文献报道的最大底物质量浓度12.5g/L[22]提高60%,产物浓度比已报道的最大产物质量浓度7.39g/L[23]高107.8%。
2.5 不对称还原2-HAP反应过程曲线
在优化反应条件下跟踪不对称还原反应转化过程,结果见图8。由图8可知:反应过程中(R)-PED的光学纯度始终大于99.9%。反应前6 h,产物合成呈线性增加;反应6 h后,由于底物浓度的降低和产物积累,反应速度逐渐减慢;反应至30 h时,水相底物浓度过低、产物进一步积累导致产物合成速率十分缓慢,底物仍有1.86g/L剩余。此时,如果继续延长反应时间,产物合成量极小(数据未列出),同时质量平衡收率随反应时间延长而下降,大大降低了反应的时空转化率,因此选择在30 h终止反应。反应过程中催化剂对葡萄糖具有较高的代谢速率,反应开始1 h葡萄糖即完全消耗。因此在反应1 h后向反应体系补加0.08g葡萄糖继续反应至24 h,催化反应产率和质量平衡收率分别为74.2%和80.4%,说明葡萄糖消耗殆尽并不是反应后期反应速率大幅下降的原因,维持补加葡萄糖反而会降低催化反应效率。另外,整个反应过程中,质量平衡收率则一直保持缓慢下降,前6 h下降速度较快,这与细胞糖耗及不对称还原反应速率有关。

图8 不对称还原2-HAP反应过程曲线Fig.8 The time course of asymmetric reduction of 2-HAP
2.6 水/[BEIM]PF6双相体系中催化剂稳定性的研究
在生物催化剂的实际应用中,催化剂稳定性对催化剂的更换频率、反应时间和产率具有重要影响[24],因此考察近平滑假丝酵母在水/[BEIM]PF6双相反应体系中循环使用的稳定性,结果见图9。由图9可知,与单水相体系相比,水/[BEIM]PF6双相反应体系中产物质量浓度提高了84%,质量平衡收率提高了96%。与单水相体系中细胞稳定性比较,水/[BEIM]PF6双相体系中近平滑假丝酵母保持了良好的稳定性,说明离子液体对细胞具有很好的生物相容性。
3 结论
使用近平滑假丝酵母全细胞作为手性催化剂合成光学纯(R)-PED,(R)-PED光学纯度大于99.9%,简化了后期分离提纯步骤,提高了产品品质。通过对离子液体进行筛选,筛选到疏水性离子液体[BEIM]PF6构建水/[BEIM]PF6双相反应体系。对该体系下各单因素对反应的影响进行研究,通过正交试验设计和响应面设计优化水/[BEIM]PF6双相体系的反应条件。单纯通过条件控制和反应体系的改变,使反应的产物浓度和质量平衡收率比水相体系中分别提高了84%和96%,成功实现批次反应产物浓度的大幅提高,同时催化剂在水/[BEIM]PF6双相反应体系中具有良好的操作稳定性。

图9 水/[BEIM]PF6双相体系和单一水相中催化剂的操作稳定性Fig.9 Operational stability of catalyst in aqueous/[BEIM]PF6two-phase system and aqueous
[1]Wang S S,Xu Y,Zhang R Z,et al.Improvement of(R)-carbonyl reductase-mediated biosynthesis of(R)-1-phenyl-1,2-ethanediol by a novel dual-cosubstrate-coupled system for NADH recycling[J].Process Biochem,2012,47(7):1060-1065.
[2]Li Z,Liu W D,Chen X,et al.Highly enantioselective double reduction of phenylglyoxal to(R)-1-phenyl-1,2-ethanediol by one NADPH-dependent yeast carbonyl reductase with a broad substrate profile[J].Tetrahedron,2013,69(17):3561-3564.
[3]肖仔君.Acetobacter sp.CCTCC M209061细胞催化潜手性酮不对称还原反应的研究[D].广州:华南理工大学,2010.
[4]沈梦秋,纪晓俊,聂志奎,等.生物制造不同立体构型2,3-丁二醇:合成机理与实现方法[J].催化学报,2013,34(2):351-360.
[5]Benaissi K,Poliakoff M,Thomas N R.Dynamic kinetic resolution of rac-1-phenylethanol in supercritical carbon dioxide[J].Green Chem,2009,11(5):617-621.
[6]Götz K,Liese A,Ansorge-Schumacher M,et al.A chemoenzymatic route to synthesize(S)-γ-valerolactone from levulinic acid[J].Appl Microbiol Biotechnol,2013,97(9):3865-3873.
[7]Zou S P,Yan H W,Hu Z C,et al.Enzymatic resolution of epichlorohydrin catalyzed by whole cells in an organic solvent/ buffer biphasic system[J].Chin J Catal,2013,34(7):1339-1347.
[8]Leuchs S,Na′amnieh S,Greiner L.Enantioselective reduction of sparingly water-soluble ketones:continuous process and recycle of the aqueous buffer system[J].Green Chem,2013,15(1):167-176.
[9]Tavares A P M,Pereira J A N,Xavier A M R B.Effect of ionic liquids activation on laccase from Trametes versicolor:enzymatic stability and activity[J].Eng Life Sci,2012,12(6):648-655.
[10]Antonia P,van Rantwijk F,Sheldon R A.Effective resolution of 1-phenyl ethanol by Candida antarctica lipase B catalysed acylation with vinyl acetate in protic ionic liquids(PILs)[J].Green Chem,2012,14(6):1584-1588.
[11]Xu J M,Wu Q,Zhang Q Y,et al.A basic ionic liquid as catalyst and reaction medium:a rapid and simple procedure for aza-Michael addition reactions[J].Eur J Org Chem,2007(11):1798-1802.
[12]Li N,Du W Y,Huang Z N,et al.Effect of imidazolium ionic liquids on the hydrolytic activity of lipase[J].Chin J Catal,2013,34(4):769-780.
[13]Kim P Y,Pollard D J,Woodley J M.Substrate supply for effective biocatalysis[J].Biotechnol Prog,2007,23(1):74-82.
[14]Schrewe M,Julsing M K,Bühler B,et al.Whole-cell biocatalysis for selective and productive C-O functional group introduction and modification[J].Chem Soc Rev,2013,42(15):6346-6377.
[15]Kim H S,Koo Y M,Effects of physicochemical properties of ionic liquids on butyl acetate synthesis using Candida antarctica lipase B[J].Kor J Chem Eng,2012,29(11):1610-1614.
[16]Chen W J,Lou W Y,Yu C Y,et al.Use of hydrophilic ionic liquids in a two-phase system to improve mung bean epoxide hydrolases-mediated asymmetric hydrolysis of styrene oxide[J].J Biotechnol,2012,162(2/3):183-190.
[17]张磊,何玉财,仝新利,等.离子液体的性能及应用[J].生物加工过程,2009,7(2):8-12.
[18]Gangu S A,Weatherley L R,Scurto A M.Whole-cell biocatalysis with ionic liquids[J].Curr Org Chem,2009,13(13):1242-1258.
[19]Bonhôte P,Dias A P,Papageorgiou N,et al.Hydrophobic,highly conductive ambient-temperature molten salts[J].Inorg Chem,1996,35(5):1168-1178.
[20]Chen W J,Lou W Y,Zong M H.Efficient asymmetric hydrolysis of styrene oxide catalyzed by mung bean epoxide hydrolases in ionic liquid-based biphasic systems[J].Bioresour Technol,2012,115:58-62.
[21]陈金燕,刘桂艳,黄申,等.含离子液体体系中固定化细胞转化甘草酸生成单葡萄糖醛酸基甘草次酸[J].生物加工过程,2011,9(5):17-21.
[22]Ridley D D,Stralow M.The stereospecific asymmetric reduction of functionalised ketones[J].J Chem Soc:Chem Commun,1975,10:400-400.
[23]Hu Q S,Xu Y,Nie Y.Highly enantioselective reduction of 2-hydroxy-1-phenylethanone to enantiopure (R)-phenyl-1,2-ethanediol using Saccharomyces cerevisiae of remarkable reaction stability[J].Bioresour Technol,2010,101(22):8502-8508.
[24]Burton S G,Cowan D A,Woodley J M.The search for theideal biocatalyst[J].Nat Biotechnol,2002,20(1):37-45.
(责任编辑 荀志金)
Biological asymmetric reduction for preparation of chiral alcohols inhydrophobicity ionic liquids
SONG Jie,MU Xiaoqing,WANG Dong,XU Yan
(Key Laboratory Industrial Biotechnology of the Ministry of Education,School of Biotechnology,Jiangnan University,Wuxi 214122,China)
Whole cells of Candida parapsilosis catalyze asymmetric reduction of 2-hydroxyacetophenone for preparation of optically pure(R)-1-phenyl-1,2-ethanediol.The multiphase extraction of bioconversion was applied to improve substrate concentration,yield and the mass balance of the asymmetric reduction reaction.Different non-aqueous reaction systems were compared and aqueous/hydrophobicity ionic liquids(ILs)1-butyl-3-ethylimidazolium hexafluorophosphate([BEIM]PF6)biphasic system shown better biocompatibility and high mass balance.The effects of the different co-substrates,co-substrate mass,substrate concentration,catalyst mass,ILs ratio,pH value and reaction temperature on the biological catalysis reaction were studied.Reaction conditions of asymmetric reduction of 2-hydroxyacetophenone was optimized by orthogonal experimental design and response surface experimental design.Under the optimized reaction conditions,product concentration,yield and mass balance reached 15.35g/L,76.8%,84.3%,respectively.The enantiomeric excess(e.e.)value of product was above 99.9%.
asymmetric reduction;whole cells;(R)-1-phenyl-1,2-ethanediol;ionic liquids;mass balance
O643.3;TQ244.2
A
1672-3678(2015)02-0001-08
10.3969/j.issn.1672-3678.2015.02.001
2014-03-13
国家高技术研究发展计划(863计划)(2011AA02A209);国家重点基础研究发展计划(973计划)(2011CB710802);国家自然科学基金(21176103);江苏省高校优势学科建设工程
宋 洁(1988—),女,河北邯郸人,硕士研究生,研究方向:手性生物催化;王 栋(联系人),副教授,E-mail:dwang@jiangnan.edu.cn
