ELISA质控血清配制方法的研究
2015-10-31刘建礼王飞徐惠芳魏海燕张伟刘来福
刘建礼 王飞 徐惠芳 魏海燕 张伟 刘来福
(北京出入境检验检疫局 北京 100026)
ELISA质控血清配制方法的研究
刘建礼 王飞 徐惠芳 魏海燕 张伟 刘来福*
(北京出入境检验检疫局 北京 100026)
[目的]探讨HIV ELISA检测质控血清配制的关键影响因素及方法。[方法]选择HIV阳性血清以阴性血清进行系列稀释,直至获得S/CO=2-3之间的质控血清,以PBS、牛血清白蛋白、二甲基亚砜(DMSO)、甘油等组成不同稀释液,探讨各种稀释液与阴性血清稀释效果的不同。[结果]HIV强阳性血清在稀释初期,S/CO值下降缓慢,在S/CO值下降至15以下时,可以用倍比稀释的方法获得相应靶值的质控血清;PBS、PBS+10%BSA、阴性血清、阴性血清+10%DMSO、阴性血清+10%甘油作为稀释液,获得的质控血清S/CO值差别不明显。[结论]强阳性血清须先采用高倍数稀释,然后再进行倍比稀释寻找S/CO在2-3的最终稀释度;PBS加BSA可以替代阴性血清作为稀释液。
质控血清;配制方法;稀释液
1 前言
质控血清一般采用阳性血清稀释的方法进行配置,但配置过程涉及到阳性样本和稀释液的选择、保护剂和防腐剂的添加与否、靶值和稀释终点的确定等系列环节。本研究对内部血清配置的过程和这些关键影响因素进行探讨,以期获得稳定可靠的质控血清。
2 材料与方法
2.1材料
2.1.1主要试剂
(1)HIV初筛试剂
ELISA双抗原夹心法HIV(1+2)试剂盒:上海科华生物工程股份有限公司,批号20091014;北京万泰生物药业有限公司,批号20090708;厦门英科新创科技有限公司,批号20081226;珠海丽珠试剂有限公司,批号20080806;生物梅里埃公司Vironostika,批号A57BA。
(2)HIV抗体确认试剂
WB确认试剂:新加坡Genelabs公司,批号AE6013。
(3)甘油:分析纯,北京五洲世纪化工;二甲基亚砜(DMSO):德国SIGMA公司产品;牛血清白蛋白:批号2013262,赛宝生物。
2.1.2仪器设备
Alisei全自动酶联免疫检测系统:意大利SEAC公司。
2.2方法
2.2.1阳性血清的选择
本研究所用HIV阳性样本为出入境人群中检出的HIV阳性血清。所有阳性样本均经以上5种HIV ELISA检测试剂盒检测为阳性,并经WB确证为阳性。
2.2.2阴性血清的选择
本研究所用阴性血清为从日常检测样品中收集到的正常人血清,它们要求必须为HIV抗体阴性、HBsAg阴性、HCV抗体阴性,同时要求无肉眼可见的溶血、黄疸、乳糜颗粒、絮状沉淀物。这些血清经56℃30 min灭活补体,并经0.45 μm微孔滤膜过滤除菌备用。
2.2.3质控血清的配制
对选择的强阳性HIV血清首先进行10倍系列稀释并进行ELISA检测,至S/CO值开始出现明显下降,并且OD值出现在3.5以下时作为获得的稀释血清作为母液,再进行1∶2、1∶4、1∶8、1∶16、1∶32、1∶64、1∶128、1∶256、1∶512、1∶1024系列2倍稀释,以HIV ELISA试剂检测其S/CO值,选择S/CO值在2-3之间的稀释度作为最终稀释度。以阴性血清或各种待选样品稀释液以上述选定的稀释度进行稀释分装,获得质控血清。
2.2.4不同稀释液的影响
对不同稀释液稀释获得的质控血清进行ELISA测试,比较其S/CO差异,以确定基质效应。
3 结果
3.1阳性血清的选择
本研究所选择的阳性血清经5种试剂检测,其S/CO值均在20以上,样本OD值均接近于4.00;WB确证结果为全条带。具体结果见表1。
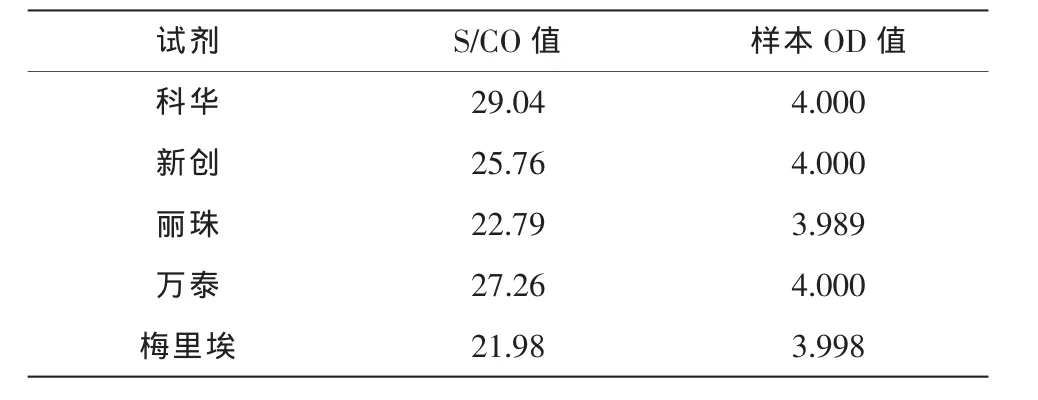
表1 强阳性血清不同试剂的ELISA检测结果
3.2稀释度的确定
对上述选定的HIV阳性血清先进行10倍系列稀释,以生物梅里埃试剂检测其S/CO值,结果发现,在1000倍稀释下其S/CO值出现下降至15.48,OD值下降至3.5以下。因此1000倍稀释液作为母液,进行下面的倍比稀释,分别以5种试剂进行检测,结果见表2。

表2 不同试剂倍比稀释检测结果
结果显示,在同一稀释倍数下,不同试剂测得的S/CO值差距很大;而同一试剂结果中,稀释倍数与S/CO值无明显的直线关系或对比关系。万泰试剂在阳性样本64倍稀释获得的S/CO值为2.34;科华试剂在64和128倍稀释度范围内获得的S/CO分别为3.15和1.98;英科试剂在样本32倍和64倍稀释分别得到了3.32和1.77的S/CO值;丽珠试剂在64倍稀释处测得S/CO值为2.75;生物梅里埃试剂在32和64倍稀释处分别测得S/CO值为3.33和1.89。
3.3稀释液对质控血清测定值的影响
分别以PBS、PBS+10%牛血清白蛋白、阴性血清、阴性血清+10%DMSO、阴性血清+10%甘油做为稀释液,对HIV阳性血清进行稀释,以生物梅里埃试剂测定其比色值并比较各组之间的差异。结果显示,各组检测所得S/CO值差别不明显,单用PBS组比阴性血清稀释组总体偏低,但统计学处理差异并不显著(T检验,P>0.05),PBS+BSA组的均值则与阴性血清组非常接近;阴性血清中添加DMSO和甘油对样本的ELISA检测结果也没有明显影响。
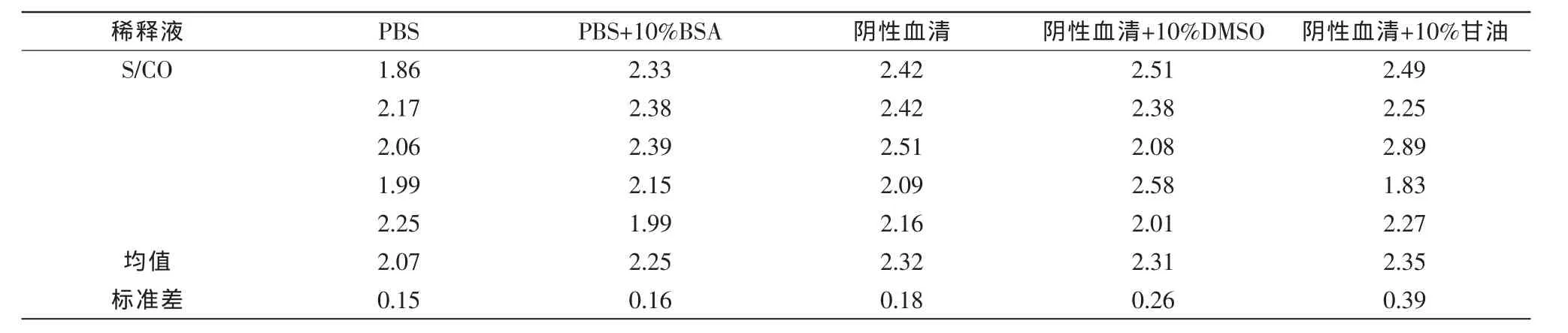
表3 不同稀释液对质控血清检测值的影响
4 讨论
ELISA检测S/CO值在2-3的阳性血清被称为临界值血清,临界值血清是HIV检测实验室对日常检测工作质量进行监控的最常用质控血清。临界值血清敏感性好,检测过程中微小的变化都可引起临界值的偏移[1,2]。理想的临界值血清应该是天然的HIV抗体弱阳性血清,也就是急性感染后HIV抗体阳转期的血清,但是这种血清一般很难得到,获得的量也很难满足长期质控需要,因此,临界值质控血清通常采用HIV强阳性血清稀释的方法获得[3,4]。
HIV强阳性血清稀释获得临界值质控血清的过程中,首先要选择高质量的阳性血清,阳性血清须经几种HIV检测试剂初筛和WB确证,以确保阳性可靠性。同时,为了增加质控血清的覆盖范围,最好将几份不同的强阳性血清混合,在WB检测中呈现全条带,这样的阳性血清能够确保其中含有种类足够多的抗体类型,以保证灵敏度和对各种不同试剂的敏感性。
需要注意的是,强阳性血清ELISA检测获得的S/CO值仅仅代表一种定性的判断,并不具有实际的定量意义,不同试剂获得的S/CO值也不具有可比性。这是因为①各试剂给出的S/CO只是为了判定阴阳性的作为临界值的一种参照,并不是真正的意义上的定量值;②由于各试剂厂家使用的单抗活性不同,检测最后获得的OD值只针对这种特定的试剂有一定的定量参考意义;③强阳性血清测定获得的OD值一般都在3.5以上,甚至基本都达到4.0左右,这些值已经处在了酶标仪比色检测的上限,反应变色与酶标仪读数值已经不在线性范围之内[5,6]。
选定阳性血清后,接下来要确定合适的稀释倍数,以便稀释获得S/CO在2-3范围内的质控血清。如上所述,强阳性血清检测产生的OD值往往已经远远超过了酶标仪的检测上限,因此,第一步一般采用大比例(如10倍系列)稀释的办法找到OD值落在酶标仪线性区间(一般在3.5以下)的稀释度。本研究中,HIV强阳性血清经10倍、100倍稀释,检测的S/CO值基本无变化,OD值4.0左右,直到1000倍稀释,才出现S/CO值的明显变化,OD值下降到了3.3(生物梅里埃试剂)左右。这进一步说明了选取的HIV强阳性血清ELISA检测信号开始是远远超出了酶标仪的检测上限。进入酶标仪检测限之后,就可以采用倍比稀释的方法进一步寻找获得S/CO为2-3的稀释度了。
阳性样本稀释时,稀释液的选择也是一个需要关注的问题。一方面,所用稀释液需要尽量考虑保持样本中抗体的天然状态,维持一个适用于抗原抗体反应的环境,在pH值、离子强度、离子渗透压、胶体渗透压、溶解极性等条件应尽量保持与生理状态下一致;另一方面,还要注意所用稀释液不能存在干扰抗原抗体反应的成分。理想的稀释液必须尽量满足上述两方面的要求。另外,为了后期保存的稳定性,稀释液中可能需要添加一些防腐和保护成分,这些成分也必须不能对样本的检测值发生影响[7]。
一般认为,正常人血清是最理想的稀释液[5],因为这样最大程度地保持了抗体的原始生理状态,同时也保证了质控样本与检测样本的反应环境的一致性。但是,由于血清成分复杂,尤其是蛋白种类非常复杂,不同批次血清中的质量有很大差别,其中的很多未知蛋白,包括不同供血者体内的某些特异性蛋白,都可能对抗原抗体的反应造成干扰,人血清中大量存在的免疫球蛋白也可能与ELSIA检测试剂中的的特异抗体发生反应。例如自身免疫病患者常有可与抗体反应的类风湿因子(RF),人体针对动物免疫球蛋白的嗜异性天然抗体相当普遍,自身抗体和嗜异性天然抗体的存在通常会引起假阳性反应[6]。另外,血液里的补体成分也能与抗体反应,从而干扰试剂抗体结合抗原及与次级抗体反应的能力,可引起假阴性,因此,用阴性血清做稀释液具有较大的不确定性。本研究结果显示,单纯用PBS作为稀释液,检测的S/CO值要比阴性血清偏低,但用PBS+BSA则与阴性血清十分接近。考虑到PBS+BSA成分相比而言更简单,质量可控,pH值、渗透压、离子强度等关键溶液因素也基本等同于血清,同时据报道,BSADMSO和甘油是细胞培养中常用的冻存保护剂,可以减少冻融过程对蛋白质活性的损害。在质控血清的保存和使用过程中,反复冻融是造成抗体滴度降低的主要因素之一[7,8],加入一些防冻保护剂将有可能降低反复冻融对抗体水平的影响。本研究结果证明了DMSO和甘油本身对样本的检测值不产生明显干扰,可以考虑用作冻存保护剂。
对抗体活性具有一定的保护作用。因此,PBS+BSA是比较理想的稀释液。
5 结论
质控血清的配制需要首先对强阳性血清进行高倍数稀释,然后再进行倍比稀释确定S/CO值为2-3的最终稀释度;PBS加BSA可以替代阴性血清作为稀释液。
[1]王治国.临床检验质量控制技术[M].北京:人民卫生出版社,2008.
[2]谢益君.ELISA法检测HIV的室内质量控制[J].浙江预防医学,2007,19:12.
[3]胡静云,陈善昌.ELISA检测HIV抗体室内质控血清的制备与应用[J].实验与检验医学,2009,27:553.
[4]刘芳,胡斌,何蕴韶.联免疫吸附试验检测HIV抗体的质量控制方法探讨[J].热带医学杂志,2008,8:796-797.
[5]李敬云.艾滋病检测方法与应用[M].北京:军事医学科学出版社,2006.
[6]中国疾病控制预防中心.全国艾滋病检测技术规范[M].2009年修订版.
[7]杨春晖,张容,郑鹏.影响抗-HIV弱阳性质控血清稳定性的几种因素探讨[J].中国输血杂志,2008,21(6):441-443.
[8]徐霞,胡金权.酶联免疫吸附试验室内质量控制方法的评价[J].检验医学与临床,2008,5(1):30-32.
Preparation of External Quality Control Serum for ELISA Test
Liu Jianli,Wang Fei,Xu Huifang,Wei Haiyan,Zhang Wei,Liu Laifu*
(Beijing Entry-Exit Inspection and Quarantine Bureau,Beijing 100026)
[Objective]To explore the crucial factors in the preparation of external quality control serum for HIV ELISA test.[Methods]HIV positive serum was confirmed by ELISA and Western blotting,then it was diluted by HIV negative normal serum until the S/CO value reached 2 to 3 in ELISA test.Four different dilutions were also used and compared with normal serum by S/CO value.[Results]Strong positive serum selected showed high S/CO value of 21 to 30.The value did not decrease notably until it reached the value blow 15,after that control serum of OD value 2 to 3 could be made by double?ratio?dilution.PBS,PBS+BSA did not show difference compared with normal serum when they were used as dilution.[Conclusion]Strong positive HIV serum often has high value of S/CO,high ratio dilution should be made before the value decrease notably,then control serum of 2-3 value could be made by serial dilution.PBS+BSA could be a substitute of normal serum as dilution.
Quality Control Serum;Preparation;ELISA
R446.61
E-mail:liujianlibj@163.com;*通讯作者E-mail:liulf@bjciq.gov.cn
国家质检总局科技计划项目(2013IK306)
2015-06-09
