注射用头孢呋辛钠室温储存质量稳定性考察
2015-10-25何英佘定平陈钦榜吴建龙
何英,佘定平,陈钦榜,吴建龙
(广东省深圳市第二人民医院药学部,广东深圳518035)
注射用头孢呋辛钠室温储存质量稳定性考察
何英,佘定平,陈钦榜,吴建龙
(广东省深圳市第二人民医院药学部,广东深圳518035)
目的研究注射用头孢呋辛钠在室温(25℃)存放一定时间后的质量变化,为该药的储存管理提供参考。方法选取3个不同厂家的注射用头孢呋辛钠,置25℃下存放,分别于0,1,2,3个月时取样,按2010年版《中国药典(二部)》头孢呋辛钠项下方法,检查其性状、颜色、水分、pH、含量及有关物质是否符合规定。结果3批不同厂家的注射用头孢呋辛钠质量差异大,主要是颜色不符合要求。结论温度对头孢呋辛钠质量影响大,应警惕近效期药品因储存不当而缩短效期。
头孢呋辛钠;温度;质量稳定性;近效期;高效液相色谱法
2010年版《中国药典(二部)》规定,注射用头孢呋辛钠的储存要求遮光、密闭、阴凉处(不超过20℃)保存[1]。而药品从出厂到临床使用要经过多个流通环节,严格执行在20℃阴凉处储存有一定难度。储存温度过高或过低都会导致药品变质[2-3],特别是在不符合规定条件下储存的近效期药品,其质量的稳定性较低。笔者分析了该药品置室温(25℃)下一定时间后药品的质量状况,为药品的储存管理提供参考。
1 仪器与试药
Waters2690/2487型高效液相色谱仪,包括自动进样器、柱温箱、2487型紫外检测器、Millenium数据处理系统(美国Waters公司);HANNA213型pH计;AB135-S型电子天平;SFY-20型水分测定仪(深圳冠亚电子科技有限公司)。头孢呋辛钠对照品(批号为FN21310050,含量为93.0%);头孢呋辛钠3批120支,3个不同国产厂家,分别为A公司、B公司及C公司,规格均为0.75 g,见表1;乙腈,醋酸,醋酸钠,枸橼酸,磷酸氢二钠,均为分析纯。
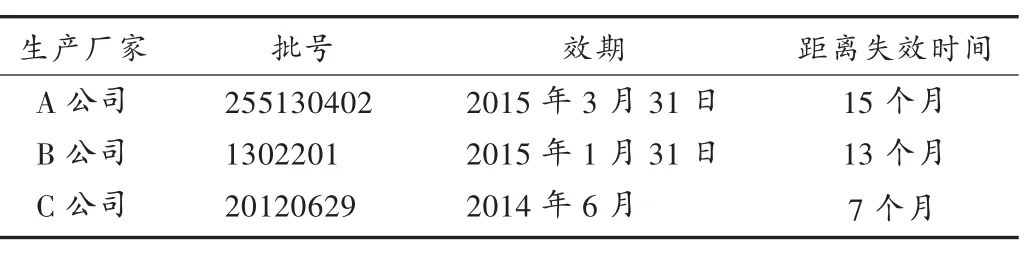
表1 3个不同生产厂家的样品情况
2 方法与结果
2.1样品准备
通过医药公司购进3个不同厂家生产的注射用头孢呋辛钠,置25℃下存放,分别于0,1,2,3个月时取样,按照2010年版《中国药典(二部)》头孢呋辛钠项下方法,检查其性状、颜色、水分、pH、含量及有关物质是否符合规定。
2.2色谱条件
色谱柱:Inertsil HPLC Column辛烷基硅烷键合硅胶柱(150 mm×4.6mm,5μm);流动相:pH=3.4醋酸盐缓冲液-乙腈(85∶15,V∶V);检测波长:273 nm;流速:1.5mL/min;进样量:20μL;柱温:40℃;保留时间:6.99min。按外标法以峰面积进行定量。
2.3样品溶液制备
精密称取3个厂家的注射用头孢呋辛钠各500mg,分别置3个100 mL容量瓶中,加水至刻度,摇匀,各精密吸取5.0 mL置25mL容量瓶中,加水至刻度,摇匀,待测。
2.4含量测定
分别于0,1,2,3个月各时段按上述方法制备溶液,按拟订色谱条件进样测定,每1个样品进3针,取平均值,计算样品含量。2.5有关物质测定
精密量取头孢呋辛钠适量,加水溶解并制成每1mL含0.5mg的溶液,作为供试品溶液;精密量取供试品溶液适量,加水制成每1mL含5μg的溶液,作为对照溶液。按2.2项下色谱条件,精密量取供试品溶液与对照溶液各20μL,分别注入高效液相色谱仪,记录色谱图至主成分峰保留时间的4倍。
2.6pH测定及颜色检查
取头孢呋辛钠适量,加水制成每1mL中含0.1 g的溶液,依2010年版《中国药典(二部)》规定用pH计测定,pH应为4.5~6.5。取头孢呋辛钠5瓶,分别按标示量加0.05mol/L乙二胺四醋酸二钠溶液制成质量浓度为0.1 g/mL的溶液,溶液应无色;如显色,依2010年版《中国药典(二部)》规定,与黄色或黄绿色8号标准比色液比较,均不得更深。
2.7水分检查
取头孢呋辛钠适量,依2010年版《中国药典(二部)》规定用水分测定仪测定,含水分不得过3.5%。
2.8结果
3个厂家注射用头孢呋辛钠各时段的含量测定结果见表2,有关物质、pH及水分均符合2010年版《中国药典(二部)》规定的标准。颜色检查项下C公司的药品性状在进行试验前为微黄色结晶性粉末,颜色浅于黄色10号标准比色液,深于2010年版《中国药典(二部)》规定的黄色或黄绿色8号标准比色液,说明在试验进行前该药已不符合标准。B公司的药品在放置2个月后,颜色浅于黄色9号标准液,也不符合2010年版《中国药典(二部)》标准。而A公司的药品放置3个月后,颜色无变化,稳定性较好。见表3。
3 讨论
通过考察注射用头孢呋辛钠在室温(25℃)储存3个月的质量变化情况发现,3个厂家药品的主药及有关物质含量、酸碱度和水分变化均符合2010年版《中国药典(二部)》标准,但颜色检查中发现,其中2个厂家的药品分别在考察前和考察第2个月的检查结果不符合规定,另1个厂家的药品直至试验结束均符合规定。颜色检查作为常规检查项目,其检验结果与未知杂质有很大联系[4]。如外观性状的变化超出了质量标准规定限度,则应判断药品失效[5]。储存温度越高,溶液颜色的变化越快[6],药品失效的速度也越快。
本研究发现,某一样品(批号20120629,C公司)考察前即出现质量不符合规定,分析可能有2个影响因素:药品在流通环节中未注意温度控制,导致样品溶液颜色不合格,有报道也做了类似分析[7];因药品储存温度变化导致效期缩短而失效,药品说明书中的有效期是基于其在规定温度范围下存放时间的质量保证[8],由于多个流通环节中储存条件不完善,特别是受到温度的影响,温度的变化将会影响药品的有效期。药品储存温度升高2℃,药品的有效期将会缩短20%[5]。该批号药品为近效期药品,纳入考察前离失效期近7个月,不排除是由于储存条件不完善导致的效期缩短,故近效期药品质量值得关注。其他2个批次注射用头孢呋辛钠在室温(25℃)条件下储存1个月质量均稳定,储存2个月受环境温度的影响有1批次不合格,考虑与原料和工艺有关。建议在实际工作中,尽量在阴凉库储存,受条件限制的不宜在室温条件下存放超过1个月。近效期药品如无阴凉库储存条件应在冷藏环境下储存。
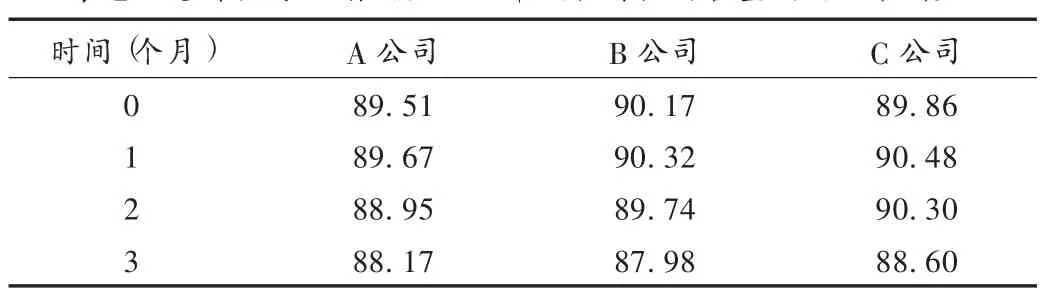
表2 3个厂家注射用头孢呋辛钠各时段的含量测定结果(%)
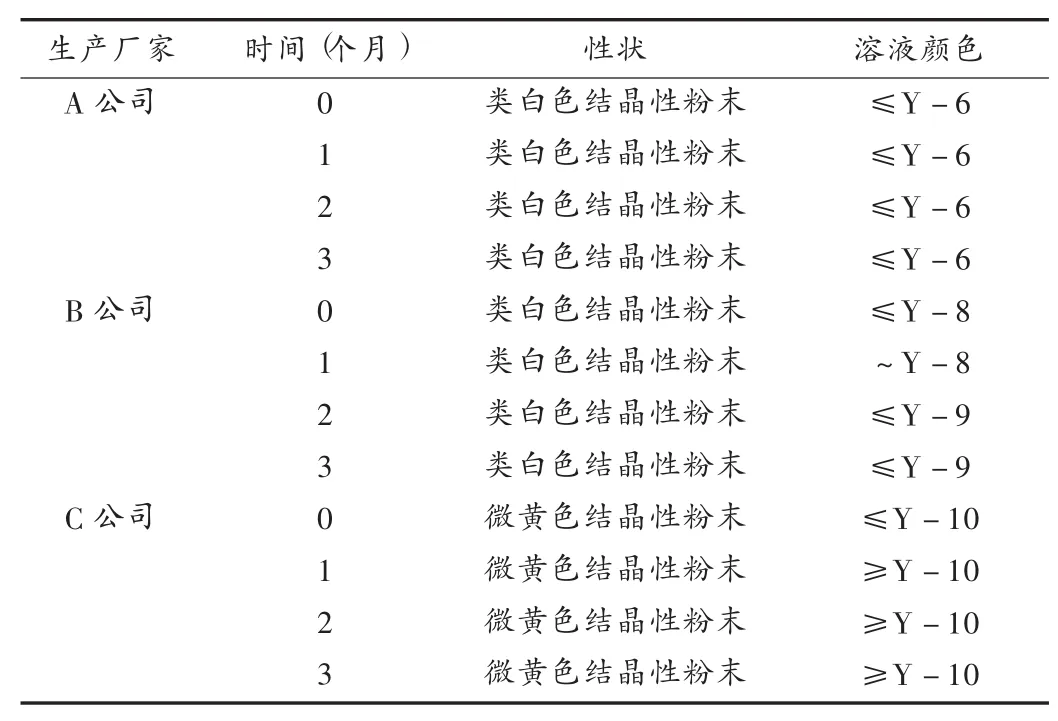
表3 3个厂家注射用头孢呋辛钠各时段的颜色变化情况
本研究为注射用头孢呋辛钠储存管理提供了更多的参考依据,但考察范围及抽样有限,有一定局限性,需要进一步扩大样本量来得出准确的结论。
[1]国家药典委员会.中华人民共和国药典(二部)[M].北京:中国医药科技出版社,2010:188-190.
[2]冯小敏,张继明,徐亮.我院药库药品贮藏温度的调查分析[J].中国药房,2008,19(13):1 034-1 035.
[3]陈宗志,金珍銮,缪存来.不同厂家注射用头孢呋辛钠在输液中稳定性的比较研究[J].海峡药学,2009,21(2):157-158
[4]陈壮生,刘丽平.注射用头孢呋辛钠粉针澄清度和颜色探讨[J].广东药学院学报,2010,26(5):459-461.
[5]霍秀敏.稳定性试验与药品的有效期[J].药品评价,2007,4(1):56-58.
[6]崔熙顺,钟萍,彭丽辉.注射用头孢呋辛钠稳定性的研究[J].中国药业,2003,12(2):49-50.
[7]张昕,黄文静,张肖群.注射用头孢呋辛钠溶液颜色检查不合格测定结果分析[J].今日药学,2010,20(2):19-20.
[8]De Winters S,Vanbrabant P,Vi NT,et al.Impact of temperature exposure on stability of drugs in a real-world out-of-hospital setting[J].Ann Emerg Med,2013,62(4):308-387.
Quality Stability of Cefuroxime Sodium for Injection′s Storage at Room Tem perature
He Ying,She Dingping,Chen Qinbang,Wu Jianlong
(Department of Pharmacy,Shenzhen Second People′s Hospital,Shenzhen,Guangdong,China 518035)
Objective To study the quality change of Cefuroxime Sodium for Injection at room temperature(25℃)for a certain time,and provide reference for the drug′s storage management.M ethods Cefuroxime Sodium for Injections from 3 manufacturers were selected and stored under room temperature at 25℃,The character,color,moisture content,pH,content and related substances of this drug were detected at 0,1,2,3 months respectively according to the provisions of cefuroxime sodium in Chinese Pharmacopoeia(2010 version).Results The quality of Cefuroxime Sodium for Injection among the 3 manufacturers have significantly differences,the main problem was that the color was not in conformity with the requirements.Conclusion The temperature can significantly influence the stability of Cefuroxime Sodium for Injection,and should pay athention to the shortening of expiration date of the drugs due to poor storage.
Cefuroxime Sodium;temperature;quality stability;expiration;HPLC
R927.11;R978.1+1
A
1006-4931(2015)18-0063-02
何英(1967-),女,大学本科,副主任药师,研究方向为医院药学,(电子信箱)heying2288@126.com。
2015-01-27)
