酵母双杂交筛选与果蝇C(2)M相互作用的蛋白
2015-10-22岳珊珊夏来新
岳珊珊,夏来新
1. 安徽大学生命科学学院,安徽 230601;
2. 中国科学院动物研究所,计划生育生殖生物学国家重点实验室,北京 100101
酵母双杂交筛选与果蝇C(2)M相互作用的蛋白
岳珊珊1,2,夏来新1
1. 安徽大学生命科学学院,安徽 230601;
2. 中国科学院动物研究所,计划生育生殖生物学国家重点实验室,北京 100101
同源染色体联会时形成的联会复合体(Synaptonemal complex, SC)是由减数分裂前期Ⅰ多种蛋白质聚集而成的超级复合结构。生殖细胞特异性的核蛋白C(2)M(Crossover suppressor on 2 of Manheim)在染色体上高度聚集可以诱导SC的形成。本文采用酵母双杂交方法,利用C(2)M的诱饵表达载体筛选果蝇cDNA文库,共发现40个可能与C(2)M相互作用的蛋白,包括多种DNA及组蛋白结合蛋白、ATPase、转录调节因子。从筛选的结果中,选取wech和Psf1基因构建了转基因果蝇,并在生殖细胞中进行了基因沉默,结果显示联会复合体的消失受到延迟。上述结果表明Wech和Psf1蛋白可能与C(2)M形成复合物,共同参与联会复合体的形成或其稳定性的维持。
减数分裂;SC;C(2)M;酵母双杂交;蛋白相互作用
减数分裂是指染色体复制一次,细胞连续分裂两次,染色体数目减半的一种特殊分裂方式。它是保证物种染色体数目稳定的机制,也促进着物种不断进化。减数分裂是由减数分裂Ⅰ和减数分裂Ⅱ两个时期组成,其中减数分裂Ⅰ又可细分为细线期、偶线期、粗线期、双线期和终变期5个时期。从偶线期起,同源染色体紧密相贴进行配对,称为联会,在同源染色体间形成了联会复合体(Synaptonemal complex, SC)。目前,对于SC的研究仅限于其本身组分相关的蛋白,而对于SC的起始、装配以及其时空性的研究还不够深入。据报道,SC的形成可分为3个时期[1]:偶线期早期,只能在着丝粒上观察到联会复合体;偶线期中期,联会复合体开始出现在常染色体的某些位点上;偶线期晚期,联会发生在染色体上的更多位点上。由此可见,SC的形成有着严谨的机制。已有的研究证实,偶线期早、中期SC的形成依赖于凝集蛋白ORD(Orientation disruptor)[2],晚期SC的形成则依赖C(2)M[3]。C(2)M是SC中的纵向元件(Later elements, LEs)的组成成分[4],在减数分裂S期开始累积,在减数分裂中期Ⅰ消失,说明C(2)M在联会复合体中发挥作用,而并不参与染色体的分离[5,6]。目前,对于C(2)M在联会这一事件中发挥怎样的功能仍知之甚少,特别是关于C(2)M如何参与SC的形成、如何引导SC的组装。
酵母双杂交系统是1989年由Fields等[7]提出并初步建立的,至今为止一直是研究蛋白间相互作用的重要实验手段。本研究利用酵母双杂技术,以C(2)M为诱饵蛋白,筛选果蝇文库中与之相互作用的蛋白,旨在研究C(2)M调控SC组装的分子机制,相关结果将有助于提高人们对同源配对分子基础及减数分裂启动的了解。
1 材料和方法
1.1材料
酵母菌株AH109,质粒pGBKT7和pACT2,宿主菌E. coli DH5α由本实验室提供;cDNA文库由上海海科生物技术有限公司构建;酵母质粒小提试剂盒和鼠、兔免疫荧光二抗购自天根生物公司;C(3)G抗体由本实验室自制,Orb抗体购自Developmental Studies Hybridoma Bank(美国)。
1.2方法
1.2.1诱饵蛋白表达载体的构建
以果蝇cDNA为模板,设计有含NcoⅠ和XhoⅠ限制性酶切位点的引物c(2)M-NcoⅠ-s和c(2)M-XhoⅠ-as(表1),PCR扩增C(2)M的CDS(Coding sequence)序列(Gene ID:34964),将扩增产物连接pGBKT7载体。
1.2.2诱饵质粒转化酵母AH109及文库筛选
醋酸锂法制备AH109感受态,转入诱饵质粒,铺于SD/-Trp缺陷培养基上,30℃培养4~6 d;取部分菌体用于检测蛋白表达;制备含诱饵质粒的AH109感受态,转入文库质粒,铺于SD/-Trp/-Leu/-His/-Ade缺陷培养基上,30℃培养5~7 d;挑取直径>2 mm的阳性克隆,接于SD/-Trp/-Leu/-His/-Ade缺陷培养基上保种。
1.2.3酵母阳性克隆质粒提取及质粒的回复和自激活验证
因酵母具有质粒相容性,可包含多种质粒,所以提出酵母质粒后,需转化E. coli DH5α,从中提取质粒;将提出的质粒同pGBKT7-c(2)M回转AH109,验证阳性相互作用;将质粒同pGBKT7回转AH109,验证阳性质粒能否自激活His和LacZ基因。
1.2.4阳性克隆的测序与分析
将重复验证结果为阳性而自激活验证为阴性的组别由北京擎科生物公司测序,测序结果在NCBI和Flybase网站上进行序列比对,利用生物信息学方法研究筛选结果。
1.2.5S2(Schneider 2)细胞内验证C(2)M和Wech/Psf1的相互作用
结合文献以及基因本身的表达特点,从筛选结果中挑选wech和Psf1 2个目标基因,在S2细胞内验证其与C(2)M的相互作用;将这两个基因沉默后,免疫荧光观察减数分裂进程是否受到影响。以果蝇cDNA为模板,设计含有NotⅠ和XbaⅠ限制性酶切位点的引物c(2)M-NotⅠ-s、c(2)M-XbaⅠ-as、wech-NotⅠ-s、wech-XbaⅠ-as、Psf1-NotⅠ-s和Psf1-XbaⅠ-as(引物信息见表1),PCR扩增c(2)M、wech(Gene ID:44653)和Psf1(Gene ID:38136)的CDS序列,构建载体pAC5.1-Flag-c(2)M和pAC5.1-Myc- wech/Psf1。将其分别共转S2细胞,29℃培养48 h;收集细胞,用PBS洗涤3遍,用细胞裂解液裂解细胞,冰上放置30 min,4℃、12 000 r/min离心10 min,收集上清;将上清与Flag beads 4℃孵育2 h,PBST洗3次,用1×SDS loading buffer重悬,95℃煮样10 min,丙烯酰胺凝胶电泳分离蛋白样品,将蛋白样品转至PVDF膜上,5%牛奶封闭1 h,以c-Myc抗体为一抗,室温孵育2 h,以鼠抗为二抗,室温孵育30 min,显影。

表1 本研究所用的引物信息
1.2.6候选基因的基因沉默型果蝇卵巢荧光观察
本研究采用GAL4/UAS系统快速获得可调控的RNA干扰果蝇。在Gene Link网站上设计wech和Psf1 mRNA干扰序列;引物稀释为100 μmol/L,各取1 μL,Taq buffer 1 μL,水7 μL,95℃变性5 min,室温复性1 h;将产物连入已有的表达载体UASP-attB中;经大肠杆菌扩增后,提取质粒,通过显微注射的方法将载体注入果蝇的卵巢,于25℃培养箱中培养,至其发育为成虫;选择有干扰序列插入的果蝇,与表达转录激活蛋白GAL4的果蝇品系杂交,收集同时含有GAL4基因和UAS序列的F1代雌蝇,显微镜下剥离卵巢,甲醛固定30 min,PBST打孔30 min,PBTA封闭1 h,C(3)G和Orb一抗4℃孵育过夜,荧光二抗孵育3 h,制片观察。
2 结果与分析
2.1诱饵蛋白表达载体pGBKT7-c(2)M的构建
以成体果蝇的cDNA为模板扩增基因c(2)M的 CDS区,片段长度为1731 bp,经NcoⅠ和XhoⅠ酶切后插入pGBKT7中,以T7和下游引物作为鉴定引物,阳性结果测序证实无移码突变。
2.2阳性克隆的筛选、自激活及回复验证
取50 μg cDNA文库转入含目的基因c(2)M的AH109中,采用SD/-Trp/-Leu/-His/-Ade缺陷培养基高压筛选,经过1周左右的时间,在SD/-Trp/-Leu/-His/ -Ade缺陷培养基上共长出直径>2 mm的克隆200个,PCR筛选阳性克隆,文库基因大小在500~3000 bp之间(图1A)。对这200个克隆分别进行自激活和回复验证实验(图1B),其中自激活的组别占总组别的35%。除去自激活现象(70个)和回复验证失败(39个)的组别,本研究最后获得91个阳性克隆,对其进行测序。
2.3阳性克隆的测序及生物信息学分析
由于酵母质粒浓度较低,将质粒转入E. coli DH5α感受态后重新提取质粒,以T7为引物进行测序,最后将这91个测序结果在Flybase上进行比对,得到40个不同的基因(表2),编码众多结合蛋白、热休克蛋白、ATP酶、具有解旋酶活性的Psf1、整合蛋白Wech以及染色体凝集蛋白Cap-G。
2.4S 2细胞内验证C(2)M和Wech/Psf1的相互作用
pAC5.1-Flag-c(2)M和pAC5.1-Myc-wech/Psf1共转S2细胞48 h后,提取蛋白,沉淀C(2)M及与其相互作用的蛋白,结果见图2。从图2可以看出,在单独转染pAC5.1-Myc-wech或pAC5.1-Myc-Psf1时,利用Flag beads免疫沉淀后,没有检测到Wech或Psf1的表达;而共转pAC5.1-Flag-c(2)M和pAC5.1-Myc-wech/Psf1后,在经Flag beads沉淀后的C(2)M相互作用的蛋白中,分别检测到Wech和Psf1的表达,说明C(2)M和Wech/Psf1均存在相互作用。
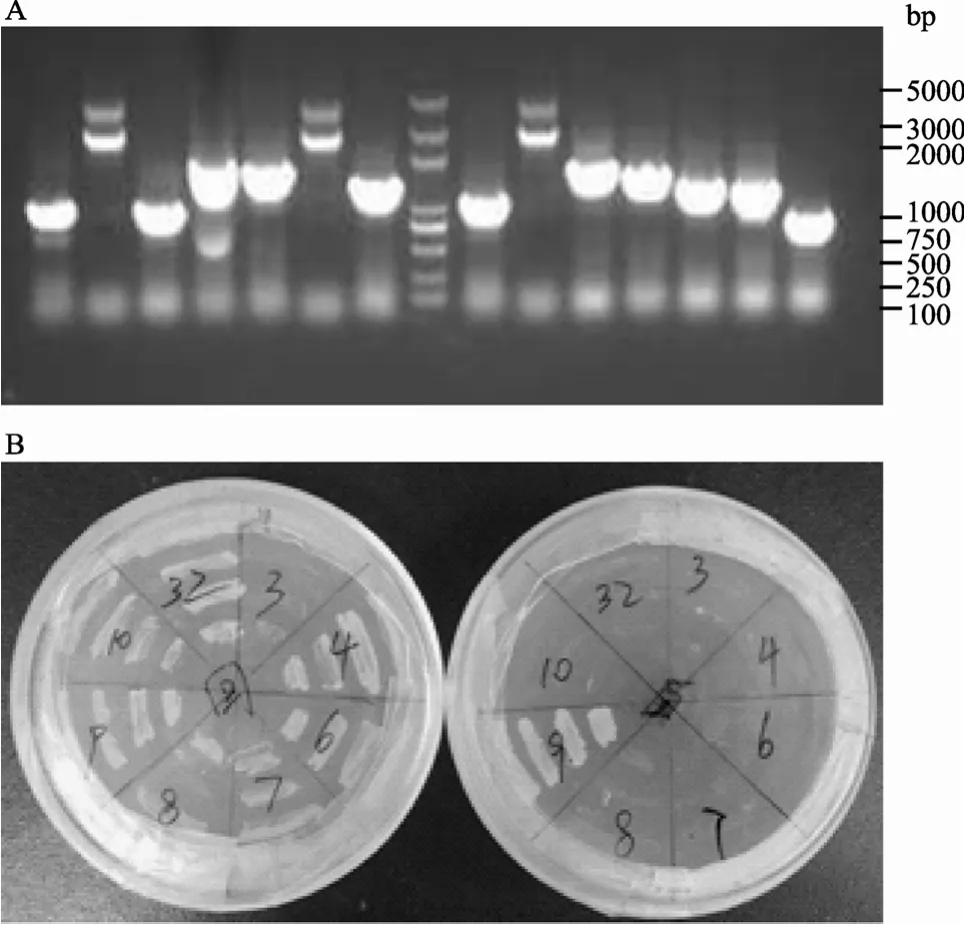
图1 酵母质粒PCR检测结果(A)及阳性克隆的回复验证(B)
2.5wech和Psf1基因沉默型果蝇卵巢的免疫荧光观察
本文成功制备了含有wech和Psf1 mRNA干扰序列的转基因果蝇,用能够标记联会复合体的C(3)G抗体,染色wech和Psf1基因沉默后的卵巢,发现与野生型果蝇不同的是,在wech和Psf1基因沉默型果蝇的卵巢中,其染色体联会受到了干扰,即在卵母细胞形成的最后阶段,会有两个细胞发育成为卵母细胞,而在野生型果蝇中,最终只形成一个卵母细胞(图3)。
3 讨 论
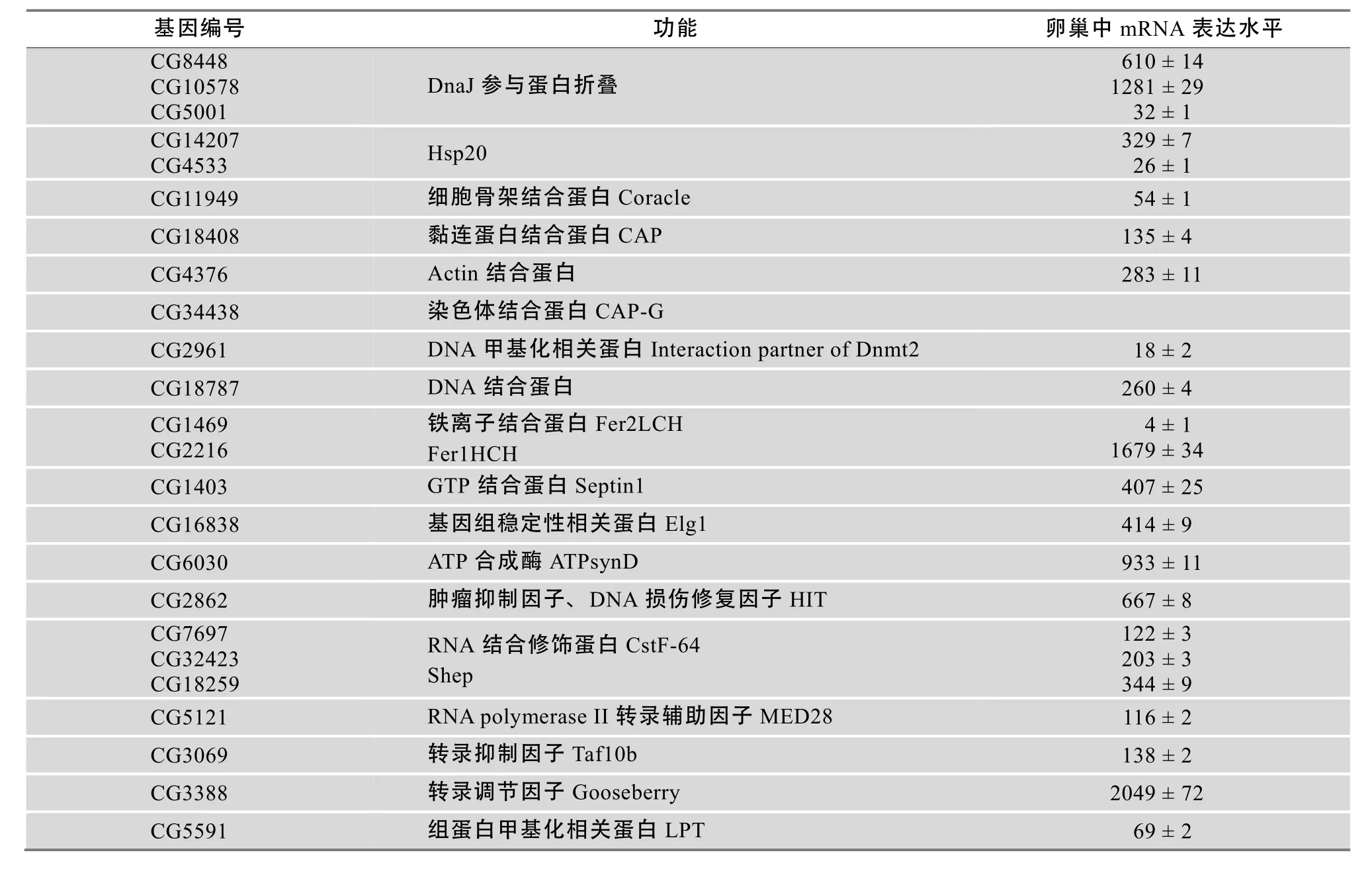
表2 酵母筛选阳性克隆比对结果
酵母双杂交技术自建立起一直是研究和鉴定两个蛋白相互作用的有效方法。其原理是依赖于转录激活因子GAL4的DNA结合结构域和转录激活结构域在空间上充分靠近,从而激活下游基因表达[8,9]。C(2)M是细胞核内减数分裂相关蛋白,为了进一步分析其功能和作用机制,本文采用了酵母双杂交的方法筛选与其相互作用的蛋白。
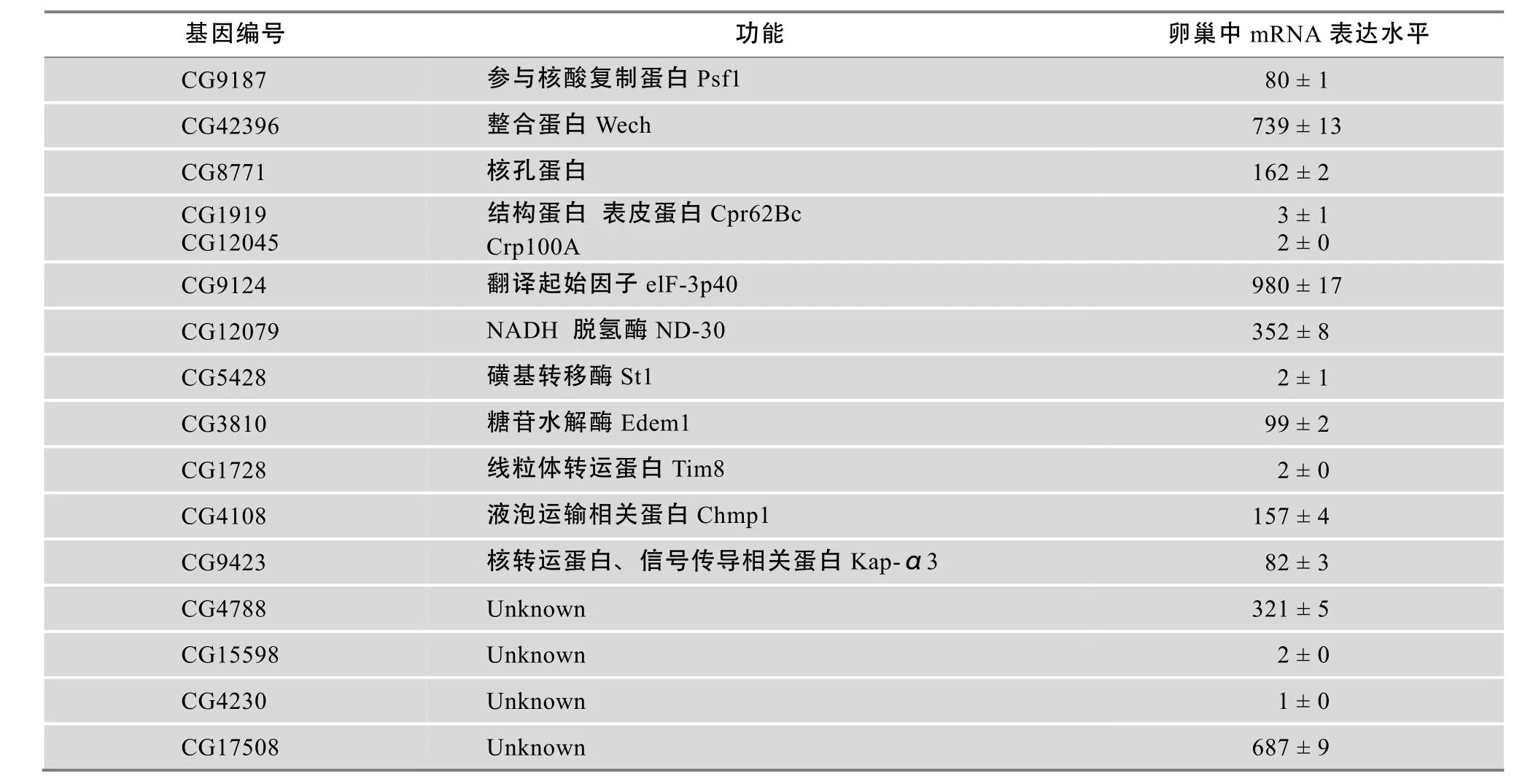
续表2

图2 免疫共沉淀验证C(2)M和Wech/Psf1蛋白之间具有相互作用
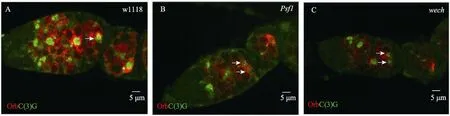
图3 wech和Psf1基因沉默型果蝇原卵区的荧光染色结果
果蝇卵细胞始于卵巢顶部的2~3个原始生殖细胞,原始生殖细胞不对称分裂,一个继续位于卵巢顶部,维持干性。另一个则离开顶部开始分化形成囊胚细胞,经过4次有丝分裂形成一个由16个细胞组成的包囊。16个细胞里只有1个细胞形成卵母细胞,并进行减数分裂,其余细胞则为滋养细胞。C(2)M是SC形成的必要因子,在本研究结果中可以看出,wech和Psf1 基因沉默后,SC的消失发生了延迟,说明wech和Psf1可能参与SC解体的过程。
Cap-G属于condensin蛋白家族中非染色体结构维持蛋白[10,11]。据报道在缺乏Cap-G的突变体中,染色体的凝集和压缩受到阻碍,从而导致姊妹染色单体不能正常分离,并且会引起着丝粒粘附力的减弱[12,13]。说明Cap-G在染色体轴形成过程中发挥重要的功能。本课题组通过酵母双杂交筛选出染色体凝集相关蛋白Cap-G,说明Cap-G有可能也参与减数分裂染色体轴的形成。然而就其如何与C(2)M共同发挥作用还需要进一步研究。
Wech属于RBCC/TRIM超家族[14],该蛋白家族含有一个锌指元件、卷曲螺旋结构域和5~6个NHL(NCL-1,HT2A,LIN-41)重复结构,在果蝇中,只有4个蛋白属于该家族,分别是Wech[15,16]、减数分裂相关蛋白Mei-P26[17]、肿瘤抑制蛋白Brat[18]和锌指串联蛋白ABBA。缺少Brat会引起脑瘤,缺少Mei-P26会导致卵巢肿瘤,研究发现Brat的肿瘤抑制功能域是NHL结构域[19]。而本研究测序结果发现与C(2)M相互作用的区域正好是Wech的C端NHL结构,猜测其与C(2)M的相互作用正是它们共同行使减数分裂相关功能的基础。Psf1作为GINS复合体中的一员[20],参与DNA复制的起始和延伸,而其在果蝇卵子发生过程中,是否通过调控DNA的复制来起始有丝分裂向减数分裂的转换,还需要深入研究。由于基因沉默受多方面因素影响,所以本文的表型并不是很强,对于Wech及Psf1是否同C(2)M共同参与减数分裂相关过程以及其具体的分子机制,还需要后期通过制备抗体和突变体等大量实验来证明。C(2)M作为减数分裂的上游因子,研究与其相互作用的蛋白有助于人们了解C(2)M调控减数分裂的具体机制以及加深对减数分裂的认识。同时还可能为相关的卵巢性生殖疾病的预防和治疗,提供新的线索。
[1] Tanneti NS, Landy K, Joyce EF, McKim KS. A pathway for synapsis initiation during zygotene in Drosophila Oocytes. Curr Biol, 2011, 21(21): 1852-1857.
[2] Balicky EM, Endres MW, Lai C, Bickel SE. Meiotic cohesion requires accumulation of ORD on chromosomes before condensation. Mol Biol Cell, 2002, 13(11): 3890-3900.
[3] Anderson LK, Royer SM, Page SL, McKim KS, Lai A,Lily MA, Hawley RS. Juxtaposition of C(2)M and the transverse filament protein C(3)G within the central region of Drosophila synaptonemal complex. Proc Natl Acad Sci USA, 2005, 102(12): 4482-4487.
[4] Lake CM, Hawley RS. The molecular control of meiotic chromosomal behavior: events in early meiotic prophase in Drosophila Oocytes. Annu Rev Physiol,2012, 74: 425-451.
[5] Heidmann D, Horn S, Heidmann S, Schleiffer A, Nasmyth K, Lehner CF. The Drosophila meiotic kleisin C(2)M functions before the meiotic divisions. Chromosoma, 2004,113(4): 177-187.
[6] Manheim EA, McKim KS. The synaptonemal complex component C(2)M regulates meiotic crossing over in Drosophila. Curr Biol, 2003, 13(4): 276-285.
[7] Fields S, Song O. A novel genetic system to detect proteinprotein interactions. Nature, 1989, 340(6230): 245-246.
[8] 杨姗姗, 孙晓丽, 于洋, 才华, 纪巍, 柏锡, 朱延明. 酵母双杂交筛选与GsCBRLK相互作用的蛋白质. 遗传,2013, 35(3): 388-394.
[9] 都建, 陈立建, 沈继龙, 花沙沙, 姚雪彪. 用酵母双杂交系统筛选CENP2E相互作用蛋白. 中国生物化学与分子生物学报, 2009, 25(8): 719-726.
[10] Lee JY, Orr-Weaver TL. The molecular basis of sister chromatid cohesion. Annu Rev Cell Dev Biol, 2001, 17: 753-777.
[11] Ono T, Losada A, Hirano M, Myers MP, Neuwald AF, Hirano T. Differential contributions of condensinⅠand condensinⅡ to mitotic chromosome architecture in vertebrate cells. Cell, 2003, 115(1): 109-121.
[12] Dej KJ, Ahn C, Orr-Weaver TL. Mutations in the Drosophila condensin subunit dCAP-G: defining the role of condensin for chromosome condensation in mitosis and gene expression in interphase. Genetics, 2004, 168(2):895-906.
[13] Herzog S, Jaiswal SN, Urban E, Riemer A, Fischer S, Heidmann SK. Functional dissection of the Drosophila melanogaster condensin subunit Cap-G reveals its exclusive association with condensinⅠ. PLoS Genet, 2013, 9(4):e1003463.
[14] Meroni G, Diez-Roux G. TRIM/RBCC, a novel class of“single protein Ring finger” E3 ubiquitin ligases. BioEssays, 2005, 27(11): 1147-1157.
[15] Löer B, Bauer R, Bornheim R, Grell J, Kremmer E, Kolanus W, Hoch M. The NHL-domain protein Wech is crucial for the integrin-cytoskeleton link. Nat Cell Biol, 2008,10(4): 422-428.
[16] Löer B, Hoch M. Wech proteins: roles in integrin functions and beyond. Cell Adhes Migr, 2008, 2(3): 177-179.
[17] Li Y, Zhang Q, Carreira-Rosario A, Maines JZ, McKearin DM, Buszczak M. Mei-p26 cooperates with Bam, Bgcn and Sxl to promote early germline development in the Drosophila ovary. PLoS One, 2013, 8(3): e58301.
[18] Lee CY, Wilkinson BD, Siegrist SE, Wharton RP, Doe CQ. Brat is a Miranda cargo protein that promotes neuronal differentiation and inhibits neuroblast self-renewal. Dev Cell, 2006, 10(4): 441-449.
[19] Arama E, Dickman D, Kimchie Z, Shearn A, Lev Z. Mutations in the β-propeller domain of the Drosophila brain tumor (brat) protein induce neoplasm in the larval brain. Oncogene, 2000, 19(33): 3706-3716.
[20] Grabowska E, Wronska U, Denkiewicz M, Jaszczur M, Respondek A, Alabrudzinska M, Suski C, Makiela-Dzbenska K, Jonczyk P, Fijalkowska IJ. Proper functioning of the GINS complex is important for the fidelity of DNA replication in yeast. Mol Microbiol, 2014, 92(4): 659-680.
(责任编委: 史庆华)
Identification of C(2)M interacting proteins by yeast two-hybrid screening
Shanshan Yue1,2, Laixin Xia1
1. School of Life Sciences, Anhui University, Anhui 230601, China;
2. State Key Laboratory of Reproductive Biology, Institute of Zoology, Chinese Academy of Sciences, Beijing 100101, China
The synaptonemal complex (SC) is a huge structure which assembles between the homologous chromosomes during meiotic prophase I. Drosophila germ cell-specific nucleoprotein C(2)M clustering at chromosomes can induce SC formation. To further study the molecular function and mechanism of C(2)M in meiosis,we constructed a bait vector for C(2)M and used the yeast two-hybrid system to identify C(2)M interacting proteins. Forty interacting proteins were obtained, including many DNA and histone binding proteins, ATP synthases and transcription factors. Gene silencing assays in Drosophila showed that two genes, wech and Psf1, may delay the disappearance of SC. These results indicate that Wech and Psf1 may form a complex with C(2)M to participate in the formation or stabilization of the SC complex.
meiosis; SC; C(2)M; yeast two-hybrid system; protein interaction
2015-03-22;
2015-08-25
SKLRB青年杰俊科研创新主任基金项目资助
岳珊珊,硕士研究生,专业方向:RNA代谢和干细胞。E-mail: yueshanshanyss@163.com
夏来新,教授,博士生导师,研究方向:RNA代谢和干细胞。E-mail: xialx@ioz.ac.cn
10.16288/j.yczz.15-118
网络出版时间: 2015-9-119:54:25
URL: http://www.cnki.net/kcms/detail/11.1913.R.20150911.0954.002.html
